抽象
EVA(肺气肿与是一个多中心项目,旨在研究慢性阻塞性肺病(COPD)中肺气肿和气道疾病的机制和识别生物标志物。本研究的目的是使用定量计算机断层扫描(QCT)指数,用一种新的基于影像的方法来客观地描述以肺气肿为主导的和以气道疾病为主导的表型。
441名慢性阻塞性肺病患者(全球慢性阻塞性肺病(GOLD) 1-3期)接受了临床和生理测量、实验室检测以及肺气肿和气道壁几何形状的标准化QCT指标的评估。
QCT指数用扫描器不合格的影响,但标准化显著减少变异性(P <0.001),并导致更健壮的表型。四个成像衍生的表型进行鉴定,反射“肺气肿显性”,“气道疾病显性”,“混合的”疾病和“柔和”的疾病。气肿显性组有显著更高肺容量,较低的气体传递系数,较低的氧(PØ2)和二氧化碳(PCO2)紧张,较高的血红蛋白和比气道疾病,显性组高血白细胞数。
QCT的在国际多中心研究的表型分型设置实用程序是通过标准化提高。肺气肿气道疾病的QCT指数可以的患者有已知与肺气肿显性和气道显性遗传病相关的典型临床表现COPD,表型组群内划定。
抽象
在一项多中心研究中,定量CT的标准化改善了肺气肿和气道表型的描述http://ow.ly/10zjhV
介绍
慢性阻塞性肺病(COPD)是一种异质性疾病,其特征是由于肺气肿、气道重塑和闭塞导致的持续性、不完全可逆的气流阻塞。为了更好地了解慢性阻塞性肺病的发病机制,我们将其称为肺气肿与研究旨在界定肺气肿和气道疾病的表型[1]。慢性阻塞性肺病的定义、诊断和分期通常采用肺量标准[2,3]。虽然肺功能检查是方便在日常临床实践应用,它不可靠区分COPD的肺气肿和气道疾病的部件[4]。定量ct (Quantitative computed tomography, QCT)成像可以客观、无创地评价肺气肿和气道形态[五因此],并在表型分型研究中一个潜在的有价值的工具,但其在多中心的研究表型分型的作用还没有得到系统的评价。
肺气肿的量化通过测定计算机断层扫描(CT)图像的日期肺密度的背面超过二十年[6),现在接受了作为一个结果测量与αemphysema-modifying治疗的病人的研究1抗胰蛋白酶缺乏[7]。CT技术来评估气道疾病的程度也已经被开发和气道壁形态被用作气道哮喘重塑的量度[8-10]。ñakano等。[11]报道,气道壁的厚度相关因素与COPD患者的气流阻塞,而高百分比的壁面积和低肺密度可以是相互排斥的。因此,我们假设,QCT能够准确细分COPD患者分为肺气肿显性和呼吸道疾病为主的情况下[11]。然而,由于EVA从10个临床中心结合数据,我们试图评估的扫描器差异的影响[12-15]并建立标准化QCT专用幽灵的潜在效用。使用这种策略,我们研究标准化CT义患者亚组是否具有独特的临床和实验室特征。一些研究结果已在文摘[形式报道过16-19]。
材料与方法
EVA的研究策略和研究设计先前已经描述1]。综上所述,EVA是跨越涉及临床检查,CT检查和支气管镜取样,以确定标志物的具体肺气肿和气道疾病COPD五个欧洲国家(德国,英国,意大利,匈牙利和波兰),多中心研究。该研究是通过在参与中心的有关伦理道德和审查委员会,并签署知情同意书的所有科目。
临床评估
一种diagnosis of COPD was based on a post-bronchodilator forced expiratory volume in 1 s (FEV1)/用力肺活量(FVC)的比率<70%。(患者被排除在外,如果他们有非常严重的慢性阻塞性肺病FEV1<30% predicted or <1 L), bronchodilator reversibility greater than 400 mL, had smoked within the previous 12 months, or had a primary diagnosis of bronchiectasis, asthma or any other significant respiratory diseases [1]。
所有受试者均通过临床病史、体格检查、肺功能测试(包括体积描记、6分钟步行距离(6MWD)、使用改良医学研究委员会(mMRC)量表对呼吸困难进行量化评估[20]和CT。所有受试者接受他们一贯的处方药。静脉取血用于临床化学,包括α1-抗胰蛋白酶和c反应蛋白。血浆样本在- 20°C冷冻,然后用干冰运送到协调地点(德国慕尼黑),在- 80°C储存。采用e-biosciences ELISA (BMS2002CE)测定血浆中的促红细胞生成素。
CT扫描和图像分析
详细的CT采集和分析方法见在线补充资料。患者扫描在通用电气(费尔菲尔德、CT、美国)或西门子(德国埃朗根)和容积CT扫描仪扫描覆盖整个肺肺微和有限扫描肺中间包括气管气道形态测量学的船底座右S1节段气道(表S1)。使用Pulmo CMS进行图像分析[21]和EmphylxJ [22]软件包。
由肺密度直方图得出的第15百分位(百分15)点用于评估肺气肿的严重程度,而右侧S1段支气管的%壁面积(%WA)用于评估气道疾病。后者可作为小气道疾病的替代参数,因为已有研究表明,CT中气道壁尺寸的测量可预测组织学中确定的小气道尺寸[23]。不过,这项研究并不能直接测量小气道的尺寸也没有比较吸气和呼气扫描,以确定气体捕集,这被认为是小气道疾病的间接测量。肺气肿的标准化及气道CT指数,专用肺气肿和呼吸道幻影在所有的中心进行扫描和而得指数来生成使用在临床前体模研究(图S1和S2和表S2和S3)验证的方法中心特异性回归方程。
统计数据
慢性阻塞性肺病患者按正常对照组的百分位值(%WA)和百分位值(95%以上)分为4组。四组分别被命名为“以肺气肿为主”(Ea)、“以气道疾病为主”(Ea)、“混合型”病理(Ea)和“轻度”疾病(Ea)。极端E型和A型是通过根据这两组中百分比15和%WA的等级乘积给每个受试者等级顺序编号,并将处于最高等级的一半的受试者划分为极端表型来识别的。统计分析采用非参数wilcoson - mann - whitney检验,Kruskal-Wallis,卡方和线性,部分和多元线性回归分析。采用Spearman检验进行非参数相关分析。应用Bonferroni-Holm校正后p值<0.05被认为是显著的。
结果
病人
我们在10个临床中心招募了534名慢性阻塞性肺病患者和280名对照组。所有病例和56例对照组均进行了胸部CT扫描。93例患者无法获得定量指标(原因列表见表S4)。在那些使用或不使用可评估CT的病例之间,或者在扫描仪制造商之间,除了在通用电气扫描仪上研究的患者中较低的气体转移外,在临床参数方面没有差异(表S5)。病例和对照组的临床特征如下图所示表格1。
QCT指数标准化
在不标准,Perc15和WA%的差异,在扫描仪制造商和型号(见差异有关图1一个和b)。临床前密度测量和气道形态测量幻影研究表明,标准化可使可变性降低84% (p<0.001)(均数±±)SDdifference of 26.2±13.4 HU in unstandardised densitometry data与4。1±2.3 HU in standardised data) (table S2 and figure S3). A mean±SD在所有EVA中心假想管的不标准,%WA,观察到2.9±1.9的差异。标准化降低了平均差至0.6±0.5,较79%(P = 0.002)(表S3和图S4)的误差降低。平均±SD幻像管%WA分别对西门子衍生成像显著下相比,通用电气衍生成像(62.0±11.6%与66.4±12.0%;p = 0.007)。
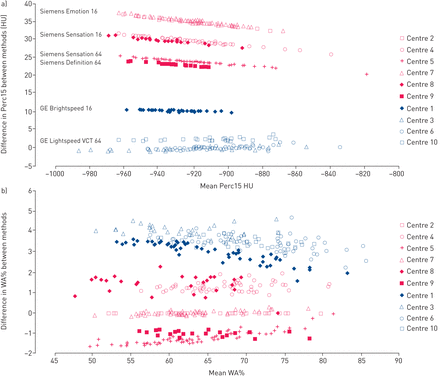
布兰德-阿尔特曼的阴谋是不标准化的与标准化的15个百分点(Perc15)和壁面积(WA)。一个)布兰德-Altman图与Perc15比较不标准Perc15(用于血液和空气与Pulmo CMS软件校正)标准化靠在密度参考扫描器(前体积校正)。b)中布兰德-Altman图比较标准化针对气道参考扫描器不标准,WA(%)对WA(%)。N = 441。
有不标准Perc15和%WA(R = 0.34,P <0.001之间的相关性;图2一个),其降低通过调节肺密度为肺体积(R = 0.27,P <0.001;图2 b),并进一步降低了以下幻象标准化相关(r = 0.11,P = 0.17;图2 c)。

体模和体模校正对墙体形状的影响与肺气肿的肺密度与慢性阻塞性肺疾病病例。a)未经校正,b)肺密度体积校正,c)遵循幽灵衍生的标准方法和体积校正。n = 441。a、b和c的s分别是0.336、0.271和0.113。
CT-定义表型的比较
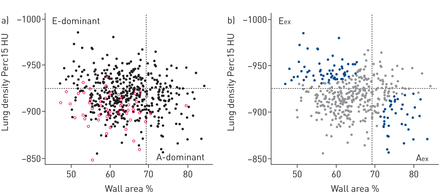
QCT data from the 56 control subjects showed that the upper 95th percentile values for Perc15 was −925.6 HU and for WA was 69.3%. The COPD cases were subsequently classified into the four pre-specified groups; “emphysema-dominant” (Ea) (n=124), “airway disease-dominant” (eA) (n=79), “mixed” pathology (EA) (n=34) and “mild” disease (ea) (n=204) (图3一)。四种表型的年龄、性别和吸烟史无差异(表2)。当比较E-dominant时与该表中以a为主的病例中,以e为主的病例(Ea)的体重指数(BMI)较低,为25.9 kg·m-2体重指数(BMI)为30.1 kg·m的a -优势组(eA)低于a -优势组(eA)-2。在最后一列中,“1”表示在成对比较中Ea与EA有显著的差距¶表明它也修正了多次测试后显著。该表还显示,E-占主导地位的情况下,有更多的阻塞性肺量测定,增加肺容量,降低气体传输,更高的血红蛋白,低PØ2和PCO2还有更多的人服用长效毒蕈碱拮抗剂。混合病理组以上肺叶为主,与“以肺气肿为主”组和“以气道疾病为主”组相比,无明显区别。轻度疾病患者的肺指标优于其他表型。中心(表S6)和扫描类型(表S7)的受试者在每种ct表型中的比例存在显著差异(p<0.001)。
肺气肿主导,气道疾病占主导地位的和极端的表型的定义基于计算机断层扫描(CT)。一个)的壁区域(WA)和肺密度在肺气肿与气道疾病(EvA)慢性阻塞性肺疾病(COPD)患者(n=441,填充圆形)和对照组(n=56,开放圆形)在此壁区与肺密度图。Ťhe upper limit of normal (ULN) for wall area (69.3%) and lower limit of normal (LLN) for emphysema (−925.6 HU) are given as vertical and horizontal dotted lines, respectively. b) wall area and lung density in the EvA COPD cases: extreme phenotypes. Rank orders were determined in that all WA% values in the upper left quadrant were given rank numbers, with highest wall area ranked as 1. Also all 15th percentile (Perc15) values in the upper left quadrant were given a rank number, with the highest lung density ranked as 1. The two rank numbers for each individual were multiplied and individuals were ordered according to the product size. Individuals in the upper half of this rank product list were classified as extreme emphysema dominant (E前)。以极端气道疾病为主(A前)在右下角,则该过程被相应地应用。与此极端CT-表型病例是由彩色点的灰点的对的剩余患者的背景显示。E-极端在左上角(N = 62)和A-极端在右下(N = 40)。Ťhe ULN for wall area (69.3%) and LLN for emphysema (−925.6 HU) are given as vertical and horizontal dotted lines, respectively.
ct定义的极端表型分析
该Perc15的分布与慢性阻塞性肺疾病(COPD)病例和对照组的脑卒中发生率(%WA)如表所示图3一与极端肺气肿主导(E前)和极端气道疾病主导(A前)所示图3 b。极端肺气肿占主导地位者(E前)(N = 62)和极端气道疾病显性(A前)(N = 40)基团表明的几个临床和实验室特性的图案被更与肺功能参数,血液气体,血红蛋白和白细胞(表S8)有较大的差别显着。
相关和多元线性回归分析
单变量分析的临床,生理和实验室指标和两个Perc15和%WA(之间进行表3)。肺密度呈正相关FEV1%预测,BMI,PØ2,PCO2与肺容积、血红蛋白和总白细胞计数呈负相关。肺密度调整的部分相关性显示,这些参数的相关性与肺密度无关(表3)。%WA与BMI呈正相关,PØ2,PCO2与肺容积呈负相关,与气道阻力小有关。%WA与肺密度调整的部分相关表明,%WA与肺密度的相关性PØ2和PCO2是独立肺密度。(%WA和小气道阻力之间的相关性[R亚历山大-伍尔兹)更显着以下调节肺密度为2.1×10的p值-8前和1×10-9调整后。多元线性回归分析表明,BMI,FEV1、总肺活量(TLC)、肺对一氧化碳的转运能力(ŤLCO)/肺泡体积(V一种) %预测值和Hb与肺密度密切相关,而%WA与BMI、6MWD、PØ2和PCO2(表4)。
讨论
目前的研究已经证明,使用标准化QCT可在具有轻度到中度气流阻塞的异质性COPD人群中勾画出以肺气肿为主的和气道疾病为主的表型组。另外,混合疾病组和轻度疾病组的吸烟史与其他组相当。我们还表明,从不同地点获得的QCT指数受扫描仪型号和模型的显著影响,使用专用的标准化模型对提高中心之间的可比性至关重要。CT测量的标准化目前与临床实践无关,但在多中心试验中对COPD患者的正确分类很重要。早前的COPDGene研究[24]。
在“肺气肿主导”,并在我们的COPD人群划定“气道疾病为主的”表型已经是在“粉红河豚”的历史描述识别临床特征和“蓝熏鱼” [25,26),分别。此外,这两个群体与之前使用聚类分析进行表型研究的群体相似[27-29]。在我们的研究中,“肺气肿占主导地位”组的受试者与“气道疾病占主导地位”组相比,有更多的阻塞性肺功能测定,肺体积增加,BMI较低,气体交换障碍更大,TLC和剩余体积(RV)更高。这两组在年龄、疾病严重程度、吸烟和炎症标志物方面具有可比性,这一发现支持了这样一种观点,即对肺气肿发展的遗传易感性可能与对气道疾病发展的易感性不同。当比较这两组的极端亚表型时,这两组的临床特征更加明显。极端表型的定义(E前和一个前)只是基于CT测量,但我们可以表明这些表型与更极端的临床实验室价值观,如FEV1和PØ2(见表S8)。这一概念是为这一特定研究开发的,需要在独立的队列中进行验证。
以往的研究显示[三十-32,我们发现肺气肿严重程度的指数与气道壁增厚呈负相关。虽然这种反向关系似乎表明这两种疾病特征是相对独立的,但我们证明这至少部分是由于吸气量的影响在扫描采集和扫描仪不一致。因此,我们假设,由于在成像过程中吸气水平的提高会导致肺密度的降低和气道扩张的增加,这将导致肺气肿指数的明显恶化,同时也会降低气道壁的明显厚度;相反的变化,将看到一个较低的吸气量成像。因此,肺容积的校正是标准化运动的重要组成部分。
混合组的表型,这是在只有7.7%我们的COPD人口的观察到的,被包括的患者的上叶主要肺气肿和气道壁增厚。这类似于最近描述簇其中castaldi等。[27]被描述为“轻度以上区为主的肺气肿和气流阻塞”。在他们的研究中,这一群人占了他们人口的15%,与“相对耐药”的患者相比,他们更有可能出现病情恶化,更有可能因呼吸问题而去急诊室或住院。在我们的研究中,“混合”组的患者与单独患有肺气肿或气道疾病的患者相比,并没有表现出更大的功能损害。因此,这些特征的组合可能会对功能损伤产生保留作用;然而,还需要进一步的研究来澄清这一发现。
多数病人在我们的研究中被归类为一种“温和” COPD表型在一组。他们证明FEV的相对保值1与QCT气体输送指数以最小的肺气肿改变,气道壁增厚,尽管可比年龄和吸烟史与其他组一致。目前尚不清楚这一表型组是否代表COPD的真正温和的形式或由亚组对异常的风口浪尖主体,谁被“误判”为当前的结果,COPD的常用定义。为了解决这个问题,我们重新分析了我们的数据和更换固定FEV10.7与使用的正常(LLN)的下限截止值/ FVC比[33];“轻度”组中只有68%仍被归类为气流阻塞,这表明在“轻度”组中几乎三分之一的受试者可能没有慢性阻塞性肺病。当比较轻度LLN组和轻度LLN组时,LLN组的TLC和TLCO/Va值与对照组相似,气道阻力明显增加(见表S9)。这个问题可以通过收集纵向数据来确定任何进行性改变,或通过澄清当前关于慢性阻塞性肺病气流阻塞定义的不确定性来解决。
偏回归分析为肺结构的QCT测量与临床参数的相关性提供了进一步的证据。与Martinez等。[32我们观察到标准化肺气肿测量(调整%WA)和BODE(体重指数,气流阻塞,呼吸困难,运动)指数之间的强相关性。的关联,主要是由于肺气肿测量和FEV之间的强相关性1体重指数;然而,在这项研究中,我们没有观察到与6分钟步行病的联系。此外,与以往的研究一致,标准化气道壁测量(按百分比15调整)与6分钟步行距离之间存在关联[32],BMI [34,35]但是不BODE指数[32]。与气体交换的措施相关的两项指数,但只有肺气肿测量负血红蛋白浓度,白细胞计数相关。该协会不能仅仅缺氧并保证在今后的研究中进一步研究来解释。
而在早期的研究中,增加血红蛋白浓度已报告COPD [36],最近的研究报告上下级一起慢性病贫血的线[37]。我们的数据现在表明,血红蛋白的增加,可以在COPD,当正在分析相应的子表型进行检测。注,增加血液中血红蛋白的发现,增加血液中的白细胞在肺气肿为主的患者,但没有对在这两个子表型的病理生理,这已经很明显在此研究早期患者根本区别气道疾病占主导地位的患者点。
在目前的研究中证实了其划定的临床相关性,并由此对肺气肿和气道疾病组,所述的明确定义的临床特点暗示被利用的表型分型的方法的有效性。我们展示的,肺幻影,有不同品牌和型号的扫描仪之间显著不符,即使使用相同的图像采集协议。Using our standardisation methodology we identified the cut-off between “normal” and emphysema as −925.6 HU and for airways disease as 69.3% WA. Further studies are required to establish normal values using a larger population of controls, with comparable age and smoking history. Furthermore, the approach used for standardisation is currently too cumbersome for use in routine clinical practice and will require refinement and further development before it can be applied to routine clinical practice.
这项横断面研究有许多局限性。首先,我们没有招募非常严重的气流阻塞患者,因为支气管镜检查的耐受性对于参与EvA研究至关重要[1]。因此,在本研究中大多数情况下表示GOLD级1和2。因此,发现本文报道的不适用的情况下,COPD的全谱,但主要是相关的轻度至中度COPD组。这是,即使在这种情况下,只有轻度至中度疾病,肺气肿主导和气道疾病,占主导地位的情况下,清晰可辨的兴趣。
其次,它很可能在目前的研究中定义的表型组可以进一步划分,如果我们有更多的包括临床参数(如。肺气肿亚型)和利用聚类分析。然而,确定我们的方法先天的并且不需要对EVA的研究,这是确定emphysema-和航空公司主导的表型的候选易感基因的主要目的,这种程度的详细表型的。然而,这里描述的更大的数据集的方法的应用可以使进一步的表型的划分。
第三,从93名患者的数据被排除主要是由于缺乏合适的成像数据的;尽管有此限制因素,在这组子分析未发现与包括在这项研究中患者的任何显著临床差异。
第四,我们的研究只包括通用电气和西门子的扫描仪获得的CT成像,并在我们的研究中所描述QCT标准化方法是否适用于对其他制造商生产的CT扫描仪成像仍不清楚。
最后,在这项研究中提出的COPD表型的基础上确定全肺密度和一个近端气道的气道形态。各种研究已证明,尽管异质性,右肺上叶段气道近端气道的肺的其余重塑一个很好的替代品[9,38]。然而,目前尚不能确定是否类似的变化将在小气道中可以看出[10]。使用吸气和呼气的扫描,以确定气体捕获,这被认为是小的气道疾病的间接测量,在今后的研究可以帮助如本文所述的来验证COPD表型小气道评估。
总之,目前的研究表明QCT的效用COPD的表型分型,专为肺气肿和呼吸道病子组的划分。QCT的标准化结果表明当成像从不同品牌和型号的扫描器获得的是至关重要的,因为经常发生在多中心研究。据预计,在目前的研究中采用的方法将有利于未来在这两个不同的COPD表型研究。此外,期望的是,这些表型组,并且该方法中,还通过纵向数据的收集,并用生物标志物和基因型的关联的示范验证;这可能会在适当的时候由EVA项目的结果来提供。此外,这将是重要的在未来的研究来确定,以不同的表型是否会表现出不同的结果,相对于病情加重,抗生素的使用,肺功能下降和死亡率。
确认
我们感谢欧洲呼吸协会在启动该项目时给予的支持。188bet官网地址我们要感谢来自华威制造集团的格雷格·吉本斯博士、亚当·兰德和肯·杨教授,他们建造了华威密度测量幻影。
作者贡献:本研究的概念、假设描述和设计:L. Ziegler-Heitbrock, C. Brightling, I. Gut, K. Haeussinger, D. Singh, D. g . Parr;获取数据或对这些信息进行分析和解释:萨勃拉曼尼亚,古普塔,d . Burggraf中华民国vom Silberberg, Heimbeck,硕士Heiss-Neumann, k . Haeussinger c·纽比b·哈格顿诉Raj, d·辛格Kolsum, t,而k . Al-shair n . Luetzen a . Prasse j . Muller-Quernheim g . Benea s Leprotti p . Boschetto d . Gorecka a . Nowinski k . Oniszh w·祖名卡斯特尔·m·哈根Barta,穹顶,j . Strausz t . Greulich c . Vogelmeier境Koczulla,即肠道,j . Hohlfeld t . Welte m . Lavae-Mokhtari l . Ziegler-Heitbrock c . BrightlingD.G.帕尔;在提交前撰写文章或大量参与修改:L. Ziegler-Heitbrock, D. Singh, S. Gupta, D. Burggraf, C. Brightling, D. g . Parr。
脚注
编辑评论:欧元和J2016年48:10-13。
这篇文章有补充资料www.qdcxjkg.com
支持声明:EvA研究是欧盟资助的第七框架计划(FP7)下的项目(#200506)。本文的资助信息已存入FundRef。
利益冲突:可以在本文的网络版旁边找到披露信息www.qdcxjkg.com
- 收到2015年11月11日。
- 公认2016年3月17日。
- 版权所有©ERS 2016