摘要
含有丝分裂剂活化的蛋白激酶(MAPK)途径在Langerhans细胞组织细胞症(LCH)中不断被激活。下游激酶的突变BRAF和MAP2K1介导LCH病变亚群的这种激活。在本研究中,我们试图识别其他可能解释未突变的MAPK激活的突变BRAF和MAP2K1LCH病变。
我们分析了26例肺和37个非玻璃LCH病变,用于存在BRAF,MAP2K1,国家管制当局方面和喀斯特突变。来自10名吸烟者患者的严重正常肺组织用作对照。患者的自发结果同时评估。
BRAFV600E在50%和38%的肺和非玻术LCH病变中观察到突变。患有40%的肺部LCH病灶国家管制当局方面Q61K./R突变,而不国家管制当局方面在非玻术LCH活组织检查中或肺组织对照中鉴定突变。在11分中的七分之一国家管制当局方面Q61K./R- 润肤肺菌病变,BRAFV600E突变也存在。分别对来自同一肺LCH病变的每个cd1a阳性区域进行基因分型,表明这些同时存在BRAF和国家管制当局方面突变由不同的细胞克隆携带。国家管制当局方面Q61K./R突变激活了MAPK和AKT(蛋白激酶B)通路。在单变量分析中,并发的存在BRAFV600E和国家管制当局方面Q61K./R突变与患者结果显着相关。
这些发现强调了……的重要性国家管制当局方面肺部LCH病变的基因分型,因为在这种情况下使用BRAF抑制剂可能导致矛盾的疾病进展。这些患者可能会受益于Mapk激酶抑制剂的治疗方法。
摘要
肺朗格汉斯细胞组织细胞增多症的遗传景观包括反复激活国家管制当局方面Q61突变http://ow.ly/YgsSm
介绍
朗格汉斯细胞组织细胞增多症(LCH)是一种起源不明的罕见疾病,包括一个大的临床范围[1].肺受累常见于年轻的成年吸烟者,并表现出不同的结果[2- - - - - -4].丝裂原激活蛋白激酶(MAPK)途径的改变参与LCH的发病机制[5].MAPK途径对于致癌信号传导至关重要,从激活生长因子受体的激活,导致细胞增殖和生存。用RA的激活开始MAPK途径,然后刺激下游激酶RAF,MAPK激酶(MEK1 / 2)和细胞外信号调节激酶(ERK1 / 2)[5](在线补充图S1)。体激活BRAFV600E30-60%的病例在LCH病变中发现突变,包括肺LCH (PLCH) [6- - - - - -12.].BRAF- 激活突变对肺炎的渐进病例中使用BRAF抑制剂(BRAFI)治疗产生了兴趣[5,6,13.].重要的是,MEK / ERK途径独立于病变的激活BRAF提示LCH中MAPK通路激活可能涉及其他机制[6].最近,在MAP2K1(Mek家族的成员)以15-50%的人确定BRAF野生型(WT)非肺LCH病变,从而解释了这些病例中的MAPK通路激活[14.- - - - - -16.].据报道了MAPK途径中其他突变的个体病例[15.,17.].然而,仍然核查额外的机制以解释在没有识别突变的基本LCH病变中的MAPK途径激活。
RAS家族的突变,MEK/ERK上游的小GTPases,能够激活MAPK通路[18.].因此,我们筛选出存在国家管制当局方面- - -喀斯特-在一系列肺LCH活检中激活突变,并与非肺LCH病变的结果进行比较。引人注目的是,而不是国家管制当局方面我们鉴定出突变存在于非玻利菌菌病变中国家管制当局方面Q61K./RPLCH病变的一个重要子集的突变。我们还评估了它们的功能后果,并寻求与患者预后的联系。
材料和方法
禄思伟活组织检查
评估了来自Plch患者的26个外科肺活检。介绍了这些患者和随访期间这些患者的特征表1.在最后一次随访时评估PLCH的预后,根据呼吸困难的变化(由纽约心脏协会(NYHA)分期评估)和之前描述的肺功能,将患者分为改善或持续(稳定)或进展性疾病[4].没有患者接受任何对肺部肺粉的治疗方法。还研究了从患者中获得的37个非玻硫蛋白酶患者,但也研究了患者患者。对于五名患者,可获得两种活组织检查部位(肺和另一个位点N = 4,骨和淋巴结n = 1)。在线补充表S1中介绍了LCH患者的整个研究人群的特征。
该研究是根据赫尔辛基宣言进行的,并得到了法国巴黎(13-130)INSERM机构审查委员会和伦理委员会的批准。所有患者均提供知情同意。
加工LCH组织
福尔马林固定、石蜡包埋(FFPE)活检评估是否存在cd1a阳性结节,并进行宏观解剖进行分子生物学分析。为了确保分析标本中始终存在CD1a阳性细胞,每10次连续组织切片进行CD1a免疫染色。
肺组织控制
在PLCH病变边界清楚的情况下,周围的肺组织包含<1%的cd1a阳性细胞作为内对照。
10例吸烟者(6例男性,中位数(四分位范围(IQR))年龄64岁(59-68岁),在进行局部肺癌(腺癌9例,鳞状细胞癌1例)胸外科手术时获得了大体正常的肺组织,并进行了分析。光镜下,这些标本表现出肺泡壁轻微的纤维化改变,色素负载巨噬细胞的聚集和肺泡上皮增生。
分子分析
根据制造商的协议,使用来自五个10-μm部分(Qiagen,Les Ulis,France)的FFPE组织的QIAAMP DNA FFPE组织试剂盒提取DNA。DNA使用Nanodrop ND-1000分光光度计(Nanodrop Technologies,Wilmington,De,USA)符合QUATIOMIED使用Qubit®2.0荧光计(Life Technologies,Saint-Aubin,France)量化。
BRAF,国家管制当局方面和喀斯特基因分型使用焦肌,高分辨率熔融(HRM)进行,增强冰-COLD-PCR(改进和完全富集共扩增在较低的变性温度PCR;E -冰-COLD-PCR) [19.,20.].MAP2K1采用Sanger测序进行基因分型[14.].
发酵杆菌
通过使用Pyromark-Q96 MD派塞术(Qiagen,Hilden,德国)进行基因分型进行突变检测,鉴定和定量。使用Pyromark-Q96真空工作站(QIAGEN)纯化PCR产物并使单链进行单链[19.].
高分辨率熔化
BRAF和国家管制当局方面人力资源管理分析是根据制造商的协议在LightCycler 480 (Roche, Boulogne-Billancourt,法国)上使用LC480人力资源管理扫描主机进行的[19.].
E-ice-COLD-PCR
突变的敏感性检测国家管制当局方面密码子12 13 61,BRAF600密码子,喀斯特密码子12和13由E-冰-Cold-PCR在LightCycler 480(Roche Applical Science,Penzberg,德国)中进行。反应含有20nmBRAFV600 50纳米国家管制当局方面Q61或40 nM喀斯特G12和G13阻滞剂探针[19.- - - - - -21.].为了国家管制当局方面使用G12和G13测定,使用200nm前进(Aatta accctgattactG)和反向(Biotin-GgatcattactcatcatacaA)引物,2μmsyto9和20nm嵌体探针(Gcgcttttccaac + A + C + C + C + C + C + C + C + C + C + C + C + C + C + C + C + C + C + C + C + C + C + C + C + C + C + C + C + C + C + C磷酸)。
通过焦磷酸测序进行突变检测、鉴定和定量。突变等位基因频率(即。等位基因的相对频率)以百分比表示。检测限为突变等位基因的0.1%。通过E-富集突变后,估计每个样本的突变百分比冰- 使用标准曲线的-Cold-PCR,包括以下突变分数:5%,1%,0.5%和0.1%(使用的细胞系:G-361BRAF, SW480喀斯特,HL-60为国家管制当局方面密码子61和THP-1国家管制当局方面密码子12/13)。
桑格测序
MAP2K1基因分型采用外显子2和3的双向Sanger测序,如Brown.等.[14.].使用BigDye Terminator version 1.1测序试剂盒(Applied Biosystems, Foster City, CA, USA)和3130xl DNA分析仪(Applied Biosystems)对DNA进行测序。
免疫组织化学
本研究使用了以下单克隆抗体:anti-CD1a(克隆O10;Dako, Eching,德国),反-BRAFV600E(克隆VE1;anti-phospho-ERK (pERK)-1/2(克隆MAPK-YT;Sigma,里昂,法国)和抗磷酸化蛋白激酶B (phospho-AKT) (Ser473)(克隆D9E-XP;Cell Signaling, Saint Quentin Yvelines,法国)。最近描述的NRASQ61R抗体(克隆SP174;(Spring Biosciences)用于评估NRAS表达Q61R蛋白质(22.].BRAFV600E- - -国家管制当局方面Q61K./R- 用化的黑色素瘤被用作阳性对照。
免疫球蛋白同型对照用来评估非特异性结合。如前所述,对连续切片进行免疫组化(IHC) [23.使用Vectastain abc碱性磷酸酶或过氧化物酶系统(Vector, Burlingame, CA, USA)。对于pERK表达,通过比较cd1a阳性细胞与最强烈染色的黑色素瘤作为阳性对照的染色强度,得出每个样本的半定量染色评分,从-(缺失)到+++(强烈阳性)。当活肿瘤细胞显示清晰的细胞质染色时,VE1抗体染色为阳性。孤立核染色、单个分散细胞弱染色、微弱弥漫性染色或单核/巨噬细胞染色均为阴性[24.].免疫染色评分由经验丰富的病理学家(v.M.)进行,该病理学家尚不知识了病变的突变状态。
免疫荧光
将抗CD1A抗体施用于FFPE PLCH组织切片,其次是Alexa Fluor 568-缀合的驴抗小鼠抗体(Life Technologies)。随后,抗NRASQ61R使用抗体,然后使用Alexa Fluor 488标记的山羊抗兔抗体(Life Technologies)。核用4,6-二氨基-2-苯基吲哚(DAPI;向量)。使用激光扫描共聚焦显微镜(徕卡激光技术,海德堡,德国)获得图像。
原位邻近连接试验
组织切片原位使用Duolink检测试剂盒(Olink Bioscience, Uppsala, Sweden),根据之前描述的制造商说明书,接近连接分析(PLA) [25.].简单地说,切片被阻断,用针对CRAF (CliniSciences, Nanterre, France)和BRAF (Santa Cruz Biotechnology, Nanterre, France)的抗体孵育,然后用PLA探针孵育,PLA探针是与独特的寡核苷酸结合的二抗(抗小鼠和抗兔)。寡核苷酸的环化和连接之后是扩增步骤。在这项实验中,一对寡核苷酸标记的二抗(PLA探针)仅在紧密结合时产生信号,从而允许检测蛋白-蛋白相互作用。使用激光扫描共聚焦显微镜(徕卡激光技术)将蛋白质复合物可视化为明亮的荧光信号(红点)。为了对PLA信号进行量化,使用ImageJ软件(http://imagej.nih.gov/ij/),每个病灶至少分析三张图片[26.].
统计分析
描述性摘要统计,即。分类变量的百分比,平均值±SD.计算定量变量的中位数(IQR)值。进行kruskal-wallis测试以比较PLA点的分布根据突变状态。使用精确的Fisher试验进行了根据随访期间持久性或吸烟的患者结果类别(改善,稳定或渐进疾病)的比较。
诊断患者特征的预测值,包括BRAF和国家管制当局方面突变,患者结果(显着改进相对通过单变量和多变量和多变量的逻辑回归模型来评估非可处生性,其中每种特征与结果之间的关联强度(95%CI)测量。多变量型号包括基于10%级别的单变量分析的结果相关的所有变量。只选择逐步选择过程所保留的那些变量,在5%水平。
所有统计分析使用SAS版本9.3 (SAS, Cary, NC, USA)和R版本3.0.2 (www.R-project.org).
结果
PLCH病变的BRAF和MAP2K1状态
纳入研究的PLCH患者的特点见表1.BRAFV600E通过焦磷酸测序和E-冰-Cold PCR在CD1A阳性细胞浓缩区域中的26个样品中的13(50%)(表2).BRAFV600EIHC中的11个(85%)中也鉴定出蛋白质的13个BRAFV600E通过基因分型检测的案例(图1和表2).
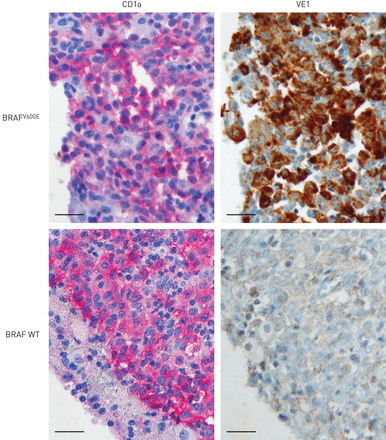
对同一标本连续组织切片进行免疫染色。CD1a和VE1在aBRAFV600E-突变(病人1)BRAF野生型(WT)(患者17)肺朗格汉斯细胞组织细胞增多症(PLCH)标本。天平条:20µm。对26例PLCH病变进行分析。
作为MAP2K1相互排斥的突变BRAFV600E在非肺LCH病变中发现突变[14.- - - - - -16.[我们测试了在犁氏病变中存在这些突变。在13中BRAFwt plch病变,三个(23%)标本表现出来MAP2K1C121S突变(表2).
在所有分析的情况下,MAPK途径被激活,尽管在可变强度,如Perk IHC评估(表2和在线补充图S2)。
PLCH病变中的NRAS突变
鉴于MAPK途径激活也被观察到BRAF和MAP2K1WT组织,我们评估了PLCH病变是否含有体细胞突变国家管制当局方面或喀斯特可能解释MAPK激活。对26个PLCH病灶进行筛查国家管制当局方面G12/13和Q61和喀斯特使用焦磷酸测序和HRM分析G12/13突变。26例PLCH病灶中,4例表现为a国家管制当局方面Q61R/K突变。使用E -冰-COLD-PCR,克隆国家管制当局方面在七种案例中鉴定了Q61突变,这是国家管制当局方面使用标准技术。因此,国家管制当局方面26个PLCH病灶中有11个(42%)出现突变(表2).相比之下,没有一个庞大的病变表现出了国家管制当局方面G12或G13突变,只有一个病变对此呈阳性喀斯特G12S突变(患者15),虽然在E-检测的极限水平冰-COLD-PCR。
对于六个PLCH样本,LCH病变很好地限制,并且周围的肺组织含有<1%的CD1A阳性细胞。在这些标本中,两个庞大的病变被忽视了一个国家管制当局方面Q61K.A.国家管制当局方面Q61R分别突变。有趣的是,没有国家管制当局方面在这两个标本周围的肺组织中检测到突变,甚至用E-冰-COLD-PCR。
为进一步证明国家管制当局方面Q61RLCH cd1a阳性细胞特异性地携带突变,我们对切片进行了系列免疫染色,以及双免疫荧光和共聚焦显微镜下与最近描述的抗NRAS抗体Q61R蛋白质(22.].如图所示图2,我们可以展示特定的nrasQ61Rcd1a阳性细胞免疫染色国家管制当局方面Q61R突变PLCH病变。
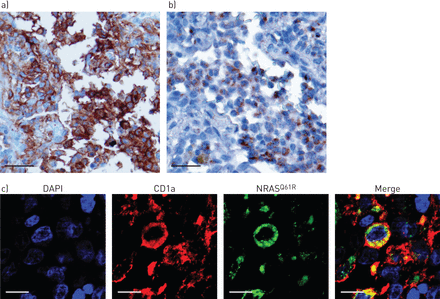
国家管制当局方面的表达Q61R蛋白质国家管制当局方面Q61R突变的肺朗格汉斯细胞组织细胞增多症(PLCH)病变。a) CD1a表达;b)抗nras免疫染色Q61R在连续组织切片上进行蛋白质抗体。秤栏:30μm。c)Anfucofoorescess染色的共聚焦显微镜图像国家管制当局方面Q61R-突变PLCH病变用4,6-二氨基-2-苯基吲哚(DAPI)(蓝色)、抗cd1a(红色)和抗nras染色Q61R抗体(绿色),以及所有三种染色的合并图像。天平条:20µm。所有面板都显示了这两种模式的代表性图像国家管制当局方面Q61R-突变病变(患者7和10)。
作为国家管制当局方面在非玻利菌菌病变中未描述突变,我们在19骨,13个皮肤和五个淋巴结LCH活检中测试了这些突变的存在。国家管制当局方面在任何情况下未检测到突变,甚至没有通过e-冰-COLD-PCR。相比之下,BRAFV600E38%的样本中发现了突变。值得注意的是,在四名同时提供肺活检和非肺LCH组织标本的患者中,一名患者(患者25;表2怀有一个国家管制当局方面Q61K.他的PLCH病变发生突变,而皮肤LCH病变是国家管制当局方面wt。
最后,由于PLCH几乎只发生在吸烟者中,我们还对10例吸烟者的对照肺组织标本进行基因分型,以评估吸烟的作用本身最后的存在国家管制当局方面肺部的突变。没有国家管制当局方面在任何这些样本中检测到突变。
并发BRAFV600E和nras.Q61K./ R肺部LCH病变中的突变
在11国家管制当局方面-突变的PLCH病变,7个都有BRAFV600E和国家管制当局方面Q61K./R观察到的等位基因频率突变有利于在这些病变中存在克隆异质性(表2).相比之下,没有MAP2K1在中观察到并发突变国家管制当局方面-突变PLCH病变(表2).
进一步研究BRAFV600E和国家管制当局方面Q61K./R在相同的PLCH样本中发现的并发突变是不同的组织细胞克隆的结果,通过分别基因分析每个CD1A阳性区域,在其中的五个病例中分析了第二个肺活检嵌段。在这些情况下,同一标本中的每个焦点CD1A阳性区域也覆盖BRAFV600E或国家管制当局方面Q61K./R单独或同时发生突变(图3.和表3).有趣的是,五种情况中有三种国家管制当局方面Q61K./R突变仅通过e-初始检测冰-COLD-PCR,这些突变通过焦磷酸测序分别在cd1a阳性基因型区域(表2和3.).这些发现有力地表明BRAFV600E和国家管制当局方面Q61K./R26个PLCH病变中有7个(27%)的突变是亚克隆的(即。不存在于整个肿瘤细胞的群体中,并由不同的CD1A阳性克隆群体携带。
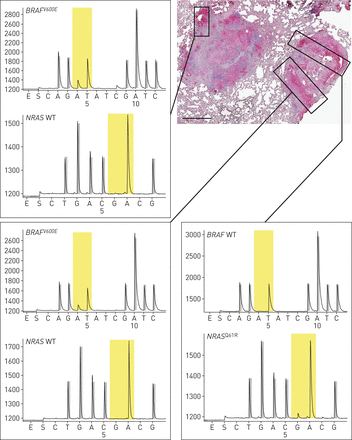
BRAFV600 /国家管制当局方面Q61肺朗格汉斯细胞组织细胞症(PLCH)病变中的克隆异质性。不同的CD1A阳性区域是单独基因分型的BRAF和国家管制当局方面突变(病人10)。热解色谱图的BRAFV600E和国家管制当局方面Q61R突变。每个序列来自相应的病变区域。分析了来自三种PLCH病变(7,10和12款)的不同CD1A阳性区域。秤栏:1.5毫米。
NRAS突变在PLCH病变中的功能后果
国家管制当局方面-激活突变已被证明可诱导BRAF和CRAF异二聚,导致MAPK通路激活[27.].使用原位PLA具有CRAF和BRAF抗体的组合,我们可以检测庞的病变窝藏中的强杂杂化物(表达为每核的红色点数)国家管制当局方面Q61K./R突变:单独突变32 (21-41);N =3例,22例,23例,25例)或并发BRAFV600E突变(38(30-47); n = 3,患者3,4和7),与...相比BRAFV600E/国家管制当局方面WT (11 (3 - 14);N =3,患者1,5和6)或BRAFwt /国家管制当局方面WT(2(2-3); n = 3,患者15,17和20)病变(P <0.0001;图4.在线补充图S3)。
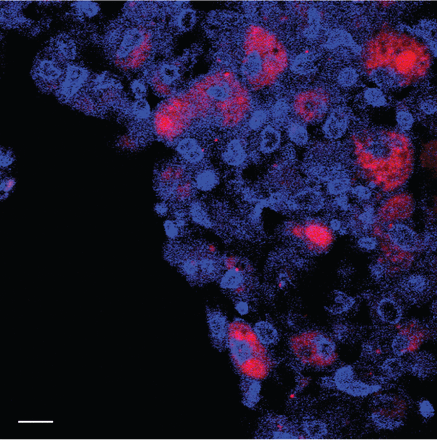
原位邻近结扎测定(PLA)证明BRAF-CRAF二聚化在国家管制当局方面Q61K.-突变病变(患者23)。BRAF-CRAF异质二聚体被可视化为红点原位聚乳酸和荧光显微镜检测;细胞核用4,6-二氨基-2-苯基吲哚(蓝色)染色。比例尺= 10µm。
作为致癌RAS是潜在的磷脂酰阳性3-激酶/ AKT信号轴活化剂[28.,29.],我们通过免疫组化检测了AKT在4个PLCH病灶中是否存在国家管制当局方面Q61单独突变。在所有分析的情况下观察到AKT途径激活,尽管具有可变强度(在线补充图S4)。
NRAS突变与临床结果的关联
吸烟的数量(包年)与是否存在国家管制当局方面突变(p = 0.67)。12例PLCH患者(46%)随访期间停止吸烟(表1).然而,虽然戒烟患者改善的比例较高,但PLCH随访中根据吸烟状况的分布差异无统计学意义(p=0.24)。
在单变量分析中,两者之间没有关联BRAFV600E单独突变和患者结果(P = 0.24;表4).有4个变量与随访期间PLCH在10%水平上的自发改善有关,其中NYHA期呼吸困难为阳性(p=0.08), 1秒用力呼气量为阴性(FEV)1) (p=0.10),则存在国家管制当局方面Q61K./R突变(p=0.05),两者均存在国家管制当局方面Q61K./R和BRAFV600E突变(p = 0.048)。然而,在多变量分析中,纳入NYHA期呼吸困难和FEV后1在基线,两者的存在国家管制当局方面Q61K./R和BRAFV600E突变不再具有统计学意义(p=0.07)。
讨论
在本研究中,我们证实了MAPK信号通路在PLCH病变中不断被激活,正如之前在非肺LCH标本中所证实的[6].可以通过存在的存在来解释这种激活BRAFV600E研究了50%的肺部LCH活检中的体细胞突变。这种患病率符合以前的研究中观察到的[6- - - - - -12.].我们还发现了MAP2K1C121S突变,这可能解释了20%的MAPK通路激活BRAFWT PLCH病变。
我们研究的主要发现是复发性的存在国家管制当局方面Q61K./R突变(即。在40%的PLCH标本中使用了标准焦磷酸测序和高灵敏度E-测序冰-COLD-PCR。应该强调的是国家管制当局方面Q61K./R最初仅通过e-检测到突变冰当基因分型专门集中在单独的cd1a阳性区域时,-COLD-PCR很容易通过焦磷酸测序进行鉴定,这强烈表明国家管制当局方面PLCH细胞携带突变等位基因。一致,使用E -冰-COLD-PCR,我们无法检测国家管制当局方面周围肺组织中cd1a阳性细胞<1%国家管制当局方面Q61K./R突变PLCH病变。最后,我们清楚地表明了nrasQ61R突变蛋白确实位于cd1a阳性细胞内。
虽然国家管制当局方面Q61K./R埃德姆 - 切斯特病报告了体细胞突变[30.,31.],这些突变以前未在LCH病变中发现[6,14.,15.].一直以来,我们都没有发现国家管制当局方面任何非肺性LCH病变的突变,甚至通过E-冰-COLD-PCR。有趣的是,在一个患者中,一个国家管制当局方面Q61K.在PLCH病变中发现突变,而未发现国家管制当局方面使用相同的基因分型技术在他的皮肤病病变中检测到突变。一起参加国家管制当局方面Q61K./R突变似乎是LCH肺受累的一个特殊特征。
为什么之前的两项研究在PLCH患者的病变中进行了大规模的靶向基因分型没有检测到国家管制当局方面突变尚不清楚[6,12.].除了对少数病例进行了分析,正如我们的研究所显示的,PLCH病变内部的异质性可能解释了这些差异。
虽然Plch几乎完全在吸烟者中出现,但吸烟并不自己解释发生的国家管制当局方面突变。事实上,我们没有在吸烟对照组的肺样本中检测到这些突变。
这项研究的另一个重要发现是识别并发国家管制当局方面Q61K./R50%的突变BRAFV600E突变PLCH病变。虽然BRAF和国家管制当局方面突变通常是相互排斥的,这两种突变最近在多发性骨髓瘤和黑色素瘤中被发现,支持这些肿瘤的克隆异质性[32.- - - - - -36.].当同时检测到这两个突变时,一个在低频处处于高频和另一个突变时[32.],这也是我们研究的大多数分析案件的情况。在这里,我们也证明了这一点BRAF和国家管制当局方面突变可能存在于同一肺活检的不同区域中,清楚地证明了患有不同的细胞克隆国家管制当局方面和/或BRAF突变。在这方面,浸润非肺LCH病灶的cd1a阳性细胞被证明是克隆起源[37.), Y舒服等.[38.[在大多数斑的情况下,这些细胞在多克隆中是多克隆的。本研究的结果进一步支持PLCH中LCH细胞的多克隆性质。
在单变量分析中,病变同时存在的患者国家管制当局方面Q61K./R和BRAFV600E突变,但不是国家管制当局方面Q61K./R或BRAFV600E只有突变,表现出较差的自发结果。需要对更大的PLCH患者进行更多的研究来证实这一发现,因为该关联在多变量分析中被消除了。
的发现BRAFV600E在LCH病变中铺平了使用BRAFI的方式(如。vemurafenib)进行渐进病例[13.,39.,40].犁病变的事实国家管制当局方面突变显示MAPK和AKT信号通路同时激活,这强调了在PLCH病变同时发生MAPK和AKT突变的患者中谨慎使用BRAFi治疗的必要性BRAF和国家管制当局方面,因为可能出现耐药性或似是而非的疾病进展[28.,29.].已经显示了在Brafi处理期间获得的电阻机制涉及多个信号通路,包括国家管制当局方面突变(28.,29.].在这方面,两者的共同发生BRAFV600E- - -国家管制当局方面Q61K.-在vemurafenib治疗进展性疾病的黑色素瘤患者的细胞中发现了激活突变[28.].在RAS激活足够水平的细胞中,RAF形成活化的二聚体。BRAFi结合到RAF二聚体的一个成员导致另一个的反式激活,并诱导ERK信号的激活,从而刺激肿瘤增殖[41.].
综上所述,本研究为LCH中MAPK通路的激活提供了进一步的认识。我们的发现也强调了国家管制当局方面PLCH病变的基因分型。PLCH中含有a国家管制当局方面突变可能受益于MEK抑制剂(MEKi)治疗[42.,或者选择BRAFi和MEKi联合治疗BRAF/国家管制当局方面-突变病例,正如最近所指出的[43.].
致谢
作者感谢Giorgia egidi - maskos博士(INRA, Jouy en Josas, France)为pERK和pAKT IHC提供服务;Silvina Dos Reis Tavares, Aurélie Sadoux, Maeva Valluci和Farah Khayati (Hôpital Saint-Louis, Paris, France)获得技术支持;Hôpital圣路易肿瘤生物银行,用于管理患者生物样本;伊丽莎白·萨瓦里奥(Elisabeth Savariau, Institut Universitaire d'Hématologie, Service d’infographie, Hôpital Saint-Louis, Paris, France),以感谢她对这些数据的帮助。
脚注
编辑评论in.欧元和J2016;47: 1629 - 1631。
本文提供了补充材料www.qdcxjkg.com.
支持声明:作者感谢Legs Poix (Chancellerie des Universités)和Fonds de Dotation Recherche en Santé respiratory的支持。本文的资金信息已存入FundRef.
利益冲突:可以在本文的在线版本旁找到披露www.qdcxjkg.com.
- 收到了2015年10月9日。
- 接受2016年2月11日。
- 版权©2016人队