摘要
C-TB,一部小说结核分枝杆菌6-kDa早期分泌抗原靶蛋白/10-kDa培养滤液蛋白(ESAT-6/CFP-10)特异性皮肤试验,对接种卡介苗健康对照具有较高的特异性。然而,C-Tb的敏感性迄今尚未确定。目的是与结核菌素皮肤试验(TST)和QuantiFERON-TB金管试验(QFT-GIT)比较,确定活动性结核病(TB)患者C-Tb的敏感性。
对253例合并或未合并HIV感染的活动性结核病患者,采用双盲法随机给予C-Tb和TST给药。皮试前进行QFT-GIT测试。
使用接收器操作特性曲线衍生切点5mm,C-TB敏感性类似于QFT-Git(73.9(95%CI 67.8-79.3)与75.1(95%CI 69.3-80.2)),艾滋病毒感染和艾滋病毒无感染患者(76.7(95%CI 69.0-83.3)与69.5(95%CI 59.2-78.5))。然而,艾滋病毒感染患者的CD4计数<100细胞·mm的患者中,敏感性显着降低3.C-TB和QFT-GIT组合的敏感性显着高于C-TB(P <0.0001)。C-TB无明显不良事件是安全的。5 mm切割点对应于先前公布的特异性研究(TESEC-04)中发现的点。
C-Tb与QFT-GIT的诊断敏感性相似结核分枝杆菌感染。敏感性仅在严重免疫抑制的hiv感染患者中降低。需要在不同的环境下进行进一步的研究,以验证拟议的5毫米切割点。
摘要
C-Tb与QFT-GIT的诊断敏感性相似结核分枝杆菌感染http://ow.ly/TtFf6
介绍
与活动性结核病(TB)患者不同,潜伏性结核病感染(LTBI)患者无症状,没有活动性疾病的放射学征象,而且无法从微生物学上检测痰液或其他生物样本中的细菌。发现和治疗LTBI对彻底根除结核病至关重要[1那2].目前诊断推定LTBI的唯一方法是通过检测宿主免疫应答结核分枝杆菌的衍生抗原,从而间接推断先前或目前存在分枝杆菌[3.那4.].这种方法已被用于使用纯化的蛋白质衍生物(PPD) - 相关的结核蛋白皮肤测试(TST)来推断LTBI的存在。PPD TST易于使用,但是在用Bacille Calmette-guerin(BCG)疫苗接种的个体中可能发生假阳性反应,特别是在出生后的婴儿,或在感染不泛滥的分枝杆菌的个体中[5.].
要解决此缺点,两种可商购在体外免疫降压测定(Quantiferon-Tb金管(QFT-git; Cellestis / Qiagen,Venlo,荷兰)和T-Spot。结核病(牛津免疫技术公司,阿宾顿,英国))。他们询问效应t细胞对两种免疫原性的反应结核分枝杆菌抗原,IE。6-KDA早期分泌物抗原靶(ESTA-6)和10-KDA培养滤液蛋白(CFP-10),其仅在几个分枝杆菌中存在结核分枝杆菌(例如marinum分枝杆菌那kansasii kansasii.等),并且在全世界使用的卡介苗毒株中均未发现[6.-9.].然而,这些检测费用昂贵,需要进行抽血(儿童和一些成人在技术上很困难),并将样本运送到具备所需设备和基础设施的实验室(如。ELISPOT和ELISA阅读器),并向外围医疗中心报告结果。这两种测试都显示有很高的复发率[10].
因此需要更简单和更友好的测试。这一未被满足的需求现在随着新型C-Tb的发展而得到了解决结核分枝杆菌-含ESAT-6和CFP-10抗原的特异性皮肤试验[11-13].中国和俄罗斯也生产了其他版本[14那15].C-TB皮肤测试可由健康服务用于测试结核分枝杆菌与TST完全相同的方法,但没有不理想的特异性。先前的两项临床试验发现,C-Tb在健康受试者和活动性结核病患者中都是安全且耐受性良好的[12那13(TESEC-01, -02和-03)。为了确定C-Tb的最佳切点,在英国151名假定未感染和接种卡介苗的健康成人中进行了一项特异性试验。这证实了与TST相比,C-Tb具有更高的特异性[13].
在这里,我们报告了TB患者的敏感性试验结果,活跃的TB曾用作替代与之前接触的替代品结核分枝杆菌.主要目的是提供C-Tb的敏感性数据,结合之前发表的特异性数据,可以得出C-Tb的最佳切点。
材料和方法
试验设计
合格的参与者是18-65岁的艾滋病毒感染者或未感染者,最近诊断为活动性结核病。该试验从4月到2011年12月在Langa,Gugulethu,Chapel Street,Du中午,表景,南非,南非,南非州开普敦南部,海风,莲花河,Phillipi,Retreat和Manenberg诊所。在访问1,参与者被评估了资格,获得了知情同意,并进行了医学检查,包括用于安全实验室测试和QFT-Git的血液取样。所有参与者在其另一个臂中以双盲方式接收一个臂和TST 0.1ml(21μm(Tu)结核蛋白PPD RT 23 SSI)的C-Tb 0.1ml(0.1μg)。用于每个干预的手臂随机化。在2-3天(参见2)后读出注射部位的硬结反应,并以毫米(mm)记录。没有硬化的情况被记录为0 mm。最后一次随访(参观3)于28天安排,并包括用于安全实验室测试的体检和血液采样。招聘和特定的ARM-的随机化是与联盟指南保持一致[16].
伦理批准
审判由血清INSTITUT赞助(www.clinicaltrials.gov.:nct01241188.;TESEC-04),受卫生科学伦理委员会,开普敦,南非(参考号515/2010)和南非药物控制委员会的批准。该试验是根据良好的临床实践原则和世界医学协会(WMA)宣布第18届WMA大会,赫尔辛基,芬兰,1964年和随后的修正案所采用的赫尔辛基宣言。
安全评估
在注射后1小时和试验人员随访时,对不良事件进行评估并记录在日记中。所有不良事件的强度、与皮试的相关性、结果和试验方案中所述的严重程度都进行了评估。试验现场使用的超出正常范围的安全实验室检测被记录为不良事件。所有不良事件根据研究者的原始描述进行编码,以MedDRA版本14.1的首选术语最低水平术语和系统器官分类(www.meddra.org).成立了一个数据安全监测委员会,由三名独立的高级临床医生组成,其职能是就参与者的安全问题向首席研究员提供专家建议。
C-TB和PPD TST
C-Tb由Statens血清研究所(哥本哈根,丹麦)根据gmp标准生产,作为重组ESAT-6和CFP-10的溶液,以重量比1:1混合。两种抗原均克隆表达Lactococcus lactis[17].结核菌素PPD RT 23 SSI 2tu /0.1 mL (Statens Serum Institut)用于PPD TST。C-Tb和PPD TST均经Mantoux技术皮内注射,如前所述[12那17].在≥5、≥10和≥15 mm的切点评估PPD TST反应。
QFT-GIT测试
QFT-GIT测试是根据制造商的说明进行和分析的。在C-Tb和PPD TST治疗前,在来访1进行QFT-GIT检测的血液取样。
统计数据
使用SAS JMP进行统计分析(www.jmp.com.),或Prism 6或GraphPad在线统计软件(www.graphpad.com).
结果
审判人口
合格的参与者是18-65岁的艾滋病毒感染者或未感染者,最近诊断为活动性结核病。258名志愿者被筛选,253名参与者被纳入试验(图1).非资格的原因是使用泼尼松龙,TB治疗> 2周,结核复发和母乳喂养。在253中,153个艾滋病毒未感染,100名艾滋病毒感染。
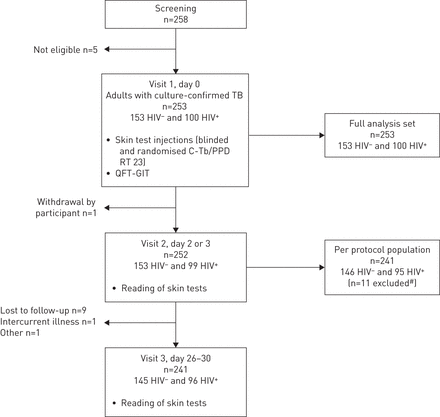
试验程序和试验人群流程图。结核病:肺结核;QFT-GIT: QuantiFERON-TB金管。#:排除的原因是各方案人口的原因是主要的协议偏差,包括注射失败(n = 2),未经证实的TB诊断(n = 6),注射衰竭和未经证实的TB诊断(n = 1),使用免疫抑制药物(n = 1)或第二次访问访问窗口(n = 1)。
所有HIV-uninfected参与者在TB治疗中进行了最近诊断的活性TB,通过至少一种正痰涂片显微镜或阳性培养结果证实。所有艾滋病毒感染的参与者(通过阳性快速测试证实的HIV感染或通过阳性enzygnost抗HIV-1/2加elisa的一个正快速试验)都是在TB治疗中,用于最近诊断的活性TB,根据TB的临床图像南非指南。没有参与者在包含时接受了> 2周的结核病治疗。所有253名参与者都包含在安全分析中。一名参与者在第二次访问前退出了审判。每种议定书群体中共有241名参与者(95艾滋病毒感染和146个艾滋病毒,用于免疫应答分析。由于主要的协议偏差,11名参与者被排除在每个议定书中。
人口统计学
大多数基线特征对于艾滋病毒无感染和艾滋病毒感染的患者的患者类似的是,艾滋病毒感染的人群包括更高比例的女性,非洲血统和负痰涂片显微镜结果(表1).C-TB硬化大小之间没有显着相关性与年龄或性别(Logistic回归,数据未显示)。
C-TB,TST和QFT-GIT反应的幅度
中位C-TB响应为23毫米(95%CI 20-25;所有参与者中的23毫米(IQR)0-34),23毫米(95%CI 20-26; IQR 10-33)在艾滋病毒 - 未感染和22 mm(95%CI 18-25; IQR 0-34)在艾滋病毒感染(图2 a - c).中位TST反应为25 mm (95% CI: 23-26;IQR 19-30)在所有参与者中,25 mm (95% CI 24-28;IQR 21-31)和24 mm (95% CI 19-25;IQR 15-29)的hiv感染者(图2D和f).在HIV感染和HIV-未染色的C-TB或TST分布之间没有显着差异(p = 0.3452和p = 0.1348)。QFT-GIT中位反应为2.3 IU·ml-1未感染艾滋病毒者和已感染艾滋病毒者(网上补充图S5)。C-Tb应答与TST呈正相关(未感染艾滋病毒者的Spearman评分r=0.6442,感染艾滋病毒者的Spearman评分r=0.7253;p<0.0001)和QFT-GIT反应(r=0.4897在hiv未感染和r=0.5977在hiv感染;p < 0.0001)。
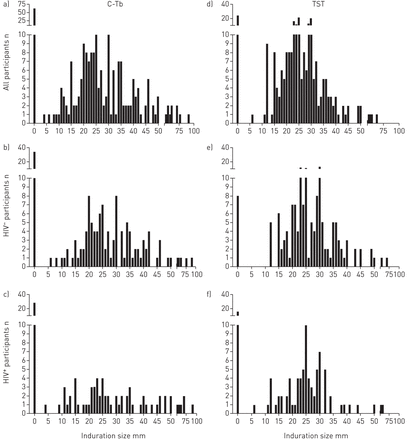
a) c - tb和d - f)结核菌素皮肤试验(TST)的硬化大小a, d)所有按方案人口的参与者(n=241), b, e) hiv未感染参与者(n=146)和c, f) hiv感染参与者(n=95)。每条黑色的条形代表在给定硬度下的参与者人数。注意x轴在50毫米处分裂。
C-TB截止点分析
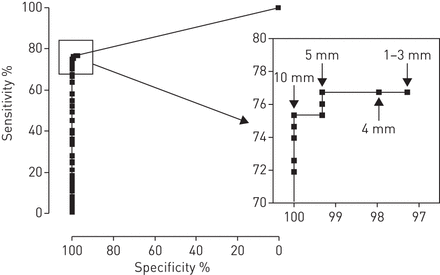
通过受试者工作特征(ROC)曲线分析,确定了C-Tb试验阳性的切点。ROC曲线分析比较了146名未感染hiv的确诊结核病患者和147名之前发表的特异性试验中接种过bcg的健康对照者的C-Tb硬化反应(数据见在线补充图S6) [13].曲线下的面积为0.88,建议≥5mm,为C-TB的最佳截止(图3.).随后将艾滋病毒感染的参与者进入分析中产生相同的结果(未示出)。在所有后续分析中使用C-TB≥5mm切割点。≥5mm的C-TB特异性为99.3%(95%CI 96.0-100),如a报道Ggerbeck.et al。[13].
C-TB接收器操作特征(ROC)曲线显示依赖于测试切割点的灵敏度和伴随特异性之间的关系。每个黑色方块表示从0到65mm的给定切点处的灵敏度和特异性。ROC曲线基于每种议定书群体的146名艾滋病毒无感染者参与者的数据,147名艾滋病毒无感染的Bacille Calmette-Guerin接种的健康治疗健康对照,从前发表的特异性试验[13](在线补充图S6)。为了澄清,部分曲线被放大。最佳切割点为5mm。
C-Tb、TST、QFT-GIT的敏感性
C-Tb总体敏感性为73.9% (95% CI 67.8-79.3),在hiv感染和hiv未感染参与者中相似(76.7% (95% CI 69.0-83.3)与69.5% (95% ci 59.2-78.5);p = 0.232)。C-Tb和QFT-GIT的阳性检测结果具有可比性(73.9%)与在所有参与者中分组的75.1%)以及艾滋病毒无育和艾滋病毒感染。在所有参与者中,TST比C-TB和QFT-Git在所有参与者中的敏感性更高,以及在艾滋病毒未感染和艾滋病毒感染之间的分裂时(表2).19名参与者(7.9%)患有不确定的QFT-GIT结果(13个HIV-未感染和六个艾滋病毒感染;在线补充表S5)。如果QFT-Git不确定结果被排除在分析之外,则QFT-Git敏感性高于C-TB(P = 0.03)。
不和谐的结果
除了QFT-Git不确定的结果中,C-TB和QFT-GIT在78%的所有测试结果中同意,艾滋病毒无感染的75%,艾滋病毒感染的83%(在线补充表S6)。在McNemar的边际均匀性测试中,两次测试显着差异(P = 0.030),但在艾滋病毒 - 未感染和艾滋病毒感染之间的分裂时(P = 0.164和P = 0.121)。相比之下,对于C-TB与TST,无论TST切割点是否在15mm的艾滋病毒未感染,5 mm的艾滋病毒感染(P <0.0001和P = 0.0002)中,麦克奈米尔的测试都是显着的,或者为所有人保持5mm(P <0.0001和P <0.0001;在线补充表S6)。
在所有参与者中,结合C-Tb和QFT-GIT结果显著提高了敏感性,从C-Tb单独的73.9%提高到83.4% (p<0.0001),在未感染艾滋病毒的参与者中从76.7%提高到91.1% (p<0.0001),在感染艾滋病毒的参与者中从69.5%提高到81.1% (p<0.0026)。表3).
低CD4计数在艾滋病毒感染参与者中的影响
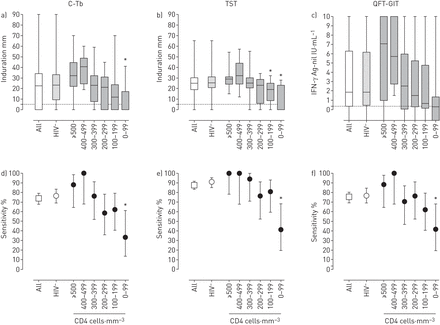
通过将所有艾滋病毒感染的参与者分组到亚组中,评估了低CD4 T细胞计数对C-TB,TST和QFT-GIT反应的影响,以降低CD4计数(图4.).所有三次测试显示趋势,用于减少响应势幅(硬结大小或干扰素-γ释放),降低CD4计数(图4A-C).与hiv未感染试验人群的反应幅度相比,CD4计数<100细胞·mm时,这种下降是显著的3对于C-TB和<200个细胞·mm3对于TST。
A-C)箱子和晶须图,显示所有参与者的免疫应答幅度(全部,n = 240),艾滋病毒无感染参与者(HIV−,n = 146)和艾滋病毒感染的参与者根据CD4细胞计数分成六个亚组(≥500,n = 12; 400-499,n = 21; 300-399,n = 17; 200-299,n = 17; 100-199,n = 10; 0-99,n = 17)。一名参与者缺少CD4计数。晶须表示最小值和最大值。D-F)线图显示所有参与者的敏感性(95%CI),艾滋病毒未感染的参与者和HIV感染的CD4计数亚组。TST:Tuberculin皮肤测试;QFT-GIT:Quantiferon-TB金管;IFN:干扰素;AG:抗原。将每个CD4计数亚组与艾滋病毒未感染的组进行比较。*:P <0.05。
为了评估降低的临床影响,我们计算了三次测试的每个CD4计数间隔的测试敏感性(图4D-F).与艾滋病毒无感染的试验相比,仅针对CD4计数<100个细胞·mm显着降低敏感性3对于所有三种测试(P = 0.0029,P = 0.0001和P = 0.0139,分别用于C-TB,TST和QFT-Git)。
C-Tb和TST的安全性
Fas中所有不良事件的大多数是注射部位的反应(表4和在线补充表S7)。对于C-Tb,报告了228例反应,其中81%为轻度反应,15%为中度反应,4%为重度反应。对于TST,报道了276例反应,其中83%是轻度反应,15%是中度反应,3%是重度反应。最常见的注射部位反应是瘙痒。与TST相比,经历至少一次注射部位不良反应的受试者明显减少(47.4%)与59.3%;p = 0.0003)。在艾滋病毒感染的参与者中,44/110(44.0%)对C-TB的不良注射部位反应与76/153(49.7%)的艾滋病毒未感染的参与者(P = 0.440)。对于TST,与97/153(63.4%)相比,比例为53/100(53.0%)(p = 0.117)。
由于试验设计包括C-TB和TST的伴随,不可能区分系统事件是否与C-TB或TST相关,或可能两者。在审判期间,36名(14%)的参与者经历了现场调查人员评估的相关系统不良事件。最常见的相关系统不良事件是头痛(8.7%)和程序疼痛(1.6%)。其中大多数被评为温和。艾滋病毒感染和艾滋病毒无感染者之间没有观察到的差异。大多数参与者(TB患者)在含有的正常范围内具有血液学参数,但在皮肤测试注射后28天的范围内值的百分比下降。试验期间有五次严重的不良事件报告(阻塞性黄疸,药物诱导的肝炎,右侧湿疗法,降低CD4 T细胞计数和高血糖)。所有评估为与C-TB皮肤测试无关。
讨论
在这里,首次据我们所知,我们报告了衍生自注册253例TB患者的双盲随机临床试验的C-TB的敏感性,其中100次受到艾滋病毒感染。使用ROC曲线分析,我们发现最佳切割点为≥5mm。在这种切割点,C-TB敏感性为73.9%,类似于QFT-Git(75.1%),但在22%的参与者中看到两次测试之间的不和谐导致。虽然TST敏感度高于C-TB和QFT-Git,但主要关注的是缺乏特异性,特别是在BCG接种疫苗的个体中。如果CD4计数<100个细胞·mm,则在参与者中,参与者敏感性敏感性仅在参与者中显着减少3.
随着C-TB和QFT-GIT共享广泛类似的抗原性曲线,预期具有类似的灵敏度。然而,通过QFT-Git检测到29名患者被视为阴性或不确定的患者,并检测到由C-TB视为阴性的32名患者。不景气可能反映略微不同的抗原谱(QFT-GIT中的TB 7.7),从根本上测量的免疫途径(复杂的皮肤测试反应)与单细胞因子在体外试验),不同的生物读数和不同的t细胞被询问(循环与专门的皮肤归巢T细胞),其中包括[18那19].一个明显的差异是较长的时间跨度在其中T细胞暴露于抗原的抗原(高达72小时,与16-24小时),因此可能反映了中央和效应存储器T细胞读数。遗传因素也可能影响皮肤测试是否发生和其相对幅度[20.].相比之下,TST敏感性为〜89%。虽然这似乎高于其他研究报告的[21],它与南非以前的研究一致[22].后者可能是由于感染力的高力量[23[持续通过环境分枝杆菌的高患病率进行T细胞启动[24]之前的BCG疫苗接种[9.].
通过HIV状态和CD4计数分层参与者,我们观察到较低CD4计数下C-TB,TST和QFT-Git的较低响应势幅度和降低测试敏感性的趋势。这是艾滋病毒诱导的免疫抑制的众所周知的效果[25-28].CD4计数<400个细胞·mm的患者中,反应幅度下降是明显的3.对于C-Tb和比较者来说,只有在最低的CD4计数区间(0-99细胞·mm)才达到显著性3).我们认为这是由于炎症性皮肤试验反应的能力减弱。
现时建议将爱滋病病毒感染者的TST切割点降低至5毫米[4.,就像在本工作中所做的那样。在这个切点上,TST敏感性明显优于QFT-GIT和C-Tb,这与其他研究中看到的一致[29].相反,将5至1mm的C-TB切点降低到HIV感染的个体中并未提高测试性能。值得注意的是,与TST相比,C-TB 5 mm切割点显示出BCG接种的健康志愿者的优异特异性[13].重要的是,这些数据共同表明,与TST相比,C-Tb可以使用单一的通用切入点来解释,这将提高使用的易用性,并可能减少不明艾滋病毒状态的假阴性应答者的数量。事实上,在检测高危患者,包括艾滋病毒感染者、儿童和正在接受免疫抑制治疗的患者时,需要最大的敏感性,如。抗肿瘤坏死因子-α治疗[9.].因此,在最大敏感性至关重要的日常使用中,如果C-Tb为阴性,增加QFT-GIT检测似乎是明智的,但需要在适当设计的研究中进一步探索。
C-TB在艾滋病毒感染和HIV-未感染的TB患者的试验中耐受良好。大多数不良事件是注射部位反应,但与PPD驱动的TST相比,频率显着降低。由于试验设计包括伴随C-TB和TST,因此不可能区分特定事件是否与C-TB或TST相关,或两者。这几乎没有结果,随着相关的系统不良事件的数量小,不良事件一般温和。值得注意的是,许多血液参数在包容性时异常,反映了招募人群的患病状态。实际上,它们在治疗过程中得到了改善。
我们的研究结果有几个局限性。这里报道的敏感性估计由识别截止的相同数据确定。因此,需要在不同设置中进行额外的验证研究来确认这里报告的敏感性。活性TB的灵敏度估计可能与LTBI的敏感性估计不类似,并且由于TB是免疫抑制条件,可能会降低。然而,由于LTBI没有可靠的诊断标准,因此活性TB用作可比较的代理。我们没有执行或测试替代代理的性能衡量标准,例如包括近触点,以将测试结果与曝光梯度相关,并评估有源TB的预测值。QFT-Git和TST都已知QFT-Git和TST对TB疾病的进展具有差的预测值。随着C-TB与QFT-GIT共享相同的抗原,这种新型皮肤测试预计不会成为这方面的主要进步。与QFT-GIT相比,C-TB的主要优点预计将简单,因为C-TB不需要血液抽取,无血液样本的处理和运输,而且没有专门的实验室设备。然而,QFT-GIT具有内置的负面和阳性控制管的优点,不存在于皮肤测试格式。 A future trial will report on C-Tb performance in a contact-tracing design, thus correlating C-Tb positivity rates with an exposure gradient. A phase 3 trial evaluating C-Tb in TB suspects is in the process of being concluded.
总之,与QFT-git相比,活性TB中C-TB的第一次评估显示出类似的灵敏度。与TST相比,无论BCG和HIV状态如何,C-TB都可以与单一通用切割点一起使用。进一步的研究将验证,如果C-TB可以是有价值的或替代的PPD TST和/或QFT-GIT的替代品。
确认
我们感谢所有试验现场的调查人员、工作人员和试验参与者。我们感谢数据安全监测委员会的成员:Pernille Ravn博士、Luca Richeldi博士和Christian Lienhardt博士。
脚注
编辑评论在:EUR RESPIR J.2016;(DOI 47: 704 - 70610.1183 / 13993003.01910-2015].
本文提供了补充材料www.qdcxjkg.com.
临床试验:本研究注册于www.clinicaltrials.gov.使用标识符号码nct01241188..
支持声明:该试验由Statens血清研究所资助。本文的资金信息已存入乐趣.
利益冲突:披露可以在本文的在线版本旁边找到www.qdcxjkg.com.
- 已收到2015年9月3日。
- 公认2015年10月9日。
- 版权所有©2016