摘要
特发性肺纤维化(IPF)与致命的预后相关,在60岁以上可能有合并症的患者中表现出来。共病的患病率和对IPF临床病程的影响尚不清楚。
本系统文献综述研究了IPF患者共病的患病率和与共病相关的死亡率。1990年1月至2015年1月发表的相关英文观察性研究发现通过包括MEDLINE和EMBASE;还检索了文章的参考书目。
纳入的126项研究中,肺动脉高压(PH)的患病率为3-86%,阻塞性睡眠呼吸暂停的患病率为6-91%,肺癌的患病率为3-48%,慢性阻塞性肺病(COPD)的患病率为6-67%。非呼吸系统共病包括缺血性心脏病(IHD)(3-68%)和胃食管反流(GER)(0-94%)。IPF和肺癌患者的死亡率最高。大多数研究评估了相对较小的IPF患者样本。
PH、COPD、肺癌、GER和IHD是重要的共病;IPF严重程度、病例定义和患者特征的差异限制了研究结果的可比性。合并症的识别和及时治疗可能对IPF患者的总体预后有临床意义,这对IPF患者有意义。
摘要
发现并及时治疗合并症对IPF患者的预后有显著的临床影响http://ow.ly/Q2AfI
简介
特发性肺纤维化(IPF)是一种严重的、进行性的、使人衰弱的疾病,诊断后的中位生存期为2-3年[1].在诊断时中位年龄为66岁的老年人群中[2],多病是常见的[3.].常与IPF相关的共病包括胃食管反流[4]、肺动脉高压(PH) [5]、慢性阻塞性肺病/肺气肿[6]及阻塞性睡眠呼吸暂停[7].
IPF的治疗选择有限,合并症及其治疗的影响可能会影响疾病的临床病程[8].合并症的识别和治疗可能与改善预后相关(如。改善生活质量和潜在的生存)。在观察性和回顾性研究中,IPF患者的抗酸治疗和GER治疗与IPF进展率降低和生存时间延长有关[9,10].COPD/肺气肿并存可影响肺容量和病程以及对治疗的反应,并被认为是联合肺纤维化和肺气肿(CPFE)的独特综合征[11,12].这些病人亦有罹患PH的风险[11],这与死亡率增加有关[1].此外,急性恶化患者的支气管肺泡灌洗液中胃蛋白酶量增加的微抽吸,称为急性IPF加重,可能会影响疾病的临床病程。关于这种快速下降的病因和定义,有不同的观点(如。“急性加重”与一种与渴望相关的表现)。然而,急性IPF加重虽然肯定与高发病率和死亡率相关,但不是本综述的重点。按照目前对指规数急性加重的看法[13],我们认为急性加重属于IPF的自然病程范围,而不是共病。
对于临床医生来说,了解IPF患者人群中共病的程度是至关重要的。关于IPF患者中哪些合并症最普遍以及合并症如何改变病程的最新、全面的知识对于提供最佳护理并最终改善该患者人群的临床结果非常重要。
本系统文献综述的目的是估计IPF患者共病的患病率。第二个目标是总结与IPF患者共病相关的死亡率数据。感兴趣的共病包括呼吸道疾病(COPD、PH、OSA、肺癌和肺栓塞(PE))和非呼吸道疾病(如。GER,心血管和代谢)合并症。
方法
数据源和搜索
进行文献检索,从观察性数据中确定自1990年以来英文发表的报道IPF患者共病的出版物。用于执行此审查的方法涉及电子和手动组件,并遵循已建立的系统审查研究的“最佳实践”指南[14,15].搜寻工作在MEDLINE (通过PubMed)和EMBASE数据库(通过OvidSP平台)识别1990年1月1日至2015年1月21日发表的目标人群相关研究。本综述中使用的具体搜索词和策略在在线补充材料中有详细说明。对所有已接受的研究的参考文献列表的人工审查进一步补充了电子检索。
研究选择
研究选择通过预先指定的纳入和排除标准的两级研究筛选完成。在每个摘要的筛选过程中,审稿人为每个感兴趣的主题确定了相关数据。所有论文的摘要都由两位研究人员审阅,并由首席研究员对随机样本进行交叉检查。在I级筛查中,任何符合排除标准的研究都被拒绝。排除标准包括:研究类型错误(介入性研究或基于介入性研究数据提取的研究、专家意见、系统评价、荟萃分析和报告生活质量结果或肺移植后结果的研究被排除在本综述之外);以英语以外的语言发表的研究;无IPF患者。由于IPF的定义随着时间的推移而发生变化,我们在在线补充表中指出,研究中是否使用了分别于2000年或2011年发表的美国胸科学会(ATS)/欧洲呼吸学会(ERS)或ATS/ERS/日本呼吸学会(JRS)/拉丁美洲胸科学会(ALAT)对IPF的定义[188bet官网地址1,16].II级筛查包括对从i级筛选的文献全文的回顾。要通过II级筛查并纳入本综述,研究必须是观察性(非介入性)的,并报告至少一种感兴趣的结果(IPF共病)。IPF和共病的定义标准基于各自研究中报道的数据。
数据提取和质量评估
从每个被接受的研究中提取的感兴趣的数据元素被提取到专门为本综述开发的数据提取表单中。提取的信息包括研究水平(如。发表年份、地理区域、研究设计和人群)和患者水平特征(如。样本量、平均年龄/性别分布和患病率/发病率估计)。一名研究人员从每项研究中提取数据,另一名研究人员独立审查提取数据的完整性和准确性,以对照原始研究。
由于本研究的主要目的是确定报告有IPF的患者共病的患病率,因此本综述只选择了观察性研究。牛津大学循证医学中心(CEBM)的证据水平被用于评估研究质量[17].根据症状流行度研究设计的标准,随访>的前瞻性队列研究评分为“1b”,回顾性队列研究评分为“2b”,病例系列评分为“4”[17].
数据综合与分析
由于所提取数据的异质性,没有进行荟萃分析,并在这里提出了证据的定性综合。研究和患者特征采用描述性统计,如均值、中位数、标准差和极差。流行率和死亡率数据在适用时采用范围。
本研究由勃林格殷格翰制药有限公司提供资金。
结果
研究磨损
共鉴定出1016个摘要进行筛选。经复查,606例因符合研究排除标准(无观察性研究设计、无IPF患者或无感兴趣的结果)而被拒绝。在二级筛选审查的410篇全文文章中,146篇符合初始搜索的纳入标准。人工审查了纳入研究的参考文献列表,以确定最初搜索中没有确定的相关论文。从手动检索中,又检索了48篇全文文章,其中23篇符合初始检索的纳入标准。在符合初始检索标准的169篇论文中(146篇来自MEDLINE/EMBASE检索,23篇来自手动参考文献检查),有126篇论文报告了本综述感兴趣的结果(图1).
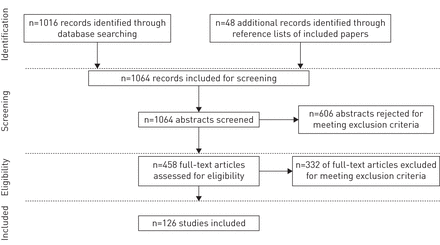
学习减员流程图。
研究特点
近三分之二的研究(n= 85,67%)是回顾性队列研究的分析;25项(20%)为前瞻性队列研究,10项(8%)为病例对照研究,5项(4%)为横断面研究,1项(1%)为病例系列研究(表1).研究中纳入的IPF患者人数从8到9286人不等。IPF患者的平均年龄为53.4 ~ 80.5岁。大多数研究(n=97;77%)报告患者样本由50%的男性组成,尽管所有研究均未报告患者性别。72% (n=91)的论文集中在呼吸系统共病;33% (n=41)包括一种以上共病类别的数据。从地理上看,40% (n=50)的研究报告来自北美,29% (n=36)来自亚洲,29% (n=36)来自欧洲,两项研究来自南美(巴西),一项来自大洋洲(澳大利亚),一项来自非洲(埃及)。
呼吸系统并发症
慢性阻塞性肺病
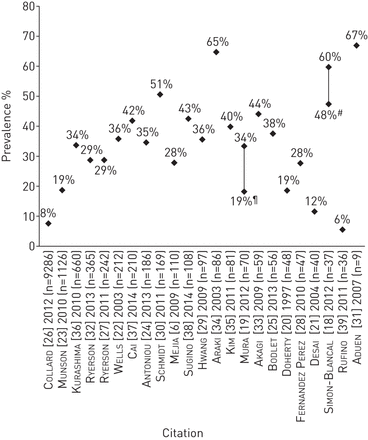
23项研究报告了COPD(包括肺气肿)的患病率(在线补充表S1),其中8项来自欧洲[18- - - - - -25], 8个来自北美洲[6,26- - - - - -32],六名来自亚洲[33- - - - - -38]另一个来自南美洲(巴西)[39].报告的COPD患病率为6%至67% (图2)(按国家划分的流行程度:12% [21]至51% [18]在欧洲,8% [26]至67% [31], 34% [36]至65% [34在亚洲)。肺气肿患者的最高报告比例(67%)是IPF患者中肺对一氧化碳的孤立扩散能力(DLCO)减少,因此可能高估了IPF中肺气肿的患病率[31].在日本的一项研究中,计算机断层扫描显示肺气肿与生存时间缩短有关。在该研究中,来自呼吸科诊所的129例肺气肿IPF患者的中位生存期为7.5年,与该研究中233例未患肺气肿的IPF患者(8.5年)相比显著降低(p=0.0472) [36].墨西哥的一项研究也发现,与该研究中未患肺气肿的IPF患者的中位生存期(34个月)相比,伴有肺气肿的IPF患者的生存期(25个月)显著降低(p=0.01) [6].然而,在调整PH值后,肺气肿不再与死亡率显著相关。一项对加州大学旧金山分校和梅奥诊所罗切斯特间质性肺病数据库的分析没有发现CPFE和IPF患者与非CPFE IPF患者的死亡率有显著差异(危险比(HR) 1.14, 95% CI 0.61-2.13;(p = 0.69)32].
特发性肺纤维化(IPF)患者中慢性阻塞性肺疾病(COPD)/肺气肿的患病率有关个别研究中使用的COPD/肺气肿的定义和研究样本的描述,请参阅在线补充表S1。#受试者为住院IPF患者,经历急性发作;肺气肿的患病率从急性加重幸存者的48%到幸存者的60%不等。¶:研究包括新收集的IPF患者的数据,以及对IPF患者现有数据的回顾性回顾;前瞻性队列中受试者肺气肿患病率为34%,回顾性队列中受试者肺气肿患病率为19%。
肺动脉高压
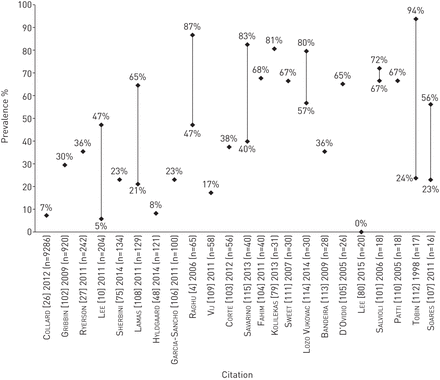
共有43项研究采用基于右心导管或超声心动图的各种定义,纳入了IPF患者PH患病率的数据(在线补充表S2)。总体而言,欧洲的研究中PH的患病率与此相似[18,25,40- - - - - -45,47- - - - - -49]、北美洲[5,6,26,28,46,50- - - - - -67]、亚洲及非洲[37,68- - - - - -75],尽管大多数证据来自北美(n= 23,53%)。在研究中,IPF患者中PH的患病率从3%到86%不等;大多数估计在30%至50%之间(图3) [25,43,44,47,50,52- - - - - -66,68,71- - - - - -73].7项研究报告了IPF加ph患者的死亡率或生存时间。来自3项欧洲研究[44,45,76], PH患者IPF诊断的中位生存时间约为2-3年至4年[44,45,76].PH的存在与死亡风险的增加相关(死亡的HR, PH与无PH 4.03, 95% CI 1.17 ~ 27.9;p=0.03(研究人群为CPFE患者)[76];HR 3.6, 95% CI未报告;p = 0.0001 (44])。然而,对来自丹麦一家医院的121名IPF患者的数据进行的分析并未发现PH值与死亡率之间存在显著相关性,尽管在调整年龄、性别和用力肺活动量(FVC)后,数值趋势仍然存在(HR 2.2, 95% CI 0.94-5.2;(p = 0.068)48];同样,一项对美国一所大学医院接受肺移植评估的IPF患者的综述未发现平均肺动脉压(mPAP)与死亡率之间的显著相关性[67].在一项基于美国25例IPF患者现有数据的综述中,1年死亡率为29% [57].美国的另一项研究发现,患有严重酸碱度(即。经胸超声心动图显示收缩压(sPAP) >50 mmHg)与无PH值(中位生存4.8年)或轻度或中度PH值(中位生存4.1年)患者相比,生存期(中位生存0.7年)显著(p=0.009)差[5].墨西哥国家呼吸疾病研究所对连续IPF患者临床记录的研究表明,在多变量模型中,存在严重PH(经胸超声心动图测量sPAP≥75 mmHg)与死亡率显著相关(HR 2.25, 95% CI 1.12-4.54;(p = 0.022)6].来自日本的24例IPF患者中,采用>17 mmHg右心导管mPAP, 5年死亡率为83%,中位生存时间为29个月[69].在同一队列的6例>25 mmHg mPAP患者中,5年死亡率为100%。来自中国一家医院数据库的210名IPF患者的数据发现,sPAP≥37 mmHg和非sPAP患者的平均生存时间为24与分别为57个月(p=0.008);在多变量分析中,PH值与死亡风险显著增加相关(风险比3.393,95% CI 1.444-7.973;(p = 0.005)37].mPAP也独立且显著地与5年死亡率相关(风险比1.064,95% CI 1.015-1.116;p=0.010),对日本某医院的101例IPF患者进行分析[74].受试者工作曲线分析发现20 mmHg为最佳临界值(曲线下面积0.679,敏感性55.0%,特异性75.4%)。Kaplan-Meier曲线显示,mPAP为>20 mmHg的患者的生存率明显低于mPAP≤20 mmHg的患者(log-rank检验p=0.001)。中位生存期分别为20.8个月和37.5个月[74].
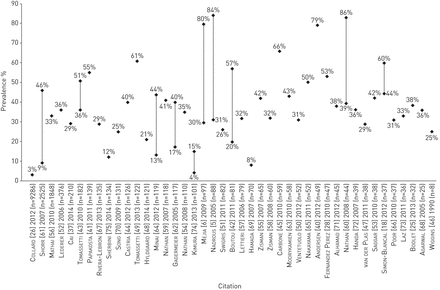
特发性肺纤维化患者肺动脉高压(PH)的患病率。个别研究中使用的PH值定义见在线补充表S2。
阻塞性睡眠呼吸暂停
7篇论文报道了IPF患者OSA患病率的数据,其中3篇来自欧洲[77,79,80]和4个来自美国[7,26,28,81(在线补充表S3)。在对两个美国索赔数据库中确定的9286例IPF患者的分析中,OSA的患病率从5.9%不等[26在接受多导睡眠图检查的31名希腊间质性肺病门诊患者中,提高了91% (图4) [79].在本综述中纳入的研究中,OSA似乎在身体质量指数(BMI)较高的患者中更为常见。在美国的一项研究中,IPF患者的患病率为61%,仅在中度至重度肥胖的IPF患者中观察到OSA (即。BMI 35.3-44.3 kg·m−2) [81].在美国的一项研究中,发现88%的患病率,OSA患者的平均BMI显著(p=0.05)大(平均BMI 33±6.7 kg·m)−2)与无(26±2 kg·m−2);但BMI与OSA仅呈弱相关(r=0.30, p=0.05) [7].对21例IPF患者的分析发现,呼吸暂停-低通气指数(AHI)≥5的患者BMI较高(29.72±0.81)。与< 5(27.50±1.71;p=0.053), BMI与AHI正相关(r=0.59, p=0.001) [80].一项研究调查了阻塞性睡眠呼吸暂停和死亡率之间的关系[79].在夜间低氧血症和死亡率之间发现了一个显著的相关性,假设睡眠期间由于OSA而发生的间歇性氧饱和度降低有助于PH值和相关的死亡率。
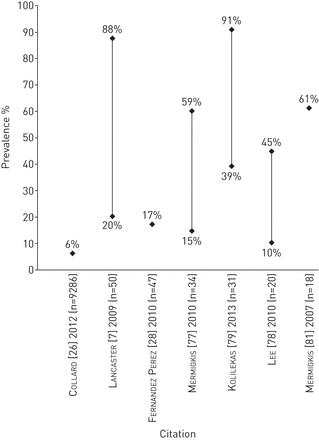
特发性肺纤维化患者中阻塞性睡眠呼吸暂停(OSA)的患病率。个别研究中使用的OSA定义见在线补充表S3。
肺癌
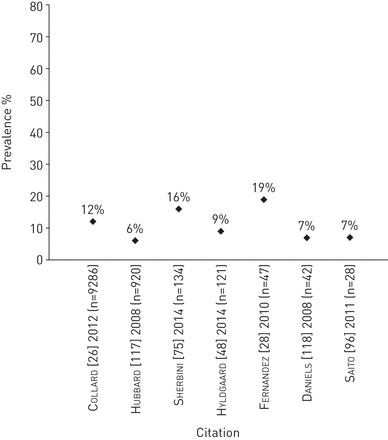
15项研究报告了IPF患者中肺癌的患病率[26,28,34,48,82- - - - - -92](在线补充表S4和图5),通常低于其他呼吸道合并症的患病率。根据对美国和英国的保险索偿和电子医疗记录数据库的分析,肺癌的患病率估计为3-4% [26,82,83].两个IPF患者的医院数据库,一个来自丹麦,一个来自韩国,报告了相似的低患病率,分别为6%和4% [48,92].在对亚洲IPF患者的医疗记录和尸检数据进行的其他研究中,肺癌的估计患病率较高,在20%至23%之间[34,84,85,90].估计IPF合并肺癌患者的死亡率受到不同研究随访时间、不同的癌症和IPF严重程度、癌症治疗方法的差异以及其他患者特征的影响。报道IPF肺癌患者死亡率和生存率的论文由于样本量小而受到限制。一项来自美国的研究包括24例经组织学证实的普通间质性肺炎(UIP)和原发性肺癌患者,这些患者是通过计算机搜索罗切斯特梅奥诊所1990年至1998年的数据库确定的。IPF诊断后平均随访2.2年,癌诊断后平均随访1.2年,报告的死亡率为67% [93].诊断为IPF后平均生存期为2.3年,诊断为癌后平均生存期为1.6年[93].21例接受全身化疗的IPF和非小细胞肺癌患者中,化疗开始后的中位总生存期为11.4个月,1年生存率为28.6% [94].在接受肺癌手术治疗的患者中,术后死亡率(如。30天,90天,住院)倾向于低(0例死亡[95,96], 4% [96,97], 5% [98], 7% [97], 8% [98,99], 12% [93,98]),尽管来自中国的一个小型数据库回顾报告了33.3%的术后死亡率(6例患者中有2例)[84].IPF诊断后的中位生存期为7个月(95% CI 2.51-11.49)至26.9个月(95% CI 14.67-39.05) [84,89].两项研究报告了IPF与IPF合并肺癌患者的中位生存期无显著差异[84,85].然而,仅使用ipf的患者的生存期往往更长,这些研究可能受到样本量小的限制。一项规模更大的研究发现,无肺癌的IPF患者(n=1571)与有癌症的IPF患者(n=114)相比,生存时间明显更长(文中以图形形式显示生存时间,未报道无肺癌患者的具体时间)[89].调整后的肺癌死亡HR与无肺癌报告为2.4 (95% CI 1.4-4.3;(p = 0.002)89].在日本的一项回顾性单中心研究中,在387例接受手术切除的原发性肺癌患者中,组织病理学证实的IPF被确定为术后死亡率和长期生存的一个显著的负预后因素[98].
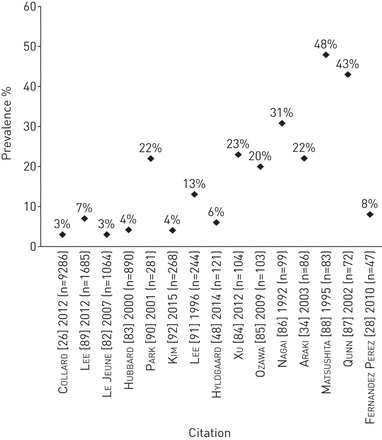
特发性肺纤维化患者肺癌患病率。个别研究中肺癌的定义见在线补充表S4。
肺栓塞
两项美国研究和一项意大利研究报告了IPF患者中PE的患病率,其范围为3% [26]来自意大利医院数据库的9286名经医疗索赔确定的IPF患者和122名IPF患者[49]至38名入住重症监护室的IPF患者中的6% [One hundred.](在线补充表S5)。美国一项大型行政索赔数据库的回顾性研究报告称,IPF患者中PE的发生率为10.7/1000人年,而非IPF患者中PE的发生率为4.8/1000人年(风险比2.24,95% CI 1.69-2.98) [26].IPF患者中与PE相关的死亡率仅在沙特阿拉伯的一项研究中报道,该研究中61例IPF/UIP患者中有15例在随访期间死亡(24.6%)[71].在这15名死者中,有一人的死因是PE [71].
非呼吸道并发症
胃食管反流病
23项研究报告了异常GER的患病率[4,10,26,27,48,75,79,80,101- - - - - -115](在线补充表S6),在爱尔兰参加一项探索睡眠呼吸障碍程度和机制的研究的20名IPF患者中,范围为0,且没有记录GER病史[80在从单个美国中心招募的连续新诊断IPF患者的分析中,该比例为94.1% [112) (图6).然而,94%的发病率是基于异常酸性GER的24小时动态生理定义:一种最敏感的确定异常酸性GER的方法,包括食管远端和/或近端异常酸性暴露。美国仅有一篇摘要报道了IPF患者的GER发生率,其中26例非住院患者的GER发生率为11.5%,住院IPF患者的GER发生率为71.4%;GER的定义未见摘要报道[116].虽然没有研究公布IPF和GER患者的死亡率,但一项美国回顾性研究报告称,IPF合并GER患者的中位生存时间为IPF诊断之日起的1499天[10].观察到服用GER药物的患者中位生存期较高(1967天),而接受尼森基金复制手术的患者中位生存期较高(2252天)[10].在对基线人口统计学和临床特征进行调整后,GER药物使用仍与较长的生存期相关(HR 0.47, 95% CI 0.24-0.93;p=0.03),但调整后未观察到Nissen基金复制史与生存之间的相关性(HR 0.74, 95% CI 0.21-2.59;(p = 0.64)10].
特发性肺纤维化患者胃食管反流病的患病率个别研究中胃肠道合并症的定义见在线补充表S6。
心血管和代谢状况
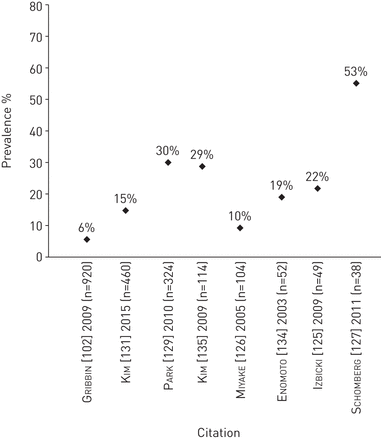
大多数研究还报告了心血管合并症(即。心律失常及心房颤动[26,28,48,75,96,117,118](在线补充表S7和图7)、心力衰竭或充血性心力衰竭[5,26,28,43,49,96,One hundred.,119,120](在线补充表S8和图8)、缺血性心脏病[5,26,28,41,43,48,49,52,80,108,118,119,121- - - - - -132](在线补充表S9和图9)、脑血管病及中风[26,48,117,118](在线补充表S10),以及全身性动脉高血压[5,23,28,39,41,48,52,75,119,125- - - - - -127,129- - - - - -131,133- - - - - -135](在线补充表S11和图10),以及代谢并存病(即。糖尿病(23,39,41,48,75,80,92,102,106,108,119,125,127,129- - - - - -131,134,136](在线补充表S12和图11)、高胆固醇血症/高脂血症[102,125- - - - - -127,129,131,134,135](在线补充表S13和图12)和体重失调[10,23,26,125,131,134,137](在线补充表S14))。IHD是最常报道的心血管共病(在24篇论文中报道)。流行率估计,范围从3.2% [26在接受肺移植资格筛查的IPF患者中,68%为非显著性或显著性冠状动脉疾病(CAD),由于这些研究中评估的患者群体和IHD的病例定义不同,差异很大。在特定的IHD诊断方面,在器官共享联合网络中列入肺移植的IPF患者中,CAD的范围从~ 4%到上述筛选肺移植资格的IPF患者的65.8%不等。从索赔数据库中,国际疾病分类第九修订版(ICD-9) MI代码发现3.2%的IPF患者[26], 7%的连续IPF患者接受了a事后剖析评价(118]和12%的意大利医院肺气科数据库中确定的IPF患者[49].据摘要报道,在38名来自医疗保健提供者的连续IPF患者中,8名(21%)患有st段抬高性心肌梗死[127].在评估代谢合并症的研究中,糖尿病被报道的频率最高(n=18)。在英国,IPF患者中糖尿病的患病率一般为10% [102]至日本的32.7% [134],尽管最高的患病率(39%)在31名延迟医疗≥4年的美国患者中报告[108].在一项研究中,心血管合并症与生存期呈负相关,患有CAD和IPF的患者自左心导管插入之日起的中位生存时间为572天,而无显著性CAD或无CAD患者的中位生存时间为1499天[121].一项研究提供了肥胖与长寿相关的证据。1994年至1996年,在美国明尼苏达州罗切斯特市梅奥诊所接受评估的197例IPF患者中,BMI正常/体重过轻(<25)的患者中位生存时间为3.6年,BMI≥30的肥胖患者中位生存时间为5.8年[137].在多变量模型中,生存与BMI显著相关(BMI每增加1个单位,HR 0.93, 95% CI 0.89-0.97;(p = 0.002)137].
特发性肺纤维化患者心律失常或心房颤动的发生率。个别研究中使用的心律失常或心房颤动的定义见在线补充表S7。
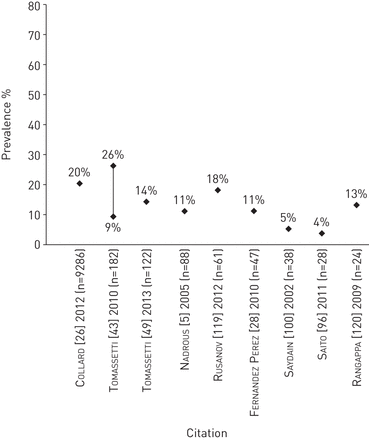
特发性肺纤维化患者心力衰竭的患病率。个别研究中使用的心力衰竭定义见在线补充表S8。
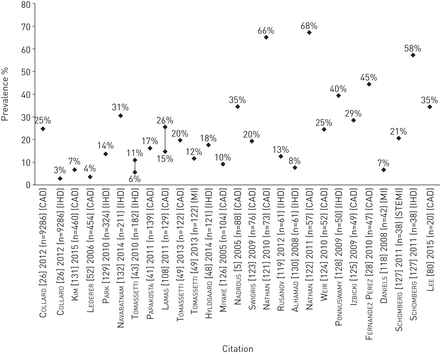
缺血性心脏(IHD)在特发性肺纤维化患者中的患病率个别研究中IHD的定义见在线补充表S9。CAD:冠状动脉疾病;MI:心肌梗死;主干:st段抬高型心肌梗死。
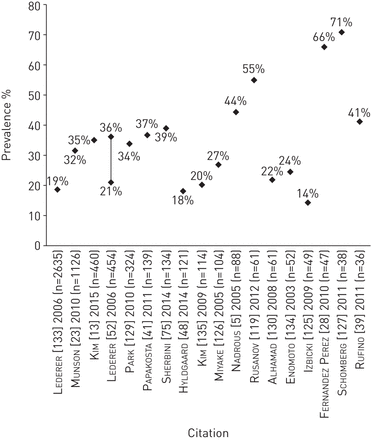
特发性肺纤维化患者中动脉高血压的患病率。个别研究中使用的动脉高血压定义见在线补充表S11。
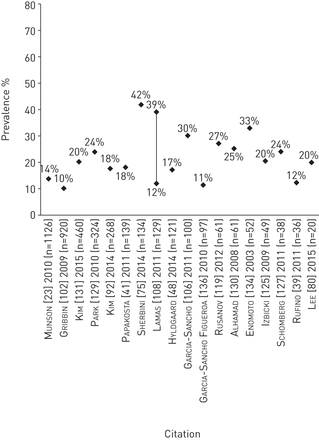
特发性肺纤维化(IPF)患者中糖尿病的患病率。个别研究中使用的糖尿病定义见在线补充表S12。#: IPF患者的糖尿病患病率按症状出现至三级护理中心护理的时间分层,范围为12%至39%。
特发性肺纤维化患者中高胆固醇-甾醇血症/高脂血症的患病率。个别研究中使用的高胆固醇血症/高脂血症的定义见在线补充表S13。
讨论
IPF是一种致命疾病,绝大多数患者为60岁以上的男性[2].虽然这一年龄组的人确实存在一些健康问题和疾病的风险,但IPF患者共病的发病率和患病率尚不清楚。认识到IPF患者可能存在的特定共病是很重要的,因为及时发现和治疗共病可能对IPF患者的总体结局具有重大的临床意义和有意义的影响。据我们所知,本系统综述首次总结了IPF患者共病患病率和相关死亡率的相关文献。呼吸系统共病,包括COPD、PH和OSA,在许多研究样本中很常见,尽管估计值因来源人群而有很大差异。非呼吸道合并症,如GER、全身性动脉高血压、IHD和糖尿病在这组老年患者中也非常普遍。值得注意的是,直到最近,由于缺乏有效的治疗方法,全身性类固醇一直是治疗IPF的主要治疗方案,这可能是该人群糖尿病高发的原因之一。报告的死亡率较低,但在伴有COPD(23-77%)和肺癌(38-81%)的患者中最高;PH和IHD也与死亡风险增加有关。在一项临床试验中,对明确患有IPF和轻度至中度FVC损伤的患者进行右心导管DLCO表明10%的患者有PH [138].在IPF患者中观察到与PH相关的功能下降[139,140].
文献中报告的流行率估计的广泛变化可能是由于几个因素。与前瞻性队列研究相比,使用行政声明和电子病历数据的分析通常报告较低的患病率估计,这是由于合并症的漏报。例如,一项美国回顾性索赔分析发现,根据ICD-9诊断代码(278.0x), IPF患者的肥胖患病率为0.6% [26].然而,疾病控制和预防中心国家卫生统计中心2012年发布的一份简报称,2009-2010年,35.7%的美国成年人肥胖(BMI≥30)[141].
IPF和相关共病的病例定义和诊断标准的差异可能也导致了本文观察到的估计值的差异。超过一半的研究使用当时相关的ATS/ERS 2000共识指南诊断IPF患者(70/126;56%),尽管其他研究使用肺活检结果或索赔数据中的诊断代码来确定IPF患者。此外,本综述中包括的许多研究是在最近的ATS/ERS/JRS/ALAT指南于2011年发表之前进行和报道的[1].IHD一词经常被用于分类相关疾病,如急性冠脉综合征、心绞痛和CAD,但这些疾病的定义随着时间的推移而变化,研究者或研究方法通常缺乏这些定义。例如,CAD中的“显著”一词在三个独立的研究中使用不同:定义干预的必要性或>50%病变的大血管[121],左心导管/高分辨率计算机断层扫描结果中冠状动脉钙化的定量[124]及经冠状动脉造影诊断为一条或多条冠状动脉狭窄≥50% [125].
根据牛津大学的CEBM证据级别,本综述中包括的大多数研究符合“2b”的评分,保留给随访不良的回顾性队列研究和前瞻性队列研究[17].基于现有数据的研究可能会受到信息偏倚的影响:由于随访缺失或随着时间的推移结果测量方式的差异,相关数据可能会丢失。如果要求患者记住详细的病史或治疗方法,也可能存在回忆偏倚。由于本综述未评估具体的研究结果,如疗效或安全性,因此未评估个别研究的偏倚风险。
本综述中纳入的大多数研究评估了相对较小的IPF患者样本,这可能限制了对更大范围IPF患者的推广。符合本综述标准的相关研究在非洲(n=1)、澳大利亚(n=1)和南美(n=2)的文献中并不多见,这也限制了本报告结论的普遍性。由于只纳入了英文发表的研究,我们可能遗漏了非英文文献中IPF患者共病的相关数据。同样,我们的综述仅限于在MEDLINE和EMBASE中索引的论文,有可能我们没有包括在这些数据库之外发表的相关数据。然而,本研究的一个优点是采用了系统的方法。此外,虽然其他研究人员报道了IPF患者中个别选择的合并症的患病率,但本综述首次在一篇文献中总结了大量合并症。
虽然这篇综述集中于IPF患者的特定共病,但需要更清楚地了解潜在的定义以及不同共病及其治疗对IPF患者生存的影响。在单独的III期临床试验中,尼达尼布和吡非尼酮均已被证明可减缓疾病进展,最近已在美国获得批准[142,143]和欧盟基于1年内通过植被覆盖度纵向测量评估的肺功能衰退显著减少;在这些研究中,两者都与全因死亡率的数值风险降低有关[144].然而,迄今为止,没有一项充分设计的研究表明药物治疗可以提高生存率。目前尚不清楚新的抗纤维化药物是否对IPF合并共病患者的预后有影响[145].及时发现并适当治疗这些合并症可能有助于提高IPF患者的生存期。IPF患者中常见的呼吸道和非呼吸道共病的诊断和治疗是适当的考虑因素,因为未发现和因此未治疗的共病有独立的不良结局。例如,未诊断的OSA确实会导致疲劳和随后的PH值发展;治疗PH值可能是一个值得考虑的因素,肺癌的早期诊断都可能导致整体的改善结果。在这方面,虽然改善IPF患者生存的治疗方案尚未确定,但在52周研究期间参与临床试验的明确的IPF患者和轻度至中度生理损伤患者中观察到的相对较低的死亡率(约10%),以及在没有任何特定治疗IPF的情况下保持稳定的患者,提高了IPF患者由于针对合并症的“治疗”而提高生存的可能性[142,143].最近的一项回顾性研究表明,抗酸治疗和异常GER手术治疗可提高IPF患者的生存率[10].在一个明确的IPF患者队列中,参与了三个前瞻性临床试验,抗酸治疗后IPF的进展率下降[9].然而,由于治疗组不是随机的,“指征偏倚”可能在这里发挥作用,在这一领域迫切需要正式的随机安慰剂对照试验。同样明显的是,IPF患者的一般护理标准已得到改善,这可能是IPF自然病程发生明显变化的原因[146].
虽然本综述总结了个体共病的数据,但本文所述共病的广泛流行反映了个体研究中使用的不同定义。未来的研究应使用完善的共病定义,以更深入地了解影响IPF患者的共病。需要这些信息来更有效地设计临床试验,并解决可能改善IPF患者整体健康结果的共病疾病的治疗。关于患者特征的独立影响的进一步研究(如。年龄、性别、种族和疾病严重程度)与共病对发病率和死亡率的影响将有助于了解共病对IPF临床病程的总体影响。除了对个别共病的治疗外,对IPF的未来临床试验进行设计,根据已知在IPF患者中普遍存在的特定共病进行分层,可能会更好地理解真正的治疗效果和更好的总体结果。
确认
Boehringer Ingelheim Pharma GmbH & Co. KG的Heike Schürmann协助文献检索策略。Kristin Kistler博士在作者的指导下协助撰写手稿。作者完全负责所有内容和编辑决定,并参与了手稿发展的所有阶段,并批准了最终版本。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:本研究由勃林格殷格翰公司资助。本文的资助信息已存入FundRef.
利益冲突:可以在本文的在线版本中找到信息披露www.qdcxjkg.com
- 收到了2014年12月17日。
- 接受2015年6月29日。
- 版权所有©ERS 2015