文摘
Riociguat是可溶性鸟苷酸环化酶刺激器,批准肺动脉高血压。在为期12周的PATENT-1研究中,riociguat良好的耐受性和改进的几个临床相关的端点在肺动脉高血压患者治疗天真或已经使用内皮素受体拮抗剂或前列腺素类。PATENT-2开放扩展riociguat的长期安全性和有效性评估。
符合条件的患者从PATENT-1研究收到riociguat单独调整到最大剂量的2.5毫克,每日三次。的主要目的是评估的安全性和耐受性riociguat;探索性疗效评估包括6分钟步行距离和世界卫生组织(世卫组织)功能的类。
总的来说,396例患者进入PATENT-2研究和324年(82%)正在进行的中期分析(2013年3月)。riociguat的安全性PATENT-2类似于观察PATENT-1,例咯血和肺出血在PATENT-2也被观察到。改善病人的,6分钟步行距离,功能类中观察到PATENT-1 PATENT-2持续1年。在观察到的人口在1年的时间点,意味着±sd6分钟步行距离改变了由51±74 m和功能类改善了33%,稳定在61%,6%的病人恶化与PATENT-1基线。
长期riociguat在肺动脉高血压患者耐受性良好,并导致运动能力的持续改进和功能能力长达1年。
文摘
Riociguat PAH患者耐受性良好,持续的好处在6随钻测量和FC长达1年http://ow.ly/EskBj
介绍
肺动脉高压(PAH)是一种慢性的、危及生命的疾病,特点是增加肺血管阻力(PVR)由于进步的血管重塑,最终可导致右心衰和死亡(1,2]。虽然有几种授权疗法,多环芳烃仍是一种无法治愈的疾病,需要额外的治疗方案(3,4]。
Riociguat是一种新型可溶性鸟苷酸环化酶(国网公司)刺激行动的双重模式,使感光国网公司的内源性一氧化氮稳定氮oxide-sGC绑定和直接刺激国网公司通过不同的结合位点,独立于一氧化氮(5]。这将导致增加生产环磷鸟苷(cGMP) [5]。Riociguat首次发现药物功效在两个单独的肺动脉高压(PH)的迹象,多环芳烃和慢性血栓栓塞肺动脉高压(CTEPH) [6,7],并已被批准用于治疗的适应症(3]。
在为期12周的PATENT-1研究(肺动脉高血压可溶性鸟苷Cyclase-Stimulator试验1),riociguat显著提高6分钟步行距离(6随钻测量)多环芳烃与安慰剂相比,患者36米的最小二乘均值差异(95% CI 20-52 m, p < 0.0001) (6]。Riociguat也大大改善了一些次要的端点,包括PVR (p < 0.0001),脑利钠肽的氨基端激素原(中位数水平以上病人)(p < 0.001),世界卫生组织(世卫组织)功能类(p = 0.0033),时间的临床恶化(p = 0.0046)和Borg呼吸困难评分(p = 0.002)。在PATENT-1 Riociguat一般耐受性良好;最常见的严重不良事件(节约)晕厥,恶化的PH值、胸痛和右心室衰竭(6]。
病人完成PATENT-1都有资格进入PATENT-2,非盲、扩展研究,评估的长期安全性和有效性riociguat PAH患者。这里我们报告一个临时的结果分析PATENT-2,大多数病人收到≥1年的治疗。
方法
病人
入选标准为PATENT-1发表之前(6]。病人被邀请参与PATENT-2 PATENT-1完成后没有进行研究与毒品有关的节约。患者退出PATENT-1,由于PH-related临床恶化,是不合格的。
这项研究是按照良好的临床实践指南和赫尔辛基宣言。研究协议是所有参与中心的伦理委员会批准,所有病人给他们的书面知情同意。PATENT-1研究注册www.clinicaltrials.gov标识号NCT00810693。
研究设计
PATENT-2是一个多中心、非盲、单一群体的研究,在97年进行的124个中心(在30个国家的27)参与PATENT-1。这项研究由一个8周,双盲相位调整剂量,紧随其后的是一个开放研究阶段,将会继续,直到所有患者转换到商用的药物。
在开放研究阶段,患者接受一个单独调整剂量的riociguat最多2.5毫克,每日3次。调查者可以调整riociguat剂量根据病人的需要,考虑收缩压,副作用和发展潜在的多环芳烃。的详细描述riociguat剂量在专利研究补充附录中可以找到。
评估
这项研究的主要目的是评估长期riociguat治疗的安全性和耐受性。安全参数包括不良事件(AEs)和实验室变量。探索性疗效评估包括6随钻测量,中位数水平以上病人功能类,临床恶化,Borg呼吸困难评分,EuroQol显示组件(EQ-5D)问卷和生活与肺动脉高压(液体变阻器)问卷。评估发生在进入PATENT-2,星期2,4,6,8 - 12,每3个月。所有的病人停止研究药物停药后30天安全后续访问。
分析
所有的变量进行了分析叙述地在这个非盲、non-comparative研究。基线是指PATENT-1研究的开始。
PATENT-2第12周的研究中,缺失数据估算根据去年观察结转(LOCF),除了在死亡或临床恶化的情况下没有后续访问,使用以下规则:6随钻测量,最坏的可能值(0米);功能类,糟糕的分数(IV)病例的临床恶化没有后续的访问和坏的可能值+ 1例死亡(V);Borg呼吸困难评分,最坏的可能值(10);EQ-5D液体变阻器问卷,糟糕的分数。最可能的值中位数水平以上病人没有估算。
此外,下面的探索性缺失数据敏感性分析在1年PATENT-2研究:LOCF,没有最坏情况价值归责,6随钻测量;LOCF,最坏情况+ 1 (V)归责为死亡的情况下,谁的功能类;重复和混合模型(MMRM)分析6随钻测量措施。MMRM应用与基线值,访问,前治疗组的交互访问和基线的交互访问和前治疗组,作为非结构化固定效应和协方差矩阵的一个病人的观察。
临床恶化的生存和1年使用kaplan meier分析估计,在患者审查如果他们没有达到治疗1年或如果他们退出了没有经历一个事件。此外,最坏情况分析在1年临床恶化(假设一个病人辍学经历临床恶化后立即退出),和生存(假设一个病人辍学死后立即退出)。
结果
病人
的405名患者完成了PATENT-1研究中,396(98%)进入PATENT-2研究(图1)。病人的特点是组织PATENT-1研究基线之间的平衡;62%的患者有特发性多环芳烃和97%的功能类II或III (表1)。在截止2013年3月的数据,324名患者(82%)接受持续治疗和84%收到治疗≥1年(图1)。治疗持续时间是95周(中位数91周)和累积治疗剂量为718 (。
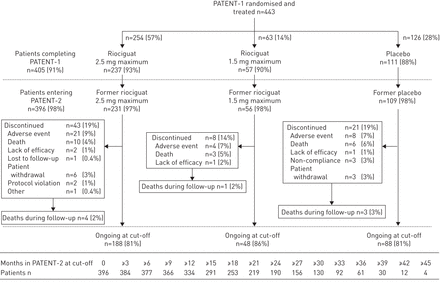
病人性格和PATENT-2期间的患者数量在指定时间点的研究。
最后8周,双盲,调整剂量期间,大多数患者在前riociguat 2.5毫克最大的集团,前者riociguat最大1.5毫克组和安慰剂组接受riociguat 2.5毫克的剂量每天三次(分别为79%、91%和77%)。这个剂量是维持在1年的大多数病人PATENT-2研究(86%)(图S1)。PATENT-2期间开放阶段的研究中,49个患者接受≥1 up-titration riociguat剂量,和41名患者接受≥1 down-titration riociguat剂量。
开始的时候PATENT-2研究中,199名(50%)患者接受额外PAH-specific药物(所有的预处理子群PATENT-1研究);171例(43%)接受内皮素受体拮抗剂(时代),25(6%)接受non-intravenous前列腺素类和三个(1%)接受时代和前列腺素类。PATENT-2 1年的研究中,164名(54%)患者接受额外PAH-specific药物前therapy-naive(11%的患者和97%的前进行预处理的病人);140(46%)接受时代,11(4%)接受前列腺素类和13(4%)接受时代和前列腺素类。
安全
最常见的AEs PATENT-2研究中所示表2。低血压被报道在9%的病人和晕厥在7%。与PATENT-1研究的最初12周相比,降低exposure-adjusted利率每100人(被认为在扩展阶段最常见的AEs和AEs的特殊利益(表S1)。
与毒品有关的AEs是在54%的患者报告;最常见的是头晕(9%)、头痛(8%)和消化不良(8%)。节约是在52%的患者报告,和毒品节约7%。最常见的毒品节约包括晕厥(2%)和恶化PAH (1%)。所有病例都解决,除了两种情况恶化的PAH(一个死亡,一个没有解决)。
PATENT-2研究期间,25例(6%)病人报道AEs和10个(3%)病人报告节约咯血/肺出血。的报道节约PATENT-2研究中,五个被研究人员分级严重一样温和的和五个等级。在两个(1%)病人,由调查人员相关的情况下被认为是研究药物。一个(0.3%)病人死亡(毒品),一个(0.3%)病人需要riociguat撤军(这个病人随后死亡)和一个(0.3%)病人中没有解决/解决研究分界点。在剩下的七个病人(2%)、咯血/肺出血已经解决或者解决不需要riociguat撤回或减少剂量。
在PATENT-1研究中,六名(2%)患者最大riociguat 2.5毫克组报道AEs和两个(1%)病人报告节约咯血/肺出血。然而,exposure-adjusted咯血/肺出血率低PATENT-2研究与PATENT-1研究相比,由于PATENT-2研究的治疗持续时间更长。在PATENT-2研究中,咯血的速度/肺出血AEs / 100是6.3白细胞数量与9.9 riociguat组和安慰剂组的11.1 PATENT-1研究。对于节约,exposure-adjusted咯血/肺出血率每100年PATENT-2白细胞数量为1.8与4.3 PATENT-1 riociguat组的研究(没有节约咯血/肺出血报告PATENT-1安慰剂组的研究)。
总的来说,61%的患者在PATENT-2研究接受口服抗凝血剂。然而,之间没有链接已被确认的风险增加呼吸道出血事件和抗凝治疗,用维生素K拮抗剂治疗或国际正常化率的范围。此外,之间没有链接已被确定呼吸道出血和剂量riociguat或治疗后启动的时间。
总的来说,有27人死亡,其中三个被认为是与毒品有关的研究。这些都是由于咯血/肺出血和肺炎;心肺逮捕和hypoxic-ischaemic脑病;和多环芳烃恶化。
探索性分析
6随钻测量
改进PATENT-1 riociguat组6随钻测量的研究持续PATENT-2第12周和1年的研究中,和病人的安慰剂组PATENT-1研究显示相应的提高与前者riociguat团体后过渡到riociguat (图2)。PATENT-2 1年的研究中,通过均值±6随钻测量改变了sd前riociguat 53 70±2.5毫克最大组(n = 192), 56±88在前riociguat最大1.5毫克组(n = 50), 46±76在前安慰剂组(n = 85)和51±74总人口(n = 327) (图2)。在整个人口,绝对均值±sd随钻测量是419±97 1年(n = 327),与367年相比±67在基线(n = 396)。
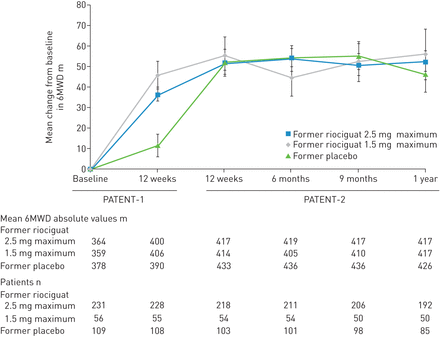
意味着改变基线的6分钟步行距离(6随钻测量)PATENT-1和PATENT-2研究。数据观测值和误差代表标准错误的意思。#:绝对的价值。
缺失的数据敏感性分析、使用不同的归责方法显示改善6随钻测量与观测值相比略低(表S2)。这是由于患者退出倾向于较低6随钻测量前退学。然而,整体的解释研究结果没有影响。
Riociguat增加患者达到6的比例随钻测量≥380 PATENT-1研究,这持续了1年PATENT-2研究。前服用安慰剂的患者的比例达到6随钻测量≥380后会增加类似的过渡到riociguat PATENT-2研究(图S2)。
中位数水平以上病人
riociguat组中位数水平以上病人的减少PATENT-1研究PATENT-2持续长达一年的研究中,与安慰剂的患者前显示一个类似的减少后过渡到riociguat (表3)。
那些功能类
在1年,功能类有所改善,稳定或恶化:36%,57%,7%的患者,分别在前riociguat最大2.5毫克组(n = 199);31%、67%和2%的患者在前riociguat最大1.5毫克组(n = 51);26%、66%和8%的患者在前安慰剂组(n = 89);和33%、61%和6%的患者在整个人口(n = 339) (图3)。我的病人比例功能类,II, III和IV总人口的8%,61%,28%和2% (n = 339)在1年,这一比例为3%,43%,54%和1%在基线(n = 395)。
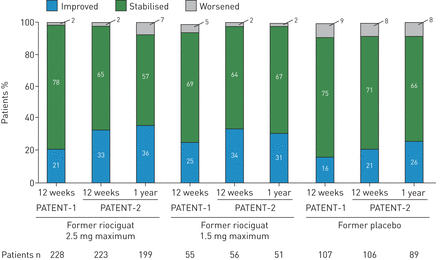
世界卫生组织的病人的比例提高功能类,稳定或恶化前riociguat 2.5毫克最大病人组,前者riociguat 1.5毫克最大病人组和前病人安慰剂组。数据观测值。比例可能不加起来100%由于舍入。
类似于6随钻测量,缺失数据敏感性分析显示,谁稍微降低改进功能类与观测值相比(表S2),但整体的解释研究结果没有影响。
生存和临床恶化
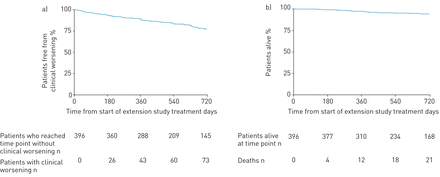
总体而言,21%的患者经历了临床恶化事件期间PATENT-2研究(表4)。估计的临床worsening-free生存1年为88%(95%可信区间,84 - 91%)(图4)。估计在1年生存率为97% (95% CI 94 - 98%) (图4 b)。然而,这些分析假设病人辍学有相同的事件率随着那些不断,这可能会导致正偏压辍学后如果事件率更高。因此我们的生存表现最糟糕的敏感性分析和临床恶化,患者退出被认为已经死亡或有经验的临床恶化。使用这些分析,临床worsening-free生存1年为84% (95% CI 80 - 87%)和1年的存活率为90% (95% CI 87 - 93%)。
kaplan meier情节)临床恶化和b)生存在总人口PATENT-2研究。在1年,临床worsening-free生存的估计速度为88% (95% CI 84 - 91%)和估计的存活率为97% (95% CI 94 - 98%)。使用最坏情况分析临床恶化,患者退出被假定拥有经验丰富的临床恶化,临床worsening-free生存1年的利率是84% (95% CI 80 - 87%)。使用生存的最坏情况分析,患者退出被认为已经死亡,在1年存活率为90% (95% CI 87 - 93%)。
特发性患者存活率相似/家族多环芳烃和多环芳烃与结缔组织疾病(图S3),估计1年生存率为97% (95% CI 94 - 99%)和97% (95% CI 90 - 99%),分别为。生存也是类似的首次治疗病人和病人之间使用时代或前列腺素类(图S4),估计1年生存率为97% (95% CI 93 - 99%)在两个子组。
讨论
生成的数据从PATENT-2研究支持结果PATENT-1研究中,即。riociguat是很有效的治疗有症状的患者多环芳烃,首次治疗的病人或病人已经接受一个时代或前列腺素类。AE概要的riociguat PATENT-2研究类似的PATENT-1研究[6),没有新的安全信号识别。riociguat的良好的耐受性是这一事实突显出,多数患者接受的最大riociguat每日三次,每次2.5毫克剂量为1年。
晕厥是一个关键的AE PAH患者中观察到,并可能增加了PAH-specific疗法(8- - - - - -11]。晕厥的速度在PATENT-2研究是每100人5.9例(7%的患者),白细胞数量略低于最大riociguat 2.5毫克组中观察到的速度在PATENT-1研究(每100人8.8例白细胞数量(1%的患者)。值得注意的是,利率PATENT-1晕厥的研究是高于安慰剂组相比riociguat最大2.5毫克组(4%与1%)(6]。晕厥的发病率在PATENT-2研究与观察患者的长期研究多环芳烃与西地那非(11%)(11)和treprostinil (4%) (9]。
咯血和肺出血的并发症多环芳烃(12,13]。咯血的速度和肺出血的节约PATENT-2研究是每100人1.8例白细胞数量(3%的患者)相比,每100人4.3例riociguat组的白细胞数量PATENT-1研究(1%的患者)。肺出血的风险可能增加在一些病人反映riociguat警告在当地处方信息(产品特征的总结),应视为与毒品有关。然而,咯血和肺出血的风险可能会受到其他因素的影响,如年龄、疾病的严重程度,恶化肺血液动力学和伴随的抗凝剂治疗(12,14]。riociguat如何引起咯血的机理和肺出血尚不清楚。一个假设是,观察可能与常riociguat对支气管动脉循环,过分生长和体循环与血管生成相关即。支气管动脉,在PH值(13,15),增加了流动和偏袒咯血。
6随钻测量的改进和功能类,观察riociguat组在12周的PATENT-1研究PATENT-2持续长达一年的研究。6 PATENT-2第12周的研究中,随钻测量在前增加了52米riociguat 2.5毫克最大组(积极治疗后6个月)。患者达到治疗1年,增加6随钻测量观察51米,有33%和61%的病人,显示改善和稳定,分别在那些功能类。重要的是,在前安慰剂组,在6随钻测量和改进前的功能类接近riociguat组12周和1年后的PATENT-2研究。6随钻测量的改进和功能类是一致的使用各种归责缺失数据的方法。
估计在1年存活率PATENT-2研究为97%,临床恶化的发生率和住院治疗,由于多环芳烃,是相对较低(分别为21%和10%,平均治疗时间91周),支持的长期疗效riociguat PAH患者。使用最坏的敏感性分析,患者退出被认为已经死亡或有经验的临床恶化,1年期和clinical-worsening自由生存的存活率分别为90%和84%,分别。
其他PAH疗法显示效果在长期的扩展研究8,9,11,16- - - - - -18]。最接近的研究PATENT-2研究中,在研究设计和人口方面,可能是PHIRST-2研究(他达拉非肺动脉高血压和响应),PAH患者接受非盲的他达拉非(20毫克或40毫克)长达1年(17]。最近,结果报告的第三阶段SERAPHIN研究(研究内皮素受体拮抗剂在肺动脉高血压改善临床结果),一个长期的事件驱动的研究调查macitentan PAH (19]。然而,由于时间的差异,终端和研究人群,inter-study比较困难。
PATENT-2的研究也有一些局限性,是常见的所有开放的长期的扩展研究。尽管没有安慰剂对照集团在目前的研究中,长期管理安慰剂患者进行性疾病,如多环芳烃、可能导致临床恶化。知道后续的一个初始的随机研究提供了额外的安全数据和强化疗效结果。缺乏一个安慰剂组,大约有50%的患者接受相应治疗额外PAH-targeted疗法,也意味着不可能明确属性的所有riociguat疗效和安全性研究。然而,相对较低的附加治疗1年之后的首次治疗组(11%)支持的长期疗效riociguat,今年五月,在某种程度上,是由于缺乏PAH-specific药物中心。
进一步限制是患者退出可能导致偏向患者在之后的时间点riociguat治疗反应良好。这可能导致一个高估的改善功效参数在1年。为了解决这个问题,我们进行了敏感性分析6随钻测量和世卫组织功能的类。这些分析导致低但可比估计的有效性。
此外,访问的频率在非盲阶段PATENT-2研究(每3个月)低于PATENT-1研究访问的频率(每2周)。这可能导致低水平的估计的频率较轻的AEs在PATENT-2研究与PATENT-1研究相比,由于潜在的回忆偏倚。
总之,长期治疗riociguat在PAH患者耐受良好。PATENT-1研究,咯血/肺出血病例中观察到PATENT-2长期扩展研究。提高运动能力和功能能力维持长达1年的治疗,存活率为97%和88%的临床worsening-free生存1年(分别为最坏情况分析分别为90%和84%)。这些结果支持riociguat长期治疗是一种有效的多环芳烃,作为单一疗法,结合时代和前列腺素类。
脚注
社论评论看欧元和J2015 45:1211 - 1213 . DOI:10.1183/09031936.00032715]
可以从本文的补充材料www.qdcxjkg.com
临床试验:这项研究是在注册www.clinicaltrial.gov标识号NCT00863681。
支持声明:本研究得到拜耳医药保健有限公司的支持药品(德国柏林)。编辑提供的援助是艾德菲通讯有限公司(英国Bollington)由拜耳保健药品。
利益冲突:披露可以找到与本文的在线版本www.qdcxjkg.com
- 收到了2014年5月16日。
- 接受2014年11月11日。
- 版权©2015人队