文摘
Omalizumab已被证明会降低恶化率在中度到重度过敏哮喘。我们的目的是评估omalizumab疗效和安全性在真实环境中严重哮喘的孩子。
104名儿童(6 - 18岁),然后在儿科肺三级保健中心、包括初omalizumab治疗。哮喘控制水平,加重,吸入皮质类固醇剂量,肺功能和不良事件进行评估/ 1年。
孩子们的特点是过敏敏化作用三个或更多过敏原(66%)、高IgE水平(平均1125 kU·L−1每年),发作率高(4.4)和医疗使用在前一年,和高吸入皮质类固醇剂量(平均每天703μg当量fluticasone)。哮喘控制水平定义为好,部分或贫穷,改善从0%、18%和82%,加入53%,20周后30%和17%,67%,25%和8%分别为52岁的周(p < 0.0001)。恶化和住院率下降了72%和88.5%,分别。在12个月里,用力呼气量在1 s提高了4.9% (p = 0.023),和吸入皮质类固醇剂量下降了30% (p < 0.001)。6个病人停止omalizumab相关的严重不良事件。
Omalizumab改善哮喘控制在儿童严重过敏哮喘和一般耐受性良好。观察到的好处大于在临床试验报告。
文摘
Omalizumab改善哮喘控制儿童患有严重哮喘和过敏一般耐受性良好http://ow.ly/oLoBp
介绍
严重哮喘儿童的管理仍然是一个挑战,其患病率估计哮喘人口的5% (1]。“有问题的严重哮喘”这个词最近喜欢描述这些学龄儿童哮喘控制不佳,尽管维持治疗≥400μg fluticasone每天或同等的吸入型皮质类固醇激素(女性)加上吸入长效β-agonist(腊八粥)或白三烯受体拮抗剂或茶碱2]。每天孩子们的特征在不同程度的症状,严重或频繁发作,医疗利用率高,持续的肺功能改变和改变生活的质量。问题严重的哮喘是一种昂贵的疾病在童年尽管相当低的频率。Omalizumab是最近和昂贵的治疗设计作为添加治疗难治性过敏性哮喘患者。儿童纳入临床试验的一部分,大年龄组第一临床试验主要包括成年人(年龄12 - 79年)(3),然后具体的儿科试验(4- - - - - -8]。这些研究表明显著减少急性加重和医疗使用,和改善生活质量,但症状和肺功能测试影响不大(肝功能)。法国卫生当局的利用率有限omalizumab过敏儿童不受控制的持续哮喘和/或严重的急性加重,气道阻塞严重的肝功能评估> 12岁的时候,尽管服用高剂量ICS或口服糖皮质激素与至少腊八。在法国,omalizumab自2006年以来一直使用> 12岁儿童和总IgE≤700 kU·L−1自2009年以来,对于那些> 6岁和总IgE≤1500 kU·L−1。一些真实的研究一直在进行成人(9,10]。后者不仅证实也扩展以前的药物有效性和安全性观察随机化试验。相反,知识omalizumab利用率和安全仍然有限的童年11,12]。这是标记为青少年(12 - 18岁)被稀释在大主要研究[3]。此外,omalizumab对疾病控制的影响尚未作为疗效评估结果(4- - - - - -7]。
这一观察性研究报告的真实有效性和安全性插件omalizumab治疗在一大群孩子过敏严重的哮喘。的主要目的是评估附加omalizumab哮喘控制的影响,如前所述在步骤5中全球倡议的哮喘(吉娜)指南13]。我们也评估其他功效的结果(恶化率、医疗利用率,ICS爱惜效应和肺功能变化),以及安全。
材料和方法
设计
这项研究是在12个儿科肺学一年真实的多中心调查和过敏三级保健中心(图1)。
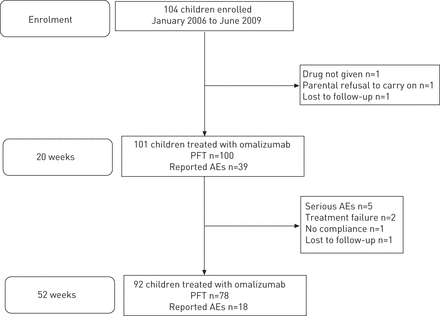
流程图显示研究的进程。击球:肺功能测试;AE:不良事件。
主题
所有确认过敏严重哮喘患者来说,omalizumab治疗发起2006年1月至2009年6月,< 18岁,谁是被包括在研究[14]。他们收到了长期随访(> 12个月的三级护理中心)。这使得描述他们的哮喘表型和评价治疗疗效和遵从性。批准的调查是北方不加人力保护委员会临床研究以及国家信息自由委员会(委员会国家de l 'Informatique et des自由)。
方法
基线特征从医学文件:收集人口数据,哮喘历史(年龄在哮喘的诊断,住院治疗哮喘、重症监护室(ICU)承认曾经),哮喘严重程度在过去的一年中评估使用的发作率要求系统性皮质类固醇和/或医疗利用率(急诊科(ED)访问和住院),过敏敏化作用评估皮肤刺痛测试,具体和总IgE水平,并存病(过敏性鼻炎、特应性皮炎、食物过敏和超重由身体质量指数>第97个百分位年龄和性别)。
评估的有效性和安全性
数据收集和记录在一个标准化文件的第一个政府(V0), 20±4周(V1)和52±4周(V2)。哮喘控制水平是评估在每个访问前4周,归入穷人,部分或根据吉娜3水平:良好的控制,在一定程度上控制和不受控制的哮喘(13]。发作被分别量化,只有那些需要全身性类固醇爆发≥3天保留在评估,强调了在先前的试验(4- - - - - -7]。医疗利用估计的数量ED访问或住院或进入ICU哮喘。肝功能由煤层瓦斯曲线和post-inhaledβ2-agonists,通常在每个中心执行。用力呼气量在1 s (FEV1)和用力呼气流在25 - 75%的用力肺活量(FVC) (FEF25 - 75%)被表示为%预测值,FEV1/ FVC比例的比例。维持治疗的数据收集每一次访问太阳系时和ICS剂量标准化每天等效剂量(丙酸μg·−1),根据法国指南。在每个访问,任何重大不良事件(AEs)据报道,评价药物的安全性。他们描述的叙述形式,然后分类在重大或严重的AEs,欧洲药品局的要求。重要的AE导致任何干预,如。治疗停药,严重的AE导致住院,或无任何危及生命的事件。
分析
主要结果omalizumab响应能力的标准是实现良好的哮喘控制的治疗。我们定义良好的哮喘控制根据控制哮喘的吉娜标准(白天症状:每周两次或更少;活动限制:没有;夜间症状/觉醒:没有;需要释放/救援治疗:每周两次或更少,FEV正常1根据吉娜指南(13])。二级标准减少严重的恶化率和医疗使用期间观察到的与前一年相比,ICS剂量减少,肺功能改善的治疗。安全分别进行了分析。
统计数据
数据提出了n为定性变量(%),意味着为定量变量(95%置信区间)。对比V0, V1和V2 MacNemar测试进行的定性变量和一个配对样本t检验的定量变量。
在我们的人口,双变量分析进行检查潜在的因素,可能影响响应omalizumab V1和V2。年龄的关系(< 12或≥12年),FEV1/ FVC(< 0.8或≥0.8),前一年的恶化(< 3或≥3)、敏化作用(< 3或≥3),过敏并存病(现在或缺席),IgE水平(≤700或> 700 kU·L−1),给药方案(每2或4周)和应对omalizumab进行了卡方测试。确定之间的关系很好的应对omalizumab和IgE水平,Mann-Whitney测试使用。连续变量之间的相关性被皮尔逊相关系数的测量。
我们也分析了患者的子群中的所有结果IgE水平> 700亏·L−1。一个假定值≤0.05被认为是显著的。所有分析使用SAS软件版本9.2 (SAS研究所Inc .,卡里、数控、美国)。
结果
描述性的数据
104名儿童被包括在内,所有满足严重哮喘的标准(表1)。44%的人已经住院期间,与20个孩子需要不止一个承认,导致87年,八在加护病房。6(5.8%)孩子们需要连续口服皮质类固醇疗法。这种过敏性人口的特点是:1)IgE水平很高,价值高于阈值700桥·L−157例(55%)孩子,IgE水平在1500 - 3000年间kU·L−13000年20名儿童和>桥·L−1七个孩子;16这些27岁儿童IgE水平最高的< 12年;2)polysensitisation: 66%的人至少有三个过敏原过敏敏化作用;3)高频率的食物过敏(35%);和4)高频过敏性鼻炎(85%)(表1和图2)。肺功能测试结果显示与FEV气道阻塞1< 36%,80%的pred或FEF25 - 75%FEV pred < 60% 51%1/ FVC < 0.8和< 0.7 53% 26%的孩子。
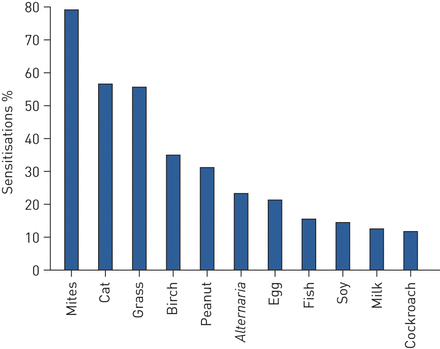
过敏原检测到敏化作用在基线总人口(n = 104)。食物过敏,链格孢属和蟑螂敏化作用在这些严重的哮喘儿童过多。
结果是在101名患者在V1和V2 92例(图1)。在V1,在八个孩子,医生停止治疗。一个病人失访V1和V2之间。
Omalizumab剂量
Omalizumab是管理所需的计量表可用时最初的处方,建立剂量长达700年< IgE水平kU·L−1根据重量。因此,IgE水平高于该阈值的孩子收到的最大推荐剂量375毫克每2周。68%的儿童接种omalizumab每2周,其余32%收到每4周治疗。由于高IgE水平遇到在这个人口,有两个注射部位的儿童和76%升至三个站点数量6%的病人。总体而言,58%利多卡因局部麻醉的要求/ prolicaine注射应用程序的网站。
哮喘控制
控制明显改善哮喘的治疗(图3)。哮喘控制水平在0%,部分在18%,82%的人口的贫困治疗起始和提高至53%,20周后30%和17%,67%,25%和8%分别为52岁的周(p < 0.0001)。20例(20%)患者部分(n = 16)或不受控制的控制(n = 4)哮喘在V1成为良好控制V2。相反,六个孩子改善在V1,然后V1和V2之间失去了控制。此外,11(10.5%)与哮喘控制不佳的孩子在V1和V2 V0搬到部分控制。因此,只有14%的儿童并没有改善。患者平均基线IgE水平没有差异控制,没有控制好(部分或不好控制)在V1和V2 (V1: 1214 (385 - 1797) kU·L−1与1040年(380 - 1445)kU·L−1分别,p = 0.32;V2: 1173 (365 - 1714) kU·L−1与891年(276 - 1061)kU·L−1分别p = 0.21)。
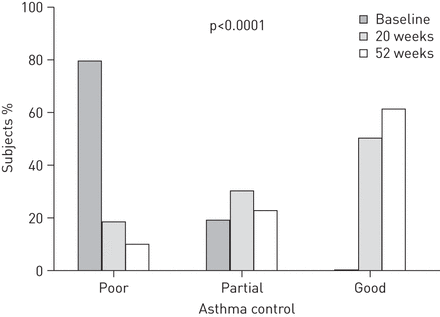
哮喘控制水平基线(n = 104),在20±4周(n = 101), 52±4周(n = 92)附加omalizumab起始后的治疗。
急性加重
显著减少急性加重的数量下观察治疗,与前一年相比(图4)。严重发作的平均利率从4.4(3.7 - -5.2)/减少病人在前一年为1.25(0.55 - -1.95)在治疗(p < 0.0001)。这代表在今年减少72%。恶化率低(0.66(0.33 - -0.99)/病人)同期观察V0-V1早期,并维持在0.57(0.23 - -0.93)/患者同期v2 v1。此外,孩子需要住院的比例在过去一年中从44%下降到6.7% (n = 7, 10招生),没有迫使一个呆在ICU治疗(p < 0.001)。住院都减少了88.5%。
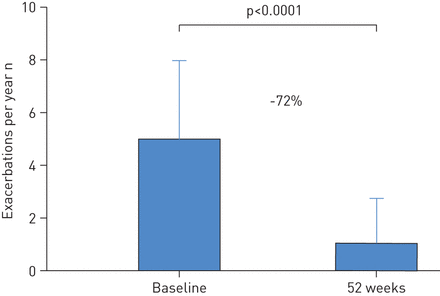
恶化率的变化在一段时间内的52周附加omalizumab与不受控制的严重的过敏哮喘儿童治疗。数据意味着(95%置信区间)。
肺功能测试
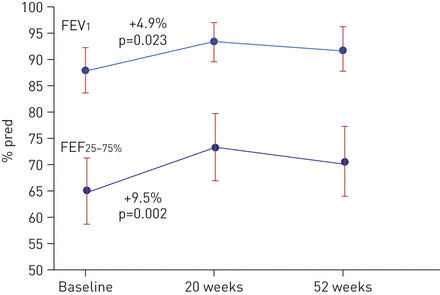
FEV1是在78年和FEF有空吗25 - 75%在64名儿童的随访(图5)。的意思是改善肺功能评估V2 pred 4.9% (95% CI 0.69 - -9.19;pred p = 0.023)和9.5%(95%可信区间3.7 - -15.2;FEV p = 0.002)1和FEF25 - 75%,分别。
变化意味着(95%置信区间)pre-bronchodilator用力呼气量在1 s (FEV1),用力呼气流量在用力肺活量(FEF的25 - 75%25 - 75%从基线omalizumab治疗期间)。
吸入类固醇的影响
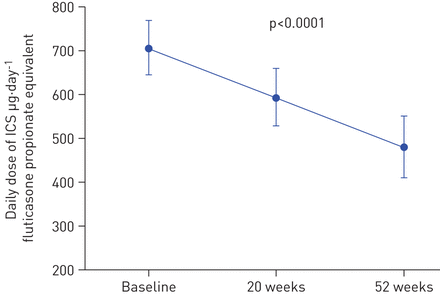
年治疗,ICS的效应是-212(-284 - -140)μg,相当于减少了30% ICS剂量(图6)。FP的平均服用剂量或同等是703(642 - 764)μg V0, 592年(528 - 656)μg V1和481(412 - 551)μg V2 (p < 0.0001)。减少46.7%的患者达到≥50%的服用剂量,只有5.4%保持不变ICS剂量之间,V2。口服糖皮质激素被撤回所有与这六个孩子维持疗法在基线。
变化的每日剂量吸入激素(ICS)(μg·−1fluticasone propionate-equivalent)从基线omalizumab治疗期间。数据意味着(95%置信区间)。
影响响应omalizumab的修饰符
唯一重要的因素与一个好的回应omalizumab是年龄。< 12岁儿童比大一些的孩子较少控制在V2 (53.5%与76%;p = 0.02)和发作更频繁接受治疗(1.85 (0.33 - -3.38)与0.76 (0.45 - -1.08);p = 0.049)(表S1和S2)。上面详细的特征、过敏并存病(过敏性鼻炎、特应性皮炎和食物过敏)和过敏敏化作用,在V1和V2预测良好的控制。我们也分析了管理频率(每2周与每4周),我们没有发现任何差异在所有结果(表S1和S3)。
接下来我们重复分析的子群的孩子IgE水平高(> 700 kU·L−1)。我们没有找到任何关系IgE水平和所有结果(表S4)。
安全
总体而言,至少有一个AE被报道在47个孩子(图1)。最常见的AEs在注射部位疼痛(n = 23),这导致一个病人停药,局部反应10人。注射后衰弱等症状(n = 6),头痛(n = 3),腹痛(n = 3)和迷走神经的问题(n = 3)也报道。严重的AEs由于omalizumab根据医生的评估,使一个精确的描述(5在V1和V2),导致治疗停药6个病人,如下:长荨麻疹(n = 1),过敏反应(n = 1),和系统性反应与腹部和肌肉疼痛、疲劳和头痛(n = 4)。Omalizumab成功三周进行医学监督两个病人。最后宣布事件是速发型过敏反应的情况下与异国情调的水果过敏,和omalizumab无关。
讨论
我们报告一个观测调查的104例重度过敏哮喘,过敏性儿童和青少年谁受益于omalizumab治疗作为一个附加疗法高水平的维持治疗。本系列所有的孩子收到了长期随访三级保健中心,让他们有一个精确的描述哮喘,与哮喘控制不佳和目标相关的辅助因子,例如合规或环境暴露。观察性研究的兴趣是提供完整的真实的数据,这可能不同,在临床试验中获得的(表S5)。我们的调查显示,更大的改善哮喘控制、减少更大的恶化率和医疗利用和steroid-sparing效应大于在药效试验报告。值得注意的是,孩子们似乎更严重的影响学习,更少的控制和更多的特异反应性比前面的临床试验,表明一个特定的临床资料omalizumab的目标。这些结果在童年是在协议与最近其他观察性研究中观察到的成人和青少年严重过敏持续哮喘患者(9,10]。这个调查的主要结果点的数量的孩子取得了良好的控制水平(根据吉娜标准(13),从而提供新数据的临床相关性。肯定的临床试验显示omalizumab功效恶化率。相比之下,这种效应不明显症状的控制(4- - - - - -7]。在这个调查中,控制了一半的孩子在前20周的药物管理局。此外,长期治疗的1年启用三分之二的这些孩子能达到良好的控制。这些数据表明,推荐的4个月的意思是公认的时间间隔对药物反应评价必须考虑在个案基础上。考虑到那些从贫困部分控制,只有14%的儿童没有改善。这意味着应该视为nonresponders六分之一。减少夜间症状的观察支气管扩张剂和使用需求ilgromet al。(6),但不是由L再次等(5]。在不太严重的哮喘儿童,Busse等。(4]报道减少25%的症状评分,包括日夜症状,学校旷工和活动干扰,超过2周。这些作者观察到显著提高哮喘控制、评估哮喘控制测试,只在6-11-year-old年龄范围。在我们的调查中,反应也观察到在这个年龄段,但不明显。年轻的时候不应该延迟ige治疗需要时。
的另一个主要发现是减少72%的严重恶化,只有少数参与者需要住院,没有被承认,当收到omalizumab ICU。恶化率的减少归因于omalizumab最显著的影响,据估计,导致43 - 45%减少在最近的一项荟萃分析11]。之前我们的结果强化了43 - 50%减少报道在中度或重度哮喘患儿5,7]。此外,影响加重了第一个月的治疗期间,按照28 - 16周的研究ilgrom等。(6)和Brodlie等。(8),分别。相比之下,K但等。(7)观察到的最高减少恶化在最后6个月1年的审判。
一个额外的好处中观察到这种严重的过敏哮喘患者的调查corticosteroid-sparing效果。口服类固醇破裂的下降是一个预期的结果戏剧性的减少急性加重。此外,所有六个孩子之前需要每日口服类固醇治疗能够停止服用,根据最近的一份报告(8]。可以减少ICS剂量在几乎所有的病人。这与报告的适度的ICS剂量减少4%的儿童类似ICS剂量高,但不太严重的哮喘5]。相反,米ilgromet al。(6]ICS剂量中值下降了100%年轻患者暴露于低剂量的5倍比在本系列和其他5]。目前虽然有限,但这些数据支持这一事实下台不是ICS剂量相关omalizumab发作。Busse等。(4)也公布了109年ICS剂量显著差异µg·−1budesonide-equivalents omalizumab和安慰剂组之间,在那些孩子暴露敏感蟑螂和那些更严重的哮喘。
最后,两个大(FEV1)和小(FEF25 - 75%)气道功能参数提高了治疗,并没有观察到在以往试验(4,6]。虽然增加很小,可能没有临床相关,它提供了一个积极的结果,作为一个下降严重哮喘儿童肺功能被描述在多年跟踪(15]。持久的积极影响肺功能随时间会说明一个修饰词影响长期严重哮喘患者疾病进展与吸入糖皮质激素药物。
这种改善哮喘控制观察尽管近一半的患者可能会被视为接受一种次优的omazilumab剂量,因为欧洲计量表的研究仅限于IgE水平< 700 kU·L−1。尽管如此,对治疗的反应取决于自由IgE水平的降低(16),这是与测量IgE水平,不能定期评估。最后,对治疗的反应不是由政府修改频率。这支持这项提议减少注射的频率每4周总剂量时≤600毫克每4周。
我们不能绝对排除,可能与改善皮下omalizumab管理模式,提高合规相比,吸入的药物。然而,我们的人口组成的控制不佳的哮喘患儿,跟进多年在三级保健中心合规是定期评估2,14]。这表明他们中的大多数哮喘属于真正的概要文件。相比之下,孩子们在美国儿科试验(包括4- - - - - -7),包括病人在我们的研究中有更严重的哮喘和更高的利率每年需要口服类固醇(4.4的恶化与每年1.9 - -2.7),住院治疗上(74%与18 - 52%)和需要医疗利用率高。事实上,欧洲omalizumab认可比我们更严格的认可,限制政府严重哮喘控制不好用高剂量的ICS治疗或口服类固醇与至少一个腊八。情况常常如此严重儿童哮喘相关的肺功能的改变依然温和,但与大范围的变化(15,17]。一半的孩子,然而,削弱FEF显示25 - 75%,这似乎是最敏感的标志功能变化在严重哮喘1,18]。
这些孩子中有一种特殊的严重的过敏性表型。总免疫球蛋白e浓度超过两个,以前在omalizumab试验报告(5,6],三分之二的孩子们polysensitised,三分之一有食物过敏,鼻炎发病率几乎是常数。提升生产总量的IgE被证明是儿童哮喘严重程度的一个标志(19),与更大的医疗利用率,改变肺功能和气道高反应性20.,21]。相比之下,如此严重的过敏的地位尚未明确个性化问题严重哮喘风险作为一个集团在先前的军团(15,17最近指南[]或2]。polysensitisation三个或更多过敏原不过严重[联系在一起22,23)或不受控制的哮喘(24]。这是按照最新发现,它定义了一个特定的儿童严重哮喘的表型与多个敏化作用不仅吸入,而且食物过敏原(25]。食物过敏已确定的风险因素危及生命的哮喘急性加重(26,似乎也参与了哮喘病例的困难。最后,一个敏化作用链格孢属,以前严重哮喘过敏原27在这群),也过多。8倍高于2.8%法国最近决定在一个大型研究[28]。
系统性反应或一般症状的比例相媲美,最近详细的Milgrom等。(29日)在一个安全审查,没有区别的数量或类别AEs药物和对照组之间的显示在前面的试验。注射后疼痛或当地的反应不仅是最常见也最期望的现象,考虑到产品的粘度时的调查。这些AEs目前减少最近修改的药物成分。相比之下,这个安全审查(29日),我们报告更少的例荨麻疹,头痛和只有一个相关的过敏反应。6个病人出现严重的不良反应和停止治疗管理。根据应对omalizumab受益,两个在医院和患者成功撤退没有发生不利影响。这表明,收益和风险的平衡应该重新评估抗哮喘儿童治疗。
总之,omalizumab是一种有效和安全的附加治疗在不受控制的严重哮喘和过敏的孩子。这些特点是高IgE生产、polysensitisations和/或食物过敏的认识形成一个族群的真实高度过敏严重的哮喘,和omalizumab反应良好。
确认
我们感激安妮Sardet(服务de Pediatrie、透镜、法国)为她贡献和Phillippe Fauquembergue,席琳Clairet(中心d 'Investigations倩碧Pediatriques,里尔大学医院,里尔,法国)和卡罗尔Langlois(生物统计学部门,里尔大学医院、里尔、法国)为数据收集和管理。我们感谢尼基Sabourin-Gibbs(鲁昂大学医院、鲁昂、法国)为她援助与英语写作和审查的手稿。
脚注
可以从本文的补充材料www.www.qdcxjkg.com
支持声明:本研究拨款支持诺华公司法国和法国儿科肺学和过敏的社会(SP2A)。
利益冲突:披露可以找到与本文的在线版本www.www.qdcxjkg.com
- 收到了2012年9月20日。
- 接受2013年2月14日。
- ©2013人队