摘要
GSK961081是一种双官能分子,展示了毒蕈碱拮抗剂和β-激动剂活动。
这是一个4周,多期,随机,双盲,双伪,安慰剂和萨尔梅托尔控制的并行组研究。剂量在中度和严重的慢性阻塞性肺病(COPD)患者中评估了两次两次每日剂量和三次一次每日剂量。1 s中的槽强制呼气量(fev1)在第29天是主要终点。在第1天和第28天,12-H FEV1所有患者均行肺活量测定。一组患者在第28天接受了完整的24小时肺活量测定。
该研究招募了436名患者。GSK961081在所有剂量和低谷FEV中的安慰剂中均有统计学和临床上显着差异1在第29天(155-277毫升)。最佳的总日剂量为400μg,每天每天400μg或每日两次为200μg,在第29天槽FEV中有所改善1分别为215 mL和249 mL。其他疗效终点也有改善。对血糖、钾、心率、血压无影响,对校正QT伸长无剂量反应效应。
该研究表明,GSK961081是一种有效的COPD支气管扩张剂,安全性和耐受性良好。
摘要
IIb期研究结果显示,毒蕈碱拮抗剂- β-激动剂GSK961081β是一种有效的COPD支气管扩张剂http:///wly/lh7mu.
介绍
慢性,稳定的慢性阻塞性肺病(COPD)的药理管理主要旨在改善生命的症状和质量,优化肺功能,降低加剧和改善运动耐受性[1那2].吸入性支气管扩张剂,包括β2- Aganists和抗血清素,是患者诊断为COPD的患者的主要疗法[1].
虽然不完全理解双支气管扩张剂的机制,但添加β2- 激动剂对抗血清胰岛素的结果导致气道中的大胆膨胀,而不是单独的组分。机械地思考添加β2通过预先接线β通过调节胆碱能神经递血来降低乙酰胆碱(ACH)的释放2(β肾上腺素能受体2-ARs),放大毒蕈碱拮抗剂引起的支气管平滑肌松弛。其次,添加毒蕈碱拮抗剂降低了乙酰胆碱的支气管收缩作用,乙酰胆碱的释放被β修饰2- 方形是,从而放大β引起的支气管扩张2通过直接刺激平滑肌β2-ARS [3.].
临床研究证实了添加β2- 以毒蕈碱拮抗剂对肺功能和患者以患者为中心的成果更有效,而不是单独的组分,并且没有不提供的安全问题[4.-9.].在评估噻托溴铵与福莫特罗或沙美特罗联合用药的研究中,单药联合用药与单药联合用药长达1年的不良事件报告数量和类型相似[6.-10.].
截至2012年,目前没有长效β-激动剂/长效毒蕈碱拮抗剂的许可组合,无论是同一装置中的两个单独药物还是单独的药物。具有毒蕈碱拮抗剂和β-激动剂活动的化合物为药理学活动提供单一的药代动力学曲线,其可能最大化两种机制之间的协同作用,以及与两种化合物的共录相比的更简单的技术和临床发展途径[11.].GSK961081是双官能分子,并在分子的一端具有毒蕈碱拮抗活性,与β分开2通过惰性连接器部分的方面的活动。已经证明了GSK961081的双功能性质体外[12.),在活的有机体内在豚鼠支气管保护模型中[13.].在一项健康志愿者的研究中,服用和不服用普萘洛尔(β2- 肾上腺素能受体阻断)GSK961081在两个受体中显示出在β中的活性2- agagist效果比抗血清胰岛素活动更持久[14.].在50个中度COPD患者中的一个小型,14天的交叉研究中,发现GSK961081是安全且耐受性的,并且显示支气管扩张相对与噻托溴铵加沙美特罗相媲美的安慰剂[15.].
本研究旨在确定GSK961081,剂量和计量间隔的支气管扩张剂效果(使用槽FEV1在第29天作为主要结果),以及中度和严重COPD患者的安全性和耐受性。该研究评估了三种每日剂量和三次两次的每日剂量,安慰剂臂和活性比较器,Salmeterol。
方法
学习规划
这是4周,阶段IIB,多期,随机,双盲,双伪,安慰剂和主动控制,并行组,剂量间隔和剂量测量研究。在筛选访问和7天的运行期后,符合条件的患者被随机化并进入了28天的治疗期。诊所访问是第1,2,14,28和29天,并在最后的诊所访问后的第7天和第7天和两个电话联系人。
在隔夜住宿的患者招待中心的患者在第28天进行了24-H串行肺活量测定量。
样本大小计算
样本量的计算基于主要疗效终点,假设在在线补充材料S1中显示。符合条件的患者被随机分为8组,每日一次剂量为100 μg、400 μg或800 μg,或每日两次剂量为100 μg、200 μg或400 μg的GSK961081,每日两次剂量为50 μg的沙美特罗或安慰剂(表1),比例为2:2:2:2:2:2:2:3。患者配备了两个Diskus吸入器(GlaxoSmithkline,Ware,UK和STEVENAGE,英国),一个用于早上使用,一个用于晚间使用。对于曾经的日常治疗,晚上吸入者是一个安慰剂。该研究通过可逆性与沙丁胺醇和吸入的皮质类固醇(ICS)使用分层。
研究患者
本研究包括当前和前吸烟者≥40岁,患有≥10包的吸烟历史。患者临床诊断为中度至严重的稳定COPD(1 s后支气管扩张剂强迫呼气量(FEV)1)/强迫肺活量(FVC) <70%和FEV1根据国家健康和营养考试调查III [营养考试调查,预测≥30%和≤70%16.].服用稳定剂量ICS的患者被允许参与研究。
目前对哮喘的诊断是排除性的。由于给予高剂量GSK961081的狗存在声带糜烂,有症状(或有记录史)咽喉返流、食管外返流、后喉炎或咽喉溃疡和糜烂的患者也被排除在外。这是为了确保已有喉咙问题的患者不会混淆在研究中识别任何新的喉咙刺激病例的可能性。在线补充材料(S2)显示了COPD人群的进一步特征。
该研究得到了参与中心的医学道德委员会批准,所有患者均提供书面知情同意。该研究根据良好的临床实践根据赫尔辛基宣言进行。
研究评估
功效
肺活量测定使用Vitalograph(生物医学系统(BMS),布鲁塞尔,比利时)(在线补充材料(S3))进行。BMS还对痕迹进行过读。如果受试者增加沙丁胺醇前FEV则是可逆的1在筛选访问时施用400μg的沙丁胺醇后≥200毫升,≥12%15分钟。
安全评估
在电子案例报告表中记录了所有不良事件的发病率和严重程度。ECG,血液化学和生命体征的详细信息在于在线补充材料(S4)。为任何报告喉咙症状7天或更长时间的患者收集数据,包括声音的声音,喉咙痛,喉咙肿块,吞咽困难或喉咙中的任何异常感觉。这些患者还通过专家进行了协议定义的灵活喉镜检查。
终点
研究的主要终点是从槽FEV中的基线变化1在29天。波谷定义为第28天晚给药后11和12小时的平均值。
次要终点包括0 - 24小时连续FEV的加权平均值1夜间肺活量测定,连续FEV的病人子集的测量1在每天28天,在经过一夜肺活量测定的患者的亚组中,每次点为24小时剂量后24小时,血液测量症患者患者1在整个队列的第1天和第28天0-12小时。
统计分析
使用重复措施模型进行分析主终点,针对基线FEV的固定效果1、可逆性、同时使用ICS、性别、年龄、吸烟状况(筛查时)、治疗、研究日、研究日治疗互动以及患者是否参与24小时肺活量测定评估。为了保持5%的整体α水平推断相对安慰剂在每个给药方案中使用闭合的顺序测试程序,其显着性水平为2.5%,最初将最高剂量与安慰剂进行比较。仅在前面的比较显着时,较低剂量以下剂量的随后比较仍然继续进行。对于多重性,未调整次要端点的推论。一种事后进行分析以提供所有组与沙美特罗之间的推论。
结果
群体特征
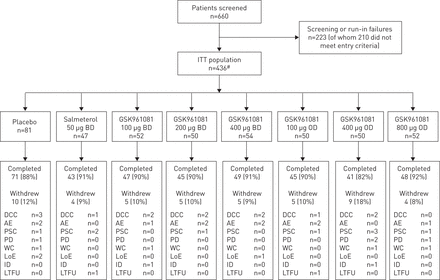
437名患者随机分为研究。一名患者没有接受任何调查产物并撤回,给予来自九个国家和49个患者的436名患者的改性意图,46%的患者在过夜队列中。可以找到研究人口的人口特征表1和患者的处置图1。
主体性格组合图。ITT公司:intent-to-treat;双相障碍:每天两次;OD:每天一次;DCC:不符合延续标准;AE:不良事件;PSC:协议定义的停止标准;帕金森病:协议偏差;WC:撤回同意;LoE:缺乏功效; ID: investigator discretion; LTFU: lost to follow-up.#:将437名受试者随机化,但一个受试者没有收到任何随机药物,为ITT人口留下436个。
对于主要终点(早晨低谷FEV1第29天),所有剂量的GSK961081均与安慰剂有显著差异(p<0.001) (表2).每日一次剂量的差异为155 mL (100 μg)至277 mL (800 μg),每日两次剂量的差异为173 mL (100 μg)至258 mL (400 μg)。在观察治疗效果时相对在预定义的地层中的安慰剂,FEV1对于不经常并发ICS用户的患者,对含沙丁醇莫尔的患者的改善通常更大,对患者更高,而不是并发ICS用户的患者(在线补充表S1)。在研究期间,低谷FEV1在前14天内增加,持续到28天(在线补充表S2)。
将活性比较Salmeterol与A中的所有治疗进行比较事后分析。在该分析中,与安慰剂(77mL差异,P = 0.046)相比,有一个标称统计差异,有利于Salmeterol(P = 0.046)。GSK961081剂量和Salmeterol之间的差异从78ml(每日100μg)到200ml(每日800μg),具有除100μg每日100μg之外的所有剂量的统计学上显着的差异(表2).
次要终点
对于夜间患者的子集(n = 18-23),24-h加权平均fev124小时内所有剂量和方案从226 mL (100 μg,每日2次)到335 mL (800 μg,每日1次),与基线第28天的差异与安慰剂相比具有统计学意义(p<0.001) (表3).Salmeterol的加权平均改善为85毫升,但与安慰剂的差异没有统计学意义。
0-24-H FEV1第28天(n= 18-23)的数据显示,服用安慰剂的患者FEV降低1在11小时的晚上剂量之后(无花果。2).Salmeterol还反映了FEV的晚上下降1尽管GSK961081每日100μg和400μg的GSK961081,在第二天早上从基线<200毫升降低平均变化。每日200μg和400μg的每日剂量诱导12-14小时的额外峰,这确保了基线的平均变化仍然存在> 200ml过夜,直到第二天早晨。
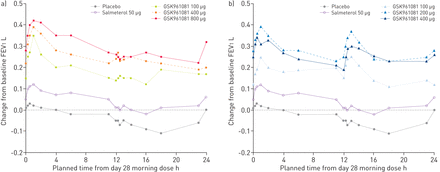
1秒连续用力呼气量(FEV)1在过夜主题的第28天,在第28天概况超过0-24小时。a)每日剂量方案;b)每日两次剂量方案。
在第1天,所有GSK961081治疗方法对安慰剂的差异差异,在早上0小时至12小时的所有时间点超过100毫升,除以100μg每日两次,每日100μg,每天11小时和12小时。后剂量(图3).在第28天,每天两次,每日两次,每日两次,每日每天400μg和800μg每日一次GSK961081治疗差异,在早晨0小时至12小时的所有时间点超过200毫升的安慰剂(图3 b).
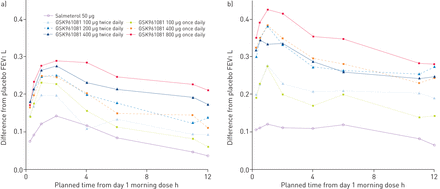
1秒连续用力呼气量(FEV)1)在所有科目中的第1天和B)第1天和B)第1天和B)。
其他终点
GSK961081剂量的患者在15分钟内提高100毫升的患者的比例为60%和81%(表4),与43%的患者相比,患有Salmeterol治疗。峰值fev.1从第1天到第28天,除100 μg每日一次剂量外,所有剂量的GSK961081的反应均增加表4。
所有剂量的GSK961081的槽FVC测量显示标称统计差异与安慰剂(P = 0.014每日100μg,所有其他GSK961081剂量的P <0.001),并为GSK961081100μg每天变化至381ml每日一次剂量800-μg(表3).Salmeterol(第29天与安慰剂120毫升差异)与安慰剂没有统计学不同。
治疗前Salbutamol使用的每天的平均次数为1.49。在该研究期间,对于GSK961081剂量的每天的每天的每天的每天减少,有一个标称统计差异(P <0.01),每天每天剂量每天一次剂量为0.74时,为400μg两次每日剂量 (表3).沙美特罗显示了名义上的统计差异(p=0.026),在研究期间每天减少0.39次。
安全
在治疗和所需的住院期间报告了一个非常规严重不良事件。这是胆道的事件,患者在患者中报道,在胆结石的疑似过去历史中,在每日GSK961081治疗组的400微克中,并未被认为与研究药物有关。不良事件的发生率显示在表5。GSK961081具有良好的耐受性,头痛,咳嗽,痛苦usia(不良味道)和鼻咽炎是最常见的不良事件。在GSK961081组中比在安慰剂或沙尔米尔武器中更频繁地报告了与药物相关的不良事件。最常见的事件咳嗽和痛苦乌西亚。研究期间发生了六次COPD的六种加剧:四个在安慰剂组中,每天一次,每日一次,每次每日两次GSK961081组;没有必要住院治疗。有四种后心ECG异常。一个是在每日两次的100μg两次的心动过速,被调查员判断与研究药物无关,并没有导致撤回。另外三个被视为与治疗有关,并导致GSK961081撤离。左束分支块和Wolff-Parkinson-White综合征的病例被诊断为剂量后ECG,尽管对ECG的审查表明,这些异常都存在于给药前获得的ECG。 In addition, a patient was withdrawn for first-degree atrioventricular block (PR 244 ms) and had a normal ECG at screening (PR 177 ms) but had a day-1, pre-dose PR interval of 215 ms.
心率和收缩性和舒张性血压表现出对GSK961081的影响很小。在用GSK961081处理时,葡萄糖和钾的变化也是最小的。对于心率(QTC(F))的QT间隔(QTC(F))与第28天相比,QT间隔校正了GSK961081的药理效应,并且在第28天相比,没有剂量 - 反应关系是明显的。
讨论
本研究旨在评估新型双支气管扩张剂GSK961081,中度和严重COPD患者的疗效和安全性。该研究表明临床上的临床和统计上显着的改进槽1治疗28天后,减少使用救援药物。在400μg和800μg的同一总日剂量的给药间隔的比较表明,与槽FEV相比,每日一次和两次给药之间没有显着差异1,FVC槽,救援药物用法和安全参数。低谷FEV有一个小幅增加1随着每日总剂量从400μg增加至800μg。槽式FEV增加1大于100毫升的广泛接受的临床重要差异[17.]对于每天一次每天100μg的剂量为100μg,每天两次观察一次支气管扩张剂;但是,在槽中增加了1这些剂量未观察到200mL(正如双支气管扩张剂的预期)。因此,与400μg的总日剂量相比,日常剂量较低将被视为次优。使用安全数据,随着剂量增加,关注的安全参数没有明显增加。因此,我们得出结论,最佳每日剂量为400μg,为200-μg两次每日剂量或400μg,中期至严重的COPD患者的每日每日剂量。
在研究的28天,一个事后分析显示,GSK961081在改善肺功能方面始终优于活性比较物沙美特罗。GSK961081改进了槽式FEV1在第29天,用平均差异(与安慰剂相比)超过所有剂量超过150ml,并且在每日剂量的总剂量≥400μg的情况下明确超过200ml。
过夜患者子集在第28天的24小时肺活量谱显示,安慰剂治疗患者的FEV呈日变化1过夜减少约100毫升。尽管由于昼夜效应而波动,但所有活性处理臂至少跟踪了变化,并与安慰剂相比,肺功能的差异保持。有一个建议,每天两次GSK961081≥200μg每天两次或≥400μg的差异降低,导致平均肺功能差异与晚间时期的安慰剂相比。患者在24-H周期内持续支气管扩张,所有剂量的GSK961081,尽管每天一次或每日两次100μg,但每日100μg较少。
所有患者的12-H肺血管谱表明槽FEV的改善有所增加1相对从第1天到第28天的安慰剂。低谷FEV1增加到第14天,然后在研究的其余时间保持不变(在线补充表S1)。
GSK961081起病迅速,在所有GSK961081剂量组中,≥60%的患者FEV达到100毫升改善1与安慰剂相比,GSK961081在低谷期FVC和救援药物使用方面也显示了名义上的统计学改善。
总的来说,GSK961081耐受性良好。最常见的不良事件为头痛、咳嗽、味觉障碍和鼻咽炎。与安慰剂或沙美特罗相比,GSK961081治疗与QTc间隔延长3 - 5 ms多相关。然而,并没有明显的剂量-反应关系,在之前的研究中[15.[如果使用每日一次的剂量为1200μg,则没有延长QT间隔。在患有患者前的临床前研究中,高剂量的GSK961081显示了喉部中的声带折叠腐蚀的发展。由于预先存在的喉咽回流或食水回流,两名患者被排除在筛选中。在整个研究中监测喉咙症状。在治疗中,有两次报告的喉咙症状持续超过7天,但喉镜检查显示没有声音折叠糜烂的证据。
这项IIb期研究的主要局限性是它选择了中度和重度COPD患者人群。本研究中观察到的效应大小是否会在更广泛的COPD人群中维持更长的时间,将需要在未来的研究中解决。
COPD治疗指南推荐最初使用单一支气管扩张剂。单个支气管等唾液表,中度或严重的COPD患者提供〜80毫升的槽式1相对安慰剂,而Tiotropium和indacaterol展示~100 ml改进[18.-20.].如果患者仍然存在症状,指南建议用不同的机制添加支气管扩张剂[1].临床研究为此提供了证据[3.-10.].在两项独立的研究中,在中至重度COPD人群中,噻托溴铵加入茚达特罗可改善60-90毫升相对仅仅看到了Tiotropium [21.].在双盲26周的患有针对固定剂量双支气管扩张剂QVA149的中度至严重的COPD患者的26周的研究中,有200毫升(P <0.001)改善相对安慰剂 [20.].因此,期望是具有两种动作机制的支气管扩张剂将提供〜200ml的槽。低谷FEV的改善1每日800μg每日800μg每日400μg,每日200-μg和400μg两次每日GSK961081方案,实现≥200ml相对安慰剂。每日100μg每日和100μg两次的每日方案,而单个支气管扩张剂的改善,则在200毫升槽FEV方面是次优1对带有两个机制的支气管扩张剂的期望。尽管GSK961081总日剂量≥400μg的肺功能的改善似乎类似于当前组合,但需要在随机对照试验中进行直接比较。
总之,GSK961081是双功能,具有毒蕈碱拮抗剂和β2-激动剂在同一分子中的活性。研究结果表明,GSK961081的日总剂量为400 μg,每日一次为400 μg,每日两次为200 μg。GSK961081起效迅速,在中、重度COPD患者中是一种有效的支气管扩张剂,安全性和耐受性良好。
致谢
Glaxosmithkline学习团队包括:Helen Griffiths和Ginny Norris(Glaxosmithkline,Uxbridge,英国)和Dmitriy Galkin(Glaxosmithkline,研究三角公园,NC,美国)。调查人员:I. Abdullah(南非),K.Arpasova(斯洛伐克),Z.Aisanov(俄罗斯联邦),T.Bantje(荷兰),E. Bateman(南非),L.Bjermer(瑞典),v。Blazhko(乌克兰),A.花红(南非),D. de Munck(荷兰),M. Dzurilla(斯洛伐克),Y.Feshchenko(乌克兰),K。Foerster(德国),V.Gavrysiuk(乌克兰),M. Goossens(荷兰),M. Hajkova(斯洛伐克),H. Hukelova(斯洛伐克),L.Iashyna(乌克兰),E. irusen(南非),R. Jogi(爱沙尼亚),J. Joubert(南一种frica), O. Kornmann (Germany), E.M. Kuulpak (Estonia), I. Leshchenko (Russian Federation), A. Lindberg (Sweden), A. Linnhoff (Germany), M. Löfdahl (Sweden), B. Lundback (Sweden), A. Ludwig-Sengpiel (Germany), T. Mihaescu (Romania), S. Mihaicuta (Romania), Y. Mostovoy (Ukraine), R. Nemes (Romania), L. Ogorodova (Russian Federation), M. Ostrovskyy (Ukraine), T. Pertseva (Ukraine), E. Pribulova (Romania), A. Rascu (Romania), D. Richter (South Africa), P. Samaruutel (Estonia), I. Schenkenberger (Germany), W. Schroeder-Babo (Germany), H. Sinninghe Damste (The Netherlands), E. Sooru E (Estonia), R. Stallaert (The Netherlands), V. Sushko (Ukraine), V. Trofimov (Russian Federation), P. Wielders (The Netherlands), J. Wuerziger (Germany), V. Zorin (Ukraine). The patients themselves, without whom this research could not be conducted. Editorial support (in the form of assembling, copy-editing and graphic services) was provided by Ian Grieve at Gardiner-Caldwell Communications (Macclesfield, UK) and was funded by GlaxoSmithKline.
脚注
对于编辑评论看885页。
这篇文章有补充资料可从www.www.qdcxjkg.com.
临床试验:本研究登记www.clinicaltrials.gov标识号nct01319019.和www.clinicaltrialsregister.eu使用标识符号mab115032。
支持声明:该研究由葛兰素史克资助。编辑支持由葛兰素史克(GlaxoSmithKline)资助。
利益冲突:披露可以在此手稿的在线版本旁边找到www.www.qdcxjkg.com.
本文于2016年4月进行了修改,以纠正许可证信息中的错误。
- 收到了2012年10月16日。
- 公认2013年2月10日。
- ©2013年
ERJ开放文章是开放式访问和分发的(188滚球软件知识共享署名非商业许可3.0)