抽象
活化蛋白C(APC)抑制凝血和在人类和动物的肺部炎症的静脉给药。在啮齿类动物调查证实APC的是直接肺内递送也发挥抗凝和抗炎作用。重组人的支气管内给药的效果(RH)APC对脂多糖(LPS)诱导的在人类支气管肺泡空间止血和炎性变化进行了研究。
8名受试者接受rhAPC治疗通过通过支气管镜支气管内滴注,而在对侧子段受试者接受盐水;所有受试者双边与同一肺子段LPS挑战。四个附加受试者接受rhAPC(75微克),用生理盐水作为在对侧子片段的控制,而他们双边“挑战”用生理盐水。6小时后,进行支气管肺泡灌洗,测定凝血和炎症参数。
rhAPC增强LPS诱导的凝血激活在支气管肺泡空间,当与对照相比侧。此外,rhAPC扩增LPS诱导的促炎性应答,由较高浓度的细胞因子和趋化因子所指示的。rhAPC本身并不具有促凝血或促炎症效应。
局部施用rhAPC具有意想不到促凝血和在LPS激发的肺子片段的促炎作用。这些数据反对肺内交付rhAPC作为在人类肺部炎症性疾病治疗策略的作用。
介绍
气道是机体的一个部位,其中促凝和抗凝机制可在局部启动和调节[1,2]。活化的蛋白C(APC),一个重要的抗凝血剂,已显示出在以各种肺部炎性疾病支气管空间[活性降低3-11]。APC水平的降低可能导致患者肺内血流平衡紊乱,使生理抗凝环境变为净促凝状态。APC除了具有抗凝血作用外,还具有多种抗炎和/或细胞保护作用,其特征是促炎途径的下调、抗炎途径的上调和中性粒细胞活性的抑制[12,13]。
我们最近证明,作为革兰氏阴性细菌细胞壁组成部分的脂多糖(LPS)经abronchial灌注后,可以复制炎症性肺部疾病中发现的止血改变,包括健康志愿者肺中APC水平的降低[14,15]。这种人体内LPS递送模型也被用来研究体内对肺炎症和凝血[静脉注射重组人(rh)APC治疗的效果15,16]。静脉rhAPC在支气管肺泡空间减少LPS诱导的中性粒细胞聚集[16和抑制局部凝血激活[15]。同时,LPS诱导的血纤维蛋白溶解的抑制部分被静脉内rhAPC [防止15]。
当静脉给药时,rhAPC的强抗凝血作用可能有助于严重的全身性副作用,例如性颅内出血[17-20],其可以通过rhAPC的局部给药来规避。虽然临床前动物研究表明APC的给药通过气道产生局部的抗炎和抗凝作用[21-24],没有研究存在有计算直接rhAPC管理的作用进入人体的肺部。本研究中,因此,试图确定抑制LPS诱导的肺部炎症和凝固在人类rhAPC的地方,支气管内给药的可行性。
方法
研究对象和材料
12名不吸烟的男性(23.2岁±1.1岁)的患者。筛选,由问卷调查,体格检查,血常规,尿调查,心电图和肺功能检查,没发现任何异常。该协议被批准的机构医学伦理审查委员会。所有受试者只要在入学前签署知情同意书。LPS是源自大肠杆菌○:113(参考内毒素,CC-RE-LOT-3,卫生,马里兰州贝塞斯达,美国国家研究院)。rhAPC(drotrecoginα(激活); Eli Lilly公司,印第安纳波利斯,IN,USA)中的溶液从商业供应商购买。
学习规划
这项研究是建立与剂量升级和后续阶段单盲干预研究。2个对侧肺子段的双边挑战是由LPS的支气管内滴注(4纳克·公斤执行-1),用10毫升无菌生理盐水稀释。在一个肺亚段,LPS灌注后立即在同一肺亚段给予rhAPC (10ml),而在对侧肺亚段LPS灌注后仅灌注10ml生理盐水。受试者被随机分配到左肺或右肺进行横纹肌钙蛋白灌注。在dose-escalating阶段的研究中,五倍rhAPC剂量的增加是为了每剂在群四个科目,从15μg。预先设定的主要终点是,与对侧LPS损伤侧相比,经腹侧LPS损伤侧6小时后,经rhapc处理的肺中的凝血酶-抗凝血酶复合物(TATc)浓度降低30%;这个终点是基于我们之前的研究中,静脉注射rhAPC抑制lps诱导的支气管肺泡灌洗液(BALF)中TATc浓度上升约30%的能力[15]。根据每个研究设计,在研究的后续阶段,将达到这一主要终点的rhAPC剂量组的样本量将增加到总共12名受试者。完成后的前两个军团剂量递增阶段(15和75μg;n=4为每剂),我们决定停止研究,因为它被认为是极不可能达到主要研究终点。相反,四个额外的受试者包括75接受μg rhAPC在一个肺亚节没有以前intrabronchial有限合伙人的挑战;在这些志愿者中,生理盐水作为对照给予对侧肺亚段。
方法
术后6小时采用标准化方法进行双侧支气管肺泡灌洗(BAL) [14,25]。柠檬酸和肝素化血液是采取的第一(T = 0 H)静脉穿刺之前和第二(T = 6小时)支气管镜检查。所用的测定法在网上补充材料进行说明。
统计分析
值表示为平均值±扫描电镜..配对t检验用于建立数据集之间的显著性。p-<0.05为差异有统计学意义。
结果
临床症状和全身性炎症反应
将LPS灌注于两个对侧肺亚段(合并一个肺段的rhAPC),耐受性良好。灌注LPS 6小时后,体温略有升高(从t=0小时时的36.0±0.2℃上升到t=6小时时的36.6±0.1℃;p < 0.05)。血中性粒细胞计数升高(2.3±0.2×10)9到6.6±0.8×109细胞·L-1;P <0.001),而盐水激发的组中的嗜中性粒细胞计数无显著上升,看到(2.0±0.2×109到4.1±0.8×109细胞·L-1)。最后,intrabronchial有限合伙人或生理盐水滴剂,与添加rhAPC肺亚节,不是与TATc血浆浓度的变化有关,肺动脉栓塞、肿瘤坏死因子(TNF) -α或白介素(IL) 6(数据未显示)。
支气管APC浓度
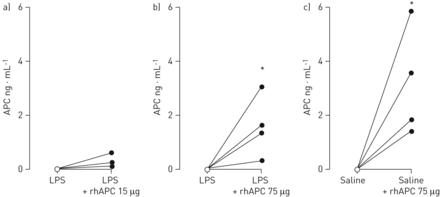
rhAPC的支气管内滴注后6小时,APC是从APC处理的侧获得所有BALF样品中可测量:APC水平分别为0.33±0.14和1.60±0.57毫微克·毫升-1在用15和75微克rhAPC,分别为(P = 0.07和P处理过的LPS激发的受试者<0.05肺子片段用15处理的和75微克rhAPC与控制肺子分段;图。图1A和1B)。在用75微克rhAPC处理的盐水激发的组,BALF APC水平分别为3.2±1.0纳克·毫升-1(P <0.05;图1 c)。APC的水平在75年μg rhAPC-challenged LPS-challenged没有差异和saline-challenged科目子分段。在对照组的肺亚段中均未检测到APC (即。那些不与rhAPC施用)。
活化的蛋白C(APC)的浓度支气管肺泡灌洗样本英寸健康受试者(每组n = 4)双侧肺子段的挑战通过用脂多糖(LPS支气管镜; 4纳克·公斤-1体重)(a和b)或盐水(c)中。此后直接受试者接受溶解于10毫升盐水在一个子片段和10mL盐水中的其他肺子段的重组人(rh)APC 15微克(a)或75微克(b和c)。双侧支气管肺泡灌洗被攻击后进行6个小时。APC水平在任何不与rhAPC给予对照肺子片段的不可检测的。*:P <0.05。
支气管内rhAPC增强LPS刺激后支气管凝血激活
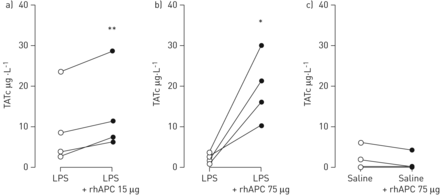
在急性肺损伤和/或肺炎患者中,TATc的屋内浓度已被用来确定支气管肺泡凝血激活的程度[7,8,10]。健康人群中LPS的宫内灌注也与BALF中TATc水平的升高有关[14,15]。一项较早的研究表明,静脉注射rhAPC可使脂多糖诱导的BALF中TATc浓度升高约30% [15]。本研究的主要目的是确定经abronchially灌注的rhAPC是否能够抑制lps诱导的BALF中TATc的升高,如果是,这种抗凝血作用是否伴有抗炎作用。考虑到我们之前使用静脉rhAPC的调查结果[15],我们预定义的当前研究的主要终点为建立所述支气管内rhAPC剂量诱导BALF中LPS诱导的TATC浓度降低了30%。我们选择管理LPS两分对侧肺子分段,从而消除了LPS反应的个体差异,并允许每一个主题作为自己的控制对于rhAPC效果。令我们惊奇的是,支气管内滴注rhAPC,在任一15微克或75微克给予,当与不具有rhAPC(rhAPC 15微克治疗的对侧相比诱导的增加,而不是减少,在LPS攻击后BALF TATC浓度:13.5±5.2与9.8±4.8微克·L-1在对侧,p<0.01,图2一个;75年rhAPCμg: 19.4±4.2与2.9±0.8微克·L-1在对侧,p<0.05,图2 b)。由于这些结果使得它极不可能的,我们能达到我们预定的终点,我们决定不与其他增加五倍于rhAPC剂量但是,相反,增加了一个额外的研究小组没有LPS挑战着手,设法确定是否支气管内rhAPC本身引起促凝反应。因此,主题获得了与盐水的双边挑战,结合rhAPC(75μg)放在一边。这些研究并没有发现rhAPC促凝血的影响:BALF TATc水平相似的肺子分段灌输rhAPC(1.6±1.4μg·L-1)当与对侧(2.4±1.2微克·L相比-1;图2 c)。C蛋白活性,总的和游离蛋白S,可溶性血栓调节蛋白,蛋白C抑制剂和血管性血友病因子抗原浓度均低于在BALF检测限。
重组人活化蛋白C (rhAPC)经abronchial灌注可增强脂多糖(LPS)诱导的支气管肺泡腔内凝血功能。健康受试者(每组n = 4)双侧肺子段的挑战通过支气管镜伴LPS (4 ng·kg)-1体重)(a和b)或生理盐水(c),之后直接收到rhAPC 15μg (a)或75μg (b和c)溶解在10毫升的盐水在另一亚节和10毫升的盐水肺亚节。在支气管肺泡灌洗液中测定6小时后的凝血酶-抗凝血酶复合物(TATc)水平。*:p < 0.05;* *:p < 0.01。
支气管内rhAPC的纤溶作用LPS攻击后
证据来自体外研究表明,APC可能通过抑制纤溶酶原激活物抑制剂1型(PAI-1)来刺激纤溶[26]。我们测量的PAI-1水平,组织类型纤溶酶原激活物(tPA)和plasmin-α2-antiplasmin复合物。虽然intrabronchial rhAPC基于15μg的剂量并不影响LPS-induced PAI-1释放BALF (p = 0.57;图3),rhAPC在75微克给予三个出了四组(192.5±42.1的增加LPS诱导的PAI-1水平的BALF与55.0±17.1 pg·毫升-1在对侧;P = 0.07;图3 b)。值得注意的是,支气管内rhAPC也有增加的趋势PAI-1在支气管肺泡灌洗液从谁没有收到LPS(70.0±45.3学科水平与7.5±7.5皮克·毫升-1在对侧;p = 0.26;图3 c)。既不LPS也不rhAPC影响纤溶酶α2抗纤溶酶复合物的浓度BALF,而tPA的水平低于所有BALF样品中的检测限(未示出数据)。
重组人活化蛋白C (rhAPC)对脂多糖(LPS)诱导的纤溶酶原激活物抑制剂I型在支气管肺泡内释放的影响。健康受试者(每组n = 4)双侧肺子段的挑战通过支气管镜伴LPS (4 ng·kg)-1体重)(a和b)或生理盐水(c),之后直接收到rhAPC 15μg (a)或75μg (b和c)溶解在10毫升的盐水在另一亚节和10毫升的盐水肺亚节。纤溶酶原激活物抑制剂1型(PAI-1)水平在支气管肺泡灌洗液中测定。
经LPS刺激后,骨内rhAPC与组织因子途径抑制剂浓度增加有关
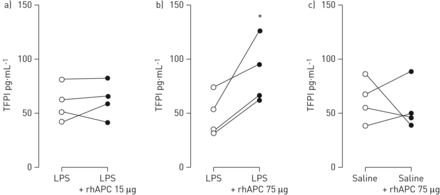
最近的数据表明,APC可以凭借其蛋白水解活性的促凝效果。APC据报道,从棚组织因子途径抑制剂(TFPI),Kunitz结构-1结构域导致增加的组织因子活性,因此,凝血激活[27]。我们在BALF测量TFPI的水平。虽然支气管内rhAPC剂量15微克没有影响的定LPS诱导的BALF中TFPI释放(图4),rhAPC在75微克施用在所有四个受试者(48.1±9.9增加LPS诱导的BALF TFPI水平与87.9±14.8 pg·毫升-1在对侧;p<0.05;图4 b)。支气管内rhAPC没有支气管肺泡灌洗液从谁没有收到LPS科目改变TFPI的水平(图4摄氏度)。
重组人活化蛋白C (rhAPC)对脂多糖(LPS)诱导的支气管肺泡内组织因子途径抑制剂释放的影响。健康受试者(每组n = 4)双侧肺子段的挑战通过支气管镜伴LPS (4 ng·kg)-1体重)(a和b)或生理盐水(c),之后直接收到rhAPC 15μg (a)或75μg (b和c)溶解在10毫升的盐水在另一亚节和10毫升的盐水肺亚节。支气管肺泡灌洗样品中测定组织因子途径抑制剂(TFPI)的水平在攻击后获得了6个小时。*:P <0.05。
支气管内rhAPC LPS给药后增加白细胞募集
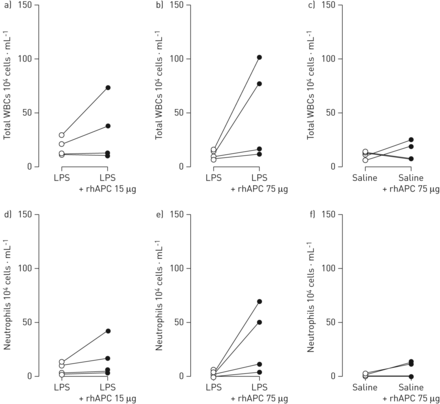
静脉rhAPC已上报降低中性粒细胞募集到在健康人LPS的支气管内滴注支气管空间16]。与此相反,支气管内rhAPC治疗增加白细胞的总数在后双边LPS攻击BALF 6小时,虽然与对侧对照侧的差异没有达到统计学显着性(APC 15微克:33.6±14.6×104与18.6±4.1×104细胞·mL的-1在对侧,p=0。25,图。5A;APC 75微克:52.0±22.4×104与11.1±1.5×104细胞·mL的-1在对侧,P = 0.13,图。5B)。在用LPS攻击肺的子部分的总细胞数的rhAPC诱导增加,是由于在嗜中性粒细胞的数量的增加(APC 15微克:16.8±9.0×104与7.5±2.7×104中性粒细胞·毫升-1,P = 0.25,图。5D;APC 75微克:34.1±15.8×104与1.5±0.6×104中性粒细胞·毫升-1,P = 0.13,图。5E)。支气管内rhAPC不影响未用LPS攻击肺子段细胞计数(图。5C和f)。
支气管内的重组人活化蛋白C(rhAPC)对脂多糖冲击(LPS)诱导的增加的总白细胞和中性粒细胞计数在支气管肺泡空间。健康受试者(每组n = 4)双侧肺子段的挑战通过支气管镜伴LPS (4 ng·kg)-1体重)(a和b)或生理盐水(c),之后直接收到rhAPC 15μg (a)或75μg (b和c)溶解在10毫升的盐水在另一亚节和10毫升的盐水肺亚节。攻毒后6小时支气管肺泡灌洗液,测定白细胞计数(WBCs)和中性粒细胞计数。
支气管内rhAPC增强一些细胞因子和趋化因子的LPS滴注后局部释放
为了研究局部给予rhAPC对脂多糖诱导的炎症介质释放的影响,我们测量了48种细胞因子、趋化因子和生长因子的BALF浓度。这些分析的结果显示在在线补充表S1中。rhAPC低剂量组(15μg), rhAPC显著增强LPS-induced释放il - 6, CCL8 CXCL6而不影响其他介质的水平(在线补充表S1)。75年rhAPCμg队列,rhAPC显著增强LPS-induced TNF-α,亚兰,CCL8 TNF-related凋亡诱导配体(TRAIL)浓度(图。6及网上补充表格S1)。CCL20,此外,IL-1βCCL14a CXCL7, CXCL9 CXCL11更高层次表现出强烈的趋势在这个rhAPC高剂量组(p = 0.052, p = 0.081, p = 0.078, p = 0.075, p = 0.092, p = 0.074,分别;图。6及网上补充表格S1)。rhAPC在75μg没有有限合伙人不引起肺部炎症介质的释放,除了温和上升CCL15浓度(在线补充表S1)。综上所述,这些结果表明,在脂多糖感染的肺亚段内灌注rhAPC可增强多种促炎介质的释放。
重组人活化蛋白C (rhAPC)经胞内灌注可增强脂多糖(LPS)诱导的支气管肺泡腔内炎症介质的释放。健康受试者(每组n = 4)双侧肺子段的挑战通过支气管镜伴LPS (4 ng·kg)-1体重)。此后直接受试者接受rhAPC 75微克溶于10mL盐水的在一个子片段和10mL盐水中的其他肺子段。支气管肺泡灌洗样品中,测定介体的水平在攻击后获得了6个小时。TNF:肿瘤坏死因子;IL:白细胞介素;TRAIL:肿瘤坏死因子相关凋亡诱导配体。*:p < 0.05;* *:p < 0.01。
讨论
一些临床前研究表明,APC可以保护损伤引起的炎症肺[28]。此外,rhAPC的静脉内给药报道了通过支气管镜在肺子段用LPS攻击健康人的支气管肺泡空间施加抗凝和抗炎作用〔15,16]。动物研究表明,气管内滴入APC发挥本地抗凝和抗炎作用[21-24,29-32]。考虑到与静脉APC相关的出血风险,我们首次研究了经abronchial rhAPC给药抑制人类肺部凝血和炎症的潜力,认为这种给药途径将避免严重的副作用[17-20]。为此,我们使用LPS的支气管内滴注引起的肺部炎症的建立人体模型通过支气管镜[14-16,25]。我们研究的主要发现是显着的:支气管内给予rhAPC诱导促凝剂,并与LPS而不是凝血和炎症的预期抑制作用挑战肺子分段促炎症反应。我们从受试者的结果不是用LPS攻击通过气道进一步表明,rhAPC增强件LPS在人肺的影响,同时不会引发炎症检测或凝固本身..
我们的研究有一个小的样本量。因此,虽然rhAPC明显增强凝血和炎症生物标志物的LPS诱导释放,与安慰剂对照侧的差异往往没有达到统计学显着性。然而,目前的研究旨在证明rhAPC对支气管凝血和炎症的抑制作用。该rhAPC 75微克队列完成后,我们认为这是不可能的,预定义的终端点(即。可将BALF TATc水平降低30%)。因此,我们决定提前终止研究。此外,我们认为这不是道德扩大样本容量的军团为了加强统计的研究,在此基础上,促凝血的促炎症的影响本地管理rhAPC不会为病人的临床价值组和希望避免暴露额外的健康受试者侵入性程序。
在早期的研究中,在相同的人lps诱导的肺部炎症模型中,发现静脉注射rhAPC可抑制凝血和中性粒细胞内流[15,16],在BALF APC浓度约为15毫微克·毫升-1停药后2 h衡量rhAPC注入(24μg·公斤-1·H-1)15]。虽然BALF APC电平检测后静脉rhAPC输注不能容易地转换为一个可行rhAPC剂量在支气管肺泡空间中施用时,我们保守与支气管内rhAPC的15微克开始剂量递增研究中,考虑到所引起的BAL稀释程序和50-60%的估计恢复。在目前的研究中测量BALF APC等级,滴注后6小时,用静脉内施用APC [比在先前的研究中显着更低15](·0.33纳克的平均水平毫升-1和1.60 ng·毫升-1在rhAPC 15微克和75周微克的同伙,分别地)。可以说,BALF APC浓度rhAPC给药后直接较高。从支气管肺泡空间APC的间隙是困难的,在所需的侵入性手术的光人类研究;然而,证据表明,APC被慢慢地从车厢肺泡清除。事实上,尽管谁是静脉rhAPC治疗多数患者脓毒症没有检测APC血浆2小时输液,停药后[33, APC仍可从早2小时停止类似rhAPC灌注的健康人的BALF中恢复[15]。因此,尽管APC BALF浓度在本(支气管内rhAPC)和先前(静脉内rhAPC)测量[15]调查不能被容易地比较,这些组合的数据表明,在BALF取得的APC电平在这里有可能相同或更低的范围比静脉rhAPC输注后达到内。
如何才能静脉rhAPC的明显不同的影响[15]和支气管内rhAPC在LPS诱导的人肺炎解释?APC可以发挥在内皮细胞中的抗炎,抗凋亡和阻挡保护信号通过蛋白酶活化受体(PAR)1通过需要APC的对内皮细胞蛋白C受体(EPCR)的结合的机制[34]。细胞保护抗炎APC-PAR1信令也已在其它细胞类型表现出来,尤其是树突细胞(EPCR依赖性[35])和巨噬细胞(CD11 / CD18依赖性[35,36])。此外,APC直接结合活化的α3β1,α五β1和αVβ3整合素和该相互作用是必不可少的中性粒细胞外渗的APC诱导抑制到小鼠的支气管肺泡空间[37]。这些“细胞保护”和/或消炎效果APC体内可能取决于哪类型的细胞的影响,从而对rhAPC给药途径。此外,涉及这些APC影响受体的分布可以在不同的身体部位不同而不同。此外,最近的数据表明APC可以凭借其蛋白水解活性的促凝效果;APC据报道,从棚TFPI的Kunitz结构-1结构域,从而产生增加的组织因子活性,因此,凝血激活[27]。在这项研究中,我们在测量BALF TFPI水平和显示rhAPC的施用在75微克队列用显著增强TFPI水平相关。我们假设增加TFPI水平可能是促炎性状态的结果,由于rhAPC管理。应当指出的是,TFPI测定中使用的检测二者的全长和切割的TFPI。因此,可能的是,升高的TFPI水平通过rhAPC完整蛋白质的裂解的结果,从而有助于促凝血剂的效果。我们没有对APC的肺内递送在小鼠的影响我们目前的研究结果与先前的报告之间的差异明确的解释[21-24],虽然在确切的给药方法的差异,研究的剂量和种类可以是参与。
我们的研究并没有提供一个明确的机制背后的人肺横纹肌钙蛋白的意外促炎和促凝作用。我们尝试使用呼吸上皮细胞(A549)和人肺泡巨噬细胞或巨噬样THP-1细胞在混合细胞培养系统中复制APC的作用,但均未成功(数据未显示)。
总之,这是在支气管内给予rhAPC在人类控制的肺部炎症模型效果的第一项研究。我们的数据表明,局部施用rhAPC在暴露于LPS肺段促凝和促炎作用。这些数据反对肺内交付rhAPC作为在人类肺部炎症性疾病治疗策略的作用。
致谢
作者感谢自动跟踪德·沃斯·d·Kruijswijk和特区勃洛克(所有实验和分子医学中心学术医学中心/阿姆斯特丹大学、阿姆斯特丹,荷兰)对他们的援助在研究天,g . van Mierlo (CLB Sanquin研究部门的免疫病理反应,阿姆斯特丹,荷兰),W.F. Kopatz,硕士Weijne, L.M. Leverink和j Marquart(所有部门实验血管医学学术医学中心/阿姆斯特丹大学,(荷兰)协助进行凝血测量和E.M. Kemper,住院药剂师(学术医学中心/荷兰阿姆斯特丹大学药理学部)协助准备研究药物。
脚注
这篇文章有提供补充材料www.www.qdcxjkg.com
临床试验:这项研究是在注册www.clinicaltrials.gov具有标识符数NCT00943267而在www.trialregister.nl具有标识符号码NTR1544。
支持声明:这项研究是由研究经费从ZonMW(至L.M. Kager,授权号:92003504)的支持,荷兰哮喘基金会(J.D.德布尔;项目3.2.08.009)和斯蒂廷BeGeTu(以L.M。Kager)。
利益冲突:无申报。
- 收到2012年4月5日。
- 公认2012年9月29日。
- ©ERS 2013