摘要
研究比较了肺炎严重程度指数PSI(肺炎严重程度指数)、认知混乱指数CURB-65、尿素>7 mol·L的能力−1,呼吸频率≥30次·min−1通过血压、收缩压< 90mmhg或舒张压≤60mmhg,年龄≥65岁)、CURB和CRB-65量表以及严重社区获得性肺炎(SCAP)评分来预测医疗相关肺炎(HCAP)患者的30天死亡率,并分析社区获得性肺炎(CAP)、HCAP和免疫功能受损患者肺炎在人口统计学、病原学和结局方面的差异。
一所三级护理大学医院收治的629名连续患者被前瞻性地分为CAP (n=322)或HCAP (n=307), HCAP患者进一步细分为免疫功能低下(n=219)或免疫功能正常(n=88)。
CAP组30天死亡率为9.0%,HCAP组为24.1%。在HCAP组中,PSI和SCAP评分具有相似的预后能力(曲线下面积(AUC)分别为0.68和0.67),并且表现优于CURB-65评分(AUC≤0.62)。在免疫功能正常的HCAP患者中,PSI和CURB-65评分在每个阈值上都比其他患者更敏感,而SCAP则比这两者更特异性。在免疫功能低下组,PSI在所有阈值上高度敏感但特异性差。
我们的结果提示预后工具应针对HCAP患者的子集进行设计。
2005年,美国胸科学会(ATS)及美国传染病学会(IDSA)在有关院内肺炎的指引中,引入“医疗相关肺炎”(HCAP)一词[1]。这一新类别基于的数据显示,在医院感染中普遍存在的耐多药(MDR)病原体可以在与医疗保健系统持续相互作用的受试者中发现,尽管他们的身份是门诊患者[2,3.];指南建议联合使用对耐多药病原体有效的广谱抗菌药物集中治疗HCAP患者[1]。
2005年ATS/IDSA指南还考虑到养老院中居住的老年人和/或严重残疾患者数量的增加,以及由于疾病和/或治疗而严重免疫功能低下且更有可能经历耐多药感染的患者。
最近的观察性研究表明,因肺炎住院的患者中有17%至38%患有HCAP [4- - - - - -7]。尽管抗菌素治疗和支持性护理取得了最新进展,但HCAP仍是发病的主要原因,并导致约20%的死亡率,是社区获得性肺炎(CAP)患者死亡率的两倍[3.- - - - - -9]。与CAP患者相比,HCAP患者通常年龄较大,有更多的合并症和残疾,与医院获得性肺炎(HAP)或呼吸机相关肺炎(VAP)患者更相似[3.,8,10]。因此,他们需要充分的住院治疗,并为重症监护室(ICUs)分配适当的资源,以尽量减少发病率和死亡率。
为改善CAP患者的临床管理并确保更好地分配资源,已开发了许多评分系统[11- - - - - -13]。研究最广泛的两种是20种肺炎严重程度指数(PSI) [14]和五变量CURB-65(混淆,尿素>7 mol·L−1,呼吸频率≥30次·min−1,收缩压< 90mmhg或舒张压≤60mmhg,年龄≥65岁)评分[15]。最近为严重社区获得性肺炎(SCAP)患者开发了八变量评分[16,17],似乎是准确的ICU入院。
目前还没有评估HCAP患者严重程度和预后的具体规则,仅在少数主要是回顾性研究中评估了CAP预后工具的性能[7,18- - - - - -20.]。此外,大多数前瞻性研究都调查了居住在疗养院或长期护理设施的HCAP患者或以前住院的患者[9,12,21]。然而,HCAP是一种异质性疾病,在不同的患者群体和接触医疗保健系统的原因不同的患者中,可能会或多或少地严重[22]。特别是,免疫功能低下患者的肺炎是否可以被认为是一种HCAP形式,还是一种不同的实体仍存在争议[23],目前尚无关于在非中性粒细胞减少或hiv阴性的免疫功能低下门诊患者中使用严重程度评分的公开数据。
这项前瞻性研究的目的是:比较PSI、CURB、CURB-65、CRB-65和SCAP评分在评估住院HCAP患者肺炎严重程度和预测30天死亡率方面的表现;讨论CAP和HCAP患者以及属于不同HCAP亚群的患者在人口统计学、病因学和结局方面的差异;并探讨评分系统对免疫功能低下(IC)和非IC HCAP患者的预测能力。
方法
研究对象
2005年至2010年间,意大利米兰的一家急诊三级大学医院——红十字基金会(Fondazione IRCCS Ospedale Maggiore Policlinico)内科收治了1066名年龄≥18岁的肺炎患者。其中,629人被认为符合这项前瞻性观察研究的条件。CAP和免疫损害的定义是基于意大利内科CAP管理研究中使用的标准[24],作者自2002年开始参与该研究。入院前90天内住院≥2天的患者被归为HCAP;如果他们住在专业护理机构或其他机构;如果他们一直在接受慢性透析;在过去30天内接受过家庭或1天医院输液治疗;是否接受过家庭或医院的伤口护理,或是否有家庭成员受到耐多药病原体的影响[1]。
免疫损害被定义为存在恶性肿瘤(活动性实体肿瘤或血液病)、免疫疾病或免疫抑制治疗(如。细胞毒性化疗,使用> 20mg强的松每天,或任何其他免疫抑制剂在过去4周),严重营养不良或恶病质。
排除标准为VAP、HAP、疑似或已知吸入性肺炎、活动性肺结核感染、真菌或巨细胞病毒肺炎和HIV阳性。获得了当地机构审查委员会(Fondazione IRCCS Ca' Granda Ospedale Maggiore Policlinico伦理委员会,米兰,意大利)的批准和患者的知情同意。在所有病例中,入院的决定和治疗的选择完全由主治医生自行决定。
数据收集和评估
记录了人口学变量、就诊时的临床表现、合并症、入院前治疗、胸部x线检查结果、实验室参数、微生物学研究、有创机械通气的需要、并发症、住院时间(LOS)、住院死亡率、出院时和入院后30天的结局。通过查阅医疗记录和/或电话采访评估30天全因死亡率。无法确定30天死亡率的患者被排除在外。
临床预后模型
根据PSI、CURB、CURB-65、CRB-65评分系统和SCAP评分,将患者分为30天死亡风险组,所有这些评分均使用入院时收集的预后指标进行计算。每种预后工具的参数都转换为二分变量。以PSI为例,将患者分为低、中、高危三类[14];至于“遏制”、“遏制-65”及“CRB-65”,则按符合标准的数目进行分层,分为低、中及高风险三类[15]。计算入学时的SCAP分数后验使用前瞻性记录变量,将患者分为低、中、高危三类[16]。
统计分析
描述性统计依据社会科学统计包第17版(SPSS,芝加哥,伊利诺伊州,美国)进行计算。对HCAP和CAP患者之间以及HCAP组内IC和非IC患者之间的基线特征进行卡方检验或非配对t检验(视情况而定)。采用逐步logistic回归选择与30天死亡率相关的变量集,并计算CAP、HCAP IC和HCAP非IC患者的调整后死亡率估计值。这些组之间的生存差异使用log-rank检验。使用Kaplan-Meier积极限估计评估生存期。对于不同的分界点,评估每种预后规则的表现(在敏感性、特异性和阳性和阴性似然比方面)。敏感性和特异性的确切置信限由二项分布得出。追踪每个预后评分系统的受试者工作特征(ROC)曲线,并计算每个ROC曲线下的面积(AUC)。用Wald检验检验五种预后评分系统的AUC之间的两两差异。使用SAS Proc Logistic (SAS/STAT用户指南版本9,SAS研究所公司,Cary, NC,美国)拟合逻辑回归模型,评估预后评分系统的性能并进行ROC曲线分析。 The two-tailed significance threshold was set at p<0.05 for all tests, with the exception of the pairwise comparisons between AUCs. In this case the threshold was set to p<0.005, in accordance with Bonferroni principle.
结果
患者特征和预后
在629例入组患者中,307例(49%)被归为HCAP, 322例(51%)被归为CAP。表1显示了两个群体的特点。
34.2%的HCAP患者和48.8%的CAP患者年龄为80岁(p<0.001),因此,在HCAP组中脑血管疾病的患病率为21.5%与32.0%;p=0.004)和COPD (13.7%与25.8%)较低。然而,HCAP的相关合并症比CAP多(66.1%)与51.9%;P <0.001),更多发生恶性肿瘤(69.4%)与4.0%;p < 0.001)。HCAP患者在入院前使用抗生素的比例(45.1%)高于CAP患者(27.7%;p < 0.001)。入院时,x线检查显示HCAP患者(26.1%)比CAP患者(18.9%;p = 0.035)。13例CAP患者和8例非ic HCAP患者的恶性肿瘤可归因于原位癌症(皮肤、前列腺或子宫癌)。
包括PSI、SCAP、CURB-65、CURB或CRB-65评分在内的大多数二分实验室变量能够区分HCAP和CAP患者。
HCAP组死亡率为24.1%,CAP组为9%。住院死亡率与30天死亡率相似。
HCAP组30天死亡率的单因素几率高出3倍(OR 3.21, 95% CI 2.020-5.096)。在调整PSI后,HCAP组的几率仍然较高(OR 5.56, 95% CI 2.02-15.26)。经逐步logistic回归分析,死亡率与年龄≥80岁、多叶受累、血尿素氮≥11 mmol·L有关−1,钠<130 mEq,脉搏频率≥125次·min−1脑血管疾病、恶性肿瘤和胸腔积液,r平方16.1%;残差卡方13.1(18个自由度),p=0.78。这些协变量调整后的优势比(OR 4.65, 95% CI 1.22-17.75)仍然显著。HCAP患者的LOS较长(p=0.004)。
HCAP亚群中的患者特征和结局
表2显示了HCAP患者的背景,其中许多患者满足一项以上的HCAP标准:24.7%在过去90天内住院≥2天,5.9%是养老院居民,45.8%接受过1天的医院静脉药物治疗(化疗或支持护理),34.2%接受过家庭伤口护理或家庭输液治疗。在过去30天内住院1天的137名患者中,114名患有血源性恶性肿瘤,8名患有实体恶性肿瘤,15名患有地中海贫血或自身免疫性疾病。
大多数(71.3%)患者因疾病和/或治疗而发生IC,所有患者至少符合一项HCAP标准,没有人被归类为患有CAP。由于这是一个鉴别参数,219名IC患者与88名非IC患者进行了比较。后者和前者分别为13.6%和2.7% (p=0.001)。8例非ic HCAP患者的恶性肿瘤可归因于原位癌症。这些患者被定义为HCAP,因为2例在过去90天内住院≥2天,3例接受了1天的医院静脉药物治疗,2例接受了家庭伤口护理。
表3显示两个HCAP亚组的合并症、临床和实验室变量。非ic患者年龄较大(平均77.8岁)与70.8年;P <0.001),其中≥80岁的患者是免疫功能低下患者的3倍。
两组患者30天死亡率的单因素变异率相似(OR 0.93, 95% CI 0.52-1.65)。即使对逐步logistic回归选择的协变量进行调整后,优势比(OR 1.02, 95% CI 0.35-2.96)仍然接近1。
两组间PSI评分和LOS无差异。
图1显示研究队列中30天生存的Kaplan-Meier图:IC和非IC HCAP患者的趋势相似(p=0.713)。
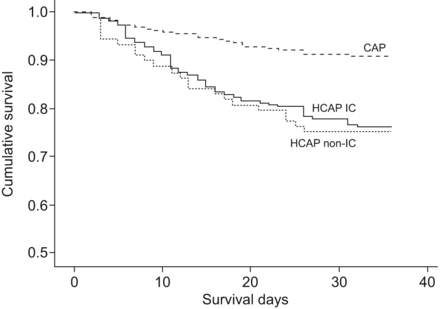
卫生保健获得性肺炎(HCAP)、免疫功能低下(IC)、HCAP非IC和社区获得性肺炎(CAP)患者30天生存Kaplan-Meier图
微生物研究
对322例CAP患者中的253例(78.6%)和307例HCAP患者中的266例(86.6%)进行了微生物学研究。23.3%的CAP患者阳性,30.8%的HCAP患者阳性。表4显示各组和亚组的微生物学结果。上的数据肠球菌由于肠球菌被认为是肺部感染的罕见原因,除了在免疫功能受损的情况下,因此包括了物种隔离。粪肠球菌而且肠球菌都有效已在IC、危重患者和伴有共病(中风、高血压和血管疾病)的老年患者中出现多重耐药的医院病原体。
严重程度评分
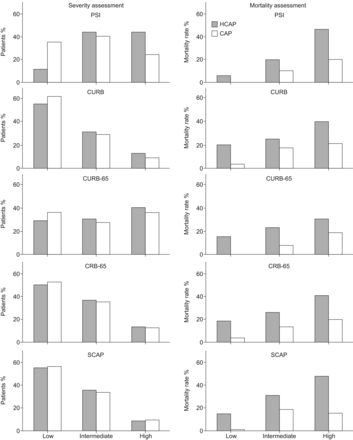
如图2,所有5个评分系统均显示死亡率随风险组的恶化而增加的趋势。在每个评分的所有风险类别中,HCAP组的死亡率较高。在分布上,CURB、CRB-65和SCAP将最大比例的患者划分为低风险,而PSI和CURB-65将最低比例的患者划分为低风险。在HCAP患者中,PSI低风险组的30天总死亡率低于所有其他评分的低风险组。
根据风险等级评估严重程度和30天死亡率。PSI:肺炎严重程度指数;CURB:混乱,尿素>7 mol·L−1,呼吸频率≥30次·min−1,收缩压< 90mmhg或舒张压≤60mmhg;CURB-65:混淆,尿素>7 mol·L−1,呼吸频率≥30次·min−1收缩压< 90mmhg或舒张压≤60mmhg,年龄≥65岁;CRB-65:意识模糊,呼吸频率≥30次·min−1收缩压< 90mmhg或舒张压≤60mmhg,年龄≥65岁;SCAP:严重社区获得性肺炎评分;医疗获得性肺炎;CAP:社区获得性肺炎。
严重程度评分和表现的比较
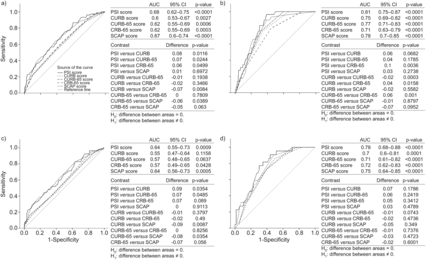
图3显示所有组和亚组中所有分数的ROC曲线、auc及其差异。CAP患者的所有预后评分均优于HCAP患者。在整个HCAP组中,PSI似乎比三个遏制得分更好地预测死亡率,尽管差异不显著;同时,SCAP曲线的表现似乎略好于CURB曲线。在非ic HCAP患者亚组中,所有预后评分的表现与CAP组相似。在IC HCAP患者中,只有PSI和SCAP评分具有预后价值。
在每个患者组中,识别30天死亡风险患者的评分系统的受试者工作特征曲线。表格详细描述了曲线下的区域(AUC)和分数之间的比较。a)医疗获得性肺炎(HCAP)患者;B)社区获得性肺炎患者;c) HCAP免疫功能低下患者;d) HCAP非免疫功能低下患者。PSI:肺炎严重程度指数;CURB:混乱,尿素>7 mol·L−1,呼吸频率≥30次·min−1,收缩压< 90mmhg或舒张压≤60mmhg;CURB-65:混淆,尿素>7 mol·L−1,呼吸频率≥30次·min−1收缩压< 90mmhg或舒张压≤60mmhg,年龄≥65岁;CRB-65:意识模糊,呼吸频率≥30次·min−1收缩压< 90mmhg或舒张压≤60mmhg,年龄≥65岁;SCAP:严重社区获得性肺炎。
在每个阈值,报告在表5, PSI比CURB和SCAP评分更敏感,但特异性较低,且负似然比(0.19)最好。
讨论
这项前瞻性研究分析了有效的CAP评分系统(PSI、CURB及其衍生物和SCAP)作为住院HCAP患者(包括免疫功能低下患者)30天死亡率的预测指标;所有的分数都不能很好地预测30天的死亡率。免疫能力对两组的分析显示,在无免疫抑制的HCAP患者中,所有得分都能很好地预测30天的死亡率,其中PSI最好,而在免疫抑制的HCAP患者中,所有得分都不能很好地预测30天的死亡率。本研究还调查了HCAP的流行病学和IC型HCAP患者的肺炎情况。CAP和HCAP队列主要由具有许多慢性合并症的老年受试者组成。脑血管疾病和慢性阻塞性肺疾病(COPD)在CAP组中更为普遍。CAP患者最常见的病原菌为链球菌引起的肺炎,而HCAP患者继发肺炎的发病率增加金黄色葡萄球菌(耐甲氧西林金黄色葡萄球菌和methicillin-sensitive金黄色葡萄球菌),假单胞菌和其他革兰氏阴性细菌。如先前报道,HCAP组的30天死亡率和住院死亡率分别为24.1%和20.2% [3.,5,7,9];CAP与30天死亡率的比值比为3.2。
我们的HCAP患者的风险类别分布是我们的研究与以前发表的研究之间的主要区别[3.- - - - - -7]。我们没有纳入任何正在进行血液透析或吸入性肺炎的患者,而且只有很小比例的养老院居民,但有很多癌症患者或因治疗而导致IC,因此我们的HCAP队列与P相似约柜等.[25],他们报告的平均PSI为104,其中29.7%的患者属于低危类,10.4%的患者属于高危的CURB-65类。然而,他们的研究是回顾性的,可能遗漏了一些信息。
本研究中HCAP患者的平均PSI为126.7,其中11.4%属于低危类。然而,在CAP组和HCAP组中,PSI和SCAP得分呈现相反的趋势:低风险PSI组得分最小,低风险SCAP组得分最高。在我们的研究中,PSI在排除严重HCAP方面比CURB-65或SCAP更有用,因为在所有截断点上,PSI对30天死亡率的高阴性预测值和低阳性预测值,而SCAP可能更适合捕捉急性疾病中的异常生命体征,因为它包括多肺x线片浸润、缺氧、酸中毒和高龄。但其对HCAP的阳性预测价值低于CURB和CRB-65,这可能意味着它们都不能指导住院患者的决策。
有人认为,HCAP人群是高度异质性的,HCAP概念可能具有误导性,并在肺炎的管理中造成混乱[22]。然而,通过比较IC HCAP患者亚组与非IC患者亚组,我们克服了这一限制。许多HCAP研究[26]不包括IC患者,尽管IC患者的研究包括艾滋病毒阳性受试者[5,27,28],但关于非中性粒细胞减少性癌症患者在接受化疗时耐药病原体引起的肺炎相关风险的数据缺乏。此外,一项对嗜中性粒细胞减少性癌症患者的研究发现,恶性肿瘤的类型并不能导致风险的差异,即。固体与血液系统恶性肿瘤[29]。
IC和非IC患者两个亚组之间的主要差异是年龄、脑血管疾病和COPD:非IC HCAP在人口统计学和共病方面与CAP相似。除了与IC患者的潜在恶性肿瘤和/或治疗相关的低红细胞压积水平和白细胞减少外,我们没有观察到入院参数的任何差异。两个HCAP亚组也有相似的30天死亡率和住院死亡率,值得注意的是,两者在30天生存率上表现出相同的趋势。这表明伴有相关合并症的高龄患者和晚期恶性肿瘤患者在肺炎期间死亡的概率同样高。
一些作者试图找到一种预测IC肺炎患者(主要是hiv感染或中性粒细胞减少症患者)死亡风险的方法[30.,31]。年代安德斯等.[32回顾性调查了IC hiv阴性患者的PSI表现,并发现按死亡风险排名反映了按不同免疫损伤原因分组。他们指出,PSI是“对未接受积极癌症治疗的患者的预后同样有效的预测指标”。我们没有将IC患者分成亚组,发现PSI在预测30天死亡率方面相当好。
然而,有必要进行进一步的研究,以评估是否可以在PSI的20个变量中添加任何其他血液生物标志物或参数,以改善其在IC患者中的表现。使用抑制因子及其衍生物来预测(特别是IC) HCAP患者30天的死亡率受到其低预后准确性的限制。
我们的数据表明,在IC患者的临床管理中使用SCAP评分可能是有用的,在这些患者中,SCAP评分似乎可以适当地反映急性肺炎相关疾病。SCAP是高危组中最特异的评分,这些患者无一存活。
我们的研究有许多局限性:它只涉及一个中心;从急诊科直接转到重症监护室的年轻重症肺炎患者丢失;我们无法确定病人的表现状态对病人结果的真正影响。此外,绝大多数因肺炎而入院的HCAP门诊患者患有恶性肿瘤或因治疗而发生IC。
HCAP人群的异质性是一个主要问题,因为已知HCAP的分布和特征取决于当地环境,这可能会影响具有不同抗生素耐药率的不同致病生物的发生率[33]。一些作者甚至声称IC患者不应被视为HCAP,但在做出治疗决定时应考虑各种疾病特异性特征[23,34]。
我们研究的优点似乎是完整的前瞻性数据收集和每个HCAP亚群的同质性,其中一些可能有自己独特的流行病学和危险因素。总之,在等待一种最佳预测仪器的开发过程中,似乎结合不同的和互补的预后系统提供的信息可能对不同的HCAP患者组有用。
致谢
特别感谢K. Smart (LINK,米兰,意大利)的英语复习。
脚注
支持声明
这项研究得到了Ricerca Corrente基金、意大利米兰的Fondazione IRCCS Ca’Granda Ospedale Maggiore Policlinico基金的支持。
权益声明书
没有宣布。
- 收到了2011年10月27日。
- 接受2012年2月14日。
- ©2012人队