摘要gydF4y2Ba
莫西沙星(MFX)是一种强大的二线抗结核药物,但最佳剂量尚未确定,长期安全性数据缺乏。gydF4y2Ba
我们回顾性回顾了2006年1月1日至2009年1月1日期间在格罗宁根大学医学中心beatrixord结核病中心接受治疗的结核病患者的医疗图表,这些患者每天接受一次MFX 400 mg作为结核病治疗的一部分。安全性数据和药物-药物相互作用进行了评估。药效预测是基于浓度-时间曲线下的面积,直到24小时后(AUC)gydF4y2Ba0-24hgydF4y2Ba)/最低抑菌浓度(MIC)比值。gydF4y2Ba
89例患者中位剂量为6.9 mg·kggydF4y2Ba−1gydF4y2BaMFX每日一次,平均持续74天。只有三名患者因胃肠道副作用和过敏而停止治疗。药代动力学分析显示AUCgydF4y2Ba0-24hgydF4y2Ba/MIC比值<100的患者为8 / 16。蛋白质结合的巨大差异影响了未结合的AUCgydF4y2Ba0-24hgydF4y2Ba很大。gydF4y2Ba
这些数据显示,89例患者接受每日一次400mg剂量的MFX治疗,耐受性良好,持续时间较长。考虑(un)bound AUC的可变性gydF4y2Ba0-24hgydF4y2Ba/MIC比值,建议对选定患者进行治疗药物监测(gydF4y2Ba即。gydF4y2Ba利福平co-medication;麦克风≥0.25 mg·LgydF4y2Ba−1gydF4y2Ba)以评估最佳治疗方法。gydF4y2Ba
莫西沙星(MFX),氟喹诺酮类药物gydF4y2Ba在体外gydF4y2Ba和gydF4y2Ba在活的有机体内gydF4y2Ba杀菌活性对gydF4y2Ba结核分枝杆菌gydF4y2Ba,用于治疗耐多药(MDR)结核病(TB)或对一线结核病药物不耐受的情况,目前正在评估其缩短结核病治疗时间的潜力[gydF4y2Ba1gydF4y2Ba].此外,MFX似乎在对早期一代氟喹诺酮类药物耐药性的情况下有用[gydF4y2Ba2gydF4y2Ba].尽管MFX已被广泛用于结核病的治疗,但人们应该记住,该药物并没有标明这一适应症[gydF4y2Ba3.gydF4y2Ba目前每日一次400mg MFX方案治疗时间超过2周的最佳剂量和安全性/耐受性数据缺乏。gydF4y2Ba
对于其他氟喹诺酮类药物,建议以血药浓度-时间曲线(AUC)相对于最低抑菌浓度(MIC)的面积作为预测的最佳参数gydF4y2Ba在活的有机体内gydF4y2Ba对革兰氏阴性菌有效gydF4y2Ba结核分枝杆菌gydF4y2Ba[gydF4y2Ba4gydF4y2Ba- - - - - -gydF4y2Ba6gydF4y2Ba].建模研究表明,应考虑每日600-800 mg MFX的最佳杀灭细菌,并获得86-93%的概率达到与耐药突变体抑制相关的靶点(gydF4y2Ba即。gydF4y2Ba给药后24小时浓度-时间曲线下的未结合区域(AUCgydF4y2Ba0-24hgydF4y2Ba)/MIC比率53)[gydF4y2Ba7gydF4y2Ba,高于目前每日一次400毫克的剂量。由于治疗效果是由蛋白未结合(自由)浓度决定的,因此还应考虑MFX蛋白结合[gydF4y2Ba5gydF4y2Ba].gydF4y2Ba
结核患者中临床最相关的药物相互作用是MFX和利福平(RIF),导致MFX暴露预期减少31% [gydF4y2Ba8gydF4y2Ba,gydF4y2Ba9gydF4y2Ba].铁和锌等矿物质补充剂或抗酸剂也可能降低MFX的生物利用度[gydF4y2Ba10gydF4y2Ba],但在每日服用400 mg MFX与食物或钙补充剂联合使用后,MFX的AUC未受显著影响[gydF4y2Ba10gydF4y2Ba].gydF4y2Ba
长期治疗的主要问题是,不良反应可能导致依从性降低,可能导致耐药。MFX的副作用,例如呕吐和腹泻[gydF4y2Ba10gydF4y2Ba,会影响MFX的耐受性。MFX的一个潜在的严重但不常见的副作用是QT延长[gydF4y2Ba11gydF4y2Ba].gydF4y2Ba
MFX 400mg每日一次是安全的,且在少数患者的长期治疗研究中耐受性良好[gydF4y2Ba12gydF4y2Ba,gydF4y2Ba13gydF4y2Ba].尽管使用MFX治疗结核病患者的经验不断增加[gydF4y2Ba14gydF4y2Ba- - - - - -gydF4y2Ba16gydF4y2Ba],需要进行更大规模的研究以确认适当剂量的疗效和长期安全性。支持改用建议的更高剂量的安全性数据很少[gydF4y2Ba11gydF4y2Ba,gydF4y2Ba17gydF4y2Ba,gydF4y2Ba18gydF4y2Ba].gydF4y2Ba
本研究的目的是回顾性评价MFX在结核病治疗中的药代动力学和药效学参数、药物相互作用和安全性/耐受性,以评估是否已经给予最佳治疗。因此,这些发现将有助于在未来结核病患者中发现MFX的剂量,并提高对其药代动力学的认识。gydF4y2Ba
患者和方法gydF4y2Ba
对所有接受MFX (Avelox®;拜耳,勒沃库森,德国)至少5天(稳定状态)作为他们的结核病治疗的一部分[gydF4y2Ba19gydF4y2Ba2006年1月1日至2009年1月1日在格罗宁根大学医学中心(哈伦,荷兰)beatrixord结核病中心进行了一项研究。从病历中收集人口统计学和医学数据,包括年龄、性别、体重、身高、种族、共病、诊断、结核定位、MIC、耐药模式、病史、MFX治疗剂量和持续时间、(TB)联合用药剂量和持续时间以及MFX引起的不良反应。根据本研究的回顾性性质,不需要我们当地伦理委员会的批准。gydF4y2Ba
药物动力学和药效学gydF4y2Ba
可用时,MFX在血浆和血浆超滤液中的浓度(室温20分钟,1640 ×gydF4y2BaggydF4y2Ba在固定角度转子,hetich EBA 21;Andreas Hettich GmbH and Co.KG, Beverly, MA, USA)采用有效的液相色谱-串联质谱分析方法测定[gydF4y2Ba20gydF4y2Ba].在处理后至少5天的稳定状态下获得的样品符合评价标准[gydF4y2Ba19gydF4y2Ba].不同的药代动力学参数,包括AUCgydF4y2Ba0-24hgydF4y2Ba采用标准的单室药代动力学方法,使用MW\Pharm 3.60 (Mediware, Zuidhorn,荷兰)的kininfit模块进行测定。的AUCgydF4y2Ba0-24hgydF4y2Ba按对数线性梯形法则计算。由于MFX蛋白结合可能是浓度依赖的(范围为0.077-0.6)[gydF4y2Ba5gydF4y2Ba,我们选择测定血浆超滤液中的未结合浓度为低(<1.0 mg·LgydF4y2Ba−1gydF4y2Ba血浆总MFX(蛋白结合+非结合)浓度较高(>1.0 mg·LgydF4y2Ba−1gydF4y2Ba)的浓度-时间曲线。平均蛋白非结合浓度被用来评估非结合浓度-时间曲线。gydF4y2Ba
可用药敏试验gydF4y2Ba结核分枝杆菌gydF4y2Ba采用Middlebrook 7H10琼脂稀释法分离[gydF4y2Ba21gydF4y2Ba荷兰国家结核病参考实验室(国家公共卫生和环境研究所,荷兰比尔托芬)。gydF4y2Ba
蛋白质结合和非结合的AUCgydF4y2Ba0-24hgydF4y2Ba/MIC比值,以及发生AUC的患者人数gydF4y2Ba0-24hgydF4y2Ba/确定MIC比率>100。由于治疗效果由蛋白质未结合(游离)浓度决定,因此(gydF4y2Ba即。gydF4y2Ba绑定和未绑定)AUCgydF4y2Ba0-24hgydF4y2Ba/MIC比率>100 [gydF4y2Ba5gydF4y2Ba,gydF4y2Ba22gydF4y2Ba将转换为未绑定的AUCgydF4y2Ba0-24hgydF4y2Ba/MIC比率超过至少60。这一比例源于MFX最常报道的约40%的蛋白结合值[gydF4y2Ba23gydF4y2Ba,结果是一个未绑定的分数0.6。gydF4y2Ba
药物之间相互作用gydF4y2Ba
药物-药物相互作用可能通过干扰MFX的吸收、代谢或排泄而影响MFX的疗效。我们评估了以下药物的联合用药:RIF、抗酸剂、粘膜保护剂、矿物质(gydF4y2Ba如。gydF4y2Ba锌和铁)和二氰胺[gydF4y2Ba8gydF4y2Ba,gydF4y2Ba10gydF4y2Ba].gydF4y2Ba
根据两名同时使用和不同时使用MFX和RIF的患者的药代动力学曲线,使用MFX剂量、TB患者的体表面积、血清肌酐浓度和观察到的MFX plas生成两个单独的单室药代动力学群体模型,具有一级吸收,无滞后时间使用迭代两阶段贝叶斯程序的ma浓度(MW\Pharm 3.60)[gydF4y2Ba24gydF4y2Ba].所有的药代动力学曲线都是在达到稳态MFX浓度后获得的,而不是在达到稳态RIF浓度后同时使用MFX和RIF。gydF4y2Ba
安全/耐受性gydF4y2Ba
为了评价MFX治疗的安全性,从病历中检索了所有记录的不良反应,包括腹泻、呕吐和QT间期延长。MFX禁忌用于转氨酶高于正常水平5倍以上的患者[gydF4y2Ba3.gydF4y2Ba].如果在MFX治疗期间,以下至少一种酶的值超过正常水平的5倍以上,且无肝功能障碍,则为肝损伤(gydF4y2Ba即。gydF4y2Ba(3级普通毒性标准(CTC)):天冬氨酸转氨酶(ASAT;> 200 U·LgydF4y2Ba−1gydF4y2Ba),丙氨酸转氨酶(ALAT;>225 U·LgydF4y2Ba−1gydF4y2Ba)和-谷氨酰转肽酶(GGT;> 200 - 275 U·LgydF4y2Ba−1gydF4y2Ba) [gydF4y2Ba25gydF4y2Ba].肾损伤定义为血清肌酐水平较基线升高25%(1级CTC) [gydF4y2Ba25gydF4y2Ba].血清肌酐值为112.5 μmol·L时为正常上限值gydF4y2Ba−1gydF4y2Ba(雌)或137.5 μmol·LgydF4y2Ba−1gydF4y2Ba(男性)。QT间期>500 ms与心脏事件风险增加相关[gydF4y2Ba26gydF4y2Ba].在治疗~ 2周后,如果MFX的剂量增加,医生会对每个患者进行常规的三导联心电图检查。任何心电图上的异常观察都记录在用药图上。为了评估长期MFX治疗导致QT延长的风险,我们确定了(除了使用MFX之外)可能导致或加重使用MFX治疗的TB患者QT延长的危险因素。评估患者的以下危险因素:女性、肝功能障碍、心律失常前病变(gydF4y2Ba即。gydF4y2Ba低钾血症(<3.5 mmol·LgydF4y2Ba−1gydF4y2Ba低镁血症(<0.7 mmol·L)gydF4y2Ba−1gydF4y2Ba血液),同时使用IA类和III类抗心律失常药物、抗精神病药物、三环抗抑郁药物或抗组胺药物特非那定[gydF4y2Ba3.gydF4y2Ba,gydF4y2Ba27gydF4y2Ba,gydF4y2Ba28gydF4y2Ba].gydF4y2Ba
为了确定副作用和MFX治疗之间的潜在因果关系,使用了Naranjo算法(0-9点,其中9点代表最高可能性)[gydF4y2Ba29gydF4y2Ba].探讨总药物暴露(AUC)与不良反应的关系。gydF4y2Ba
特别注意停止制造外汇。原因分为四类:1)MFX是基于预期耐药性(原产国、病史)开始的,在药敏模式可用并显示对一线药物敏感后停止;2)因对一线TB药物不耐受而启动MFX,不良反应消除,一线药物再次成功导入后停用MFX;3)完成MFX处理;4) mfx诱发的不良事件。gydF4y2Ba
统计数据gydF4y2Ba
当非正态分布时,使用非参数检验,gydF4y2Ba即。gydF4y2Ba排序数据采用Mann-Whitney u检验和Wilcoxon秩和检验,名义数据采用卡方检验。gydF4y2Ba
结果gydF4y2Ba
病人的特点gydF4y2Ba
对89例中位(四分位区间(IQR))年龄为35(27-47)岁的患者进行回顾性分析;女性32例(36%),男性57例(64%)。一名患者(变性人)被排除在外,因为给药激素对几个重要临床参数的未知影响。肺结核是最常见的诊断(67例(75%)患者)。32例(36%)患者在治疗史的基础上由于预期耐药(MDR-TB)而开始使用MFX。患者接受MFX 400 mg,每日1次,相当于中位(IQR)剂量6.9 (6.0-8.1)mg·kggydF4y2Ba−1gydF4y2Ba.患者接受MFX治疗的中位(IQR)期为74(29–186)天。在治疗期间,有四名患者每天一次的剂量增加到800毫克。由于AUC,所有病例的剂量都增加到800毫克gydF4y2Ba0-24hgydF4y2Ba/MIC比值<100(gydF4y2Ba即。gydF4y2BaAUCgydF4y2Ba0-24hgydF4y2Ba/MIC 56-83)结合AUCgydF4y2Ba0-24hgydF4y2Ba值< 50 mg·h·LgydF4y2Ba−1gydF4y2Ba(n=3)或低AUCgydF4y2Ba0-24hgydF4y2Ba(gydF4y2Ba即。gydF4y2BaAUCgydF4y2Ba0-24hgydF4y2Ba24.1 mg·h·LgydF4y2Ba−1gydF4y2Ba)在治疗开始时(n=1)结合未知的耐药模式。此后,根据AUC将剂量降至600 mg,每日一次gydF4y2Ba0-24h -gydF4y2Ba/MIC比值>100 (n=2)或基于耐药性模式,在治疗开始时尚不清楚(n=1)。两名患者死于艾滋病和结核病,与MFX无关。对基线患者特征和抗结核药物的概述见gydF4y2Ba表1gydF4y2Ba和gydF4y2Ba2gydF4y2Ba.gydF4y2Ba
药物动力学和药效学gydF4y2Ba
从16名患者获得了完整的血浆药代动力学曲线。平均血浆浓度-时间曲线如所示gydF4y2Ba图1gydF4y2Ba.其中9例患者可用血浆超滤液。我们观察到个体间可变的血浆蛋白结合从11.0到41.7%不等。血浆中中位(IQR)蛋白结合率为25.1(18.1-34)%,中位浓度为2.6 (2.3-2.8)mg·LgydF4y2Ba−1gydF4y2Ba(高)和29.7(24-35.6)%,中位浓度为0.3 (0.24-0.33)mg·LgydF4y2Ba−1gydF4y2Ba(低),差异无统计学意义(p=0.500)。MFX的稳态药代动力学参数见gydF4y2Ba表3gydF4y2Ba.服用MFX 400 mg,每日1次,AUCgydF4y2Ba0-24hgydF4y2Ba在血浆中是高度可变的。最高血浆浓度(CgydF4y2Ba马克斯gydF4y2Ba或mfx后4h血药浓度(CgydF4y2Ba4gydF4y2Ba)和AUCgydF4y2Ba0-24hgydF4y2Ba(r=0.8和0.9,p<0.001;斯皮尔曼相关系数)。MFX的中位(IQR) MIC为0.25 (0.125-0.5)mg·LgydF4y2Ba−1gydF4y2Ba.gydF4y2Ba
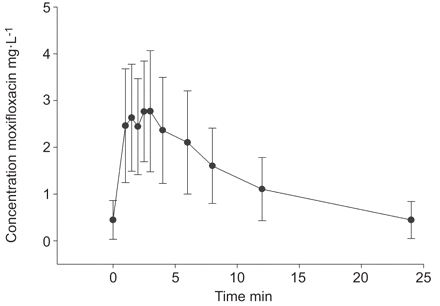
血浆中莫西沙星平均浓度-时间曲线(n=16)。莫西沙星的平均血药浓度用实心圆表示。标准偏差用误差棒表示。gydF4y2Ba
几何平均AUCgydF4y2Ba0-24hgydF4y2Ba/MIC比值(n=16)为82(范围21-320)。在血浆中,16例患者中有8例出现下弧gydF4y2Ba0-24hgydF4y2Ba/MIC比>100和8的比值<100(范围21-83)。几何平均未结合等离子体AUCgydF4y2Ba0-24hgydF4y2Ba和不受约束的AUCgydF4y2Ba0-24hgydF4y2Ba/MIC = 22 (12-64) mg·h·LgydF4y2Ba−1gydF4y2Ba和59 (16-257)mg·h·LgydF4y2Ba−1gydF4y2Ba,分别。在血浆超滤液中,9例患者中有5例有未结合的AUCgydF4y2Ba0-24hgydF4y2Ba/MIC比>60和4的比值<60(范围16-49)。3例患者的MIC为1 mg·LgydF4y2Ba−1gydF4y2Ba因此,一个较低的未绑定和总AUCgydF4y2Ba0-24hgydF4y2Ba/麦克风比率。gydF4y2Ba
安全/耐受性gydF4y2Ba
MFX耐受性良好;只有3例(3.4%)患者因胃肠道不良反应(n=2)和过敏反应(n=1)而停止服用。不良反应的概述见gydF4y2Ba表4gydF4y2Ba.在治疗期间,肾功能检查没有恶化。我们观察到显著下降(ASAT: p=0.004;ALAT: p=0.020)。然而,在一名患者中,正常GGT值增加到正常水平的5倍以上(Naranjo评分3)。在四名患者中,血清肌酐值在治疗期间增加,同时体重增加,但仍在正常范围内,血清肌酐的增加可能反映了肌肉质量的增加和肾功能的稳定。有2人出现呕吐(2%;纳兰霍得分为3分,腹泻得分为8分(9%;Naranjo评分为3或4)患者。35例患者至少有一个额外的QT延长危险因素,17例患者有两个额外的危险因素,1例患者有四个危险因素,但没有观察到QT延长。 In our study population, female sex was the most common potential risk factor for QT prolongation. AUC0-24hgydF4y2Ba值不能与不良事件相关,因为不良事件很少,且AUCgydF4y2Ba0-24hgydF4y2Ba这些值仅在一部分患者中确定。gydF4y2Ba
药物之间相互作用gydF4y2Ba
RIF常与MFX合用。在68.5、10.1和1.1%的患者中,MFX联合RIF,剂量分别为600、450和150 mg。gydF4y2Ba
在6名单独服用MFX的患者和10名服用RIF和MFX的患者中可获得完整的药代动力学浓度-时间曲线。与RIF联合用药不会显著降低血浆AUCgydF4y2Ba0-24hgydF4y2Ba值的几何平均值为36.8(范围为12.7-50.4)gydF4y2Ba与gydF4y2Ba21.3(范围8.5-72.2)mg·h·LgydF4y2Ba−1gydF4y2Ba(p=0.104)。以mg·kg为单位的MFX剂量之间无显著差异gydF4y2Ba−1gydF4y2Ba在有或没有RIF联合MFX治疗的患者之间观察到(p=0.871)。人群药代动力学分析(gydF4y2Ba表5gydF4y2Ba)显示,在同时使用MFX和RIF的患者中,MFX的明显清除是(没有显著)诱导的(p=0.083),但这种诱导是由于两组患者间的差异。MFX不与抗酸剂、粘膜保护剂、矿物质或二氰胺同时服用。gydF4y2Ba
讨论gydF4y2Ba
我们观察到蛋白质结合的巨大变化。这是一个重要的发现,因为只有未结合的药物有助于抗菌效果。入院时营养不良和临床状况恶化是这些巨大变化最合理的解释。然而,由于本研究的回顾性和相对较小的l样本量(n=9)和已知的未结合MFX浓度,我们无法证实这一假设。因此,只要设施可用,确定每个个体中的未结合MFX浓度似乎是合乎逻辑的。因为未结合MFX的分数似乎不依赖于浓度,与早期报告相反[gydF4y2Ba5gydF4y2Ba],单个血样可用于评估治疗期间特定时间的血浆蛋白结合,因为血浆蛋白水平可能在治疗期间发生变化。gydF4y2Ba
的AUCgydF4y2Ba0-24hgydF4y2Ba/MIC比值是预测MFX疗效的最佳参数,其比值超过100为宜[gydF4y2Ba5gydF4y2Ba,gydF4y2Ba6gydF4y2Ba,gydF4y2Ba22gydF4y2Ba].16名患者中有8名患者的AUCgydF4y2Ba0-24hgydF4y2Ba/MIC比率<100。通过每天一次增加剂量至600 mg,AUCgydF4y2Ba0-24hgydF4y2Ba会增加约1.5倍[gydF4y2Ba11gydF4y2Ba,导致AUCgydF4y2Ba0-24hgydF4y2Ba/麦克风比率≥100。测量未结合的血药浓度可以避免剂量调整,如果未结合的AUCgydF4y2Ba0-24hgydF4y2Ba/MIC比率>60,而总AUCgydF4y2Ba0-24hgydF4y2Ba/MIC比值<100。gydF4y2Ba
我们观察到AUC有很大的变异性gydF4y2Ba0-24hgydF4y2Ba,这是本研究所独有的。观察到的变异性(9倍)可能具有临床意义。基于中值AUCgydF4y2Ba0-24hgydF4y2Ba24.8 mg·h·LgydF4y2Ba−1gydF4y2Ba(gydF4y2Ba表3gydF4y2Ba)每日一次,标准剂量400 mg的MFX可用于治疗最大MIC为0.25 mg·L的分离物gydF4y2Ba−1gydF4y2Ba.即MIC值较高,AUC较低gydF4y2Ba0-24hgydF4y2Ba标准剂量不足以满足所有患者。在增加标准剂量之前,AUCgydF4y2Ba0-24hgydF4y2Ba/MIC比率最好通过测量AUC来评估gydF4y2Ba0-24hgydF4y2Ba最后,对选定的患者进行MFX治疗药物监测(TDM)(gydF4y2Ba即。gydF4y2BaRIF co-medication;麦克风> 0.25 mg·LgydF4y2Ba−1gydF4y2Ba),因此这种选择偏差可以解释观察到的MFX AUC的变异性gydF4y2Ba0-24hgydF4y2Ba.尽管如此,标准剂量400mg MFX每天一次会导致AUC的变化gydF4y2Ba0-24hgydF4y2Ba因此,对所有的病人来说可能是不够的。gydF4y2Ba
66例(74.2%)患者RIF合并MFX。然而,根据早先的报告[gydF4y2Ba8gydF4y2Ba,gydF4y2Ba9gydF4y2Ba],同时使用RIF和MFX确实可减少MFX暴露。然而,这种下降并不显著。此外,我们观察到,在同时使用MFX和RIF的患者中,表观清除率没有显著增加。这可能是由于缺乏统计能力,因为并非所有患者都获得了完整的药动学曲线;此外,AUC的组内变异gydF4y2Ba0-24hgydF4y2Ba因此,我们的结果不排除RIF和MFX之间存在显著的药物-药物相互作用,特别是在存在相互作用趋势的情况下。gydF4y2Ba
在早期发表的研究中,MFX (400 mg)在19例结核病患者中具有良好的耐受性,持续180天[gydF4y2Ba12gydF4y2Ba],在38内,为期174天[gydF4y2Ba13gydF4y2Ba],在74年的56天内[gydF4y2Ba14gydF4y2Ba],并在53内,为期60天[gydF4y2Ba15gydF4y2Ba].每周3-5次较少密集的MFX计划也具有良好的耐受性[gydF4y2Ba16gydF4y2Ba].我们的研究有89名患者,中位治疗时间为74天,这增加了重要的安全信息,因为我们的患者群体没有被选择,因此代表了真实的生活状况。MFX在我们的研究人群中耐受性良好;Naranjo评分显示,观察到的不良反应发生的可能性较低,只有3例患者停用了MFX。虽然一线抗结核药物引起肝酶升高,但我们在MFX治疗期间没有观察到任何严重的不良事件,事实上,肝酶降低了。这种现象可能是由于一线抗结核药物的转换,导致肝酶升高到MFX。MFX的一个潜在的严重但不常见的副作用是可能加重QT延长[gydF4y2Ba11gydF4y2Ba].尽管有一些额外的QT延长危险因素,但在我们的人群中没有观察到QT延长。为了防止治疗失败和抑制对MFX的耐药性,大多数结核病患者理论上需要更高剂量的600-800 mg [gydF4y2Ba7gydF4y2Ba].健康志愿者服用800 mg MFX后观察到QT延长[gydF4y2Ba11gydF4y2Ba].然而,在这些志愿者中,观察到的几何平均AUCgydF4y2Ba0-24hgydF4y2Ba800 mg·h·L的MFX为87 mg·h·LgydF4y2Ba−1gydF4y2Ba,是预期AUC的1.8倍gydF4y2Ba0-24hgydF4y2Ba24.8×2=49.6 mg·h·LgydF4y2Ba−1gydF4y2Ba(2×AUCgydF4y2Ba0-24hgydF4y2Ba400毫克MFX(gydF4y2Ba表3gydF4y2Ba在我们的结核病患者中使用800毫克MFX。考虑到这些结果,必要的剂量增加对大多数结核病患者是安全的。然而,对于AUC高的患者,建议进行心电图监测gydF4y2Ba0-24hgydF4y2Ba以及QT延长有额外危险因素的患者[gydF4y2Ba3.gydF4y2Ba,gydF4y2Ba11gydF4y2Ba,gydF4y2Ba18gydF4y2Ba].gydF4y2Ba
血浆蛋白结合(AUC)差异大gydF4y2Ba0-24hgydF4y2Ba, MIC和药物-药物相互作用对AUC有较大影响gydF4y2Ba0-24hgydF4y2Ba/MIC比率,这个问题没有得到完全解决。我们假设CgydF4y2Ba马克斯gydF4y2Ba或CgydF4y2Ba4gydF4y2Ba可以作为AUC的替代预测因子gydF4y2Ba0-24hgydF4y2Ba因此,在有限的样本下,TDM应该是可能的。接受RIF的患者或感染MFX MIC≥0.25 mg·L的分离株的患者gydF4y2Ba−1gydF4y2Ba我们建议测量至少一个峰值MFX水平和测定血浆蛋白结合,因为这些病例有AUC的风险gydF4y2Ba0-24hgydF4y2Ba/麦克风比< 100。然而,对于因腹泻或呕吐而怀疑吸收不良的患者,也应评估MFX血浆浓度。MDR-TB患者可能受益最大,因为MFX的MIC在这些患者中通常较高,但MFX在600-800 mg剂量下的安全性应仔细监测。gydF4y2Ba
结论gydF4y2Ba
89例患者对MFX治疗耐受性良好,每日一次,剂量为400 mg(中位剂量为6.7 mg·kg)gydF4y2Ba−1gydF4y2Ba),平均持续时间为74天。评估(unbound) AUCgydF4y2Ba0-24hgydF4y2Ba/MIC的比例需要制定最佳的给药计划(固定的或TDM指导的),以治疗结核病患者和预防耐药性。gydF4y2Ba
致谢gydF4y2Ba
感谢德国拜耳公司提供莫西沙星用于我们的分析方法。gydF4y2Ba
脚注gydF4y2Ba
感兴趣的语句gydF4y2Ba
有关本研究的兴趣声明可在gydF4y2Bawww.www.qdcxjkg.com/site/misc/statements.xhtmlgydF4y2Ba
- 收到了gydF4y2Ba2010年11月15日。gydF4y2Ba
- 接受gydF4y2Ba2011年1月31日。gydF4y2Ba
- ©2011人队gydF4y2Ba
参考文献gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba















