摘要gydF4y2Ba
盘状蛋白结构域受体(DDR)1是一种细胞外基质(ECM)敏感受体酪氨酸激酶,由胶原激活,在支气管上皮表达。DDR1负责维持皮肤和肾脏上皮的正常结构,我们假设DDR1通过转导来自气道ECM的信号在支气管上皮的完整性中发挥调节作用。gydF4y2Ba
通过RNA干扰原代人支气管上皮细胞(HBECs)和BEAS-2B细胞,研究了DDR1缺失的影响。利用质粒载体研究了过表达DDR1a和DDR1b对BEAS-2B细胞的影响。我们使用划伤模型测量了对上皮修复的影响,并通过明胶酶谱(MMP-2和-9)和ELISA (MMP-7)测定了基质金属蛋白酶(MMPs)的水平。gydF4y2Ba
我们发现,DDR1的下调使上皮修复减慢了50%,这与MMP-7水平的降低有关,而DDR1过表达增强了上皮修复。DDR1的敲除减少了HBECs的增殖,但对I型胶原蛋白或其他基质基质的粘附没有显著影响。gydF4y2Ba
这些数据表明ECM信号gydF4y2Ba通过gydF4y2BaDDR1在气道中调控支气管上皮修复、完整性和MMP表达等方面。gydF4y2Ba
维持上皮细胞的完整性对支气管上皮细胞的正常功能至关重要,包括宿主防御和上皮屏障功能。支气管上皮的损伤与修复是呼吸道疾病的特征,如哮喘和对病毒感染的反应。直接的毒性损伤、创伤或炎症过程导致上皮细胞丢失,导致基底上皮细胞和基底膜暴露,然后开始修复过程[gydF4y2Ba1gydF4y2Ba,gydF4y2Ba2gydF4y2Ba].上皮修复是一个复杂的过程,包括增殖、迁移和粘附。最初,剩余的上皮细胞分泌临时基质,主要由胶原I和III和纤维连接蛋白组成。通过粘附在这个临时基质上,这些细胞迁移到损伤部位。随后,远离伤口边缘的细胞进行增殖反应[gydF4y2Ba2gydF4y2Ba,gydF4y2Ba3.gydF4y2Ba].恢复的过程也与分泌因子的产生有关并依赖于这些分泌因子,如表皮生长因子(EGF)和三叶因子,它们通过增加上皮细胞的运动性来促进支气管上皮的修复[gydF4y2Ba3.gydF4y2Ba- - - - - -gydF4y2Ba5gydF4y2Ba].基质金属蛋白酶(MMPs)可以改造细胞外基质(ECM),影响细胞- ECM的相互作用,是上皮修复的重要组成部分。MMP-7由支气管上皮细胞组成性表达,在MMP-7敲除小鼠模型中,机械损伤后支气管上皮修复完全取消[gydF4y2Ba6gydF4y2Ba].MMP-7的底物包括ECM成分纤维连接蛋白、细胞-细胞相互作用分子e -钙粘蛋白和蛋白酶,包括在上皮修复过程中也上调的pro-MMP-2 [gydF4y2Ba7gydF4y2Ba].gydF4y2Ba
ECM受体的整合素家族和细胞表面糖蛋白CD44与ECM成分相互作用,促进上皮细胞的粘附和迁移[gydF4y2Ba8gydF4y2Ba- - - - - -gydF4y2Ba16gydF4y2Ba].盘状蛋白结构域受体(DDRs)是一个受体酪氨酸激酶家族,其同源配体是胶原蛋白家族,特别是胶原I - v:胶原I和III是上皮修复过程中产生的ECM的重要组成部分[gydF4y2Ba17gydF4y2Ba- - - - - -gydF4y2Ba19gydF4y2Ba].DDR1在支气管上皮中表达,并已被证明在维持皮肤和肾脏上皮的正常结构中起重要作用[gydF4y2Ba20.gydF4y2Ba- - - - - -gydF4y2Ba22gydF4y2Ba].DDR1也是损伤后动脉伤口修复所必需的[gydF4y2Ba23gydF4y2Ba].特发性肺纤维化是一种以持续性上皮损伤为特征的疾病,在特发性肺纤维化患者的全肺样本中[gydF4y2Ba24gydF4y2Ba],与正常组织相比,DDR1 mRNA与MMP-7、MMP-2、MMP-9均强烈过表达[gydF4y2Ba25gydF4y2Ba].综上所述,这些数据表明DDR1可能在这种疾病中发挥作用,可能是通过调节上皮修复和MMP活性。gydF4y2Ba
我们假设DDR1通过在ECM和上皮细胞之间转导信号来调节上皮修复和修复效应物(如MMPs),从而在气道上皮修复中发挥作用。在本研究中,我们通过实验确认了DDR1在支气管上皮中的存在,并研究了DDR1对上皮创面愈合、增殖、粘连以及MMP-7、MMP-2和MMP-9水平的影响。我们还研究了哮喘(一种以上皮完整性和修复异常为特征的疾病)患者和非哮喘对照组的上皮细胞中DDR1的表达,以检查DDR1在哮喘中的表达是否存在差异。gydF4y2Ba
方法gydF4y2Ba
细胞培养gydF4y2Ba
BEAS-2B细胞(American Type Culture Collection, Manassas, VA, USA)在Dulbecco 's modified Eagle 's medium (DMEM)/F12 (Invitrogen, Paisley, UK)中培养,添加10%胎牛血清(FBS;PAA Laboratories, Yeovil, UK), 37°C, 5% COgydF4y2Ba2gydF4y2Ba.用胰蛋白酶- edta进行传代培养(Sigma, Poole,英国)。人类支气管上皮细胞(HBECs)来自Lonza (Wokingham, UK)或通过支气管镜检查获得的活检。支气管活检立即转移到温PBS (Invitrogen)细胞培养实验室。然后在低倍解剖显微镜下解剖活检以分离上皮组织。将外植体转移到具有最小体积支气管上皮生长培养基(支气管上皮基础培养基(bron支气管上皮基础培养基,BEBM)补充支气管上皮生长培养基SingleQuot kit;龙沙),在37°C在5% CO中孵育gydF4y2Ba2gydF4y2Ba过夜,便于粘附。然后增加培养基体积,外植体在水下培养中生长,直到细胞数量足够大,可以转移到烧瓶中。使用胰蛋白酶- edta收集外植体衍生的HBECs和细胞。用大豆胰蛋白酶抑制剂(Invitrogen)在PBS中中和胰蛋白酶。gydF4y2Ba
DDR1击倒gydF4y2Ba
培养的BEAS-2B细胞在支气管上皮“损伤”培养基(BEWM)中洗涤[gydF4y2Ba3.gydF4y2Ba],由含有维甲酸、三碘甲状腺原氨酸、牛垂体提取物和重组人胰岛素的BEBM组成。然后暴露于由2 μL·mL组成的RNA干扰(RNAi)转染复合物gydF4y2Ba−1gydF4y2BaLipofectamine™2000 (Invitrogen)与20 nM小干扰RNA (siRNA)预孵育至DDR1或对照号1 (DDR1检测序列:GCC AGU GAC ACU AAA ACA Att;DDR1反义序列:UUG UUU UAG UGU CAC UGG Ctt;应用生物系统公司,沃灵顿,英国)。对于HBECs,细胞暴露于RNAi 4小时,然后在BEWM中恢复48小时。gydF4y2Ba
DDR1过度gydF4y2Ba
用pIRES2-EGFP载体(Clontech, saint - germainen - laye, France)转染BEAS-2B细胞,或者不使用插入物作为对照,或者含有活性DDR1a、活性DDR1b或激酶死亡(kd) DDR1a变体的载体,该变体已被证明在I型胶原激活时可阻止DDR1所有酪氨酸残基的自磷酸化(K618A,激酶结构域功能取代的丧失)[gydF4y2Ba26gydF4y2Ba].所有转染均使用Fugene (Roche, Burgess Hill, UK)进行。DDR1结构是由已故的W. Vogel(多伦多大学,多伦多,加拿大;个人沟通)。对于过表达研究,使用稳定转染,并根据标准程序使用Geneticin (Invitrogen)抗生素选择获得稳定转染的pIRES2-EGFP表达细胞。gydF4y2Ba
DDR1表达:Western blottinggydF4y2Ba
细胞裂解物使用Cytobuster (Merck Biosciences, Nottingham, UK)和完全蛋白酶抑制剂(Roche Diagnostics)获得。细胞在冰上孵育30min,以10000 ×离心去除不溶性细胞碎片gydF4y2BaggydF4y2Ba将样品与等体积的加载缓冲液结合3分钟。蛋白质用10%聚丙烯酰胺-十二烷基硫酸钠凝胶电泳分离,印迹到聚偏氟乙烯膜上,用抗ddr1抗体(Santa Cruz Biotechnology, Heidelberg, Germany)检测,然后用辣根过氧化物酶标记的多克隆山羊抗兔二抗(Sigma)检测。用增强的化学发光法观察条带(Amersham Biosciences, Amersham, UK)。α-肌动蛋白(Sigma)重探针印迹法证实蛋白含量相等。gydF4y2Ba
定量聚合酶链反应gydF4y2Ba
使用QIAGEN RNeasy试剂盒(QIAGEN, Crawley, UK)提取RNA,并使用DNAse I (QIAGEN)去除污染的基因组DNA。cDNA用上标II (Invitrogen)合成。RT-PCR采用Invitrogen Recombinant在Biometra Thermal Cycler上进行gydF4y2BaTaqgydF4y2BaDNA聚合酶。程序是按照制造商的说明进行的。条件是94°C 30 s, 60°C 30 s和72°C 30 s,共35个循环。PCR产物溶解在2%琼脂糖凝胶上,用溴化乙锭染色。对于定量PCR, SYBR Green技术用于Stratagene Mx3005P实时PCR系统(Agilent Technologies, Stockport, UK),设置为以下40个循环:95°C 30 s, 60°C 30 s和72°C 30 s。每个反应含有12.5 μL Brilliant Green (Agilent Technologies)、6.5 μL水、5 μL cDNA和1 μL 5 μM引物混合物。解离曲线呈单峰。引物效率用稀释曲线计算。转录本的相对表达通过计算相对于管家基因(βgydF4y2Ba2gydF4y2Ba微球蛋白)[gydF4y2Ba27gydF4y2Ba].引物从已发表的文献中获得如下[gydF4y2Ba28gydF4y2Ba- - - - - -gydF4y2Ba30.gydF4y2Ba].βgydF4y2Ba2gydF4y2Ba-microglobulin-forward: GAGTGCTGTCTCCATGTTTGATGT;βgydF4y2Ba2gydF4y2Ba-microglobulin-reverse: AAGTTGCCAGCCCTCCTAGAG;DDR1-forward: ATGGAGCAACCACAGCTTCTC;DDR1-reverse: CTCAGCCGGTCAAACTCAAACT;DDR2-forward: GGAGGTCATGGCATCGAGTT;DDR2-reverse: GAGTGCCATCCCGACTGTAATT。gydF4y2Ba
组织培养塑料的ECM涂层gydF4y2Ba
大鼠尾胶原蛋白(Sigma)稀释至10 μg·mLgydF4y2Ba−1gydF4y2Ba应用于组织培养塑料薄层,并允许风干一夜。大量清洗后,用1%的牛血清白蛋白(BSA;Sigma),然后再次广泛清洗。gydF4y2Ba
伤口愈合试验gydF4y2Ba
使用了两种上皮细胞类型。稳定的DDR1a-、b-和kd过表达,以及对照的BEAS-2B细胞,以及暴露于DDR1或对照RNAi的BEAS-2B细胞,在DMEM/FBS中以每孔1ml的密度在24孔板中播种(康宁,阿廷顿,英国)。4小时后,用BEBM交换培养基使细胞血清饿死24小时。HBECs以60%的汇合度播种,然后培养到24孔板中汇合,每48小时交换一孔BEGM 2 mL。汇合时转染HBECs,并在BEWM中孵育48小时。在24孔板的每孔平行产生两个划痕[gydF4y2Ba3.gydF4y2Ba].使用Insight QE数码相机和软件(Image Solutions, Preston, UK)连接到尼康Diaphot 300显微镜(尼康仪器公司,Melville, NY, USA),使用2.5× NA 0.08蔡司镜头或4.0× NA 0.075蔡司镜头(Carl Zeiss Ltd., Welwyn Garden City, UK),在每个创口的固定点拍摄照片。HBECs在8小时或BEAS-2B细胞在24小时获得进一步图像。使用Spot软件(4.6版;图像解决方案)。gydF4y2Ba
明胶zymographygydF4y2Ba
损伤实验的上清液与等体积的2× Novex样品缓冲液(Invitrogen)结合,采用Invitrogen Novex系统通过10%明胶凝胶(Invitrogen)电泳分离。凝胶电泳后暴露在Novex复生缓冲液中,然后在37°C下过夜。以重组MMP-2作为阳性对照。凝胶用考马斯蓝(VWR International, Lutterworth, UK)染色,溶解在40%甲醇,10%醋酸的蒸馏水中,使用不含考马斯蓝的相同溶液洗涤和染色。图像采集使用连接到GeneGenius图像采集系统(Synoptics, Cambridge, UK)的SynGene GeneSnap v7.04g。使用ImageJ 1.39计算MMP带的相对大小(美国国立卫生研究院,Bethesda, MD, USA;gydF4y2Bahttp://rsb.info.nih.gov/ij/gydF4y2Ba).选择每个凝胶上最大的条带作为感兴趣区域的参考尺寸。然后将相同大小的感兴趣区域连续应用于频带,并确定平均密度。通过测定明胶凝胶中已知浓度的MMP-2标准物的密度,并确认密度与MMP-2浓度之间的线性关系(数据未显示),证实了该方法的有效性。gydF4y2Ba
MMP-7 ELISAgydF4y2Ba
采用ELISA法测定MMP-7 (MMP-7最低检测浓度0.016 ng·mL)gydF4y2Ba−1gydF4y2Ba)根据制造商的说明(研发系统,阿宾顿,英国)。在使用Vivaspin 500色谱柱(科学实验室供应,诺丁汉,英国)分析之前,将损伤实验的上清液浓缩5倍。gydF4y2Ba
手机号gydF4y2Ba
等量的细胞被播种到12孔板(康宁)。对于BEAS-2B细胞,这些细胞要么是i型胶原蛋白涂层,要么是bsa涂层。将BEAS-2B细胞暴露在RNAi转染复合物中48小时,然后以等密度播种。4小时后,将培养基交换为进一步的BEWM,细胞孵育过夜,然后用4%的多聚甲醛固定。在每个孔中等量播种HBECs,以20%的汇合量转染。4小时后交换培养基。48小时后再次交换培养基。24 h后固定细胞,10 μg·mL孵育核染色gydF4y2Ba−1gydF4y2Ba4 ',6-二氨基氨基-2-苯基吲哚(Sigma)在PBS中室温放置30分钟。荧光图像由4×蔡司镜头连接到尼康Diaphot 300显微镜,使用Spot 4.7软件和Slider RT3相机(Image Solutions)获得。用ImageJ 1.41计数细胞核。通过计算细胞悬液的连续稀释倍数(数据未显示),证实了这种方法的准确性。gydF4y2Ba
胸腺嘧啶核苷掺入gydF4y2Ba
等量的细胞被播种到48孔板(康宁)。对于BEAS-2B细胞,这些细胞要么是i型胶原蛋白涂层,要么是bsa涂层。将过表达DDR1或空载体对照的BEAS-2B细胞接种于DMEM/FBS中,一旦粘附后进行血清饥饿24 h。在HBECs中,以等密度播种细胞,暴露于转染复合物4小时,然后在BEWM中孵育过夜。10 ng·毫升gydF4y2Ba−1gydF4y2Ba加入EGF,孵育8 h后,以1 μCi (37 kBq /孔)的活性加入氚化胸苷。在进一步的16小时后,细胞暴露于10%三氯乙酸(Sigma)在4℃下30分钟,DNA通过0.2 M NaOH (Sigma)在4℃下孵卵过夜沉淀。在每瓶加入10ml闪烁液后,在Wallac闪烁计数器(PerkinElmer, Waltham, MA, USA)上评估崩裂数量。gydF4y2Ba
附着力试验gydF4y2Ba
HBECs暴露于RNAi转染复合物后孵育48小时。使用包含预包被ECM底物(vitronectin,纤连蛋白,层粘连蛋白,I型胶原蛋白,IV型胶原蛋白和白蛋白对照)的Chemicon cytomatrix粘连检测试剂盒评估粘连性;Fisher Scientific, Loughborough,英国)。处理后,收集细胞,在各种细胞基质因子上孵育2小时,37°C, 5% COgydF4y2Ba2gydF4y2Ba附着力根据制造商的说明定量。gydF4y2Ba
细胞凋亡gydF4y2Ba
HBECs以等密度播种到8个井的载玻片中。播种24小时后,将细胞暴露于RNAi转染复合物中并孵育48小时。然后用3.7%多聚甲醛固定HBECs,用含有0.1% Triton X-100和0.1%柠檬酸钠(均为Sigma)的PBS渗透,然后用荧光素孵育gydF4y2Ba原位gydF4y2Ba细胞死亡检测试剂盒(罗氏),根据制造商的说明。使用ImageJ 1.41获取荧光图像,并对荧光细胞进行计数。gydF4y2Ba
重要染料排除gydF4y2Ba
细胞转染后进行凋亡检测。用0.02%台盼蓝在PBS中室温孵育5分钟。按上述方法获取Brightfield图像,使用ImageJ 1.41计数细胞。gydF4y2Ba
DDR1表达:免疫组化gydF4y2Ba
采用纤维支气管镜进行支气管活检。招募稳定期哮喘患者。对照组患者没有哮喘,正在接受支气管镜检查,以检查其他适应症,包括可能的肺癌和咯血。这些患者的肺活量正常,组织学上气道正常。该研究得到了诺丁汉研究伦理委员会(Nottingham, UK)的批准,并获得了所有患者的知情同意。支气管活检取自第一个或第二个隆突。染色标本在4%多聚甲醛中固定,蜡包埋,切割并安装。玻片在切片机(RA Lamb Ltd, Eastbourne, UK)中脱蜡,并通过乙醇系列再水化。切片用1%伊红(努斯坦,诺丁汉,英国)和苏木精(西格玛)染色,或根据制造商的说明使用vecastain ABC试剂盒(矢量实验室,彼得伯勒,英国)进行免疫染色。简单地说,切片在10 mM柠檬酸缓冲液中煮沸20分钟,过氧化物酶活性被阻断,用抗ddr1 C20抗体(Santa Cruz)和根据制造商说明书应用的二抗孵育过夜。 Diaminobenzidine was then applied using the Vectastain DAB kit (Vector Laboratories). Nuclear counterstaining was achieved using haematoxylin. Slides were then dehydrated through a reverse ethanol series and mounted using Vectamount (Vector laboratories).
统计分析gydF4y2Ba
观察结果采用非配对t检验或单因素方差分析进行比较。采用Bonferroni后验进行组间分析。数据以均数±表示gydF4y2Ba扫描电镜gydF4y2Ban≥3。gydF4y2Ba
结果gydF4y2Ba
DDR1在培养的上皮细胞中表达gydF4y2Ba
为了证实DDR1在HBECs和BEAS-2B细胞中都有表达,我们对BEAS-2B细胞和HBECs的细胞裂解液进行了Western blotting (gydF4y2Ba图1一个gydF4y2Ba).DDR1在HBECs中表达较强,在BEAS-2B细胞中表达较低。阳性对照是一个已知含有DDR1的细胞裂解物的样本,该细胞裂解物来自W. Vogel(多伦多大学;个人沟通)。gydF4y2Ba
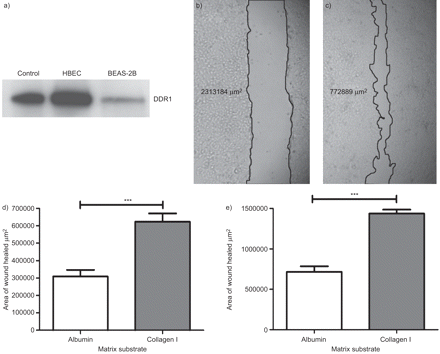
a) Western blot显示盘状蛋白结构域受体(DDR)1在人支气管上皮细胞(HBECs)和BEAS-2B细胞中的表达。b) 0和c) 24小时时,BEAS-2B细胞中具有代表性的划痕。d) 8小时时HBEC单层膜和e) 24小时时BEAS-2B单层膜中I型胶原蛋白增强划痕修复面积。数据以平均值±表示gydF4y2Ba扫描电镜gydF4y2Ba.n≥3。* * *: p < 0.001。gydF4y2Ba
I型胶原蛋白促进上皮修复gydF4y2Ba
为了研究临时基质的主要成分I型胶原在上皮修复中的作用,我们比较了I型胶原在划伤模型中的上皮修复作用gydF4y2Ba与gydF4y2Ba白蛋白包衣组织培养塑料[gydF4y2Ba31gydF4y2Ba].细胞被播种到接近汇合点,然后一夜之间缺乏生长因子,这样细胞产生的其他ECM因子就可以最小化。在初步实验中,我们发现HBECs的伤口愈合明显快于BEAS-2B细胞,8小时和24小时后伤口愈合率分别为50%。因此,这些时间点被用于这些细胞类型的进一步实验(gydF4y2Ba图1b和cgydF4y2Ba).在24小时的BEAS-2B细胞单层中,I型胶原蛋白比白蛋白对照组增加了伤口愈合面积(2.0倍增强,95% CI 1.58-2.57;p<0.001)和8小时HBECs(2.0倍增强,95% CI 1.41-3.36;p < 0.001) (gydF4y2Ba图1d和egydF4y2Ba).gydF4y2Ba
DDR1在上皮修复中的作用是什么?gydF4y2Ba
I型胶原蛋白是DDR1和DDR1的同源配体gydF4y2Ba-/-gydF4y2Ba小鼠的平滑肌细胞已被证明对I型胶原蛋白的附着和迁移受损[gydF4y2Ba32gydF4y2Ba],我们假设所观察到的胶原蛋白对上皮修复的影响是由DDR1介导的。我们首先利用RNAi技术研究了DDR1敲除对HBECs和BEAS-2B细胞上皮修复的影响。在最初的实验中,我们通过Western blotting显示,在转染后48小时,与Ambion Control Number 1 (Ambion, Warrington, UK) siRNA相比,DDR1 siRNA导致HBECs中DDR1蛋白减少89%,BEAS-2B细胞中减少53%。gydF4y2Ba图2a和bgydF4y2Ba).为了检验siRNA的选择性,我们还测量了上皮细胞中DDR转录本的水平(gydF4y2Ba图2c和dgydF4y2Ba).在HBECs中,RNAi使DDR1转录物减少了74%,而DDR2 mRNA表达水平较低(比DDR1低300倍),尽管DDR1 siRNA使其略有减少,但影响不显著。与对照siRNA相比,DDR1敲除导致BEAS-2B细胞24小时伤口愈合面积减少46% (95% CI 13-79%;p = 0.01), 8小时后HBECs伤口愈合面积减少44% (95% CI 16-72%;P = 0.006) (gydF4y2Ba图2e和fgydF4y2Ba).gydF4y2Ba
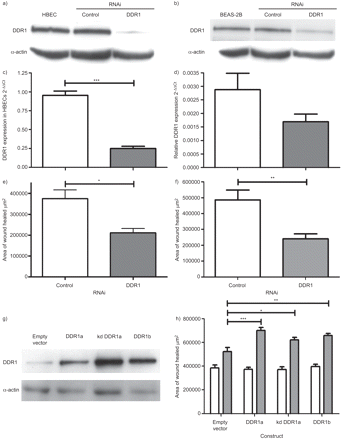
转染48 h后,在a)人支气管上皮细胞(HBECs)和b) BEAS-2B细胞中通过Western blotting证实disdisidin结构域受体(DDR)1蛋白下调。c)转染48 h后,定量RT-PCR也证实了HBECs中DDR1转录本的下调。d)对DDR2转录水平无显著影响。与对照RNA干扰(RNAi)相比,DDR1敲除导致I型胶原底物上的HBEC单层和f) BEAS-2B细胞单层的伤口修复受到抑制。g) Western blotting证实DDR1过表达。h)所有DDR1异构体的过表达,包括激酶死亡(kd) DDR1,导致I型胶原底物的伤口修复增强。数据以均数±表示gydF4y2Ba扫描电镜gydF4y2Ba.n≥3。*: p < 0.05;* *: p < 0.01;* * *: p < 0.001。gydF4y2Ba
由于敲低DDR1会减少上皮修复,我们继续研究过表达DDR1对上皮修复的影响,以及这种影响在DDR1亚型之间是否不同。此外,我们评估了通过DDR1磷酸化的信号通路对上皮修复的贡献。我们使用过表达DDR1、DDR1a和DDR1b两种主要异构体的BEAS-2B细胞。使用kd版本的DDR1a(在激酶结构域中有一个单氨基酸取代K618A)来检测修复过程是否依赖于激活后DDR1的磷酸化。Western blotting证实三种DDR1亚型均过表达(gydF4y2Ba图2 ggydF4y2Ba).在这些白蛋白底物实验中,空载体对照细胞和过表达DDR1a、kd DDR1a或DDR1b的细胞在伤口愈合方面没有显著差异。然而,在I型胶原底物上,BEAS-2B细胞中DDR1a、kd DDR1a和DDR1b的过表达都与伤口愈合的增强有关(gydF4y2Ba图2 hgydF4y2Ba).对于DDR1a,与空病媒对照相比增强了1.34倍(95% CI 1.17-1.52;p<0.001), kd DDR1a为1.19倍(95% CI 1.01-1.36;p<0.05), DDR1b为1.26倍(95% CI 1.09-1.44;p < 0.01)。gydF4y2Ba
DDR1的下调与HBECs增殖减少有关,但对粘附无影响gydF4y2Ba
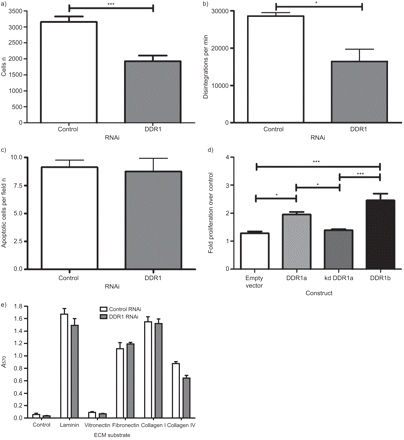
为了确定上皮修复的哪个方面受到DDR1的影响,我们继续研究了DDR1敲低对HBEC增殖和粘附的影响。根据我们的初步发现,为了给DDR1的翻转留下时间,与之前的实验一样,我们测量了DDR1敲除48小时后HBECs中I型胶原暴露48小时所诱导的细胞数量的增加。我们在BEWM中培养细胞,通过细胞计数,与对照RNAi相比,在48小时内细胞数量减少了30% (gydF4y2Ba图3gydF4y2Ba)及以胸腺嘧啶掺入(gydF4y2Ba图3 bgydF4y2Ba).DDR1之前已被证明影响p53的水平,p53是细胞凋亡的重要调节因子[gydF4y2Ba33gydF4y2Ba].为了确认所看到的影响不是由于DDR1 siRNA降低细胞活力,在平行实验中,我们证实,尽管DDR1 siRNA降低了细胞增殖,但这不是由于细胞死亡,因为TUNEL(末端脱氧核苷酸转移酶尿苷三磷酸划痕末端标记)试验证实,发生凋亡的细胞数量在DDR1 siRNA和对照siRNA之间没有差异(gydF4y2Ba图3 cgydF4y2Ba).在使用台锥蓝排除法测定细胞活力的平行实验中观察到类似的结果(数据未显示)。在BEAS-2B细胞中,与空载体对照相比,活性DDR1的存在增强了增殖,但kd DDR1没有增强(gydF4y2Ba图3 dgydF4y2Ba).DDR1a过表达增强增殖1.6倍(95% CI 1.1 ~ 2.3倍;p<0.05), DDR1b过表达可使细胞增殖增强2.2倍(95% CI 1.6 ~ 2.7倍;p < 0.001)。gydF4y2Ba
disdisidin结构域受体(DDR)1的敲除导致人支气管上皮细胞(HBECs)增殖减少,通过a)细胞计数和b)胸腺嘧啶掺入,但c)不促进凋亡(TUNEL试验)。d)胸腺嘧啶掺入后,活性DDR1过表达可促进BEAS-2B细胞增殖,但激酶死亡(kd) DDR1过表达无影响。e) DDR1敲除对HBECs与细胞外基质(ECM)蛋白的粘附无影响。RNAi: RNA干扰。数据以均数±表示gydF4y2Ba扫描电镜gydF4y2Ba.n≥3。*: p < 0.05;* * *: p < 0.001。gydF4y2Ba
为了检验DDR1对细胞粘附的作用,在敲除DDR1 48小时后收集细胞,并将等量的细胞播种到涂有ECM因子的条带上。临时基质和基底膜组分(层粘连蛋白、纤维连接蛋白、胶原I和IV)的粘附明显高于vitronectin或对照(gydF4y2Ba图3 egydF4y2Ba).粘附力不受DDR1 siRNA在任何ECM底物上的影响。gydF4y2Ba
MMP的表达gydF4y2Ba
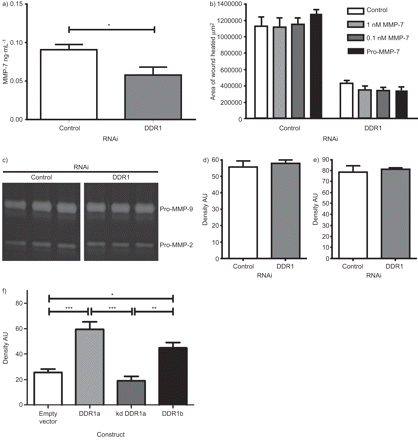
基质金属蛋白酶参与支气管上皮的修复。由于MMP-7由HBECs组成性表达,是气道上皮修复的必要效应物[gydF4y2Ba34gydF4y2Ba],我们验证了MMP表达与DDR1信号通路相关的假设。我们收集DDR1 siRNA上清,并在I型胶原底物上伤24小时后转染对照HBECs,用ELISA法检测MMP-7蛋白,用明胶酶谱法检测mmp -2和MMP-9的活性和活性。在HBECs中,DDR1消耗与MMP-7蛋白减少50%相关,类似于伤口愈合的减少(gydF4y2Ba图4gydF4y2Ba).为了确定DDR1对上皮修复的影响是否仅通过MMP-7介导,我们在DDR1 siRNA存在下进行了损伤实验,并添加了重组MMP-7;将pro-MMP-7添加到1 nM,或将氨基苯乙酸汞激活的MMP-7添加到0.1 nM或1 nM。DDR1敲除后,添加MMP-7不能恢复上皮修复(gydF4y2Ba图4 bgydF4y2Ba).当MMP-7浓度高于上述水平时,会导致上皮脱离(数据未显示)。HBECs中的Pro-MMP-2和pro-MMP-9水平不受DDR1敲低的影响(gydF4y2Ba图4汉英gydF4y2Ba).接下来,我们研究了DDR1过表达对I型胶原底物BEAS-2B细胞中MMP表达的影响:尽管BEAS-2B细胞不产生MMP-7(数据未显示),但我们通过酶谱观察到,DDR1a过表达导致MMP-2蛋白增加2.3倍(95% CI 1.6-3.0;p<0.001), DDR1b过表达导致MMP-2蛋白升高1.8倍(95% CI 1.1-2.4;p < 0.05)。但过表达kd DDR1对MMP-2蛋白表达无影响(0.74倍变化,95% CI 0.054-1.4) (gydF4y2Ba图4 fgydF4y2Ba).gydF4y2Ba
a)人支气管上皮细胞(HBECs)中盘状蛋白结构域受体(DDR)1的下调导致基质金属蛋白酶(MMP)-7水平降低。b)替换MMP-7,无论是氨基苯乙酸汞激活的还是pro-MMP-7,都不能恢复DDR1敲除后的伤口修复。HBECs中DDR1敲除后c, d) MMP-2和c, e) MMP-9水平无变化。f)在BEAS-2B细胞中,过表达DDR1a和DDR1b会增加MMP-2的表达,而激酶死亡(kd) DDR1a则不会。RNAi: RNA干扰。数据以均数±表示gydF4y2Ba扫描电镜gydF4y2Ba.n≥3。*: p < 0.05;* *: p < 0.01;* * *: p < 0.001。gydF4y2Ba
DDR1在支气管上皮细胞表达gydF4y2Ba
在证明DDR1在培养的原代和转化的HBECs中表达,并有助于上皮修复后,我们接下来测试了正常支气管上皮和哮喘患者中DDR1的表达,哮喘是一种以上皮损伤和修复为特征的疾病。通过纤维支气管镜从9名哮喘患者和6名对照组中获得样本。根据英国胸科学会哮喘指南,1例哮喘患者在第1步接受治疗,4例在第2步接受治疗,2例在第3步接受治疗,第4步和第5步各1例[gydF4y2Ba35gydF4y2Ba].所有对照组患者均接受支气管镜检查作为另一指征,肺活量测定正常。患者特征见gydF4y2Ba表1gydF4y2Ba.8例哮喘患者和5例对照组标本进行了DDR1免疫染色。组织学上,大部分上皮标本外观正常。5例哮喘患者标本显示基底膜增厚或上皮细胞脱落的特征性特征。对照组和哮喘源性支气管活检的所有上皮细胞均为DDR1强阳性(gydF4y2Ba图5gydF4y2Ba).整个上皮细胞染色均匀。上皮下结构染色极少。用免疫球蛋白G同型对照代替DDR1一抗消除了这种染色。在6名患者(3名哮喘患者和3名对照组患者)中,从活检中传代培养了HBECs。从这些细胞中获得的蛋白裂解物进行了DDR1的Western blotting。所有患者均表达一条与DDR1一致的蛋白带。gydF4y2Ba
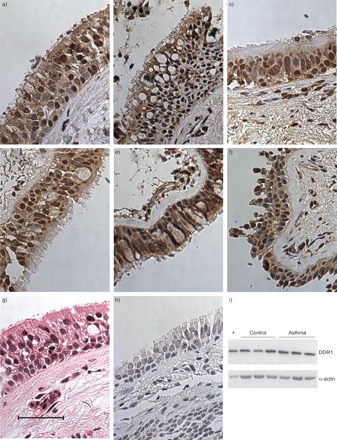
三种代表性的a-c)非哮喘对照组和d-f)哮喘患者的盘状蛋白结构域受体(DDR)1免疫染色。g)苏木精和伊红,h)染色特异性显示同型对照。i)细胞裂解物的Western印迹证实了哮喘患者和对照组上皮细胞中DDR1的表达。+:阳性对照。比例尺= 50 μm。gydF4y2Ba
讨论gydF4y2Ba
我们已经证明DDR1在正常支气管上皮中表达,并通过对细胞增殖和迁移的共同作用参与上皮修复。DDR1是HBECs中MMP-7表达所必需的,这也可能有助于上皮修复。gydF4y2Ba
我们在这里观察到的影响很可能与上皮修复有关gydF4y2Ba在活的有机体内gydF4y2Ba,其中上皮损伤暴露出含有I型胶原蛋白的ECM,导致DDR1的激活。我们和其他人的工作表明,DDR1可能通过多种机制促成这些效应。在NIH3T3小鼠成纤维细胞系中,I型胶原激活DDR1导致DDR1与细胞骨架蛋白非肌肉肌球蛋白重链(NMHC)-IIA在30-60分钟内共定位,这比DDR1的最大磷酸化动力学更快[gydF4y2Ba19gydF4y2Ba].NMHC-IIA随后与肌动蛋白骨架结合。在伤口边缘转染ddr1的NIH3T3细胞比野生型(DDR1-null)细胞迁移更快[gydF4y2Ba36gydF4y2Ba].这与已知DDR1在系膜细胞、血管平滑肌、胶质瘤细胞和白细胞中的前迁移作用密切相关[gydF4y2Ba23gydF4y2Ba,gydF4y2Ba37gydF4y2Ba- - - - - -gydF4y2Ba39gydF4y2Ba].在支气管上皮中,我们的研究表明DDR1增强上皮迁移的机制可能是由于其他ECM受体相互作用的促进而独立于DDR1自磷酸化,因为所有DDR结构都增强了伤口修复,而与磷酸化无关。在NIH3T3细胞中,I型胶原与DDR1二聚体结合导致二聚体在内化之前聚集在细胞表面[gydF4y2Ba40gydF4y2Ba].受体内化比受体磷酸化发生得快得多,这表明DDR1的作用可能存在双重机制:与其他细胞表面受体相互作用,而不依赖于618位的磷酸化,从而促进迁移,而磷酸化则导致对细胞合成功能的影响[gydF4y2Ba26gydF4y2Ba,gydF4y2Ba40gydF4y2Ba,gydF4y2Ba41gydF4y2Ba].gydF4y2Ba
与观察到的DDR1的kd变体废除磷酸化和随后的下游信号一致[gydF4y2Ba26gydF4y2Ba],在我们的过表达模型中,尽管kd突变型DDR1增强了上皮修复,但与野生型DDR1不同,它对MMP-2的产生或细胞增殖没有影响。gydF4y2Ba
基质金属蛋白酶是已知的上皮修复效应物。MMP-7在HBECs中组成型表达,在再生肺上皮中上调[gydF4y2Ba7gydF4y2Ba]而敲除小鼠MMP-7可消除上皮修复[gydF4y2Ba6gydF4y2Ba].我们的研究结果表明,MMP-7的降低与DDR1的敲除有关gydF4y2Ba在体外gydF4y2Ba伤害模型。然而,上清液中MMP-7的绝对水平较低,这可能反映了该模型中伤口面积相对较小,参与修复过程的细胞数量较少。生理水平的MMP-7替代并不能恢复上皮修复,这表明DDR1在该模型中对上皮修复的作用可能通过mmp依赖和mmp独立途径起作用。我们提出了DDR1和MMP-7在上皮修复中的互补作用,其中DDR1促进迁移,MMP-7对细胞脱离的作用促进了迁移。A549细胞中活性mmp -7或pro-MMP-7过表达的观察结果支持了这一结论。A549细胞的迁移没有变化,但当活性MMP-7过表达时,更多的细胞分离[gydF4y2Ba42gydF4y2Ba].这与我们观察到的MMP-7替代不能恢复被DDR1敲除抑制的支气管上皮修复是一致的。gydF4y2Ba
DDR1已被证明对维持皮肤和肾脏的正常结构和功能至关重要[gydF4y2Ba21gydF4y2Ba,gydF4y2Ba22gydF4y2Ba],我们认为在肺上皮细胞中也有类似的作用。已有研究表明DDR1与E-cadherin共同定位,并且E-cadherin将DDR1隔离到完整上皮细胞的细胞连接上[gydF4y2Ba43gydF4y2Ba].上皮细胞丢失导致DDR1暴露于ECM成分,随后DDR1激活,细胞迁移,在我们的模型中,MMP-7上调。为了促进细胞脱离,MMP-7可能导致细胞表面E-cadherin的丢失[gydF4y2Ba44gydF4y2Ba],进一步促进DDR1的作用,直到伤口闭合,此时DDR1的激活降低,MMP-7的产生减少,E-cadherin可以将DDR1隔离到细胞-细胞连接处。在我们的研究中,即使在BEAS-2B细胞中酪氨酸激酶不活跃的情况下,DDR1过表达的存在也增强了上皮修复。这可能是由BEAS-2B细胞的细胞表面分子表达谱解释的,BEAS-2B细胞缺乏E-cadherin,允许DDR1与其他细胞表面ECM受体相互作用以促进迁移。对MMP-7的下游信号不需要中断细胞与细胞的相互作用[gydF4y2Ba45gydF4y2Ba].gydF4y2Ba
我们观察到HBECs中DDR1的敲除没有显著影响对各种ECM因子的粘附,这可能反映了其他细胞粘附分子的丰富程度,如整合素,它们加在一起对细胞粘附的影响可能比DDR1更大。与这一观点一致的是,先前在NIH3T3细胞中发现,10分钟后与I型胶原蛋白的粘附不受DDR1表达的影响[gydF4y2Ba36gydF4y2Ba].gydF4y2Ba
在哮喘和非哮喘对照组的支气管活检中,DDR1均在上皮细胞中强烈表达。这表明DDR1的表达不受哮喘上皮损伤修复过程的影响。然而,DDR1可能仍然通过转导来自上皮下ECM异常沉积的信号在疾病中发挥作用,这是疾病的特征。需要进一步的研究来解决这一点。gydF4y2Ba
综上所述,我们已经证明DDR1调节支气管上皮的修复、增殖和MMPs的表达。这些发现值得进一步研究上皮细胞被破坏的疾病,包括特发性肺纤维化和急性肺损伤,特别是考虑到已知DDR1在特发性肺纤维化中的上调。gydF4y2Ba
脚注gydF4y2Ba
支持声明gydF4y2Ba
诺丁汉大学和诺丁汉呼吸生物医学研究所(诺丁汉,英国)在项目期间支持了研究人员。gydF4y2Ba
权益声明书gydF4y2Ba
没有宣布。gydF4y2Ba
- 收到了gydF4y2Ba2010年3月12日。gydF4y2Ba
- 接受gydF4y2Ba2010年9月15日。gydF4y2Ba
- ©2011人队gydF4y2Ba
参考文献gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba