抽象的
气道平滑肌细胞产生细胞外基质蛋白,这又可以促进平滑的肌肉存活,增殖和迁移。目前可用的疗法对气道平滑肌肉矩阵产生和迁移几乎没有影响。据报道过氧化物酶体增殖剂活化受体(PPAR)配体在各种细胞系中降低迁移和基质产生。在这项研究中,我们研究了PPAR配体对人气道平滑肌(HASM)矩阵生产和迁移的影响。
通过RT-PCR和Western印迹检查PAMP表达。通过用PPAR反应元素 - 荧光素酶报告质粒转染细胞来检查内源性PPAR活性。
我们观察到HASM细胞表达PPARα,β和γ。通过用泛激动剂刺激细胞来观察六倍诱导荧光素酶活性,表明内源性PPAR活性。PPAR配体二奈酮,15-脱氧-δ12,14-前列腺素J2而WY-14643则减少了向血小板衍生生长因子受体的迁移。这不是通过抑制Akt磷酸化或促进PTEN活性介导的,而是部分通过环氧合酶-2诱导和前列腺素E介导的2生产在细胞中增加循环AMP水平。所有三种配体也通过培养的平滑肌细胞引起抑制胶原和纤连蛋白分泌。
我们得出结论,PPAR配体减少了HASM迁移和基质生产,因此可能对调制气道重塑有用。
严重哮喘患者气道墙的两个显着特征是平滑肌细胞和细胞外基质(ECM)组分的增加量[1].增加的平滑肌质量更可能是由于细胞的数量增加(增生)(肥大)[2那3.].改造的气道中平滑肌肉积聚的机制之一可以通过从粘膜下的深层平滑肌束中迁移[4.那5.],这反过来又由ECM蛋白质如胶原蛋白和纤维蛋白(纤维蛋白)部分调节[6.].这两个结构变化都有助于哮喘中的气流限制[7.],目前可用的哮喘药物没有有效逆转。因此,识别将抑制平滑肌迁移和矩阵生产的机制或策略是有吸引力的。
过氧化物体增殖物激活的受体(PPAR)是属于类固醇受体超家族的激素受体系列[8.].据报道,PPARα和γ同种型在气道平滑肌细胞上表达[9.那10.]并且它们通过配体的活化,例如噻唑烷二酮罗格列唑酮具有优于皮质类固醇的抗炎性质[11.].PPAR配体可以减少人类血管平滑肌迁移[12.]肾间隙细胞的基质生产[13.].提出的机制包括:直接转录激活或抑制靶基因[14.];其他信号依赖性转录因子的拮抗作用,如核因子-κB,活化剂蛋白-1或Caat / Enhancer结合蛋白;涉及磷酸阳性3-激酶(PI3K),SRC或丝裂原激活蛋白激酶的信号传导途径的激活[15.];通过调节环氧化酶(COX)的激活和增加细胞内循环AMP (cAMP)抑制信号,如PTEN(磷酸酶和紧张素同源物)[16.];或通过降低或中断转化生长因子(TGF)-β1水平[17.]或发信号通知[18.].已经证明了其他核激素受体,例如肝X受体的核激素受体,以降低人类气道平滑肌(HASM)迁移到趋化刺激[19.那20.].
在这项研究中,我们研究了:对HASM细胞的PPAR同种型的表达;它们的配体对平滑肌迁移的影响,以及胶原蛋白和纤连蛋白的生产;和这些效果的一些机制。具体而言,我们研究了AKT,SRC,PTEN和COX信令的作用,为我们探索的现象提供了一些解释。我们使用了四个不同的激动剂(WY-14643,用于PPARα,GW501516的PPARβ,并为PPARβ和roglitazone和15-脱氧-δ12,14-前列腺素J.2(15d-pgj2对于PPARγ)和三个拮抗剂(MK866对抗PPARα,舒林酸对抗PPARβ和GW9662的抗PPARγ),以研究特定PPAR同种型的作用。类似于其他核激素受体配体的PPAR配体抑制挥发族细胞对血小板衍生的生长因子(PDGF)的迁移,并抑制来自HASM细胞的胶原蛋白分泌。
方法
气道平滑肌培养
在St Joseph 's Healthcare (Hamilton, ON, Canada)从16名患者(表格1以他们的知情同意和医院研究道德委员会批准正在进行肺癌手术。从人支气管的无宏观无病区分离平滑肌组织。如前所述,哈姆细胞生长为汇合[4.那6.].细胞在两次和五次之间传代并用于实验。
检测PPAR转录物
根据制造商的说明(Qiagen,多伦多,加拿大,加拿大),使用Quantite逆转录分离出总RNA,1μg逆转录逆转录。然后使用应用的生物系统7900HT机器(应用生物系统,Carlsbad,USA)中的基因特异性引物扩增PPAR同种型。简而言之,反应含有12.5μLSYBRGreen PCR Supermix(Invitrogen,Burlington,Canada),10.5μLH2O、1 μL引物集(各10 μM)和1 μL cDNA。PCR扩增28个循环,参数如下:95℃变性15 min;95°C 30 s 30个循环;产品在2%琼脂糖凝胶上分离,用SYBR Green染色,并用Typhoon 9200可变模式成像仪(Amersham Biosciences, Baie D’urfe, QC, Canada)成像。
引物序列如下(均为5′-3′)。PPARα:正向引物,AGCCTAAGGAAACCGTTCTG;反向引物ACGATCTCCACAGCAAATGA。PPARβ/δ:正向引物,TCACACAACGCTATCCGTTT;反向引物,GGCATTGTAGATGTGCTTGG。PPARγ:正向引物ACCAGCTGAATCCAGAGTCC;反向引物,CGAATGGTGATTTGTCTGTTG。
PPAR转染和报告基因测定
根据制造商的指示,在六孔菜肴中用0.4μg的PPAR反应元素(PPRE) - 葡聚糖酶报告总基因转染哈姆细胞。使用效果(QIAGEN)。简而言之,每孔,0.4μg的ppre-luciferase报道酶质粒,其含有来自酰基 - 辅酶氧化酶的三个螯合酶的副拷贝,在室温下孵育5分钟,用95μl增强剂试剂和3.2μl增强剂在室温下温育5分钟。然后加入10μL的效果另外10分钟,然后加入10%胎儿牛血清(FBS)的600μLRPMI培养基并孵育过夜。转染后,将细胞在Dulbecco改性鹰培养基中孵育过夜,缺乏补充有10%的炭剥离的FBS的酚红色,1%L.-Glutamine和1%青霉素/链霉素,具有1μmPan激动剂(Full 2;从J. Berger,Merck FroSST,Montreal,QC,Canada获得)单独或与PPARα拮抗剂(MK866,10μm),PPARβ/δ组合使用拮抗剂(舒林酰基,10μm),PPARγ拮抗剂(GW9662,10μm)或全部三个另外的48小时(在24小时后加入新鲜配体)。控制细胞接受了等同量的载体。如前所述测定荧光素酶活性[19.].
迁移试验
迁移实验使用6.5 mm Transwell培养板进行,该培养板上有8.0 μm孔隙,i型胶原蛋白涂层聚碳酸酯膜分隔内外腔(Fisher Scientific Limited, Nepean, ON, Canada),如前所述[4.那6.].使用来自六种不同的肺标本的组织的组织重复进行测定。通过添加PDGF-BB(20ng·mL)研究迁移-1;Invitrogen)到外部井。通过用各种浓度处理细胞(0.1-100ng·mL来研究PPAR配体的影响(0.1-100ng·mL-1), 30 min后加入PDGF。用MTT法检测不同激动剂处理的细胞的活力,确认不同条件下的细胞数量为未处理对照的93%到151%。
埃莉莎
胶原蛋白和纤连蛋白
HASM细胞在104.96孔板中的每孔细胞。在4天后,它们在RPMI中为48小时生长,然后用0.3%牛血清白蛋白(BSA),然后用各种浓度的PPAR配体处理48小时。通过将0.02M氢氧化铵在室温下孵育5分钟,从平板收获ECM。将板储存在-70℃直至进行测定。纤维蛋白(1:5,000稀释; BD Biosciences,Oakville,On,Canda)和胶原(1:2,000稀释,西格玛,奥克维尔,加拿大,加拿大),然后与二抗孵育(山羊抗小鼠)在200μL阻断缓冲液中。用100μl开发的颜色P.- 硝基苯基溶液(Sigma)和吸光度在405nm处读取。
前列腺素E2
前列腺素(pg)e2根据制造商的指示(测定设计,ANN ARBOR,MI,USA),通过敏感酶免疫测定测量平滑肌培养上清液的水平。PGE检测限2是13.4 pg·ml-1.
循环amp.
H一种S.mcells were grown to confluence, growth-arrested for 24 h, treated with the various agonists for the same duration as the migration assay (5 h) and cAMP was assayed in the supernatant using a sensitive immunoassay according to the manufacturer’s instruction (R&D Systems Inc, Minneapolis, MN, USA).
Western Blotting.
HASM细胞在6孔板中培养,并生长至约90%的汇合。然后在RPMI中用0.2% BSA使细胞饥饿24小时。然后用PPAR激动剂预处理1小时,然后用PDGF (20 ng·mL)处理细胞-1)对于指示的时间。然后在0.1%Triton X-100洗涤剂中裂解细胞含有蛋白酶和磷酸酶抑制剂,并通过十二烷基硫酸钠 - 聚丙烯酰胺凝胶电泳分离提取物(20μg),并呈涂氮纤维素。在Tris缓冲的盐水 - Tween-20(TBS-T)中封闭膜,含有5%的奶粉1小时,并首先用磷酸血糖416(1:1,000)的抗体探测,PPTEN(1:1,000)(Cell Signaling,Danvers,Ma,USA),或Cox-1和-2(1:2,000)(Millipore,Billerica,MA,美国)在TBS-T中的5%BSA中过夜,然后进行二次抗兔抗体(1:2,000)(抗山羊,1:2,000用于COX-2),在5%乳TBS-T中为1小时。广泛洗涤膜,用标准化学发光试剂盒(Amersham Canada,Oakville,Canada)检测蛋白质。然后将印迹剥离在低pH甘氨酸溶液中并重新探测总Src(1:1,000)或总Akt(1:1,000)抗体(BioSource International,Camarillo,CA,USA)。通过使用抗小鼠多克隆抗体(1:1,000)(R&D Systems)和绵羊抗小鼠二抗(1:2,000)来检测未经处理的HASM细胞上的PPAR同种型。
磷酸酶测定
通过磷酸酶测定还评估PTEN活化。PTEN在免疫沉淀缓冲液中的1μg小鼠抗PTEN(Cell Signaling Technology),蛋白G琼脂糖(Invitrogen)(50mM Tris,pH 7.5; 100mM NaCl; 15mM EGTA; 0.1%Triton X; 0.1%Triton X; 0.1%Triton x-100)。将珠子在4℃下摇动过夜,用100mm Tris(pH8.0)洗涤,在96孔板中重悬于磷酸酶缓冲液(100mM Tris,pH 8.0; 10mM二硫代噻吩醇)中,并与5μLDIC8-磷脂酰肌醇温育-3,4,5-三磷酸盐(梯度Biosciences Inc.,Salt Lake City,US,USA),15μl磷酸酶缓冲液和100μl生物摩尔绿色(Biomol International,Plymouth会议,PA,USA)。在630nm中测量游离磷酸盐。
统计分析
ANOVA使用不同的时间点或实验条件作为受试者内部因素进行统计分析。通过预定义的对比鉴定了显着变化的来源。P <0.05被认为是显着的。所有分析都是使用SPSS版本13.0进行的(社会科学统计包,芝加哥,IL,USA)进行。
结果
PPAR表达和激活
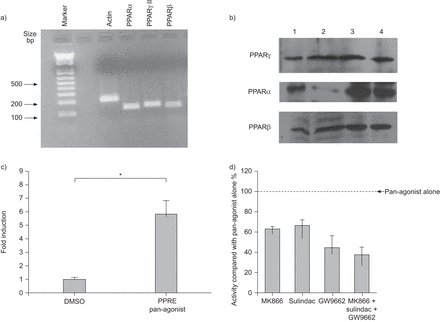
HASM细胞表达PPARα,β和γmRNA(图1一个)和蛋白质(图1 b).通过用泛激动剂刺激细胞来观察六倍诱导荧光素酶活性,表明内源性PPAR活动(无花果。1C).这被三种亚型的特异性抑制剂(无花果。1D).
a)在培养的人气道平滑肌(HASM)细胞上表达过氧化物酶体增殖物激活受体(PPAR)α、γ和β的代表性PCR产物凝胶。b) Western blotting显示四种不同供体的HASM细胞表达PPARα、β和γ。c)转染PPAR反应元件(PPRE) -荧光素酶报告基因的HASM细胞在泛PPAR激动剂刺激下显示内源性PPAR活性(与对照相比,6倍诱导)。DMSO:二甲亚砜。*: p < 0.05。d) PPAR拮抗剂在PPAR泛激动剂存在时抑制PPRE报告基因。用p前荧光素酶报告基因转染HASM细胞,并单独使用泛激动剂(1 μM)或与PPARα拮抗剂(MK866, 10 μM)、PPARβ拮抗剂(sulindac, 10 μM)、PPARγ拮抗剂(GW9662, 10 μM)联合使用。细胞孵育24 h,测定荧光素酶活性。数据以平均值±表示SD.三次实验中,单用泛激动剂的结果为100%。与泛激动剂单独使用相比,三种特异性拮抗剂和三种拮抗剂联合使用均显著降低ppre -荧光素酶基因表达(均p<0.05)。
移民
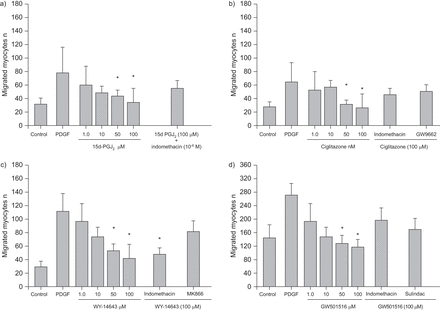
所有四个PPAR配体,西格丽氏酮,15d-PGJ2,WY-14643和GW501516,对PDGF的迁移减少(无花果。2).这些亚型的特异性是由PPAR特异性拮抗剂逆转抑制作用的能力决定的。
人气道平滑肌细胞向血小板源性生长因子(PDGF)的迁移被过氧化物酶体增殖物激活受体(PPAR)激动剂抑制。这种抑制作用被a, b, d)吲哚美辛(对于PPARγ和β激动剂)和特定的PPAR亚型拮抗剂所消除:d) GW9662对于PPARγ, c) MK866对于PPARα, d) sulindac对于PPARβ。数据以平均值±表示SD.A-C)五或d)四个实验。15d-pgj.2: 15-deoxy -Δ12,14 - 前列腺素j2.*:P <0.05与PDGF相比。
矩阵生产
我们测试的所有三种PPAR配体(西格利酮,15d-PGJ2和WY-14643)通过培养的平滑肌细胞抑制胶原和纤连蛋白产生(无花果。3.).对纤连蛋白的影响仅统计学意义只有15d-pgj2.三种激动剂的三种浓度对胶原蛋白的影响都是显著的。
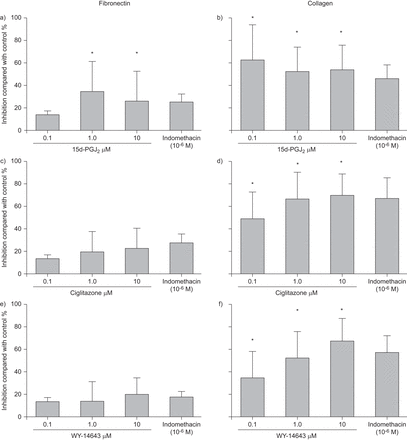
通过人气通道平滑肌细胞的A,C,e)纤维连接蛋白和B,D,F)胶原蛋白合成由过氧化物体增殖物激活的受体激动剂A,B)15-脱氧-δ12,14-前列腺素J2(15d-pgj2), c, d) ciglitazone和e, f) WY-14643。这是不受消炎痛影响的。数据以平均值±表示SD.四个独立实验。*:P <0.05与对照相比。
信令
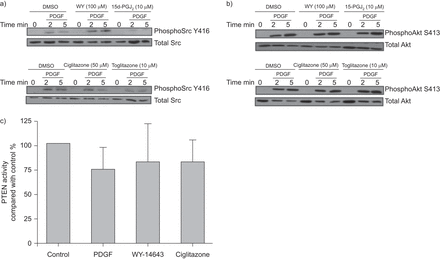
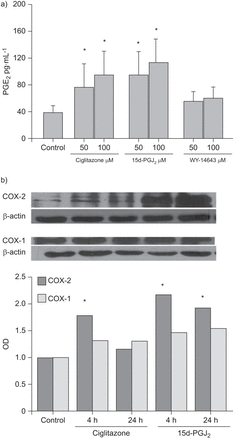
PPAR配体,除了15d-pgj2,不抑制AKT或SRC磷酸化的PDGF诱导的增加(图4and b)或增加PTEN活动(图4摄氏度)在HASM细胞中。15d-pgj.2衰减的SRC磷酸化(图4).在吲哚美辛的存在下,15d-pgj的抑制作用2,令人透露的抗PDGF的平滑肌迁移的西林酮和GW501516。这对WY-14643的抑制作用未观察到这一点(无花果。2).我们还观察到15d-PGJ2和西格丽酮增加了PGE2(无花果。5A)和cAMP水平(数据未显示)(分别为1.6倍和1.2倍)。与此一致的是,在15d-PGJ刺激后4和24小时,我们观察到COX-2的激活,而不是COX-1的激活2和西格丽酮(无花果。5B.).WY-14643没有增加PGE2水平或诱导COX-1或COX-2(数据未显示)。
a)在二甲基亚砜(DMSO)对照、100 μM xy- 14643、10 μM 15- deox-Δ12、14-前列腺素J的存在下,用血小板来源的生长因子(PDGF)处理培养的人气道平滑肌(HASM)细胞后2和5分钟,检测Src总量和磷酸化水平2(15d-pgj2),50μm的二苯基酮和10μmroglitazone。代表性的Western印迹表明,除了15d-pgj之外,过氧化物激素增殖物激活的受体(PPAR)激动剂2,不要在HASM细胞上增加总体或磷酸化的SRC。B)在用DMSO对照存在下用PDGF处理后2和5分钟,在培养的HAMM细胞上检查总和磷酸化的AKT,100μmWY-14643,10μm15d-pgj在PDGF处理后在2和5分钟上检查。2,50μm的二苯哒酮和10μmroglitazone。表现出PPAR激动剂的代表性蛋白质印迹不会增加人类气道平滑肌细胞上的总或磷酸化的AKT激酶。C)使用磷酸酶测定法测定PTEN(磷酸酶和硫脲同源物)活性,并将结果标准化为对照。PDGF之间的PTEN活性差异没有统计学意义(10 ng·ml-1),WY-14643(100μm)和十二醇酮(50μm)。数据以平均值±表示SD.三个独立实验。
a)过氧化物酶体增殖物激活受体(PPAR)激动剂ciglitazone和15-deoxy-Δ12,14-前列腺素J2(15d-pgj2),而WY-14643则无此作用2通过人气道平滑肌细胞合成(通过酶免疫测定法测量)。b)PPAR激动剂Ciglitazone和15d-PGJ2在刺激后4和24小时诱导COX -2,而不是COX-1的表达。数据以平均值±表示SD.a)三或b)六个独立实验。OD:光学密度。*:P <0.05与对照相比。
讨论
我们确认了对HASM细胞的PAMP表达的先前观察,我们报告了三种新颖的观察结果。首先,PPAR激动剂减少气道平滑肌趋于PDGF。其次,PPAR激动剂也通过气道平滑肌细胞减少胶原蛋白和纤连蛋白分泌。第三,迁移的抑制似乎部分地通过PGE的分泌部分介导2细胞内营地增加。这些结果表明,PPAR激动剂可能能够扭转慢性严重哮喘患者的气道粘膜清醒中看到的一些结构变化。
我们确认哈姆细胞表达PPARα和γ同种型的前一种观察结果[9.-11.].此外,它们还表达了PPARβ。我们通过证明了mRNA和蛋白质的存在来证实了这一点。目前尚不清楚为什么使用培养的平滑肌细胞使用培养的平滑肌细胞没有证明PPARβ/δ同种型的表达。它可能与使用的抗体的多克隆性质(Santa Cruz生物技术,圣诞老人Cruz,Ca,USA)或表达丧失细胞的晚期通道(我们的实验中的两到五次通道相对在之前的实验中超过6个段落)。ppar是内源性活性的,正如ppre -荧光素酶报告基因试验所表明的那样。它们已知对HASM细胞有有效的抗炎作用。在这里,我们报告了该分子的两个额外的生物学相关效应。类似于在血管组织中的观察[12.[我们证明PPAR配体能够将气道肌细胞迁移降低PDGF。我们检查了相关的信号机制,以了解这种现象。我们没有观察到SRC的抑制(除了15D-PGJ之外2)或PI3K活性或PTEN活性的增加作为潜在机制。然而,我们确实观察到抑制效果是通过吲哚美辛衰减的。PPARγ激动剂也引起了PGE的增加2这与PPARγ激动剂诱导COX的报道一致[16.].因此,PPARγ减少肌肉迁移最可能是由于PGE促进细胞内cAMP的增加2.这与其他药物的观察结果一致,如β-激动剂,增加细胞内cAMP和减少气道[21.]和血管[22.]平滑肌细胞及成纤维细胞迁移[23.].CAMP通过抑制RAC依赖性信号传导途径来调节平滑肌细胞的形态,导致肌动蛋白应激纤维和椎板脱落,局部粘连丧失以及小F-actin环的形成[24.]因此降低细胞迁移的能力。PPARβ可能还通过相同的途径发挥其抑制作用,因为吲哚美辛抑制效果。我们无法解释PPARα激动剂的抑制作用机制。这不太可能是由于我们没有观察到Cox诱导或增加PGE增加的途径2水平。这需要进一步调查。
虽然PPRE尚未在ECM基因上游发现,但有证据表明PPAR可能参与ECM基因的调节,尤其是I型胶原蛋白的调节[25.那26.].我们观察到患有HASM细胞的胶原蛋白和纤连蛋白分泌的小而统计学意义的小,但统计学显着的减少。精确的机制需要进一步调查。与对肌肉迁移的影响不同,这似乎不依赖于细胞内阵列水平,因为观察到的现象不易被吲哚美辛抑制。据报道,PPARγ激动剂可降低Mesangial细胞中的TGF-β表达[13.],由于TGF-β增加气道平滑肌细胞的纤维连接蛋白和胶原分泌[27.],PPAR配体可能会通过HASM细胞降低TGF-β分泌。这需要进一步的探索。
这些观察结果可能具有重要的临床意义。假设慢性结构变化对哮喘病理生理学有害[28.[用噻唑烷酮处理可能会限制或甚至可能逆转目前不适合药理治疗的重塑过程的两种组分。这需要进一步评估临床试验。总之,PPAR配体减少了哈姆族细胞迁移和基质生产,因此可能对调节气道重塑有用。
致谢
我们感谢圣约瑟夫医疗保健(汉密尔顿,加拿大汉密尔顿,加拿大)的胸部外科职业部门的胸部外科,以获得肺标本的合作。
脚注
支持声明
本研究得到了Firestone Institute-Glaxosmithkline研究奖和安大略省胸部社会阻止授予的支持。P. Nair持有加拿大钻轮测量仪的加拿大研究椅子。
感兴趣的语句
- 收到了2009年9月12日。
- 公认2012年4月17日。
- ©2013人队