文摘
微粒(MP)是磷脂囊泡脱落细胞激活或凋亡。Monocyte-derived议员移植肺上皮细胞的促炎介质的合成;此类活动的分子基础是未知的。过氧物酶体proliferator-activated受体(PPAR)已经被证实参与核因子(NF)的调制-κB转录活性和炎症。
我们调查是否upregulation促炎细胞因子的合成的人类肺上皮细胞诱导单核细胞/ macrophage-derived议员包括NF-κB激活和由PPAR-γ调制。
议员是由刺激产生的人类单核细胞/巨噬细胞的钙离子载体A23187。国会议员被孵化与人类肺上皮细胞。NF-κB易位被电泳迁移率改变分析评估。白介素8 (IL)和单核细胞趋化蛋白1 (MCP)综合评估ELISA和rt - pcr。
刺激A549肺泡细胞与单核细胞/ macrophage-derived议员导致增加NF-κB激活和抑制的引发和MCP-1合成pre-incubation与PPAR-γ受体激动剂罗格列酮和15-deoxy-Δ12日,14日-prostaglandin-J2。平行试验正常的人类支气管上皮细胞在很大程度上确认结果。PPAR-γ受体激动剂的影响被特定的拮抗剂逆转,GW9662。
Upregulation合成的促炎介质由人类引起的肺上皮细胞单核细胞/ macrophage-derived议员是由NF-κB通过PPAR-γ依赖途径激活。
微粒子(MP)是磷脂囊泡细胞激活后或在细胞凋亡。议员的大小范围从50 nm 1μm [1]。收集的证据在过去的几年中已经证明议员参与许多生理过程,包括凝血和炎症。因为存在的带负电的外层膜上磷脂MP,这些结构长期以来认为凝血作用,这一过程需要多分子的复合体的装配表面带负电荷磷脂膜。最近,然而,它变得明显,议员也携带其他组件的亲代细胞除了磷脂,大大拓宽他们的潜在影响细胞间介质的光谱(1]。例如,在monocyte-derived议员的组织因素,一个重要的辅助因子的启动凝血(2),增加了他们的角色在凝血和血栓形成(3]。
白细胞的作用——在炎症和内皮细胞衍生MP也进行了广泛的调查。议员公布的刺激多形核白细胞,例如,上调白介素(IL) 6和引发内皮细胞合成的(4),而议员来自淋巴细胞和单核细胞诱导基质金属蛋白酶和细胞因子的合成滑膜成纤维细胞(5]。
我们先前已经表明,刺激人类单核细胞/巨噬细胞钙离子载体,A23187,或与组胺,导致议员脱落,和孵化这些议员肺上皮细胞导致upregulation促炎介质的合成,包括引发和单核细胞趋化蛋白(MCP) 16]。引发是一个有力的化学引诱物,中性粒细胞参与炎症反应的发病机制的典型慢性阻塞性肺疾病(COPD)。引发浓度增加支气管肺泡灌洗fuid慢性阻塞性肺病的患者和与中性粒细胞计数和髓过氧化物酶浓度(7];此外,在第二阶段试验中,引发的单克隆抗体已被证明会降低COPD患者呼吸困难(8]。MCP-1,单核细胞化学引诱物,也被牵连在COPD的发病机制及其浓度可以增加慢性阻塞性肺病患者的痰与“健康”吸烟者和非吸烟者(9]。因此,引发和MCP-1合成诱导的upregulation议员可能导致COPD的发病机制。然而,这个活动的分子基础的议员都不知道。
过氧物酶体proliferator-activated受体(PPAR)属于核激素受体配体依赖性转录因子是总科。三种亚型的PPAR已确定日期:α,β/δ,γ。最初确定的作用,脂质和调节葡萄糖的PPAR最近一直与其他现象的规定,包括炎症(10]。PPAR-γ表示,在其他细胞,肺泡和支气管上皮细胞及其激活促炎介质的差别导致对这些生产,至少部分通过抑制核转录因子(NF) -κB转录活动11,12]。因此,PPAR-γ目前被视为一个潜在的小说在慢性阻塞性肺病治疗目标(13]。
在这里,我们表明,单核细胞的影响/ macrophage-derived议员通过NF-κB肺上皮细胞炎症介导的激活和抑制了PPAR-γ刺激。
材料和方法
试剂和试剂盒
RPMI 1640培养基,火腿F-12媒介、青霉素、链霉素、l谷氨酰胺、胰蛋白酶/ EDTA,胰蛋白酶抑制剂,台盼蓝,牛血清白蛋白,PBS, dimethylthiazolyldiphenyltetrazolium溴化(MTT) Ficoll-Hypaque,右旋糖酐,钙离子载体A23187,胎牛血清(的边后卫),溴化乙锭,琼脂糖,REDTaq基因组DNA聚合酶SuperPaK, DNA梯直接荷载100 bp和anti-cytokeratin peptide-18抗体得到从σ(意大利米兰)。iScript互补脱氧核糖核酸合成装备和智商SYBR绿色supermix取自Bio-Rad(美国大力神,CA)。NucleoSpin RNA二世是来自Machery-Nagel (Duren,德国)。BEGM子弹工具包是来自Cambrex(卡拉瓦乔、BG、意大利)。罗格列酮(Rz) 15-deoxy-Δ12日,14日-prostaglandin-J2(15 dpgj2从开曼群岛)和GW9662 (GW)获得化学(美国安阿伯市MI)。人类引发cytoset,人类MCP-1 cytoset衬底3,3′,5、5′-tetramethylbenzidine得到Biosource国际(贝南、钙、美国)。核提取工具从活跃的主题(比利时)。所有其他的化学物质被从医院药房和获得最好的成绩。
实时PCR引物
人类引发的意识和反义引物MCP-1和hypoxanthine-guanine phosphoribosyltransferase(产生HPRT)获得表达载体(意大利米兰)和下面的序列:
引发意义5′GAATGGGTTTGCTAGAATGTGATA3′和反义5′CAGACTAGGGTTGCCAGATTTAAC3′;MCP-1感觉5′CATTGTGGCCAAGGAGATCTG3′和反义5′CTTCGGAGTTTGGGTTTGCTT3′;和产生HPRT 5′AGACTTTGCTTTCCTTGGTCAGG3′和反义5′GTCTGGCTTATATCCAACACTTCG3′。
细胞培养
人类肺泡上皮细胞A549, (ccl - 195美国类型文化收藏,马纳萨斯,弗吉尼亚州,美国),请提供了r . Danesi比萨、意大利比萨大学。A549细胞保持在RPMI补充10%(体积/体积)的边后卫,100 U·毫升−1青霉素,μg·100毫升−1链霉素的湿润空气95%和5%的公司2气氛在37°C。支气管上皮细胞中被永久地传颂,BEAS-2B(美式文化收藏、crl - 9609),被美国Carnevali友情提供,摩德纳大学意大利摩德纳。BEAS-2B细胞RPMI 1640年保持在50%和50% BEGM有限公司在空气湿润95%和5%2气氛在37°C。
人类支气管上皮细胞(HBEC)获得受试者接受诊断支气管镜检查(如前所述)。短暂,在病人的知情同意过程受到,fibreoptic支气管镜是定位在船底座的水平和/或第二或三阶的水平支气管分支。局部麻醉药的使用是保持尽可能低减少对细胞活力的影响。四到六刷牙非常正常的支气管粘膜经常。细胞被删除从刷涡流火腿的F-12介质- 10%的边后卫。细胞被带到实验室在冰和孵化DNase (50 mg·毫升−1)来消除凝结。与冰冷的,洗后无血清火腿F-12介质,这些细胞被resuspended BEGM和镀Vitrogen 100 -涂布培养瓶(圣克鲁斯生物技术、圣克鲁斯、钙、美国)。间接免疫荧光法与anti-cytokeratin抗体确认的上皮起源细胞(14]。中使用特定的实验报告是来自外围肺癌患者进行诊断支气管镜检查和收获从侧主支气管。这些细胞被用于段落三到四个。
单核细胞隔离和议员的一代
单核细胞分离从新鲜的淡黄色的外套从当地获得血液银行或外周血的正常志愿者所描述。简单地说,一个全新的巴菲是1:1稀释涂PBS-EDTA(2毫米),轻轻混合0.25体积的2%右旋糖酐T500和红细胞沉降了30分钟。的leukocyte-rich上层的恢复和离心10分钟200×g。颗粒是resuspended PBS-EDTA 30 mL,分层超过15毫升Ficoll-Hypaque和离心机的30分钟350×g 4°C。单核细胞种类环在PBS-EDTA恢复和洗两次。单核细胞被resuspended RPMI / 10%的边后卫和允许坚持18 h在24-well板(10 37°C6细胞·好−1)。贴壁细胞被洗了三次用无血清培养系统预热RPMI。议员代,A23187(12μM)添加;10分钟后在37°C,上层的恢复,通过在14000×g离心5分钟在室温下去除死细胞和细胞碎片可能分离在刺激和立即用于进一步的实验。在选定的实验中,议员由超速离心法进行进一步纯化(100000 g×2小时);颗粒在RPMI resuspended使用相同的体积与原始材料。在平行实验,细胞治疗被胰蛋白酶/ EDTA分离,所述放在幻灯片使用cytocentrifuge和Diff-Quick染色。通常,∼75 - 80%细胞单核细胞/巨噬细胞,主要污染物是淋巴细胞。
生存能力测试
不同治疗方法的效果在细胞MTT比色是可行性分析。细胞被镀在2.5×103细胞·好−1150年μL完全培养基在96 - microtitre板24 h。麻省理工(5毫克·毫升−1在PBS)被添加到每个和孵化3 h。吸光度是记录在一个标(Titertek Multiskan MCC ELISA读者;美国弗吉尼亚州麦克林流实验室)的波长540 nm。治疗的效果对经济增长的抑制作用是表示为百分数细胞生存能力与未经处理的细胞。
上皮细胞激活的议员
上层清液从A23187-stimulated或未经处理的单核细胞/巨噬细胞与A549孵化,BEAS-2B细胞和HBEC,预处理与Rz或15 dpgj 2 h2或中等,成长为融合在96 -孔板为24小时37°C。在一些实验中,A549细胞与肿瘤坏死因子(TNF)刺激-α(1000 U·毫升−1)而不是单核细胞/ macrophage-derived上层清液。18-h孵化后,收获条件培养基,通过离心5分钟在12000×g和分析引发和MCP-1内容。
ELISA趋化因子检测
引发和MCP-1 A549的上层清液,BEAS-2B HEBC上皮细胞被夹心ELISA试剂盒测量根据制造商的指示。
rt - pcr
RNA是使用NucleoSpin从细胞中提取RNA II (Machery-Nagel)根据制造商的指示,18 h后议员刺激。RNA浓度和纯度测定光谱光度测量的读数在260/280 nm。RNA被反向转录cDNA或为进一步使用存储在-80°C。互补的RNA逆转录执行使用Iscript互补脱氧核糖核酸合成装备(Bio-Rad)根据制造商的指示。
rt - PCR进行使用智商SYBR绿色SUPERMIX (Bio-Rad) MiniOpticon双色实时PCR检测系统(Bio-Rad)。pcr进行复制和产生HPRT coamplified正常化的RNA数量添加到反应。所有数据分析使用OpticonMonitor3®软件(Bio-Rad)。比较mRNA的表达水平在不同样本,信使rna的相对表达水平比较ΔC计算使用T(阈值周期数)方法(15]。简单地说,使用下列公式:2-ΔΔCT,ΔΔCTC的区别T感兴趣的基因和产生HPRT之间,和CT示例= CT实际样品- CT最低的表达式示例。引物的扩增效率对测定通过运行连续稀释的互补。目标和参考基因扩增效率接近100%,R2值为0.99。
电泳迁移率改变分析
与适当的刺激,挑战后A549细胞(2×106用冰冷的PBS洗净,刮和离心机1000 g×5分钟在4°C。核提取得到商用设备(核提取设备;活动主题)根据制造商的指示。核提取物(5μg)孵化2μg保利(dI-dC)和γ(32P] ATP-labelled寡核苷酸探针(100000 - 150000年cpm;Promega,意大利米兰)绑定缓冲(50%的甘油,10毫米Tris-HCl, pH值7.6,500毫米氯化钾,EDTA 10毫米,1毫米二硫苏糖醇)在最后一卷20μL在室温下30分钟。NF-κB共识寡核苷酸(5′-AGTTGAGGGGACTTTCCCAGGC-3′)从Promega获得。nucleotide-protein复杂分离5%聚丙烯酰胺凝胶在0.5×此种缓冲(Tris-HCl 100毫米,100毫米硼酸,2毫米EDTA)在150 V冰。这种凝胶是干和放射性乐队被检测到放射自显影法。
数据显示和统计分析
除非另有指示,数据显示为±扫描电镜从n独立、连续实验;比较组间是由为重复测量方差分析Bonferroni紧随其后的分析或配对t检验,使用棱镜软件(GraphPad、圣地亚哥、钙、美国)。p < 0.05的值被认为是具有统计学意义。
结果
MP-induced upregulation A549细胞的趋化因子合成依赖于NF-κB激活
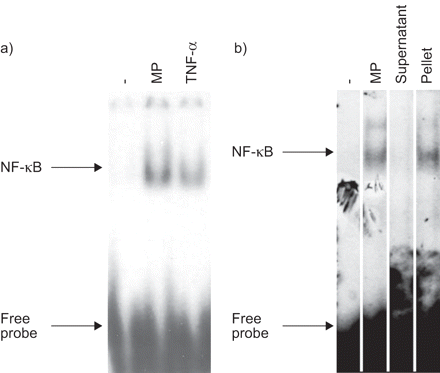
调查是否单核细胞/ macrophage-derived议员引入NF-κB的易位,A549细胞孵化议员;核提取物被检查电泳转变。图1一个表明MP-stimulated A549细胞接受NF-κB激活。确认议员,而非可溶性分子,负责这样的激活,MP-containing单核细胞/巨噬细胞条件培养基是提交给超速离心法(100000×g 2 h)。图1 b表明NF-κB激活诱导的上层清液沉淀议员更强烈。由于NF-κB并非大多数实验中,如果细胞中检测到的影响PPAR-γ受体激动剂在NF-κB基线条件没有调查。
)核因子(NF) -κB激活在A549细胞刺激1 h与未经处理的上层清液单核细胞/巨噬细胞(-),或从A23187-stimulated单核细胞/巨噬细胞(MP)和肿瘤坏死因子(TNF) -α(1000 U mL−1)。b) NF-κB激活如果A549细胞(-),在A549细胞治疗的上层清液A23187-stimulated单核细胞/巨噬细胞(MP),相同的浮层材料在超速离心法(100000×2 h g;上层清液)或超速离心法重组后获得的颗粒在同样体积的缓冲起始物料(颗粒)。单独的车道相同的凝胶。
PPAR-γ激活抑制MP-induced合成的引发和MCP-1肺上皮细胞
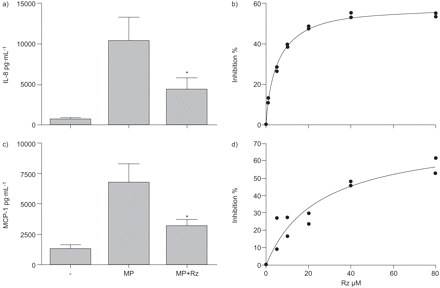
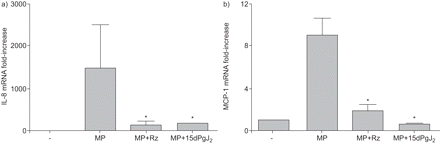
基线合成的引发和MCP-1 A549细胞没有明显影响Rz治疗(938.5±303.3 pg·毫升−1与609.8±161.7 pg·毫升−1;n = 6和1286±457.5 pg·毫升−1与464.9±124.4 pg·毫升−1;分别为n = 6)。孵化A549细胞与议员来自A23187-stimulated人类单核细胞/巨噬细胞诱导表达的引发和MCP-1如预期[6]。Rz,当合成PPAR-γ受体激动剂添加到A549细胞孵化与国会议员之前,统计学意义,减少引发的表达存在剂量依赖的相关性观察(图2 a和b)。20μM附近的抑制达到最大值。相比之下,TNF-α-induced刺激的抑制作用不强,需要相对较高的浓度,显著抑制引发表达了在80μM Rz(数据没有显示)。类似的结果与支气管细胞系盛行不衰,BEAS-2B(数据没有显示)。存在剂量依赖的相关性,显著减少MCP-1合成也观察到(图2 c和d)。评估是否Rz的抑制作用是在转录水平,我们进行了定量rt - pcr。所示图3pre-incubation A549细胞,Rz(80μM)或15 dpgj2(8μM)引起的减少引发和MCP-1信使rna。MTT测试证实,Rz并不影响A549可行性在浓度高达80μM(数据没有显示)。
a)白介素8 (IL)表达式和c)单核细胞趋化蛋白1 (MCP) A549细胞表达的基线条件(-),在一夜之间孵化与单核细胞/ macrophage-derived微粒(MP)和孵化与议员的80μM罗格列酮(MP + Rz);分别n = 8和n = 10。*:p < 0.05与方差分析MP-stimulated细胞相比。剂量反应曲线Rz-mediated抑制b)引发表达式和d) MCP-1表达式与议员A549刺激。数据从一个实验重复两人的代表。
rt - pcr分析)白介素8 (IL)和b)单核细胞趋化蛋白1 (MCP) mRNA的内容。议员:单核细胞/ macrophage-derived微粒子;Rz:罗格列酮;15 dpgj2:15-deoxy-Δ12日,14日-prostaglandin-J2。通过方差分析*:p < 0.05;n = 3。
图4显示效果的pre-incubation HBEC Rz刺激前议员。Rz显著抑制议员由这些细胞诱导引发合成。Rz在使用的浓度并不影响HBEC可行性(数据没有显示)。
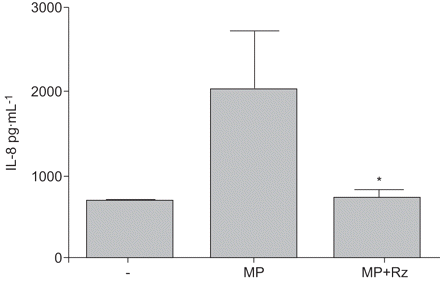
白介素8 (IL)人类支气管上皮细胞释放的基线条件(-),在一夜之间孵化与单核细胞/ macrophage-derived微粒(MP)和孵化与议员的80μM罗格列酮(MP + Rz)。*:p < 0.05相比MP-stimulated细胞通过方差分析;n = 3。
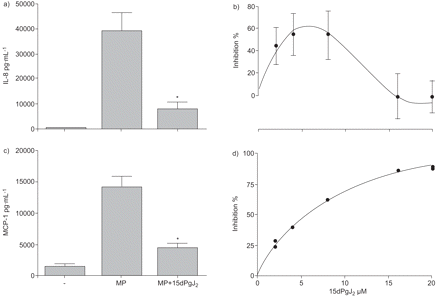
确认的抑制作用不是由于活动具体Rz,我们使用了天然,PPAR-γ活化剂,15 dpgj结构无关2。所示图515 dpgj2导致引发(明显降低图5 a和b)和MCP-1 (图5 c和d分别由A549细胞)合成。然而,剂量反应分析显示剂量反应关系只有MCP-1 (图5 d),而抑制诱导15 dpgj引发表达式2两相的出现,在6 - 8与最大抑制μg·毫升−1和进步的活动在更高浓度(图5 b)。15 dpgj MTT测试确认2没有造成重大损失,在浓度20μM A549细胞生存能力。
a)白介素8 (IL)释放和c)单核细胞趋化蛋白1 (MCP) A549细胞表达的基线条件(-),在一夜之间孵化与单核细胞/ macrophage-derived微粒(MP)和孵化与议员的存在)8μM和c) 20μM 15-deoxy-Δ12日,14日-prostaglandin-J2(MP + 15 dpgj2)。*:p < 0.05相比MP-stimulated细胞通过方差分析;分别n n = 3 = 7。15 dpgj的剂量反应曲线2介导的抑制b)引发表达式(n = 3)和d) MCP-1表达式与议员A549刺激。数据从一个实验的两个代表。
图6显示的HBEC pre-incubation 15 dpgj的效果2刺激前议员。15 dpgj2由这些细胞显著抑制MP-induced引发合成。15 dpgj2在使用的浓度并不影响HBEC可行性(数据没有显示)。
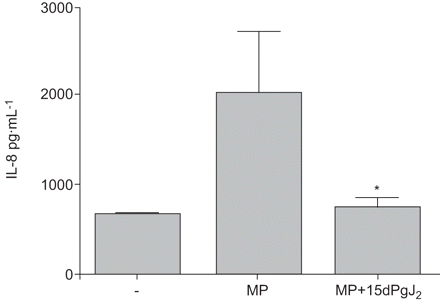
白介素8 (IL)人类支气管上皮细胞释放的基线条件(-),在一夜之间孵化与单核细胞/ macrophage-derived微粒(MP)和孵化与议员的8μM 15-deoxy-Δ12日,14日-prostaglandin-J2(MP + 15 dpgj2)。*:p < 0.05相比MP-stimulated细胞通过方差分析;n = 3。
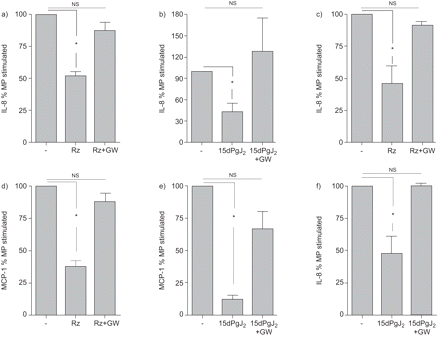
图7显示特定的抑制PPAR-γ激活GW恢复这两个化合物的影响在MP-stimulated A549 (图7 a, b, c和d)和HBEC (图7 e和f)。
a、b)白介素8 (IL)和d, e)单核细胞趋化蛋白1 (MCP)释放的微粒(MP)刺激A549细胞缺乏或存在和d)罗格列酮(Rz;80μM)或b和e) 15-deoxy-Δ12日,14日-prostaglandin-J2(15 dpgj2;分别为8和20μM),有或没有对手,GW9662 (GW)克分子数相等的浓度。c、f)引发释放MP-stimulated人类支气管上皮细胞的Rz(80μM)或15 dpgj2(8μM),有或没有对手,GW。*:p < 0.05与MP-stimulated细胞相比,配对t检验。NS:不显著;n = 3。
因为它可能是一个次要的影响细胞刺激是由于可溶性分子出现在上层清液刺激单核细胞/巨噬细胞而不是国会议员,我们也反复实验使用的一些议员由超速离心法纯化。图8显示特定PPAR-γ激活恢复的影响化合物的抑制A549细胞刺激与议员由超速离心法纯化。
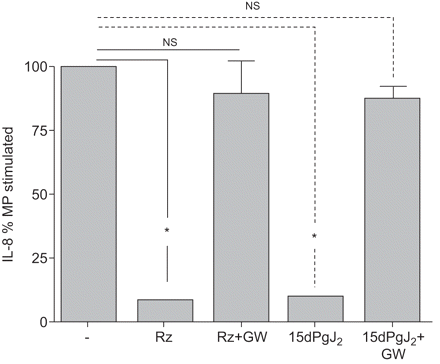
由A549细胞白介素8 (IL)发布了微粒子(MP)超速离心法纯化的缺失或出现罗格列酮(Rz;80年μM)或15-deoxy-Δ12日,14日-prostaglandin-J2(15 dpgj2;8μM),有或没有对手,GW9662 (GW)克分子数相等的浓度。*:p < 0.05与MP-stimulated细胞相比,配对t检验。NS:不显著;n = 3。
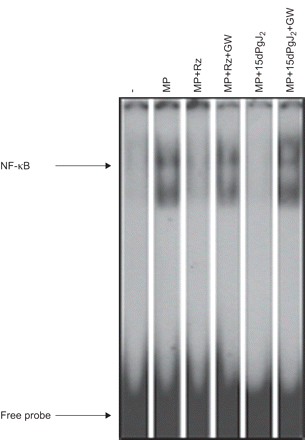
图9显示两个PPAR-γ受体激动剂抑制NF-κB激活。因为Rz和15 dpgj2有可能产生生物活性独立PPAR-γ激活(16- - - - - -18),我们试图确定的角色PPAR-γ激活的调制MP-induced肺上皮细胞炎症使用特定PPAR-γ抑制剂,GW。图9证实了GW恢复PPAR-γ受体激动剂的抑制作用。
核因子(NF) -κB A549细胞活化在基线条件(-),在孵化与微粒子(MP),在30分钟后激活与议员预处理与过氧物酶体proliferator-activated受体(PPAR) -γ受体激动剂15-deoxy-Δ12日,14日-prostaglandin-J2(15 dpgj2;20μM)或罗格列酮(Rz;80μM)和激活与MP 30分钟预处理后15 dpgj PPAR-γ受体激动剂2(20μM)或Rz(80μM)的存在GW9662 (GW)(20μM和80μM,分别)。数据从一个实验的三个代表。单独的车道相同的凝胶。
讨论
尽管最初认为代表细胞碎片没有生理意义,议员目前已知参与不同的生理现象。MP-mediated upregulation合成的促炎的受体激动剂通过内皮细胞和成纤维细胞,例如,是成为一个公认的行列式炎症(19]。的一部分,试图进一步阐明机制MP-induced炎症,本研究的目的是调查的角色PPAR-γ通路在细胞因子合成的upregulation肺上皮细胞刺激单核细胞/ macrophage-derived MP。
因为众所周知,PPAR-γ激活抑制NF-κB / DNA结合,我们第一次试图确定MP-induced刺激肺上皮细胞是通过NF-κB激活介导的。事实上,我们的数据表明,国会议员来自单核细胞/巨噬细胞诱导的易位NF-κB细胞核;可溶性分子超速离心法去除后获得议员的影响要小得多。多形核细胞,使用议员来自Mesri和阿尔提耶里20.)表明,upregulation内皮细胞的il - 6的合成不涉及NF-κB易位到细胞核。相比之下,在不同在活的有机体内和在体外模型,其他人则展示了一个角色在MP-mediated NF-κB激活炎症(5,21]。显然这些相互矛盾的结果可能反映了一个事实,议员中异构组成,根据细胞的获得和使用的刺激诱导形成(22),因此以不同的方式发挥其生物学效应。
然后我们调查了PPAR-γ激活的作用在我们的模型中。我们的数据表明,促炎介质的upregulation人类肺上皮细胞刺激单核细胞/ macrophage-derived议员是通过PPAR-γ依赖途径介导的。两个结构无关的PPAR-γ受体激动剂,合成配体Rz,和天然的活化剂,15 dpgj2在A549细胞刺激,抑制NF-κB激活单核细胞/ macrophage-derived议员。两个分子也引起显著抑制A549引发表达式,BEAS-2B HBEC细胞刺激MP。MCP-1合成也显著地抑制A549细胞,而其表达BEAS-2B细胞不是因为我们调查证实了我们之前的观察,这趋化因子不是调节实验条件下描述。值得注意的是,虽然Rz显然是剂量依赖性的抑制作用在所有使用的实验模型,与15 dpgj A549细胞的培养2造成了抑制引发合成最大的6 - 8μg·毫升−1在较高的浓度,变得不那么有效。它已经表明,15 dpgj2移植引发(但不是MCP-1)合成由单核细胞/巨噬细胞(23和由人类小神经胶质细胞24]。虽然我们不能直接解决这个问题,我们的研究结果与双15 dpgj活动相一致2在MP-stimulated A549细胞,最终抵消的抑制作用在较高的浓度直接刺激活动。许多报告表明thiazolidinediones发挥其生物活性通过PPAR-γ-dependent和独立通路(16- - - - - -18]。我们观察到这两种受体激动剂的作用是恢复的特定PPAR-γ抑制证实thiazolidinedione-mediated抑制PPAR-γ-dependent议员对支气管上皮细胞的影响。
慢性阻塞性肺病是一种病理条件定义为慢性,渐进和主要不可逆气流限制(25]。与异常炎症反应相关的疾病的肺部有害颗粒或气体,香烟是最重要的病原体(25]。慢性阻塞性肺病预计将成为全球第三大死因到2020年(25]。目前吸入长效支气管扩张剂和类固醇的组合代表了主流治疗慢性阻塞性肺病,这种治疗对死亡率的影响是适度的26),需要更好的理解疾病的机制和新治疗方法显然是认可的27]。PPARs最近获得利益的调节器,气道炎症反应和被认为是潜在的目标治疗炎症性肺部疾病(28]。我们的数据表明PPAR-γ受体激动剂抑制MP-induced上皮炎症进一步支持这种方法。
脚注
支持声明
本研究支持Ministero戴尔'Istruzione,戴尔'Universita e德拉Ricerca意大利,20074 s9kxf_002协议号码。
感兴趣的语句
语句对美国布鲁内莱斯基监督完成和p . Paggario可以找到www.www.qdcxjkg.com/site/misc/statements.xhtml
- 收到了2010年2月11日。
- 接受2010年的10月28日。
- ©2011人队