摘要gydF4y2Ba
异氰烷是由环氧化酶(COX)或脂氧基酶(LOXS)产生的花生素酸的代谢物。它们在慢性肺炎疾病中介导炎症和粘液分泌。凝胶形成粘蛋白MUC5Ac在这些疾病的患者的呼吸道中过于表达。MUC5Ac表达由细胞外信号调节激酶(ERK)/ SP1依赖机构介导。gydF4y2Ba
我们的目的是研究果香和它们的信号通路在MUC5AC表达中的作用。gydF4y2Ba
12-LOX的抑制剂,但不包括COX,5-LOX或15-LOX的,减少在支气管上皮细胞系NCI-H292诱导佛波醇肉豆蔻乙酸酯(PMA)MUC5AC表达。这些抑制剂也是由单层细胞废除生产全粘液。两种形式12-LOX(R和S)的哺乳动物中存在。使用的siRNA,我们表明12R-LOX但不12S-LOX参与由PMA,脂多糖或转化生长因子α诱导MUC5AC表达。12R-LOX也参与MUC2和MUC5B表达,虽然比MUC5AC程度较轻。相反,12R-LOX沉默不修改白细胞介素-8生产。12-LOX抑制剂减少ERK活化和PMA诱导的Sp1的易位。此外,12R-LOX产物12(R) - 羟基酸,诱导表达MUC5AC,ERK活化和Sp1的易位。gydF4y2Ba
12R-LOX参与MUC5AC表达。这发生gydF4y2BaviagydF4y2BaERK-和sp1信号通路。gydF4y2Ba
黏液蛋白是黏液中的主要蛋白,具有高度糖基化,由易发生o -糖基化的中心结构域(黏液结构域)的蛋白主干组成[gydF4y2Ba1gydF4y2Ba].形成凝胶的粘蛋白通过其富含半胱氨酸的末端结构域聚合,并在细胞外介质中分泌。在成人气道中,最具代表性的成胶粘蛋白为MUC5AC、MUC5B,在较小程度上,还有MUC2 [gydF4y2Ba2gydF4y2Ba].这些粘蛋白聚集在11号染色体的p15臂上[gydF4y2Ba3.gydF4y2Ba它们表现出共同和不同的表达调控机制[gydF4y2Ba4.gydF4y2Ba那gydF4y2Ba5.gydF4y2Ba].Muc5Ac是气道表面上存在的最丰富的凝胶形成粘蛋白[gydF4y2Ba6.gydF4y2Ba].已经广泛地研究了其表达机制,使用细胞系NCI-H292作为模型[gydF4y2Ba4.gydF4y2Ba那gydF4y2Ba7.gydF4y2Ba那gydF4y2Ba8.gydF4y2Ba].N的一些研究gydF4y2Ba阿德尔gydF4y2Ba和同事(gydF4y2Ba8.gydF4y2Ba那gydF4y2Ba9.gydF4y2Ba[已表明,Phorbol Myristate醋酸酯(PMA)诱导转化生长因子-α(TGF-α)的基质金属蛋白酶介导的释放,其随后结合并激活表皮生长因子受体(EGFR)以诱导MUC5AC合成和分泌。然后通过激活细胞外信号调节激酶(ERK)/ SP1信号传导途径的磷酸化[gydF4y2Ba4.gydF4y2Ba那gydF4y2Ba7.gydF4y2Ba].EGFR参与其他促炎刺激诱导的MUC5AC释放,如中性粒细胞弹性蛋白酶和细菌脂多糖(LPS)[gydF4y2Ba10.gydF4y2Ba].gydF4y2Ba
细胞溶质磷脂酶A.gydF4y2Ba2gydF4y2Ba(cPLAgydF4y2Ba2gydF4y2Ba)是一个关键的酶控制花生四烯酸(AA)的释放。一旦AA被释放它进一步通过环加氧酶(COXs)和/或脂氧合酶(LOXs)以产生类二十烷酸代谢。虽然早期研究表明,花生酸类调节粘蛋白的生产[gydF4y2Ba11.gydF4y2Ba那gydF4y2Ba12.gydF4y2Ba],基本的机制仍是未知的。最近,我们已经表明中国人民解放军作用gydF4y2Ba2gydF4y2Ba囊性纤维化(CF)小鼠模型粘液分泌过多[gydF4y2Ba13.gydF4y2Ba].COX催化前列腺素(如前列腺素E)的生物合成gydF4y2Ba2gydF4y2Ba(铂族元素gydF4y2Ba2gydF4y2Ba).PGE既有抑制作用,也有刺激作用gydF4y2Ba2gydF4y2Ba粘蛋白分泌的研究报告[gydF4y2Ba12.gydF4y2Ba那gydF4y2Ba14.gydF4y2Ba].最近,两个独立的实验室已经显示出在白细胞介素(IL)-1β诱导的MUC5AC生产中的COX-2作用[gydF4y2Ba15.gydF4y2Ba那gydF4y2Ba16.gydF4y2Ba].相反,LOXs是双加氧酶,催化氧加到AA上,生成氢过氧衍生物,包括氢过氧二十碳三烯酸(HpETEs)和还原形式HETE。根据AA内氧插入的位置,哺乳动物的lox传统上被分为5- lox、8- lox、12- lox或15-LOX。人类有两种不同的12- lox,血小板型,也称为12S-LOX(基因)gydF4y2Ba阿洛克1.gydF4y2Ba),表皮型称为12R-LOX(基因gydF4y2BaAlox12B.gydF4y2Ba).虽然两种LOX都产生12-HETE, 12S-LOX酶产生12(S)-HETE对映体,而12R-LOX酶几乎只产生12(R)-HETE对映体,代表唯一的哺乳动物LOX引导分子氧到AA的R位置[gydF4y2Ba17.gydF4y2Ba].gydF4y2Ba
12S-LOX介导了血小板激活AA代谢的一个主要途径[gydF4y2Ba18.gydF4y2Ba].O.gydF4y2Ba拥挤的城市gydF4y2Ba等gydF4y2Ba.[gydF4y2Ba19.gydF4y2Ba在CF患者中发现了12-LOX表达的增加,与气道上皮和粘膜腺体中的控制相比,但尚未建立12-LOX过度表达的生理相关性。12R-LOX途径在建立表皮障碍功能中起重要作用[gydF4y2Ba20.gydF4y2Ba].相反,15-LOX-1参与炎症性疾病,包括动脉粥样硬化、癌症、骨质疏松症、血管紧张素ii依赖性高血压和糖尿病[gydF4y2Ba21.gydF4y2Ba].最近,15-LOX-1在哮喘中涉及MUC5AC过表达[gydF4y2Ba22.gydF4y2Ba].gydF4y2Ba
在气道的慢性炎症疾病中,如慢性阻塞性肺病,哮喘和CF,加剧的粘液生产导致气道阻塞,有利于细菌定植。虽然已经提出了治疗粘液过度的疗法,但仍然缺乏有效的治疗方法。改善对粘液生产和分泌机制的理解将有助于设计新的药理学方法治疗粘液过度折杂。本文使用药理学和siRNA方法,我们证明了在粘蛋白表达中的12R-LOX和特别是MUC5Ac的作用。发生12r-lox的muc5ac表达式的诱导gydF4y2BaviagydF4y2BaERK和Sp1信号通路。我们首次提出12R-LOX在慢性肺部炎症疾病中的作用。gydF4y2Ba
材料与方法gydF4y2Ba
细胞培养和NCI-H292的刺激gydF4y2Ba
从ATCC(Molsheim,法国)获得的NCI-H292细胞如上所述培养[gydF4y2Ba13.gydF4y2Ba].在无血清条件下培养24小时后,用PMA(20nm),LPS(10μg·mL)刺激细胞gydF4y2Ba-1gydF4y2Ba)或TGF-α (20ng·mLgydF4y2Ba-1gydF4y2Ba)在无血清培养基中,除了LPS,加入1%的血清。从乙醇溶液中干燥12-HETE并加入细胞中。对于添加PMA和抑制剂之前,对于抑制研究,将细胞预处理1小时。该研究中使用的药物在此前发表的其他研究之后的各种浓度(0.1-50μm)中进行了测试[gydF4y2Ba15.gydF4y2Ba那gydF4y2Ba16.gydF4y2Ba那gydF4y2Ba22.gydF4y2Ba].同时测定药物对MUC5AC表达和细胞活力的影响。12-LOX抑制剂(黄芩素,肉桂酰-3,4-二羟基-α-氰酸酯(CDC))的浓度显示MUC5AC表达的最佳抑制,且无毒性。还观察到剂量-反应效应(数据未显示)。所有控制条件包括相应浓度的车辆(用乙醇处理去甲氧基愈伤组织酸(NDGA),二甲基亚砜处理PMA和其他抑制剂)。在刺激/抑制剂存在的24小时后,收集上清液,用裂解缓冲液(150 mM磷酸钠,150 mM NaCl, 1% (v/v) Triton X-100, 1% (w/v)脱氧胆酸盐,pH 7.2添加蛋白酶抑制剂鸡尾酒)裂解细胞。van buren样本(370×gydF4y2BaggydF4y2Ba在4℃下10分钟)储存在-80℃直至分析。gydF4y2Ba
细胞培养和原发性人支气管上皮细胞的刺激gydF4y2Ba
分化的人初级支气管上皮细胞MucilAir购自epithelial (epithelial Sarl, geneva, Switzerland)。这些细胞从健康受试者的支气管中分离出来,在mucilAir培养基(上皮细胞)气液界面培养3周,直到分化。为了降低粘蛋白的基础表达水平,细胞在支气管上皮细胞基础培养基中培养48 h (CC-3171;龙沙,勒瓦卢瓦-佩雷,法国)补充抗生素。然后用相同浓度的细菌上清液或等量的细菌生长培养基(Luria-Bertani)刺激细胞gydF4y2Ba(gydF4y2BaRNA提取后24 h。gydF4y2Ba
细菌的上层清液gydF4y2Ba假单胞菌铜绿假单胞菌gydF4y2Ba(PAK菌株)在IB培养基中以指数相生长收获。离心以消除细菌后,过滤上清液和LB培养基(用作对照)(0.2μm)并在-80℃下储存直至使用。gydF4y2Ba
核的实验gydF4y2Ba
自Santa Cruz Biotechnologies公司(Santa Cruz公司,CA,USA)或对照siRNA-预先设计的siRNA与中转siQUEST转染试剂(Mirus公司生物,麦迪逊,WI,USA)(每孔1μL)温育在室温下在20分钟内无血清培养基(50μL终体积)。NCI-H292生长直至亚汇合(80%)和在含有适当的siRNA(终浓度为100nM)完全细胞培养基(350微升)培养。培养24小时后,去除培养基,并加入再24小时新培养基(无血清)加刺激。实时(RT)-PCR和蛋白质印迹进行随访在24小时或在转染后48小时的沉默。gydF4y2Ba
埃莉莎gydF4y2Ba
MUC5AC酶联免疫吸附试验如前所述[gydF4y2Ba13.gydF4y2Ba那gydF4y2Ba23.gydF4y2Ba使用抗muc5ac(克隆45M1, Neomarkers, Fremont, CA, USA)和辣根过氧化物(HRP)标记的山羊抗小鼠免疫球蛋白(Ig)G抗体。因为MUC5AC在NCI-H292中的表达随细胞传代而改变[gydF4y2Ba23.gydF4y2Ba],人类MUC5AC尚无商业标准,其表达以基础生产(对照细胞)为参照,增加了1倍。45M1克隆的特异性已被证实[gydF4y2Ba24.gydF4y2Ba].为了消除刺激对细胞增殖的影响,对细胞裂解液中的总蛋白进行量化。gydF4y2Ba
引发和铂族元素gydF4y2Ba2gydF4y2Ba使用人IL-8试剂盒DuoSet夹心ELISA(R&d系统,阿宾登,UK)和特定PGE上清液中测定的浓度gydF4y2Ba2gydF4y2BaEIA(Cayman Chemicals,Ann Arbor,MI,USA)。gydF4y2Ba
rt - pcrgydF4y2Ba
通过RNEasy Mini Kit(Qiagen,瓦伦西亚,西班牙)提取总RNA。使用随机六烷烃(罗氏,Boulogne-Billancour,法国)和M-MLV逆转录酶(Promega,Charbonnières-les-Bains,法国)合成相应的cDNA。使用Sybr Green Master Mix(Applied Biosystems),在7500个快速实时PCR系统(应用生物系统,CARLSBAD,CA)中进行实时PCR。已经描述了Muc5Ac,Muc5b和Muc2的引物[gydF4y2Ba25.gydF4y2Ba].12R-LOX的引物有NgydF4y2BaigamgydF4y2Baet al。gydF4y2Ba[gydF4y2Ba26.gydF4y2Ba].使用Oligo Explorer 1.1.2软件设计了其他引物。引物如下:人β-肌动蛋白(FW:5'-ggacttcgagcaagagATGG-3'; RV:5'-GcagtgatctcctttctGCATC-3'),血小板型12-脂氧基酶(FW:5'-CCGaggagaagaAGCAATACC-3'; RV:5'-TGAGGGCAGGAACAGTGT-3'),IL-8(FW:5'-AGAGAGAGCAGAGCACACAA-3'; RW:5'-TTAGCACTCCTTGGCAAAAAC-3'),18SRNAR(FW:5'- CTTAGAGGGAGAAGTGGCG-3'; RW:5' - acgctgagcagtcagtgta-3')。使用如制造商(应用生物系统)所述的比较CT(ΔΔCT)方法在Microsoft Excel(Microsoft,Issy-Les Moulineaux,法国)中分析了三份CT值。目标的数量(2gydF4y2Ba——ΔΔCTgydF4y2Ba(除非陈述,否则使用控制细胞(任意单位= 1)归一化为β-肌动蛋白。gydF4y2Ba
西方墨点法gydF4y2Ba
在上述裂解缓冲液中的NCI-H292细胞或补充有磷酸酶抑制剂和蛋白酶抑制剂鸡尾酒的放射免疫沉淀法(RIPa)缓冲液被电泳和涂上聚偏二氟乙烯(PVDF)膜。用兔抗人磷酸-P44 / 42 mapk抗体(Cell Signaling,Danvers,MA,USA)检测特异性蛋白质,小鼠抗人类12R-LOX抗体(242-A01;亚福戈,台北,台湾),小鼠反人β-肌动蛋白抗体(A5316; Sigma,Saint-Quentin Ressavier,France)和相应的二抗(抗小鼠IgG用于12r-LOX和β-肌动蛋白的一抗或抗磷酸-P44 / 42的抗兔IgG原发性抗体)HRP标记。ECL(GE Healthcare,Saclay-orsay,法国)用作化学发光检测试剂盒。gydF4y2Ba
电泳迁移率变速测定gydF4y2Ba
核蛋白从2×10提取gydF4y2Ba6.gydF4y2Ba细胞如先前所述[gydF4y2Ba27.gydF4y2Ba].含有Sp1结合位点共识序列(5 ' - attcgatcggcggcgagc -3 ')的双链寡核苷酸标记为[γ-gydF4y2Ba32.gydF4y2BaP] DATP(3,000 CI·MMOLgydF4y2Ba-1gydF4y2Ba在10 mci·mlgydF4y2Ba-1gydF4y2Ba)使用Probequant G-50微柱(GE Healthcare)纯化。按照I描述执行以下步骤gydF4y2BaGNATOV.gydF4y2Ba和KgydF4y2Ba容易的gydF4y2Ba[gydF4y2Ba28.gydF4y2Ba].结合反应在40 mM羟乙基哌嗪乙烷磺酸(HEPES)、pH 7.6、10 mM NaCl、1.5 mM MgCl中进行gydF4y2Ba2gydF4y2Ba,2%甘油,含有1μg聚(DI-DC),0.8μCI标记的寡核苷酸(1ng)和5μg核提取物。评估具有50倍过量的冷特异性(SP1共识)或非特异性寡核苷酸(过氧化物体增殖物激活受体(PPAR)共识)的结合特异性。gydF4y2Ba
阿尔西亚蓝染色gydF4y2Ba
将NCI-H292细胞固定(福尔马林10%,10分钟),并在室温下用Alcian蓝色着色剂(pH 2.5)染色30分钟。细胞用Saphlanine染色的核观察,在尼康E 800显微镜中安装和观察。使用由Act-1软件版本2(尼康,法国芝加尼亚州Sur Marne)控制的尼康数字静止DXM 1200相机获得了图片。gydF4y2Ba
细胞活力gydF4y2Ba
用细胞毒素96非酰基活性细胞毒性测定(Promega)测量从细胞中释放的乳酸脱氢酶(LDH)活性。gydF4y2Ba
统计分析gydF4y2Ba
数据显示为平均值±gydF4y2BaSD.gydF4y2Ba.ANOVA用于确定群体之间的统计学意义差异,然后是学生 - 纽曼 - 龙尔斯多个范围测试进行配对比较。当指出时,使用未配对的T检验来比较两组。P <0.05被认为是显着的。gydF4y2Ba
结果gydF4y2Ba
LOX途径参与pma诱导的MUC5AC产生gydF4y2Ba
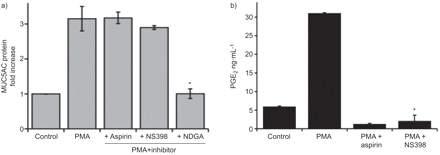
我们旨在鉴定MUC5AC表达的AA代谢物和信号通路。为此,我们检测了在pma刺激的NCI-H292细胞上清液和细胞裂解液中MUC5AC的水平,在存在特定COX或LOX抑制剂的情况下。仅给出了细胞裂解液的结果,但在上清液中也观察到类似的结果。我们检测了两种COX抑制剂(阿司匹林,NS398)和一般LOX抑制剂(NDGA)对MUC5AC表达的影响。NDGA显著降低pma诱导的MUC5AC表达,而COX抑制剂没有作用(gydF4y2Ba而是1AgydF4y2Ba).我们验证了Cox抑制剂有效地减少了PGEgydF4y2Ba2gydF4y2Ba释放(gydF4y2Ba而是1B.gydF4y2Ba).这些数据表明,在pma刺激的细胞中,参与MUC5AC表达的是LOX途径,而不是COX途径。gydF4y2Ba
muc5ac蛋白和前列腺素的表达gydF4y2Ba2gydF4y2Ba(铂族元素gydF4y2Ba2gydF4y2Ba)在环加氧酶(COX)和脂加氧酶(LOX)抑制剂存在下,肉豆蔻酸酯(PMA)诱导的分泌。a)在阿司匹林(200 μM)、NS398 (5 μM)或NDGA (20 μM)存在下,PMA (20 nM)刺激NCI-H292细胞24 h后,用ELISA法检测MUC5AC蛋白。细胞经指示药物预处理1 h后加入PMA。数据以非受刺激细胞(对照)增加-倍表示(任意单位=1)。单独使用抑制剂不能改变MUC5AC基础分泌水平(数据未显示)。b) PGE浓度gydF4y2Ba2gydF4y2Ba用EIA在NCI-H292细胞刺激上清中测量,如a)gydF4y2BaSD.gydF4y2Ba代表了三个独立实验的三倍倍。*: p < 0.05gydF4y2Ba与gydF4y2BaPMA治疗没有抑制剂。gydF4y2Ba
12-LOX在MUC5AC生产中的作用gydF4y2Ba
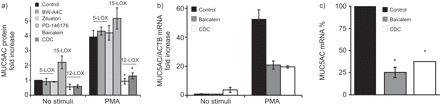
使用更多的选择性LOX抑制剂,我们观察到,只有那些目标12-LOX(CDC,黄芩素),但不是那些靶向5-LOX(BW-A4C,齐留通)或15-LOX抑制剂(PD-146176),降低的PMA诱导MUC5AC表达式(gydF4y2Ba而是2AgydF4y2Ba).相比之下,CDC和黄芩素都没有降低PMA诱导的IL-8分泌(数据未显示)。此外,黄芩素和CDC均显著降低pma诱导的MUC5AC mRNA表达(gydF4y2Ba而是2B.gydF4y2Ba).由于通过LDH释放(材料和方法部分)测量的细胞细胞毒性,这些抑制剂的效果不是由于细胞细胞毒性。因此,这些结果表明12-LOX调节转录水平的MUC5AC表达。gydF4y2Ba
Phorbol Mertiristate醋酸盐(PMA)在脂氧酸盐(LOX)抑制剂存在下诱导的MUC5Ac诱导。a)在BW-A4C,Zilueton,PD-146176,Baicalein(20μm的所有药物)存在下,在NCI-H292细胞裂解物中在NCI-H292细胞裂解物中测量MUC5AC蛋白质或B)mRNA。肉桂-3,4-二羟基-α-氰基氨基醛(CDC),10μm。在加入PMA之前,用指定的药物预处理细胞1小时。数据以非受刺激细胞(对照)增加-倍表示(任意单位=1)。c)PMA刺激细胞中的%MUC5AC表达仅提及仅用PMA刺激的细胞(100%)。在a)和c)平均值±gydF4y2BaSD.gydF4y2Ba来自三个独立实验表示一式三份的;在b)中的平均值±gydF4y2BaSD.gydF4y2Ba从一个有代表性的总共三个实验的三个副本中显示。*: p < 0.05gydF4y2Ba与gydF4y2BaPMA治疗没有抑制剂。gydF4y2Ba
12R-LOX参与MUC5AC表达gydF4y2Ba
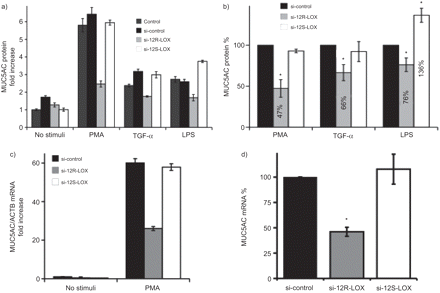
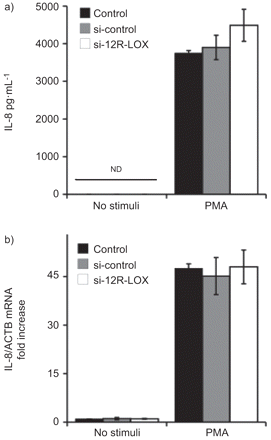
因为NCI-H292细胞表达了12S-LOX和12R-LOX(参见在线补充图),我们检查了每12-LOX形式对MUC5AC表达的转录沉默的影响。as.gydF4y2Ba而是3AgydF4y2Ba结果表明,沉默12R-LOX表达可降低PMA-、TGF-α-和lps诱导的MUC5AC表达。与TGF-α(34%)和LPS(24%)相比,PMA处理后MUC5AC抑制更明显(53%)(gydF4y2Ba而是3B.gydF4y2Ba).相比之下,12S-LOX沉默对PMA或TGF-α诱导的MUC5AC没有影响(gydF4y2Ba而是3AgydF4y2Ba然而,令人惊讶的是,它显著增强了脂多糖诱导的MUC5AC产生(gydF4y2Ba而是3AgydF4y2Bab)。接下来,我们分析了12-LOX沉默对PMA刺激细胞中MUC5AC mRNA表达的影响。沉默的12r-lox,但不是12s-lox,减少的muc5ac mRNA表达(gydF4y2Ba而是3CgydF4y2Bad).有趣的是,12R-LOX siRNA并没有改变pma诱导的IL-8分泌(gydF4y2Ba而是4AgydF4y2Bab)。将这些数据占据在一起,表明12R-LOX在诱导MUC5AC表达中的作用。gydF4y2Ba
MUC5AC在12-脂氧合酶(LOX)沉默的NCI-H292细胞中的表达。siRNA转染的细胞用佛波十四酸酯(PMA) (20 nM)、转化生长因子(TGF)-α (20 ng·mL)刺激gydF4y2Ba-1gydF4y2Ba)或脂多糖(LPS)(10μg·mlgydF4y2Ba-1gydF4y2Ba)24小时。然后,在细胞裂解物中测量MUC5Ac蛋白,作为折叠增加的折叠增加(对照)(对照)(任意单位= 1)或B),称为刺激/对照Si-RNA(Si-Control) -转染细胞(任意值= 100%)。C)测量mRNA并考虑非刺激/ Si-Contract转染的细胞表达的MRNA(任意单位= 1)。d)PMA刺激细胞中的%MUC5Ac表达被称为Si-Concep转染的细胞(100%)。均值±gydF4y2BaSD.gydF4y2Ba从一个代表性实验中示出了三份素,总共三种)和c)。在b)和d)平均值±gydF4y2BaSD.gydF4y2Ba给出了三个独立实验的三次重复。*: p < 0.05gydF4y2Ba与gydF4y2Ba用Si控制转染细胞并用相应的刺激刺激。gydF4y2Ba
在12R-脂氧基酶(LOX)沉默的NCI-H292中,Phorbol Mertirtate乙酸酯(PMA)诱导的白细胞介素(IL)-8的表达。用PMA(20nm)刺激用12R-LOX siRNA(100nm)转染的细胞24小时。然后,通过A)夹心酶的细胞上清液和B)IL-8 Phorbol Myristate通过实时RT-PCR在细胞上清液中测量IL-8蛋白。平均值±gydF4y2BaSD.gydF4y2Ba三份子酸盐显示出总共三个代表性实验。ND:未检测到;SI-CONTROL:由制造商提供的Nontargeting Si-RNA。gydF4y2Ba
12-LOX抑制剂减少PMA诱导的ERK和SP1的激活gydF4y2Ba
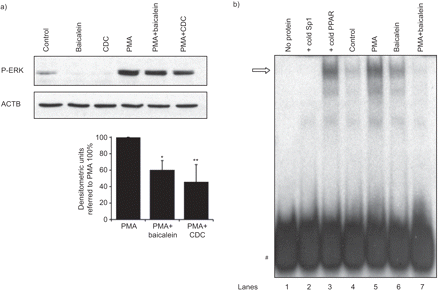
在NCI-H292细胞中,PMA激活PKC激活ERK并易位Sp1,后者结合MUC5AC启动子启动转录[gydF4y2Ba7.gydF4y2Ba那gydF4y2Ba9.gydF4y2Ba].如图所示gydF4y2Ba而是5AgydF4y2Ba, CDC和黄芩素降低pma诱导的ERK磷酸化。此外,电泳迁移移位分析(EMSA)显示,PMA刺激的细胞Sp1易位增强(gydF4y2Ba而是5B.gydF4y2Ba).相反,Baicalein减少了SP1移位带(gydF4y2Ba而是5B.gydF4y2Ba).另外一种12-LOX抑制剂CDC也获得了类似的结果(数据未显示)。综上所述,这些数据表明12-LOX在pma诱导的ERK-Sp1激活中发挥作用。gydF4y2Ba
在12-脂氧合酶(LOX)抑制剂存在下,肉豆蔻乙酸佛宝酯(PMA)诱导的细胞外信号调节激酶(ERK)激活和Sp1易位。a)用黄芩素(20 μM)或肉桂酰-3,4-二羟基-α-氰酸酯(CDC) (10 μM)预培养2 h,并在37℃下用PMA (20 nM)刺激20 min。然后在放射免疫沉淀试验(RIPA)缓冲液中收集细胞裂解液,电泳(12%十二烷基硫酸钠聚丙烯酰胺凝胶电泳(SDS-PAGE))并印迹。用抗phospho-p44/42 MAPK抗体检测活化ERK (P-ERK)。膜被剥离,用抗β-肌动蛋白(ACTB)抗体重新探针。P-ERK反应带归一化至ACTB基线值。一个有代表性的印迹显示了总共三个独立的实验。密度单位来自三个独立的实验,考虑pma刺激细胞的P-ERK/ACTB为100%。*: p < 0.05;* *: p < 0.01gydF4y2Ba与gydF4y2BaPMA治疗没有抑制剂。b)用PMA(20nm)刺激预处理或不用BaciCalin(20μm)的血清剥夺的NCI-H292细胞4小时。提取核蛋白后,将5μg孵育gydF4y2Ba32.gydF4y2Bap标记的共识Sp1探针在4°C结合缓冲液(40 mM羟乙基哌嗪乙烷磺酸,pH 7.6, 10 mM NaCl, 1.5 mM MgCl)中30分钟gydF4y2Ba2gydF4y2Ba),存在50倍摩尔过量的冷特异性共识Sp1探针(+cold Sp1, line)或冷无关过氧化物酶体增殖物激活受体(PPAR)共识探针(+cold PPAR, line)。sp1 -探针复合物(箭头)在4℃预冷的5%聚丙烯酰胺天然凝胶中从游离探针(#)中分离出来。通道1:仅探针,不含核蛋白;lanes 2,3,5: pma刺激细胞的核蛋白;通道4:来自控制细胞的核蛋白;通道6:黄芩素处理细胞的核蛋白;7号通道:黄芩素和pma处理细胞的核蛋白。从三个独立的实验中得到了一个具有代表性的凝胶。gydF4y2Ba
12(R)-HETE上调MUC5AC表达并激活ERK-Sp1信号通路gydF4y2Ba
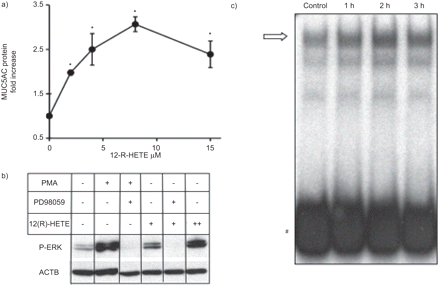
12(R),12R-LOX产物,诱导MUC5Ac蛋白以剂量依赖性方式,在8μm处具有最大效果(gydF4y2Ba而是6AgydF4y2Ba).此外,12(R)-HETE能够激活ERK(gydF4y2Ba而是6B.gydF4y2Ba),而MEK1/2 (ERK激酶)抑制剂(PD98059)阻断了12(R) hete诱导的ERK磷酸化(gydF4y2Ba而是6B.gydF4y2Ba).另外,在刺激后2小时,12(R)-HETE诱导SP1易位,在2小时后达到活性峰值(gydF4y2Ba而是6CgydF4y2Ba).这些结果表明,12(R)-HETE刺激erk - sp1信号通路。gydF4y2Ba
12(R)-羟基二十碳三烯酸(HETE)诱导MUC5AC表达,细胞外信号调节激酶(ERK)激活和Sp1易位在NCI-H292。a)细胞中加入12(R)-HETE或载体。培养24 h后,ELISA检测细胞裂解液中MUC5AC蛋白含量。均值±gydF4y2BaSD.gydF4y2Ba代表 - 来自三种独立实验的基础条件下的Muc5Ac蛋白水平标准化为-fold增加。*: p < 0.05gydF4y2Ba与gydF4y2Ba非刺激细胞(T检验)。b)如所述分析ERK磷酸化(P-ERK)gydF4y2Ba图5AgydF4y2Ba分别与PMA (20 nM)、PD98059 (20 μM)、12(R)-HETE (2 μM(+)或8 μM(++))或表中所示组合孵育20 min。在PMA或12(R)-HETE前30分钟加入PD98059。c)在指定时间(对照,t=0)用12(R)-HETE (8 μM)处理细胞,然后进行电泳迁移迁移试验,如前所述gydF4y2Ba而是5B.gydF4y2Ba.gydF4y2Ba
12R-LOX还可调节其他呼吸粘蛋白gydF4y2Ba
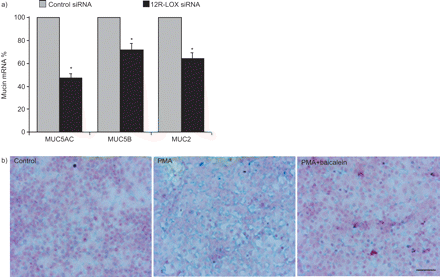
我们检查了12R-LOX是否还调节PMA诱导的MUC5B和MUC2表达。将12r-LOX的沉默减少28%和35%(gydF4y2Ba而是7AgydF4y2Ba).这些影响不如MUC5AC的显著(53%抑制)(gydF4y2Ba而是7AgydF4y2Ba).最后,我们研究了12-LOX对NCI-H292细胞产生整个黏液的作用。在黄芩素存在或不存在的情况下,使用阿利新蓝(AB)对细胞单层进行染色。与未受PMA刺激的细胞相比,PMA刺激的细胞AB染色增加(gydF4y2Ba而是7B.gydF4y2Ba),反映PMA诱导粘液产生。黄芩素强烈地减少了这种染色(gydF4y2Ba而是7B.gydF4y2Ba),当用CDC处理细胞时证实了这一发现(数据未显示)。gydF4y2Ba
12r -脂氧合酶(LOX)对气道粘蛋白和黏液的调控。a)用12R-LOX siRNA或对照siRNA转染phorbol myristate acetate (PMA)刺激的细胞,使用特定的MUC5AC、MUC5B或MUC2引物进行实时PCR,如材料和方法部分所述。转染对照siRNA的pma刺激细胞的表达水平正常化(100%)。均值±gydF4y2BaSD.gydF4y2Ba代表了三个独立实验的三倍一倍。*: p < 0.05gydF4y2Ba与gydF4y2Basi-control转染细胞。b)先用黄芩素(20 μM)预孵育或不孵育细胞1 h,再用PMA (20 nM)刺激或不孵育细胞24 h。然后细胞被固定,并用阿利新蓝(酸性粘蛋白呈蓝色)和藏青素(细胞核呈红色)染色。比例尺= 100μm。展示了两个独立实验中的一个具有代表性的图像。肉桂基-3,4-二羟基-α-氰酸酯(10 μM)处理也有相同的结果(数据未显示)。gydF4y2Ba
12-LOX调节原代人支气管上皮细胞中的呼吸粘蛋白gydF4y2Ba
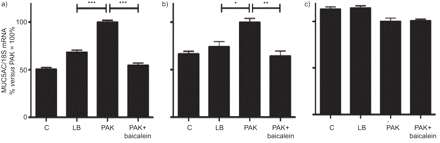
为了检查12-LOX在原代细胞中呼吸粘膜表达中的作用,人支气管上皮细胞在空气液体界面中生长,并用上清液刺激gydF4y2Ba铜绿假单胞菌gydF4y2Ba,CF患者的病理生理刺激。gydF4y2Ba铜绿假单胞菌gydF4y2Ba上清液诱导muc5ac和muc2(gydF4y2Ba而是8AgydF4y2Ba和gydF4y2Ba8B.gydF4y2Ba)但不是muc5b表达(gydF4y2Ba而是8C.gydF4y2Ba).黄芩素的存在降低了46%和36%gydF4y2Ba铜绿假单胞菌gydF4y2Ba-诱导MUC5AC和MUC2的表达(gydF4y2Ba而是8AgydF4y2Ba和gydF4y2Ba8B.gydF4y2Ba).gydF4y2Ba
Baicalim在中国的影响gydF4y2Ba假单胞菌铜绿假单胞菌gydF4y2Ba人初级上皮细胞中的上清液诱导的粘液表达。将细胞在空气液体界面中培养并用Baicalin(20μm)1小时预处理,并在用细菌治疗期间(gydF4y2Ba铜绿假单胞菌gydF4y2Ba如在材料和方法中所示,在1:8或细菌培养基中稀释的菌株PAK)稀释的上清液,LURIA-BERTANI(LB,1:8),如材料和方法所示。制备总mRNA并进行实时定量PCR以测量A)MUC5AC,B)MUC2和C)MUC5B水平。结果表明,与用Pak上清液处理的细胞相比,Baicalein对粘液mRNA表达的抑制百分比。值表示平均值±gydF4y2BaSD.gydF4y2Ba来自三个不同捐献者的三个独立实验*: p < 0.05;* *: p < 0.01;* * *: p < 0.001。gydF4y2Ba
讨论gydF4y2Ba
在目前的工作中,在NCI-H292细胞系和初级支气管上皮细胞上,我们证明了12-LOX在粘蛋白MUC5AC表达中的关键作用。我们使用PMA作为粘蛋白诱导剂,因为之前的研究表明,由该药物诱导的MUC5AC表达依赖于EGFR的激活,EGFR是控制气道中粘蛋白生成的关键受体[gydF4y2Ba10.gydF4y2Ba].EGFR中和抗体或EGFR磷酸化的抑制剂阻断PMA诱导的MUC5AC表达[gydF4y2Ba9.gydF4y2Ba].在所选实验中,更多的生理刺激(TGF-α,LPS,上清液gydF4y2Ba铜绿假单胞菌gydF4y2Ba)已经被用来证明12-LOX参与粘蛋白表达。PMA激活EGFR后的下游信号通路传导到MUC5AC表达的部分特征[gydF4y2Ba4.gydF4y2Ba那gydF4y2Ba7.gydF4y2Ba],但12-LOX在这些途径中的作用尚未被研究。gydF4y2Ba
虽然活性COX酶存在于NCI-H292细胞中,COX抑制剂对PMA诱导MUC5AC表达没有影响。以前的作品表明COX在MUC5AC表达的作用[gydF4y2Ba15.gydF4y2Ba那gydF4y2Ba16.gydF4y2Ba].然而,值得注意的是,在这些报告中,作者使用IL-1β作为MUC5AC诱导剂而不是PMA。导致粘蛋白表达的IL-1β信号通路与PMA不同。PMA诱导MUC5AC表达gydF4y2BaviagydF4y2Ba基质金属蛋白酶介导的TGF-α释放,其随后激活EGFR [gydF4y2Ba29.gydF4y2Ba],从一个不同的机制对IL-1β[gydF4y2Ba15.gydF4y2Ba].此外,克gydF4y2Ba雷gydF4y2Ba等gydF4y2Ba.[gydF4y2Ba15.gydF4y2Ba[使用了气管藻上上皮细胞的模型,其中存在不同的细胞类型(gydF4y2Ba例如gydF4y2Ba纤毛,基底,黏液细胞)。因此,在他们的模型中,一种可能性是COX代谢物通过粘液产生细胞调节MUC5AC的表达gydF4y2BaviagydF4y2Ba旁静脉机制。相比之下,我们的研究是对单一细胞类型进行的,这涉及研究粘蛋白表达的自分泌调节。gydF4y2Ba
LOX是一种具有多种生物学作用的酶。通过药理学和转录抑制,我们探索了哪一个LOX参与MUC5AC表达。我们首先研究了5-LOX(导致白三烯的产生)是否参与MUC5AC表达。事实上,白三烯已经被证明可以诱导肺中的粘液表达[gydF4y2Ba11.gydF4y2Ba[人的支气管上皮细胞表达活性5-LOX [gydF4y2Ba30.gydF4y2Ba].我们的研究结果表明,这种LOX没有参与我们的细胞系统中的MUC5AC表达。gydF4y2Ba
最近的研究表明,15-LOX-1抑制剂废除由支气管上皮细胞的长期IL-13刺激诱导表达MUC5AC [gydF4y2Ba22.gydF4y2Ba].然而,在本研究中,使用Z研究中报告的相同的15-LOX-1抑制剂gydF4y2Ba郝gydF4y2Ba等gydF4y2Ba.[gydF4y2Ba22.gydF4y2Ba],我们发现,这种酶不参与PMA诱导MUC5AC表达。我们还观察到,15-LOX-1抑制剂没有减少TGF-α诱导的表达MUC5AC(未示出数据)。这里再一次,在激活MUC5AC表达(IL-13受体依赖的信号传导途径的差异gydF4y2Ba与gydF4y2BaEGFR依赖性途径)和刺激的持续时间可以解释我们的研究结果与Z之间的这些差异gydF4y2Ba郝gydF4y2Ba等gydF4y2Ba.[gydF4y2Ba22.gydF4y2Ba].gydF4y2Ba
我们的药理学方法表明,12-LOX是起着MUC5AC表达的NCI-H292细胞作用的唯一LOX。因为由不同的基因编码的两个12-LOX(12R-LOX和12S-LOX)存在于哺乳动物细胞中,我们使用了siRNA的策略,以确定哪种形式参与粘液在我们的细胞系统的生产。我们的研究结果表明,PMA诱导MUC5AC表达受12R-LOX减少,但不是由12S-LOX的siRNA。有趣的是,使用更多的生理刺激,TGF-α和LPS(配位体对EGFR和TLR-4受体分别在肺的病理生理学两个关键受体),我们证明12R-LOX的在TGF-α-和LPS诱导的MUC5AC一个拉动作用表达。我们还发现,12R-LOX在MUC5B和MUC2表达的调节,并在由PMA诱导NCI-H292单层生产全粘液起到了重要作用。此外,感应粘蛋白由gydF4y2Ba铜绿假单胞菌gydF4y2Ba上清是一种与CF中肺功能障碍相关的病原体,12-LOX抑制剂可减少原代支气管上皮细胞中的上清。总之,我们的数据表明12-LOX在黏液蛋白表达中的作用与肺阻塞性疾病的发病机制有关。gydF4y2Ba
PMA的EGFR的跨激活[gydF4y2Ba9.gydF4y2Ba已知诱导转录因子SP1与MUC5AC启动子的ERK活化和结合[gydF4y2Ba4.gydF4y2Ba那gydF4y2Ba7.gydF4y2Ba].在这里,我们发现12R-LOX siRNA抑制TGF-α诱导的MUC5AC表达,12-LOX抑制剂减少PMA诱导的ERK激活和Sp1易位。总之,这些结果表明12R-LOX介导了pma诱导的MUC5AC表达,而不是12S-LOXgydF4y2BaviagydF4y2BaEGFR相关的信令路径涉及ERK-and SP1激活。gydF4y2Ba
接下来,我们研究了12R-LOX的产物12(R)-HETE是否介导了MUC5AC在NCI-H292细胞中的表达。我们发现添加12R-HETE可刺激MUC5AC表达、ERK激活和Sp1易位。然而,在MUC5AC的产生方面,12R-HETE的影响不如PMA的显著。这可以解释为:1)pma诱导MUC5AC表达涉及12R-LOX独立通路;2)其他来源于12R-LOX活性的代谢物(直接或间接)也可能参与这一过程。关于12(R)-HETE诱导MUC5AC的机制,12(R)-HETE是芳基烃受体(AhR)的有效激活剂[gydF4y2Ba31.gydF4y2Ba是一种与环境损伤相关的配体调控的转录因子。AhR受体的激活导致MUC5AC在小鼠肺和NCI-H292细胞中的表达上调[gydF4y2Ba32.gydF4y2Ba那gydF4y2Ba33.gydF4y2Ba].因此,可以通过12R-LOX产品的容量来解释12R-LOX刺激作用(gydF4y2Ba例如gydF4y2Ba12(r)-hete)激活ahr。gydF4y2Ba
总之,本研究表明,12R-LOX,一种产生具有R-Chirity的代谢物的酶,通过粘液产生肺部阻塞性疾病的主要特征来介导粘液产生的粘液产量。因此,12R-LOX代表治疗干预的合适新靶标,以减少这些病理中的粘液产生。此外,用过度产生与呼吸凝胶的过表达形成粘液的过表达的过度产生的支气管肺泡癌。预防EGFR活化的疗法显示了这些患者的有益效果[gydF4y2Ba34.gydF4y2Ba].12-LOX在EGFR依赖性粘蛋白生产中的作用表明12-LOX抑制剂作为用于细支气管肺泡癌的治疗中的潜在药剂。gydF4y2Ba
致谢gydF4y2Ba
作者感谢M. Huerre和P. Ave(巴斯德研究所,巴黎,法国)在粘液染色过程中的帮助和建议。Burgel(科钦医院,巴黎,法国)在MUC5AC ELISA方面提供了建议,P. Krieg(德国癌症研究中心,海德堡,德国)在脂加氧酶方面进行了富有成果的讨论。gydF4y2Ba
脚注gydF4y2Ba
这篇文章有补充资料可从gydF4y2Bawww.www.qdcxjkg.comgydF4y2Ba
支持声明gydF4y2Ba
这项工作得到了法国囊性纤维化协会“Vaincre la mucovisidose”(VLM)和“Legs Poix”基金会的支持。I. Garcia-Verdugo是由VLM支持的。gydF4y2Ba
感兴趣的语句gydF4y2Ba
没有宣布。gydF4y2Ba
- 收到gydF4y2Ba2011年2月8日。gydF4y2Ba
- 接受gydF4y2Ba2012年2月12日。gydF4y2Ba
- ©2012人队gydF4y2Ba
参考文献gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba