摘要
根据自己的基因图谱,从治疗优先选择的患者最有可能受益的原则,导致了大量的临床效益在某些类型的肿瘤,并有潜力在晚期非小细胞肺癌(NSCLC)大大细化处理。有效,可靠地使用分子生物标记物的告知临床实践需要的测试方法和生物标志物预测和预后价值的仔细评估的标准化。
虽然许多研究表明,表皮生长因子受体(EGFR)基因的外显子18-21中激活突变的患者对吉替尼和厄洛替尼进行特别良好,需要进行预期和预测值所需的前瞻性随机研究的EGFR.突变。从一个这样的研究来看,似乎突变试验应该成为诊断标准,至少对于患有从未或低吸烟历史的腺癌患者,因为临床预测因子不足以优化治疗。
但是,遗留问题仍然存在:患有抗牛油尼/吉替尼的肿瘤患者的治疗方案是什么?关于治疗的结论我们可以从中抽取EGFR.副本号码或克拉斯突变状态?抗EGFR抗体在NSCLC治疗中的作用是什么作用,在哪个患者中?
这篇综述考虑了将生物标记物谱与EGFR靶向治疗NSCLC的疗效联系起来的最新证据,以及最新发现的临床意义。
建立突变检测的原理:从其他肿瘤类型教训
针对特定基因病变的治疗和检测各自分子靶点的诊断测试,现在已成为临床实践的一部分,涵盖了各种肿瘤类型,包括慢性髓系白血病1,胃肠道基质肿瘤和上皮肿瘤,如乳腺和结肠癌2.
通过向适当的患者群体施用靶向治疗来实现存活的临床相关改善:例如,在人表皮生长因子受体阳性(HER2 +)转移性乳腺癌患者中,将曲妥珠单抗添加到标准的一线化疗中3..一种HER2.在乳腺癌患者接受曲妥珠单抗治疗之前,扩增诊断检测是必须的2.结肠癌的临床实践也反映了对突变检测的需要,以确定最有可能受益于西汀昔单抗的患者:肿瘤缺乏a的患者克拉斯突变(也称为野生型)显示出显着提高了总体存活率(OS)(中位数9.5相对4.8个月)与西妥昔单抗,而那些有克拉斯突变不能从治疗中获益4..
这些成功的例子验证了了解最有可能从靶向药物中受益的患者的遗传特征,并优先选择这些患者进行治疗的概念。然而,使用分子生物标记物来优化临床结果需要仔细评估它们在预后和治疗决策方面的作用。具体来说,将生物标志物准确区分为“预后”或“预测”,或将它们定义为两者,变得越来越重要。预后生物标志物可以被认为是一种独立于治疗干预(或缺乏治疗干预)的疾病自然史的衡量方法。5..来自随机临床研究的以人群为基础的注册或安慰剂/对照组适合于评估生物标志物的预后价值5..相比之下,一个预测性的生物标志物可以区分对治疗干预有特定反应或缺乏反应的组。为了确定哪些患者将从治疗中获益最多,以及获益多少,必须将生物标志物的预测价值与预后价值分离开来。为此,可以通过生物标志物状态和相互作用测试对实验和控制臂进行分层。在大多数情况下,建议对生物标志物进行前瞻性评估,而不是回顾性评估。
该审查考虑了将生物标志物谱系于表皮生长因子受体(EGFR)的疗效链接生物标志物谱对先进的Nonsmall细胞肺癌(NSCLC)的疗效以及最近发现的临床意义。
EGFR酪氨酸激酶抑制剂:NSCLC中的第一个靶向治疗
在非小细胞肺癌中,EGFR/HER1通路的激活导致一个促进肿瘤生长和进展的信号级联6..EGFR以大比例的NSCLC肿瘤表达7.,及其相关的信号转导通路经常失调。这些观察提供理显影的小分子酪氨酸激酶抑制剂(TKI)靶向EGFR,埃罗替尼吉非替尼和,以及EGFR靶向抗体,例如西妥昔单抗。
Gefitinib目前是全球最广泛使用的EGFR TKI。它具有先前用化疗治疗的患者的单孕激活8.那9.在Iressa肺癌生存评估(ISEL)的随机III期试验中,在二线和三线环境中,与安慰剂相比,Iressa没有延长生存期10..在一项大型III期研究中,与单药化疗相比,它并不逊于多西他赛,并改善了以前治疗过的患者的生活质量11.;在化疗初治老年患者的一个较小的,随机II期研究中,吉非替尼生活质量的提高,而不会无进展生存期(PFS)或OS递减,长春瑞滨相比12..一线加入吉替尼与顺铂和吉西他滨(Iressa NSCLC试验评估组合治疗(完整)-1)13.或卡铂和紫杉醇(完整-2)14.与单独的化学疗法相比,响应率(RR)或存活率没有显着差异。
Erlotinib是美国和欧洲联盟最广泛使用的EGFR TKI,并在先前治疗的NSCLC患者中显示出单孕抗肿瘤活性和症状改善15..相反吉非替尼,第二和第三线厄洛替尼显著改善OS与在BR.21 III期试验(安慰剂6.7相比相对4.7个月;危险比(HR)0.70;P <0.001)16..与吉非替尼的联合试验一样,厄洛替尼与一线化疗联合的III期试验(特罗凯肺癌调查和特罗凯联合紫杉醇和卡铂的反应(TRIBUTE))显示,厄洛替尼与对照组之间的生存期没有显著差异17.那18..最后,III期序批特罗凯(Sequential Tarceva in Unresectable, SATURN)试验评估了厄洛替尼与安慰剂在一线铂基双重化疗后未显示疾病进展的晚期NSCLC患者中的疗效。该试验显示,437名接受厄洛替尼治疗的患者与447名接受安慰剂治疗的患者相比,其无进展生存期(PFS)有显著改善相对17%;HR 0.71,95%CI 0.62-0.82;log-rank p <0.0001)19..
总而言之,吉替尼和厄洛替尼都被认为是在先前用化疗治疗的NSCLC患者中的活性单药疗法。当两种药物化学和尿动术时,BR.21和Isel试验结果之间差异的原因,可能是由于给药:Erlotinib在150 mg·日时给药-1,其最大耐受剂量(MTD),而吉非替尼的剂量为250 mg·天-1美国约为其MTD的三分之一至一半20..其他贡献因素可能是在两项试验中研究的人群的差异,包括最有可能响应的患者的发散代表性,以及二线患者的定义的差异,无论是患有渐进性的患者还是第一线疾病的患者治疗。
nsclc中的Egfr突变:Egfr tkis一线治疗的意义
患者的一部分尤为响应EGFR TKI。即使在早期研究中,显而易见的是,吉替尼和厄洛替尼与腺癌,从不吸烟者,来自东亚和女性的患者的患者相关的反应相关21..体细胞激活突变EGFR.现在已经确定了基因;这些突变赋予EGFR TKI介导的细胞死亡的易感性增加,并且可能在这些临床定义的群体中观察到的增加的响应22.-24..两个EGFR.外显子19缺失和外显子21 L858R替换,占所有已知EGFR激酶结构域突变的约90%25..
大量证据证明了重要性EGFR.决定哪些患者对厄洛替尼/吉非替尼治疗最有可能应答的突变状态。两项关于未选择人群中二线和三线EGFR TKI的回顾性研究,以及富集人群中一线EGFR TKI治疗的前瞻性研究已经发表(表1).在一些研究中,加权平均RR到EGFR TKI治疗突变阳性病例为78%,与大多数的系列报道中超过60%的RR。在突变阴性的情况下,相比之下,平均RR为10%38..这证明了EGFR突变与EGFR TKI治疗的反应相关。
上述研究包括的影响进行评估。EGFR.与历史控制相比,吉维特尼批准后生存的突变(EGFR.在GEFitinib批准之前被诊断和治疗的突变体)。之间的重要关联EGFR.吉非替尼显示了突变和延长生存期39..总之,这些研究表明,EGFR.突变状态可能是预测性生物标志物。此外,与外显子21 L858R点突变的患者患有外显子19缺失突变的患者的进展和增加的存活率40那41..除了证据EGFR.突变状态可能具有预测价值,来自随机对照试验的回顾性数据,包括完整和TRIBUTE研究结果,表明EGFR.突变状态也具有预后价值,患者患者窝藏EGFR.与那些没有,无论治疗组分配如何,突变都与那些没有的人相比,延长的存活42.那43..
前瞻性研究评估了第一线EGFR TKI对患者患者的疗效EGFR.突变。一个例子是Itarget试验,其中高级NSCLC窝藏的患者EGFR.突变(包括但不限于L858R和EXON 19缺失突变)获得了第一线Gefitinib30..98例患者筛选,34名患者EGFR.突变和31个接受吉替尼。RR,主要终点为55%;中位数PFS为9.2个月(95%CI 6.2-11.8个月)30..这项研究使用临床特征来丰富患者人口的人EGFR.突变阳性,证实与EGFR TKI的基因型定向治疗在美国人口,是可行的,其中的总频率EGFR.与亚洲人口相比,基因突变相对较少。
另一项关于晚期非小细胞肺癌的前瞻性研究由西班牙肺癌研究组进行,其中EGFR.选择突变来接收与厄洛替尼的一线治疗。从2105例患者肺部肿瘤进行筛选;EGFR.在350名(16.6%)中发现突变,其中217名艾尔洛替尼,其中113名患者接受Erlotinib作为一线治疗。在这些患者中,中位数PFS为14.0个月(95%CI 11.3-16.7个月)和Median OS为27个月。本研究队列表明患者的大规模筛查EGFR.EGFR TKIS的突变和定制治疗是可行的32..
在一起,上述研究表明,EGFR TKI在选定的患者中具有高度有效,与化疗相比,产生改善的反应率和PFS的治疗。这些研究的结果也支持该概念,在特定患者亚组中,用EGFR TKI的一线治疗可能是最有效的选择。一种潜在的随机研究,分辨于预测和预测价值EGFR.需要突变,并确定需要NSCLC患者的不同亚组的最佳治疗策略。最近,第一个这样的研究完成并发布。
第一线Gefitinib的Iressa Pan-Asia研究(iPass)的结果相对Carboplatin /紫杉醇在1,217名临床上选择高级NSCLC患者29.对临床实践有重要意义。符合条件的患者为组织学为腺癌的从不吸烟或轻度戒烟者;总的比率EGFR.437名可用组织患者的突变为59.7%。与化疗相比,Gefitinib具有优越的PFS,超过了试验的主要终点,这是表现出非事实的终点。分子亚组分析表明患者EGFR.P <0.001;处理通过与那些在化疗臂(HR 0.48; 95%CI 0.36-0.64相比突变具有优异的PFS在吉非替尼臂EGFR.突变状态相互作用测试,P <0.0001)29..从这项研究中一个重要的观察是从的肿瘤有野生型患者取EGFR.. 在这些患者中,所有患者都具有吉非替尼应答者的典型临床特征,与接受化疗的患者相比,接受吉非替尼的患者PFS显著下降(HR 2.85,95%可信区间2.05–3.98;p<0.001)29..这强烈地认为,突变试验应该成为诊断的标准实践,至少对于吸烟历史的腺癌患者,由于临床预测因子不足以优化治疗。如果肿瘤港口激活,这些患者应用一线EGFR TKI治疗治疗EGFR.鉴于显示的PFS益处,化疗应该是那些野生型患者的优选治疗EGFR..OS分析IPASS试用尚未完成。但是,其他研究支持其结论;例如,在较小的III期研究中,将第一线吉非替尼与Carboplatin /紫杉醇中已知的患者进行比较EGFR.中期分析显示,吉非替尼组突变阳性晚期非小细胞肺癌患者的PFS显著延长(10.4相对5.5个月;HR 0.4;日志排名P <0.001)44..最近发表的另一项III期试验也证实了这一点,该试验比较了一线吉非替尼与顺铂加多西紫杉醇治疗非小细胞肺癌患者的疗效EGFR.突变。与接受顺铂加多西他赛治疗的患者相比,吉非替尼组的中位PFS显著延长(9.2%)相对6.3个月;HR 0.489;日志排名P <0.0001)36..
值得注意的是,IPASS是亚洲研究,并激活EGFR.突变发生在高加索人群(分别〜40和〜10%),较低的频率。有些人认为,这可能在确定一线治疗前突变检测的吸收起到一定的作用,但它可以说,它在人口与突变的机会较少进行明确的测试是更重要的。除了其治疗选择的影响,IPASS还设置了收集和大型临床研究中的生物标志数据分析的新标准;这在今后的研究中对组织收集和分析具有重要影响。需要采取进一步的前瞻性临床试验来证实在研究人群是不完全的亚洲这些研究结果,验证了同样的趋势被认为是与其他化疗药物(如。培育率),并检查突变患者的化疗和EGFR TKI治疗的序列是否影响生存和其他结果。例如,在最近发表的回顾性研究中,包括152例NSCLC患者的外显子19缺失或L858R,那些接受一线吉非替尼的人比化疗治疗的患者显着更高的RR(76相对54%;p = 0.005)。然而,在化疗 - 幼稚和 - 预期的基团之间(P = 0.207和P = 0.804)之间的OS和PFS没有显着差异45..有重要的是要注意患者EGFR.与野生型患者相比,突变对化疗的RR也更高EGFR..一项III期开放标签研究证实了这一点,该研究调查了吉非替尼与卡铂加紫杉醇在非小细胞肺癌患者中的疗效。在这研究中,EGFR.显示突变阳性患者与伴有野生型患者的卡铂/紫杉醇化疗具有更高的物理RREGFR.(47.3相对23.5%)29..医生在决定是否采用一线和二线治疗时,需要同时考虑突变检测数据和患者的总体健康状况,直到有更确凿的证据;从长远来看,病人选择的数据也可能对欧洲国家的社会保障报销产生影响。除了这些考虑之外,EGFR TKIs开始治疗的时间需要澄清,在侵袭性疾病的情况下,等待结果可能是不合适的EGFR.突变测试。此外,由于大多数患者可能会在某种程度上接受与EGFR TKI的治疗,患者的风险EGFR.在选择一线治疗时,应始终考虑一线化疗的副作用,这些副作用可能导致无法进一步治疗,或在进展中出现新的转移。
抵抗EGFR TKIS:需要新一代靶向治疗
虽然患者EGFR.突变最初倾向于对厄洛替尼或吉非替尼有良好的治疗反应,长期使用这两种药物都会导致继发性耐药性,患者会经历复发或肿瘤进展25..
迄今为止,已确定两个主要机制是二次抵抗(图1).一个是在EGFR.基因,T790M47.那48.,这损害了该可逆的TKI厄洛替尼或吉非替到三磷酸腺苷结合的EGFR酪氨酸激酶口袋结合,使它们无效49..对吉非替尼/厄洛替尼产生获得性耐药的患者中约有50%出现T790M47.那50.. 一些研究表明,TKIs治疗只是选择耐药克隆,而不是导致突变发生。采用超灵敏等位基因特异性分析对27例转移性非小细胞肺癌患者的肿瘤组织进行分子特征分析,结果显示T790M水平较低EGFR.在38%的患者中存在。与在基线上没有可检测到的T790M的患者相比,T790M突变的存在与EGFR TKI治疗的显着更短的PFS相关,尽管它没有排除响应51..尽管已经鉴定出外显子19-21中的其他突变,但也赋予EGFR TKIs的抵抗力52.在美国,T790M是最常见的。
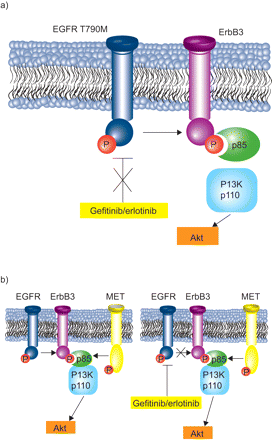
a) T790M突变阻止厄洛替尼/吉非替尼有效抑制表皮生长因子受体(EGFR)的磷酸化。b) MET扩增激活磷酸肌醇3-激酶(PI3K)信号通过erbb3,独立于EGFR。再现46.允许出版商的许可。
认为与EGFR的催化袋共价结合的不可逆TKI,以提供持续阻断EGFR信号传导,并且还可以保留对抗性突变的肿瘤的活性,例如EGFR T790M。几种这样的药剂是在临床开发中用于治疗各种肿瘤类型,包括EKB-56953.,CI-103354.,pf-0029980455.和Bibw 2992.56.(表2). 在非小细胞肺癌患者中,对这些药物进行研究至关重要EGFR.突变,无论是第一代TKI治疗naïve,如吉非替尼和厄洛替尼,以及通过之前的TKI治疗进展的患者。初步II期结果来自67名患有EGFR.接受BibW 2992作为第二线治疗的突变表明,66%达到了部分反应,51%的患者在12个月内无进展57..如果不可逆转的EGFR TKIS被证明是有效的或优于Gefitinib和Erlotinib,那么在治疗或预防获得的抵抗中定义它们的作用非常令人感兴趣。
获得抗性的第二个主要机制是MET放大,在∼20%的NSCLC患者对EGFR TKIs产生耐药性58..相容扩增激活磷酸盐3-激酶信号传导通过erbb3,独立于EGFR。这允许信令EGFR的下游,以继续进行,尽管EGFR抑制剂的存在59..虽然两者都可以在同一患者中同时发生,但相应的扩增是独立于T790M突变发生的58.那60..许多抑制MET或其配体(肝细胞生长因子)的治疗策略目前正在进行早期临床试验(表2)61..
总的来说,与EGFR TKIs和其他靶向下游或冗余途径的药物联合治疗可能具有相当大的临床潜力;mTOR(哺乳动物雷帕霉素靶点)抑制剂雷帕霉素和不可逆EGFR TKIs联合治疗已在临床前显示出活性体内EGFR L858R/T790M小鼠模型的实验研究62..
随着有关收购阻力对EGFR TKI中的分子机制的知识,临床意义,应考虑:将重复病人的治疗过程中需突变检测?如果是这样,重复活检需要或可以灵敏的方法来设计,使突变的血液样本中进行测试?其样本最翔实,那些从原发肿瘤或来自转移?以何种顺序应性治疗,以优化反应?其中代理是有效的,一旦第一代EGFR TKI的厄洛替尼和吉非替尼已不再有效?
EGFR.拷贝数非小细胞肺癌:一个更加开放的问题THANEGFR.突变
此外EGFR.已经研究了鉴定,用于鉴定可能与EGFR TKI治疗有益的患者的其他技术。这些最值得注意的是EGFR.荧光原位杂交(FISH),表明是否有整体增长EGFR.基因拷贝数63。FISH的结果已显示与吉非替尼或厄洛替尼敏感性的增加和生存率的增加有关63.-65..
BR.21和ISEL试验的结果表明,根据鱼类的基因拷贝数增加,与安慰剂相比,根据FISH的基因拷贝数增加了生存(BR.21 HR 0.43,95%CI 0.23-0.78(P = 0.004); ISEL HR 0.61,95%CI 0.36-1.04(P = 0.067))66.那67.. 然而,土星研究的生物标志物分析表明EGFR.根据FISH的拷贝数没有足够的预测能力,无法使厄洛替尼与安慰剂相比选择早期二线治疗患者68..此外,在随机试验中,将EGFR TKI与化疗进行比较,EGFR.FISH的基因拷贝数并不总是与TKI臂的改善结果相关(表3).最后,在Iressa NSCLC试验评估响应和生存与纳税机(兴趣)研究中,针对任何评估的任何生物标志物检测治疗臂之间的OS显着差异,包括EGFR.鱼,EGFR.突变比EGFR.FISH分析预测吉非替尼治疗患者的客观疗效和PFS70.
迄今为止,一项前瞻性临床试验为基于的吉替尼治疗患者EGFR.根据鱼复制数字。II期ONCOBELL研究的结果显示,在37名具有足够肿瘤组织进行分析的患者中,25名(69.4%)为非肿瘤患者EGFR.鱼阳性。患有的患者EGFR.FISH阳性状态有较显著高于RREGFR.FISH阴性患者(68.0相对9.1%;p <0.001)。EGFR.鱼阳性患者也比进展的时间明显更长EGFR.鱼类阴性患者(7.6相对2.7个月,分别;p值= 0.02)。这些数据表明,EGFR.鱼类分析确实可以预测对Gefitinib的反应71.
综上所述,EGFR.基因扩增EGFR.突变是一种常见的发现,通常影响突变等位基因72.可能是预测值EGFR.EGFR TKI有效性的鱼类更可能与其联系的结果EGFR.突变。在某些情况下,表皮生长因子受体蛋白过度表达可能导致EGFR.单独扩增,但其对EGFR TKI的反应的影响仍然是可扩张的。
克拉斯NSCLC中的突变:它们是否具有预测性或预后价值?
癌基因中的细胞突变克拉斯已与缺乏一些研究对EGFR TKI的初级反应有关。据认为,在密码子2,12,13的突变和61引到RAS蛋白,这可以允许肿瘤细胞生长的独立EGFR信号传导,并因此的组成型活化,使它们耐EGFR TKI中73.突变克拉斯在欧洲腺癌患者的~25%发生,尽管它们在亚洲患者中不太常见74.频率的增加克拉斯已显示突变与年龄,性别或吸烟历史有显着相关73.因此,仅通过观察临床特征来确定那些对EGFR TKIs治疗反应机会非常有限的患者并不是最好的选择,需要进行分子检测。
对br21研究中206例肿瘤的分析显示,15%的肿瘤密码子中有12或13个密码子突变克拉斯.这些患者似乎没有从奥罗替尼治疗中获得任何益处,而野生型患者克拉斯似乎获得了生存效益(HR0.69;p=0.03)67..在致敬的研究中,55患者中的55名(21%)患者克拉斯突变,以及那些克拉斯Erlotinib臂中的突变显着较短的操作系统,而不是唯一的化学疗法臂(HR 2.1,95%CI 1.1-3.8; P = 0.019)43..246例患者的初步结果是在非小细胞肺癌(无菌)队列中EGFR-TKIs施用EGFR-TKIS的前瞻性评估中,在预期评价中接受orlotinib患者。克拉斯突变对PFS没有显着影响,但对生存产生负面影响,而EGFR.与野生型相比,突变强烈预测PFS延长EGFR.,包括所有临床和分子标记物75.
作为EGFR.和克拉斯突变似乎是相互排斥的76-78,将这两个生物标志物定义为响应和抗EGFR TKI的预测因子的可能性通常被许多医生接受,尽管同时发生突变EGFR.和克拉斯在肿瘤中已经观察到很少43..
egfr抗体在非小细胞肺癌中的应用:等待一个预测性的生物标志物?
甲嘧胍以防止配体与EGFR细胞外结构域结合的人源化的单克隆抗体,在第一和二线设置中表明NSCLC中的NSCLC令人鼓舞的结果79-83.在ErbituX一线治疗肺癌(FLEX)研究中,西妥昔单抗联合顺铂/长春瑞滨(CV)的一项随机III期研究相对单独的CV单独治疗EGFR免疫组织化学患者(IHC) - 阳性先进的NSCLC,接受西妥昔单抗的患者均比单独接受CV的患者(初级终点)(11.3相对10.1个月;人力资源0.871;p = 0.044)。治疗组间无进展生存期无显著差异82.角色EGFR.拷贝数,克拉斯突变状态和EGFR.在FLEX研究IHC值最近报告84.无论从西妥昔单抗治疗的好处是既看到EGFR.复制编号,由FISH评估,或克拉斯突变状态84.目前,FLEX中只有一个临床特征与西妥昔单抗增加无进展生存率有关:皮疹的早期发生。然而,人们不认为EGFR.突变在西妥昔单抗活性中起着关键作用,正如它们在EGFR TKI治疗中所起的作用一样,与EGFR TKI的交叉耐药不太可能发生。
突变测试:需要标准化
取样和测试方法的标准化对于去除偏差至关重要,允许在试验中进行比较,并进一步了解哪些患者可能从特定治疗中受益。然而,这种努力因在最佳方法和实际限制方面缺乏共识而受到矛盾,包括组织可用性。向前发展,识别,标准化和验证采样和测试的方法至关重要,这些方法在广泛的医院实验室中可行,并创建基于证据的实践指南,以便于研究之间的测试结果比较。突变状态EGFR.通常由手术切除,活检或细针抽吸取样确定治疗开始前27.那85-88.虽然微创细针抽吸程序具有对患者的安全优势,但较大的组织样本,例如由核心活组织检查提供的组织样品,可能允许更具信息性和可靠的突变测试。进一步考虑是肿瘤异质性:仍然尚不清楚分离的活检样品是否真正代表整个肿瘤,以及从原发性肿瘤中取出的样品是否可以具有与转移位点不同的曲线。
如果在活组织检查样品中存在高次数的肿瘤细胞,直接测序以确定EGFR.突变状况被认为是黄金标准89. 当可用于PCR或RT-PCR的肿瘤材料有限时,基因组DNA测序的可行性受到限制。此外,直接测序技术相对昂贵且耗时。
病理保存中使用的固定剂和标本的年龄也会影响测序检测结果的质量。福尔马林固定可引起核酸降解、扩增子长度减少和PCR伪产物90.例如,在样品从第二和第三线厄洛替尼的BR.21试验中,大比例的分子分析EGFR.突变被误认为是不常见的新突变,这是由后验尸脱核细胞苷或腺嘌呤。这些小幅像差可以从低浓度的肿瘤DNA进行人工职务扩增,并且当分析小或旧样品时被解释为显着,而当使用较大量的肿瘤DNA时,这种脱胺位点被稀释,而未检测到89那91.
具有大比例非肿瘤细胞的活检样品更适合于等位基因特异性测定,但这些测定才可用于评估少量预定义突变的存在。基于PCR的测定通常是这里的优选选择,由于它们与直接测序相比的敏感性,特异性,鲁棒性和相对成本效益。因为基于PCR的测定寻找预定义变体,所以它们避免了组织微粉切除的耗时步骤和多轮DNA提取,使其在可接受的成本下临床环境中的常规用途。然而,基于等位基因的PCR基测试只能在所选的已知突变中扩增已知的突变EGFR.地区。已经发表的鉴定方法有很多EGFR.突变35.那51.那92那93.
目前正在开发新技术,以提高该技术的可行性EGFR.非组织样本的突变检测。非侵入性的测试EGFR.使用血清样本和捕获的循环肿瘤细胞的突变状态正在调查中51.那94.例如,SMart Amplification Process (SMAP)是一种基于单核苷酸多态性的诊断分析方法,可用于检测EGFR.血液样本的改变。法师等等。95适应了SMAP技术来定位激活三个已知热点EGFR.突变,在30分钟内直接从血液样本中识别突变具有高敏感性。此外,已经开发出突变特异性抗体,用于检测第19外显子缺失和第21外显子L858R突变,在NSCLC患者石蜡包埋的肿瘤样本中检测,显示出较高的敏感性和特异性96.为了简化EGFR.突变测试和缓解患者选择,一种选择是包含标准化的注册伴随诊断测试。
确保一致使用测试方法并鼓励在NSCLC中实现生物标志物的治疗方法仍有挑战。努力正在进行中:例如,法国国家癌症研究所实施了2年代,多期面,前瞻性研究(无菌)。本研究的主要目的是评估每个参与的16个中心进行生物标志物测定的能力,包括EGFR.外显子18-21和克拉斯外显子2测序石蜡包埋组织,如通过与这些外部分子参考实验室的中心之间结果的一致性来确定。试点阶段,在此期间,所有中心都熟悉了所涉及的测序技术后,前瞻性分析已开展肿瘤样本来自522 EGFR TKI初治患者与谁在这些中心接受厄洛替尼IV期非小细胞肺癌。该研究的这一部分的目的是评估的有效性EGFR.在识别可能受益于欧洲毒素治疗的患者中的测序75.
结论
已经建立的关于非小细胞肺癌的遗传分析和靶向治疗的证据目前的状态,我们可以得出什么临床意义?现在,EGFR TKI中不应该在不存在的一个给定为第一线治疗EGFR.变异测试。然而,我们现在可以现实地设想EGFR.突变的检测成为非小细胞肺癌的诊断标准的做法,尤其是在患者的合适临床预测,如never-也是前吸烟的患者。由于这种做法变得越来越普遍,重要的考虑因素包括测试和所使用的方法的标准化的定时;今后的努力应制定一个更实际的测试来指导EGFR.突变。适用于患有EGFR.突变,次级电阻的问题必须得到解决,并且必须被更清楚地定义在治疗范例化疗包括EGFR TKI中的序列。对于患者克拉斯突变,替代靶向治疗可能比EGFR TKIs更合适,需要进一步研究。对于两者都没有的患者EGFR.也不克拉斯突变,代表NSCLC患者的最大比例,还需要进一步研究建立最佳治疗方案。但是,很可能是,因为我们所学到的东西EGFR.在过去十年中,突变和EGFR TKIS,未来的目标疗法的发展将包括早期调查良好的响应者的基因型,并努力集中在限定受益于治疗中最多的特殊群体。
致谢
作者希望承认Ogilvy Healthworld医学教育的编辑辅助。
脚注
支持声明
Boehringer Ingelheim为Ogilvy Healthworld医学教育的帮助提供了财务支持。
兴趣表
所有作者的利益陈述都可以找到www.www.qdcxjkg.com/site/misc/statements.xhtml.
- 收到了2009年11月11日。
- 公认2010年5月6日。
- ©ers 2011.















