文摘
心血管的好处ω-3脂肪酸二十二碳六烯酸(DHA)等已经很成熟,但监管效果的DHA在肺动脉高压血管张力和压力在很大程度上是未知的。
DHA是一个强有力的监管机构的K+渠道,我们提出,DHA调节肺动脉平滑肌细胞的膜电位(PASMCs) K+渠道,从而发挥它对肺血管张力和压力的影响。
我们表明,DHA激活calcium-activated K存在剂量依赖的相关性引起的+(王者文化)目前在肺动脉的主要人类PASMCs和endothelium-dependent放松。这在王者文化血管扩张明显减少- / -(Kcnma1- / -老鼠)。在活的有机体内,DHA急性右心室收缩压慢性低氧诱导的肺动脉高压动物模型常氧水平的动物。有趣的是,在特发性肺动脉高血压王者文化渠道及其子单元调节。DHA激活王者文化频道在这些人类PASMCs hyperpolarised特发性肺动脉高血压PASMCs的膜电位的PASMCs从健康的捐赠者。
我们的发现表明DHA激活PASMC王者文化渠道导致肺动脉高压血管舒张。这种效应可能会提供一个分子的解释之前从未描述DHA作为急性血管舒张肺动脉高压的作用。
文摘
王者文化渠道增加改建肺动脉的DHA IPAH可能是一个治疗的机会http://ow.ly/rTUl300pn7R
介绍
肺动脉高压(PAH)是一种罕见的,威胁生命的疾病的肺部血管的特点是一个进步的肺血管阻力增加,最终,右心室衰竭。内源性血管扩张性因素和肺血管扩张的能力是主要的贡献者疾病的病理特点,和血管舒张药的疗效对多环芳烃(1,2]。在正常生理条件下,肺循环是低压,低阻系统。肺血管的低血管张力的静止膜电位在很大程度上是由肺动脉平滑肌细胞(PASMCs),主要但不限于由K+电导(3- - - - - -5]。因此,两个K的变化+频道活动和表达有直接影响PASMCs静止膜电位,从而影响肺血管的基调。有迹象表明从文学PASMCs特发性肺动脉高压(IPAH;从前主肺动脉高压)患者可能有更消除膜电位(它们长期动摇)导致血管收缩和重塑6),尽管数据底层这个假设很稀疏。先前的研究表明,内源性血管活性的物质(如。endothelin-1 (ET-1),血管紧张素ⅱ和5 -羟色胺)(7,8),缺氧或药物(达沙替尼和培高利特)(9- - - - - -11)参与了肺动脉高压的病理生理学引起膜两极化PASMCs K的抑制+渠道,导致血管收缩。因此,代理激活K+通道电流(一氧化氮,iloprost或treprostinil)引起膜hyperpolarisation PASMCs,导致血管舒张(12]。
大规模流行病学研究和随机对照试验证明,ω-3脂肪酸(二十碳五烯酸、二十二碳六烯酸(DHA)和α-linolenic酸)显著减少心血管疾病事件的发生在冠状动脉疾病患者13]。因此,美国心脏协会指南建议定期食用ω-3脂肪酸(14]。此外,食用鱼油降低肺动脉高压和血管重塑在慢性低氧诱导的肺动脉高压(15]。然而,有一个持续需要调查研究分子机制来解释脂肪酸对肺循环的有益作用。DHA阻止自由ET-1引起的细胞内钙的增加,抑制PASMC增殖(16]。此外,我们先前的研究提供了一个潜在的分子事件的综合分析这些长期的抑制效应,并表明,DHA提示calcium-dependent氧化应激导致的蛋白质反应在人类主要PASMCs从而抑制扩散的17,18]。calcium-dependent K的DHA是一种有效的催化剂+(王者文化)通道电流在大鼠冠状动脉平滑肌细胞,促进冠状动脉扩张孤立小(19,20.]。DHA是可逆激活large-conductance王者文化(BKCa)通道组成的造孔Slo1亚基(Kcnma1)和辅助单元β1 (Kcnmb1) [21]。然而,详细的机制这一重要的急性影响脂肪酸肺循环和肺动脉高压仍不明朗。
在这项研究中,我们提出,DHA激活K+渠道PASMCs导致hyperpolarisation静止膜电位和逆转的肺动脉高压。本研究检测了急性DHA在肺循环的影响,特别是在K+人类PASMCs通道功能和膜电位在初级。我们也解决了DHA的影响在肺动脉压(PAP)肺动脉高压的小鼠模型。使用BKCa (Kcnma1- / -)基因敲除小鼠,我们调查的具体贡献王者文化渠道DHA在肺循环的影响。此外,我们利用compartment-specific分析通过激光捕获显微解剖和研究BKCa渠道和亚基的表达在肺动脉获得IPAH病人和健康的捐赠者。最后,我们验证了DHA的影响,观察到的在活的有机体内和在体外研究,主要人类PASMCs孤立IPAH病人和健康的捐赠者。我们发现从IPAH PASMCs明显动摇和DHA正常化这个两极化通过激活的王者文化。
材料和方法
详细的材料和方法可在网上补充材料。
人类从IPAH PASMCs和捐赠组织的隔离
所有研究IPAH患者和供体组织样本参与本研究伦理委员会批准的维也纳医科大学,奥地利和从所有参与者获得的书面知情同意。肺组织取自IPAH经历了肺移植的患者在胸外科,维也纳医科大学。Nontransplanted收获了移植的供体肺,但未使用(如。因为size-reduced肺移植),担任控制。部分样品在液氮snap-frozen或固定在4% (w / v)甲醛激光显微解剖组织学或组织,分别。主要PASMCs从病人和隔离电阻肺动脉PASMCs是如前所述的描述(10]。供体的临床特征和患者研究中使用表1。
动物研究
当地政府批准的所有实验都是根据国家规定为动物实验(奥地利教育部、科学和文化;bmwf - 66.010/0076 - 2 / 3 b / 20116)。
统计分析
给出了数值意味着±扫描电镜。统计分析了使用棱镜5 (GraphPad、圣地亚哥、钙、美国)。的Mann-Whitney紫外线测试是用于非参数数据。采用配对t检验来评估右心室收缩压的变化(RVSP)预处理和post-DHA注入。的组间差异,单向方差分析是评估图基的紧随其后事后测试。假定值< 0.05被认为是具有统计学意义。
结果
人类PASMCs DHA主要激活王者文化频道
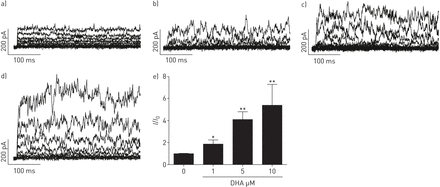
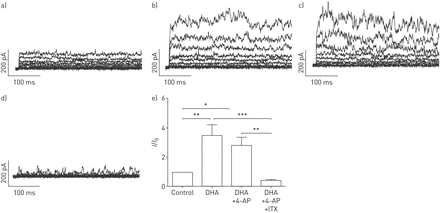
DHA显著和可逆增强全细胞K+当前记录从一个持有-20 mV的潜力在人类PASMCs剂量依赖性的方式(图1)。接下来,为了解决当前激活的来源,不同的K+通道抑制剂。DHA的增强并不影响voltage-activated K+通道抑制剂4-aminopyridine (4-AP 5µM;图2 d),但被废除的王者文化通道抑制剂Iberiotoxin(财年100海里;图2 d)。相对K的变化+当前的振幅(我/我0归纳了造成的DHA图2 e。很明显,减少了被4-AP明显大于,财年和分数的变化没有显著变化有无4-AP录音。我们的研究结果表明,DHA-activated目前主要是来源于人类PASMCs王者文化频道。
二十二碳六烯酸(DHA)剂量依赖性激活全细胞K+当前在人类肺动脉平滑肌细胞(PASMCs)。原来的全细胞K+电流跟踪了)没有浓度增加和b) 1 c) 5和10 d)在人类PASMCsμM DHA。e)总结相对large-conductance王者文化(BKCa)通道电流(我/我0)增加人类PASMCs DHA在初级的浓度。在每个设置n = 4 - 6。*:p < 0.05;* *:p < 0.01。
二十二碳六烯酸(DHA)激活large-conductance王者文化频道(BKCa)在人类原发性肺动脉平滑肌细胞(PASMCs)。原来的全细胞K+当前跟踪了)没有DHA和b), c)和电压门控钾DHA+通道阻滞剂4-aminopyridine (4-AP)和d) DHA以及电压门控K+通道阻滞剂4-AP和BKCa通道阻滞剂Iberiotoxin人类PASMCs(财年)在初级。e)总结王者文化的相对变化电流(我/我0人类PASMCs DHA)引起的主。在每个设置n = 5 - 6。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
DHA诱发快速endothelium-dependent肺放松
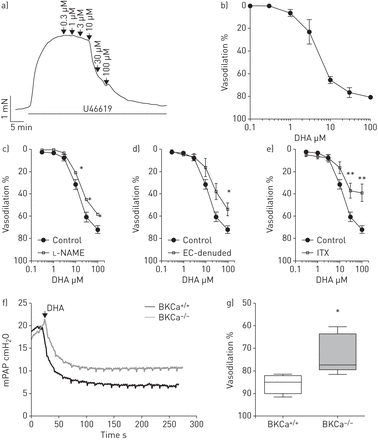
探讨人类PASMCs相关性的观察在体外肺动脉的语气,我们确定了DHA对孤立的语气pre-constricted肺动脉。与钢丝myography等长张力测量,执行,表明DHA诱发强烈的放松对肺内的动脉存在剂量依赖的相关性与U46619 pre-constricted (图3一)。DHA是浓度的放松效果最大有效浓度(EC的一半50)3.5µM (n = 6;图3 b)。接下来,我们也调查了作用的内皮DHA-mediated肺血管舒张。一氧化氮合成酶抑制剂的就业l- name (l- - - - - -NG-nitroarginine甲酯,n = 3;图3 c)或内皮剥蚀(n = 4;图3 d)大鼠肺动脉血管扩张性反应显著降低浓度增加DHA相比,对照组(n = 6)等长张力测量。接下来,我们调查的角色BKCa频道DHA-induced放松。在BKCa通道阻滞剂财年的存在(n = 4;图3 e),大鼠肺内的动脉展示出显著降低常与控制(n = 6)相比增加浓度的DHA。此外,我们调查的规定人民行动党DHA的完整的肺。在体外DHA的模型,模型包括鼠标肺,政府本身没有改变基底意味着PAP(肺动脉平均)(在线补充图S1A)。当肺部受到U46619 DHA应用程序之前,DHA(10µM)的深刻的下降导致肺动脉平均(11.6±0.9,n = 6)(在线补充图印地)。破译的角色王者文化频道的功能反应肺血管舒张DHA,老鼠缺乏的α-subunit large-conductance王者文化(BKCa- / -)及其野生型(BKCa+ / +)被孤立的灌注小鼠肺癌模型(图3 f)。的U46619-induced pre-tone并不缺乏BKCa通道的影响。然而,DHA-induced肺血管舒张BKCa明显衰减- / -老鼠与BKCa相比+/+老鼠(73±4%与每组86±2%,n = 5;图3 g)。
二十二碳六烯酸(DHA)导致endothelium-dependent在肺内的动脉血管舒张。)代表在一个孤立的小鼠肺内的动脉张力记录添加剂浓度的DHA与U46619 pre-constriction的设置。b)累积浓度常DHA对肺内的动脉。放松pre-constricted分离大鼠肺内的动脉在应对浓度增加DHA /没有c)l- name (n = 3), d)内皮细胞(EC) (n = 4)或e) Iberiotoxin(财年)(n = 4)。的血管舒张的百分比表示相对于U46619的最大响应。BKCa血管扩张性效果DHA-induced受损- / -老鼠。f)代表平均肺动脉压(肺动脉平均)从BKCa轮廓+/+和BKCa- / -老鼠在孤立,肺灌注通风模式。g)急性血管扩张性效果的DHA U46619 pre-tone BKCa+/+和BKCa- / -老鼠。数据作为中位数、四分位范围和最大和最小值。每组(n = 5。*:p < 0.05;* *:p < 0.01。
DHA会导致快速在低氧诱导肺动脉高压肺血管舒张
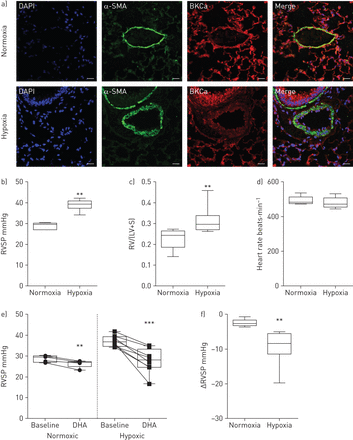
来洞察急性DHA的应用程序是否展品vasorelaxing效果在一个类似人类疾病动物模型,涉及肺血管重塑,我们使用了慢性缺氧肺动脉高压的小鼠模型。BKCa渠道的存在证明了肺动脉双immunolabellingα-smooth肌肉肌动蛋白(α-SMA)阳性细胞和BKCa通道控制(常氧)动物和改建肺动脉hypoxia-treated老鼠(图4一)。抗体特异性研究与特定的阻断肽和BKCa染色在肺组织执行+/+或BKCa- / -老鼠(在线补充图S3A和B)。确认动物开发肺动脉高压,RVSP是正确衡量心脏catheterisation (图4 b),而心率没有不同组(图4 d)。其次是测量右心室肥厚,右心室是完全从左心室解剖和隔膜。心室分离量体重,获得左心室的右心室的比例加隔(图4 c)。注入一个DHA丸的影响到中央静脉,曝露在小鼠心脏catheterisation是正确检测到。图4 e显示了显著减少RVSP DHA后应用在常氧和缺氧组。然而,DHA的影响更明显缺氧组相比,动物在normoxia (−9.4±1.7与−2.5±0.4毫米汞柱,n = 8与5;图4 f)。hypoxia-treated老鼠DHA后应用RVSP降至37±0.9到27.2±2毫米汞柱(n = 8),返回RVSP慢性疾病模型保存在normoxia水平的老鼠。因此,我们的研究结果表明,DHA-induced通过激活王者文化渠道发生血管舒张肺动脉高压模型。
二十二碳六烯酸(DHA)诱导增强小鼠的肺血管舒张肺动脉高压模型。a)的双重免疫荧光染色常氧和慢性缺氧小鼠肺显示存在large-conductance王者文化(BKCa)通道(红色)和α-smooth肌肉肌动蛋白(α-SMA;在肺动脉绿色)。DAPI: 4′, 6-diamidino-2-phenylindole。酒吧规模:20µM。b)右心室收缩压(RVSP), c)右心室肥大(右心室(RV)完全切割的左心室(LV)和隔膜(S))和d)心率常氧和缺氧的老鼠。e) RVSP前(基线)和后一丸DHA政府在常氧和慢性hypoxia-treated老鼠。f)总结RVSP常氧和缺氧小鼠DHA的变化。数据作为中位数、四分位范围和最大和最小值。n = 5和8 normoxia和缺氧。 **: p<0.01; ***: p<0.001.
DHA的原因hyperpolarisation PASMCs获得IPAH患者
从DHA的有益作用在动物模型中,接下来,我们检查了DHA的影响主要人类PASMCs从IPAH获得病人和健康的捐赠者。双immunolabelling显示BKCa渠道在肺动脉平滑肌层的健康供体肺和改建IPAH患者的肺动脉(图5一个)。
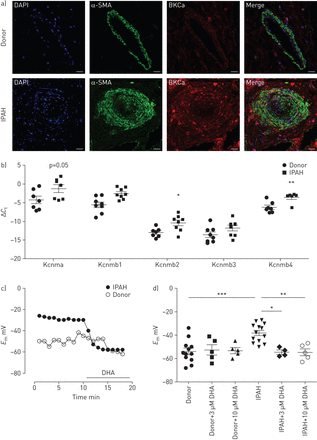
二十二碳六烯酸(DHA)导致肺动脉平滑肌细胞hyperpolarisation (PASMCs)获得特发性肺动脉高压(IPAH)患者。一)双重免疫荧光染色法显示的本地化large-conductance王者文化(BKCa)通道(红色)和α-smooth肌肉肌动蛋白(α-SMA;绿色)肺动脉的捐赠者和IPAH人类肺部。DAPI: 4′, 6-diamidino-2-phenylindole。酒吧规模:50µM。b)的表达与α-subunits BKCa渠道(Kcnma)及其β-subunits (Kcnmb1-4)激光microdissected肺附庸风雅的捐赠(n = 7或8)和IPAH (n = 6或8)患者。膜电位(c)代表E米)跟踪从捐赠者和IPAH PASMCs急性DHA曝光。d)总结与DHA含量增加,膜电位的变化没有DHA,捐赠者和IPAH PASMCs。提出了数据,b, d)作为单独的分意味着±扫描电镜。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
BKCa通道的表达是研究激光microdissected从健康的捐赠者和IPAH患者肺动脉。IPAH患者的肺动脉显示明显upregulation BKCa通道α-亚基(Kcnma1),以及β-subunits (Kcnmb1 Kcnmb2和Kcnmb4) (图5 b),而Kcnmb3保持不变。然后我们探讨了DHA的膜电位的影响主要从两组获得的人类PASMCs。一个代表性的记录(图5 c)表明,急性灌注静止膜电位的DHA hyperpolarised IPAH PASMCs,但并不影响PASMCs从健康的捐赠者。值得注意的是,从IPAH PASMCs患者的膜电位明显动摇而PASMCs从健康的捐赠者(−38.1±2.2与−54±2.8 mV, n = 12和13;图5 d)。我们进一步分析显示,急性DHA管理局(3和10µM)并没有改变捐赠PASMCs膜电位的控制。相比之下,暴露在DHA逆转的两极化PASMCs IPAH患者(−54.5±1.8 mV后3µM DHA与−38.1±2.2 mV基准,n = 4和−54.6±2.9 mV后10µM DHA与−38.1±2.2 mV基准,n = 5;图5 d的水平),返回它健康的捐赠者。这些数据表明,DHA对选择性和直接影响人类PASMCs动摇。
讨论
我们报告的作用DHA作为一个王者文化频道活化剂在肺循环和肺动脉高压模型的急性效应以及IPAH样本。我们的研究表明,急性DHA政府迅速激活全细胞K+当前在人类主要PASMCs和显示,这种激活当前绝大多数源于王者文化通道,而不是从电压门控K+频道。王者文化通道激活摄入量有关,减少肺血管张力,导致endothelium-dependent和独立的肺血管舒张通过BKCa渠道孤立pre-constricted肺内的动脉。内皮的相对贡献与PASMC BKCa渠道在这常DHA仍有待确定。此外,DHA显著降低人民行动党增加U46619隔离灌注肺;然而,它并没有改变基线PAP。DHA-induced血管舒张的影响是BKCa显著降低- / -老鼠,这表明DHA是介导的急性肺血管扩张性效果,在某种程度上,通过激活BKCa渠道。重要的是,在慢性缺氧肺动脉高压小鼠疾病模型在活的有机体内、急性DHA应用程序返回右心室收缩压水平控制动物,证明DHA是一种强有力的血管舒张肺动脉高压。此外,我们观察到的upregulation BKCa渠道改建IPAH患者的肺动脉。符合这些发现,我们也证明了DHA hyperpolarised膜电位的主要人类PASMCs IPAH病人,这是消除基线,但不是从健康的捐赠者。
血管张力的肺动脉是由PASMCs;生理(放松)条件下相对稳定的膜电位,主要是由K+渗透率,尽管氯电导不应被忽视的(5,22]。因此,膜电位是一个至关重要的血管张力控制器:膜电位/血管张力坡度很陡。因此,即使是小膜电位的变化几毫伏导致血管直径显著变化。任何生理或药理代理人改变膜电位会显著改变压力。因此,很明显,膜hyperpolarisation,通过激活K+频道,是一个强大的机制来降低压力通过血管舒张。王者文化频道,建造的造孔α-subunit (Kcnmb1)以及辅助β-subunits (Kcnmb1-4)被发现在几乎所有类型的平滑肌细胞,并导致一个令人印象深刻的hyperpolarisation和血管舒张活性(23,24]。除了增加细胞内钙2 +浓度和两极化,最强大的机制来激活王者文化通道介导的磷酸化的营地——或者cGMP-dependent蛋白激酶(蛋白激酶或G) [12,25,26]。这是非常重要的王者文化的生理功能和在战斗中提供了强大的药理工具对肺动脉高压,如前列腺素类,phosphodiesterase-5抑制剂或可溶性guanylyl环化酶催化剂开发他们常认为影响部分通过激活的王者文化。
BKCa通道表达和功能已被证明是提高慢性缺氧小鼠和PASMCs [27,28]。在演唱会与肺动脉高压模型,第一次,我们已经表明,BKCa通道和β-subunits调节改建肺动脉laser-captured得到的显微解剖IPAH病人。因此,人类PASMCs BKCa渠道可能会提供DHA的目标设置的慢性血管收缩,并可能作为一种反馈通路控制膜两极化的程度和血管收缩如模型(在线补充图S4)。
DHA是ω-3脂肪酸的主要部件之一,主要是通过饮食摄入的海洋食品。其有利影响人类健康的出现在流行病学研究和临床试验主要推荐的啊哈DHA的经常食用鱼或作为膳食补充剂预防心血管事件(14,29日]。DHA的慢性效应及其代谢衍生物在肺循环PASMCs和增生性表型的调查在体外研究证明了人类PASMC增殖DHA的抵抗能力增强,肺动脉重塑的一个标志30.]。慢性DHA治疗抑制细胞外signal-regulated激酶激活和引发了一场展开的蛋白质反应导致周期阻滞和细胞凋亡诱导17]。此外,一个早期的研究表明,DHA和刺激g蛋白耦合结合受体GPR120 EC50∼10μM [31日),表明潜在的新DHA的免疫调节效应的机制。此外,一项研究关注DHA-induced平滑肌建议DHA的变化,通过分解代谢产品,可能会导致ρ激酶途径,减少钙敏感性[32]。
相比之下,DHA的急性影响最近才被调查。DHA在肺循环的影响,研究了在急性低氧环境中,BKCa渠道的缺氧抑制政府被推翻的DHA (33]。此外,DHA暴露引起基底基调,从而迅速减少体循环血管舒张,建议直接DHA对K的影响+渠道导致hyperpolarisation的平滑肌细胞膜,因此血管舒张(21]。事实上,Hoshi等。(34)提供的证据的直接绑定DHA的孔状Slo1和辅助β1-subunits large-conductance王者文化表达人类胚胎肾细胞。我们的观察与研究表明DHA直接作用于王者文化频道活动以膜片钳,当王者文化通道,监管机构就会受到抑制,王者文化通道的激活在人类PASMCs依然没有改变(在线补充图S2A)。相比之前的发现在体循环,在我们的研究中DHA的基底肺动脉的语气并不影响模型包括老鼠肺部,老鼠一直在normoxia,减少急性DHA-induced RVSP很小。然而,在pre-constriction的肺动脉体外模型以及在活的有机体内小鼠模型的肺动脉高压,DHA诱导肺动脉压力下降,表明选择性DHA对肺血管收缩的影响。pre-constricted,隔离灌注肺的BKCa基因敲除小鼠DHA继续引起血管舒张,这表明它有额外的血管舒张药性质。因此,DHA之前已经报道过的事实作为一个强大的体循环血管舒张药,但未能改变系统性血压BKCa基因敲除小鼠,表明DHA的效果很大程度上取决于特定的细胞环境和基底的水平两个脉管系统(21]。最后,它最近报道,脂质灌注含有ω-3多不饱和脂肪酸形成一个强有力的和持续的血管舒张,长期检测胎儿羔羊的肺动脉高压模型(35]。目前的研究是符合这个,从而能够进一步证明DHA的相关性作为急性血管舒张药当人民行动党增加。
使用体外和在活的有机体内肺动脉高压的动物模型,结合调查在激光microdissected改建肺动脉和膜片钳研究孤立PASMCs IPAH患者我们进行详细的实验描述和提供分子见解DHA-induced血管舒张肺动脉高压。我们所知,这是第一个研究表明DHA展品迅速减少肺血管张力和压力升高。这种减少是通过PASMCs王者文化通道激活通过直接调制膜电位导致血管舒张。我们还表明,激活王者文化频道的DHA有利于建立肺动脉高压模型,更重要的是,这只DHA hyperpolarises PASMCs获得IPAH病人,不控制PASMCs。此外,我们发现人类IPAH BKCa渠道,增加的效用药理干预王者文化开启设备的多环芳烃。因此,我们建议,DHA是一种有效的血管舒张药通过王者文化通道激活在肺动脉高压。增加表达式IPAH王者文化频道的病人可能会进一步关注利息DHA作为一个潜在的肺动脉高压的治疗选择。
确认
我们非常感谢玛利亚海伦Schloffer,西蒙尼·迪和伊丽莎白Blanz(实验麻醉学,麻醉和重症监护医学部门,格拉茨医科大学的格拉茨,奥地利)为他们的优秀的技术支持。
脚注
可以从本文的补充材料www.qdcxjkg.com
支持声明:A.L. Meredith支持国家心脏,肺和血液研究所(批准号:HL102758)。为这篇文章一直存放在资助信息FundRef。
利益冲突:披露可以找到与这篇文章www.qdcxjkg.com
- 收到了2015年11月3日。
- 接受2016年5月14日。
- 版权©2016人队