摘要gydF4y2Ba
血浆循环无细胞DNA (cf)在肿瘤学中引起了人们的兴趣,因为它已被证明含有肿瘤DNA,因此可以用作液体活检。在非小细胞肺癌(NSCLC)中,cfDNA定量已被提议用于患者的监测和随访。然而,现有的研究是有限的,需要通过更大样本量的研究来证实,并包括接受更多同质治疗的患者。我们的目的是评估血浆cfDNA浓度在大量接受标准化疗方案治疗的非小细胞肺癌患者中的预测和预后价值。gydF4y2Ba
我们将肺癌患者的样本纳入了Pharmacogenoscan研究。提取218例患者的cfDNA,并在铂类化疗前后进行荧光定量分析。基线和化疗后浓度与RECIST(实体肿瘤反应评价标准)评估的治疗反应或患者生存之间的关系进行了分析。gydF4y2Ba
基线时cfDNA浓度高(最高分位数)的患者的无病生存期和总生存期明显差于浓度较低(最低和中等分位数)的患者(中位总生存期为10个月(95% CI 10.7-13.9))。gydF4y2Ba与gydF4y2Ba14.2个月(95% CI 12.6-15.8);p = 0.001)。在多变量分析中,cfDNA基线浓度升高是一个独立的预后因素。然而,我们没有发现cfDNA浓度与治疗反应之间的任何关联。gydF4y2Ba
cfDNA可能是评估非小细胞肺癌预后的生物标志物。然而,cfDNA的总浓度似乎不能预测化疗反应。gydF4y2Ba
摘要gydF4y2Ba
总游离细胞DNA与晚期非小细胞肺癌化疗反应无关gydF4y2Bahttp://ow.ly/QpqyxgydF4y2Ba
介绍gydF4y2Ba
肺癌是世界上最主要的癌症致死原因[gydF4y2Ba1gydF4y2Ba]。它通常在晚期或转移期被诊断出来,因为在大多数患者中,局部和区域传播在很长一段时间内仍无症状。晚期肺癌的预后非常差,转移期的5年生存率不超过5% [gydF4y2Ba2gydF4y2Ba]。主要的预后因素是疾病分期、体能状况、诊断时年龄、对一线化疗的反应、血浆乳酸脱氢酶水平以及是否存在靶向治疗的基因或途径中的体细胞突变或重排(如表皮生长因子受体(EGFR)或间变性淋巴瘤激酶)[gydF4y2Ba3.gydF4y2Ba,gydF4y2Ba4gydF4y2Ba]。晚期的治疗基于细胞毒性化疗和靶向治疗[gydF4y2Ba5gydF4y2Ba]。使用计算机断层扫描(CT)评估对治疗的反应,使用RECIST(实体肿瘤反应评估标准)标准[gydF4y2Ba6gydF4y2Ba]。到目前为止,还没有可靠的生物标志物来评估肺癌对标准化疗的反应,需要更多的预后因素来管理晚期非小细胞肺癌(NSCLC)患者。gydF4y2Ba
循环无细胞DNA (cf)最近因其作为肿瘤生物标志物的潜在用途而重新受到关注。gydF4y2Ba7gydF4y2Ba]。cfDNA对应于血液中循环的无细胞DNA片段,可以从血浆或血清中提取。它被认为是通过坏死、凋亡或有核细胞(如淋巴细胞)的活跃分泌在血液中释放的。cfDNA主要由组成型基因组DNA组成。几种情况可能与cfDNA浓度增加有关,包括炎症、组织创伤和癌症[gydF4y2Ba8gydF4y2Ba,gydF4y2Ba9gydF4y2Ba]。在癌症中,很大一部分cfDNA来自肿瘤细胞,cfDNA浓度反映了肿瘤负荷[gydF4y2Ba10gydF4y2Ba]。此外,cfDNA可能来源于循环肿瘤细胞,因此可能反映了微转移性疾病和疾病的侵袭性潜力[gydF4y2Ba9gydF4y2Ba]。gydF4y2Ba
据推测,cfDNA可能是肿瘤反应的预测因素,也是预后因素的良好候选因素。在肺癌患者中,一些研究表明cfDNA浓度可能是肿瘤对手术和放射治疗反应的预测因素[gydF4y2Ba11gydF4y2Ba,gydF4y2Ba12gydF4y2Ba],但很少有研究将cfDNA浓度作为肿瘤对化疗反应的预测因素。这些研究包括少量样本,结果相互矛盾[gydF4y2Ba13gydF4y2Ba–gydF4y2Ba15gydF4y2Ba]。对cfDNA预后价值的研究也显示出相互矛盾的结果[gydF4y2Ba11gydF4y2Ba,gydF4y2Ba13gydF4y2Ba]。gydF4y2Ba
在这里,我们评估了cfDNA浓度对接受铂类化疗的非小细胞肺癌患者肿瘤反应和生存的预测和预后价值。gydF4y2Ba
材料与方法gydF4y2Ba
人口gydF4y2Ba
本研究纳入的患者来自法国Pharmacogenoscan研究。Pharmacogenoscan是在法国Rhône-Alpes-Auvergne地区的六家医院进行的前瞻性队列研究。其目的是确定与非小细胞肺癌患者预后相关的生物学和组织学因素。主要目的是确定特定生物标志物与疾病控制率之间的关联。次要目的是确定与患者生存相关的生物标志物。所有患者都签署了知情同意书。Pharmacogenoscan研究的初步结果已在其他地方报道[gydF4y2Ba16gydF4y2Ba,gydF4y2Ba17gydF4y2Ba]。gydF4y2Ba
药理学扫描研究的纳入标准如下。1) 2005年7月至2010年8月在6个参与中心之一连续诊断为非小细胞肺癌的患者;2)癌症可以是任何阶段,但愿意接受以铂为基础的双重化疗,作为转移性或复发性疾病的新辅助治疗或一线治疗(双重药物由研究者选择);3)纳入时东部肿瘤合作组(ECOG) 0-2绩效状况[gydF4y2Ba18gydF4y2Ba]。gydF4y2Ba
所有患者在接受任何癌症治疗前和第一反应评估时都进行了血液采样,第一反应评估是在研究者选择的两到三个周期的铂类化疗后进行的。采用RECIST标准评估化疗反应[gydF4y2Ba6gydF4y2Ba]。gydF4y2Ba
从pharmacogenscan数据集中,我们将纳入的非小细胞肺癌患者限制在化疗前后收集可用血浆样本,并进行可用的RECIST反应评估[gydF4y2Ba19gydF4y2Ba]。此外,我们选择将纳入限制在IIIB-IV期。事实上,我们之前已经表明,cfDNA浓度与分期有关[gydF4y2Ba10gydF4y2Ba]。gydF4y2Ba
法国格勒诺布尔大学医院(Grenoble, France)伦理委员会批准了Pharmacogenoscan研究(gydF4y2BaNCT00222404gydF4y2Ba)。本辅助研究已获得国际癌症研究机构(IARC)伦理委员会(IEC 14-04)批准。gydF4y2Ba
等离子体cfDNAgydF4y2Ba
静脉血在基线(第一个化疗周期之前)和第一次CT扫描反应评估(发生在第二或第三个化疗周期之后,取决于中心,但在任何情况下都是在最后一个周期后3周)中收集。样品离心(~ 590x)gydF4y2BaggydF4y2Ba15分钟(室温下),采血后4小时内。分离等离子体,保存于- 80°C。所有血浆样本集中存放在格勒诺布尔大学医院。本研究使用的样本是按照国际标准用干冰从格勒诺布尔运到国际癌症研究机构的。gydF4y2Ba
按照制造商的说明,使用QIAamp循环核酸试剂盒(Qiagen, Valencia, CA, USA)从血浆样品中提取cfDNA。用50µL超纯水(分子生物学级无菌水;Eppendorf, Hamburg, Germany),在定量前将分离的cfDNA保存在- 20°C。gydF4y2Ba
cfDNA定量采用PicoGreen dsDNA试剂盒(Molecular Probes, Eugene, OR, USA),采用荧光法。在Fluoroscan Ascent FL荧光计(Thermo Fisher Scientific Oy, Vantaa, Finland)中分别以538 nm和485 nm波长读取板,用于发射和激发。通过连续稀释λ-DNA原液(由制造商提供)获得标准曲线。减去空白值,从标准曲线上测定血浆DNA浓度。gydF4y2Ba
进行DNA定量的研究人员对患者的临床结果一无所知。gydF4y2Ba
统计方法gydF4y2Ba
对所有连续变量使用Kolmogorov-Smirnov检验检验正态分布的假设。正态分布变量以平均值±表示gydF4y2BasdgydF4y2Ba;非正态分布变量表示为中位数(四分位间距(IQR))。对于非正态连续变量的比较,我们对两个相关样本使用了Wilcoxon检验,对两个或多个独立样本分别使用了Mann-Whitney u检验和Kruskal-Wallis检验。分类变量用百分比表示。使用Spearman ρ评估相关性。gydF4y2Ba
对于生存分析,我们使用Kaplan-Meier方法,中位生存(和相应的95%置信区间)使用log-rank检验进行比较。然后,我们使用Cox回归模型(进入法)来评估与生存相关的变量。首先在单变量分析中设置模型,然后用相关变量和/或单变量分析中发现的显著变量调整模型。gydF4y2Ba
所有检验均为双侧检验,p<0.05。Cox模型采用p<0.1。统计学分析采用SPSS(19.0版本;IBM,阿蒙克,纽约州,美国)。gydF4y2Ba
结果gydF4y2Ba
人口gydF4y2Ba
在2005年至2010年的Pharmacogenoscan研究中招募的537名患者中,218名患者符合本研究的纳入标准(在线补充图S1)。其中腺癌147例,鳞状细胞癌43例,大细胞癌28例(gydF4y2Ba表1gydF4y2Ba)。中位随访时间为12.3(15)个月。总的来说,176名患者患有IV期疾病,42名患者患有IIIB期疾病。在反应评估中,根据RECIST标准,没有患者表现出完全反应,51例部分反应,132例病情稳定,35例病情进展。gydF4y2Ba
纳入研究的患者的主要特征gydF4y2Ba
cfDNA浓度及其临床相关性gydF4y2Ba
采用荧光法测定218例非小细胞肺癌患者化疗前(基线)和化疗后血浆样品中的cfDNA浓度。cfDNA浓度范围为2.54 ng·mLgydF4y2Ba−1gydF4y2Ba至6451.36 ng·mLgydF4y2Ba−1gydF4y2Ba.化疗前cfDNA的中位基线浓度为29.5 (37.0)ng·mLgydF4y2Ba−1gydF4y2Ba化疗后cfDNA中位浓度为28.9 (38.1)ng·mLgydF4y2Ba−1gydF4y2Ba(p = 0.421)。基线和化疗后浓度均显著相关(Spearman’s ρ=0.459, p<10)gydF4y2Ba−4gydF4y2Ba)。gydF4y2Ba
样品保存时间(从2006年到2010年)与基线或最终cfDNA浓度之间没有相关性(Spearman ρ= - 0.022, p=0.746;ρ= - 0.045, p=0.507,分别为基线浓度和最终浓度)。此外,我们发现中位数浓度根据采样年份没有显著差异(未显示)。gydF4y2Ba
cfDNA浓度(基线和化疗后)与患者或肿瘤特征(包括诊断时的体重指数、TNM(肿瘤、淋巴结和转移)分期(IIIB)之间无统计学意义的关联gydF4y2Ba与gydF4y2BaIV)或组织学类型(数据未显示)。然而,我们发现基线cfDNA浓度与诊断时ECOG表现状态呈正相关(中位数(IQR) 24.19 (21.86) ng·mL)gydF4y2Ba−1gydF4y2Ba, 34.76 (61.74) ng·mLgydF4y2Ba−1gydF4y2Ba108.44 (3307.37) ng·mLgydF4y2Ba−1gydF4y2Ba分别为性能状态0、1、2;p = 0.001)。有趣的是,这两个变量是相关的,尽管是适度的(ρ=0.239, p<10)gydF4y2Ba−4gydF4y2Ba)。gydF4y2Ba
晚期非小细胞肺癌cfDNA浓度与肿瘤反应gydF4y2Ba
考虑三组肿瘤反应(部分反应)gydF4y2Ba与gydF4y2Ba稳定的疾病gydF4y2Ba与gydF4y2Ba进展性疾病),两组间cfDNA中位浓度(基线和化疗后浓度)无显著差异(gydF4y2Ba表2gydF4y2Ba)。此外,在治疗期间cfDNA的变异(化疗后与基线浓度的差异)在三组肿瘤反应(gydF4y2Ba表2gydF4y2Ba)。当考虑客观反应,从而比较稳定的疾病和部分反应gydF4y2Ba与gydF4y2Ba进展性疾病,没有发现关联。此外,我们根据其基线cfDNA浓度(临界值≤22.26 ng·mL)将人群分为三分位数gydF4y2Ba−1gydF4y2Ba22.27 ~ 42.12 ng·mLgydF4y2Ba−1gydF4y2Ba>42.12 ng·mLgydF4y2Ba−1gydF4y2Ba)。同样,根据肿瘤反应,基线和化疗后cfDNA浓度之间没有显著差异(gydF4y2Ba图1gydF4y2Ba)。最后,我们还使用RECIST反应作为连续变量(百分比),发现与基线和化疗后cfDNA浓度没有显著关联或相关(RECIST(百分比)与基线或化疗后的相关性分别为Spearman ρ=0.17, p=0.806和- 0.12,p=0.861)。gydF4y2Ba
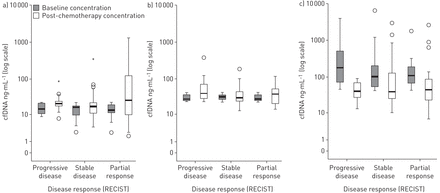
箱形图显示基线和化疗后无细胞(cf)DNA浓度,根据基线浓度的分位数和实体瘤(RECIST)反应类别的反应评价标准。a)第一极;B)第二种;C)第三片。gydF4y2Ba
根据实体瘤反应评价标准(RECIST)标准,无细胞(cf)DNA浓度和肿瘤反应gydF4y2Ba
cfDNA浓度的预后价值gydF4y2Ba
中位无进展生存期(PFS)为6.9个月(95% CI 6.1-7.7个月),总生存期为12.3个月(95% CI 10.7-13.9个月)。cfDNA基线浓度最高的各组PFS明显短于其他两组(5.7个月,95% CI 4.5-6.9个月)gydF4y2Ba与gydF4y2Ba7个月,95% CI分别为6.3-7个月;p = 0.034)。当将总生存期作为结果变量时,基线cfDNA浓度的预后价值也很显著:最高分位数为10个月(95% CI 10.7-13.9个月)gydF4y2Ba与gydF4y2Ba14.2个月(95% CI 12.6 ~ 15.8个月),低/中位数组(p=0.001) (gydF4y2Ba图2gydF4y2Ba)。gydF4y2Ba
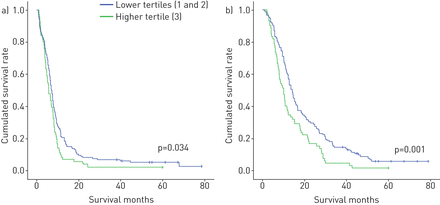
生存曲线显示a)无进展和b)按无细胞DNA浓度分类的患者总生存期(最高gydF4y2Ba与gydF4y2Ba最低的两分之一)。gydF4y2Ba
在单变量分析中,我们发现疾病分期、诊断时的表现状态和缓解率与总生存期和PFS相关(在线补充表S1)。这些变量与患者年龄在多变量Cox回归模型(gydF4y2Ba表3gydF4y2Ba)。在这个多变量分析中,基线cfDNA浓度的预后价值仍然是显著的,与总生存期和PFS有显著的相关性。对于总生存率,相应的校正风险比为10030 (95% CI 100003 - 100057, p=0.028),即每增加1 ng·mL,死亡风险增加0.003%gydF4y2Ba−1gydF4y2Ba基线cfDNA浓度,独立于分期、表现状态、年龄和反应率。gydF4y2Ba
关于基线和化疗后无细胞DNA血浆浓度的无进展生存期(PFS)和总生存期的单因素和多因素Cox回归模型gydF4y2Ba
然而,我们发现生存结果与化疗后cfDNA浓度(gydF4y2Ba表3gydF4y2Ba)。gydF4y2Ba
讨论gydF4y2Ba
在本研究中,血浆cfDNA基线浓度对非小细胞肺癌具有独立的预后价值。这与以前的报告一致。事实上,尽管一些研究没有发现cfDNA水平与生存率之间的任何相关性[gydF4y2Ba11gydF4y2Ba,gydF4y2Ba15gydF4y2Ba,gydF4y2Ba20.gydF4y2Ba],大多数报告显示血浆cfDNA浓度升高与生存不良之间存在相关性[gydF4y2Ba13gydF4y2Ba,gydF4y2Ba21gydF4y2Ba–gydF4y2Ba24gydF4y2Ba]。GgydF4y2BaautschigydF4y2Baet al。gydF4y2Ba[gydF4y2Ba13gydF4y2Ba]发现cfDNA基线浓度升高(bbb10 ng·mL)gydF4y2Ba−1gydF4y2Ba)在多变量分析中与总生存率显著相关,独立于年龄、分期和治疗史。此外,三项研究[gydF4y2Ba14gydF4y2Ba,gydF4y2Ba22gydF4y2Ba,gydF4y2Ba25gydF4y2Ba发现了与我们非常相似的结果,使用了五分之一的亚组。因此,我们的结果为基线cfDNA浓度的预后价值提供了进一步的证据,来自大量患者。gydF4y2Ba
相比之下,cfDNA浓度(基线、化疗后或治疗期间的变化)与化疗反应无关。先前的研究报道了cfDNA浓度与治疗反应之间的显著关联,其中cfDNA水平在有效的手术治疗或放射治疗后下降[gydF4y2Ba11gydF4y2Ba,gydF4y2Ba12gydF4y2Ba]。在这里,我们发现cfDNA浓度与化疗两到三个疗程后的RECIST反应无关。在肺癌领域,仅报道了三项包括接受化疗的患者的研究(gydF4y2Ba表4gydF4y2Ba)。我们的结果与其中两个一致[gydF4y2Ba13gydF4y2Ba,gydF4y2Ba14gydF4y2Ba]。lgydF4y2BaeegydF4y2Baet al。gydF4y2Ba[gydF4y2Ba14gydF4y2Ba也将被分析的人群分成几组,结果与我们的相似。考虑到治疗过程中个体cfDNA的变异,如GgydF4y2BaautschigydF4y2Baet al。gydF4y2Ba[gydF4y2Ba13gydF4y2Ba我们发现cfDNA在预测反应方面不够可靠:在一些患者中,尽管疾病进展,cfDNA水平仍会下降,而尽管对化疗有反应,cfDNA水平仍会升高。因此,这似乎证实了cfDNA浓度不能预测非小细胞肺癌化疗时的治疗反应。gydF4y2Ba
无细胞DNA (cf)作为监测治疗反应的工具gydF4y2Ba
cfDNA并不是肿瘤所特有的。在炎症和感染性疾病中也可能升高。因此,高浓度cfDNA与不良预后之间的关联可能与肿瘤负荷和/或合并症有关[gydF4y2Ba6gydF4y2Ba]。然而,我们的结果强调了cfDNA总量分析的局限性。事实上,cfDNA总浓度的变化可能不仅反映了循环肿瘤(ct)DNA的变化,还反映了可能导致cfDNA增加的其他医疗条件,包括诱导正常细胞溶解的化疗,从而促进正常cfDNA释放到血液中。这也许可以解释为什么cfDNA的总浓度可能不能预测对化疗的反应。关注ctDNA(可以通过原发肿瘤特有的遗传和表观遗传改变来检测)可能是一个更合适的替代标志物。例如,NgydF4y2BaewmangydF4y2Baet al。gydF4y2Ba[gydF4y2Ba20.gydF4y2Ba最近报道了一种名为CAPP-Seq(癌症个性化深度测序分析)的方法,该方法可以灵敏地检测多种类型的体细胞改变并量化ctDNA。另一项研究,由MgydF4y2BaarcqgydF4y2Ba等gydF4y2Ba.[gydF4y2Ba26gydF4y2Ba]表明,监测接受靶向EGFR -酪氨酸激酶抑制剂(TKI)治疗的患者血浆中EGFR突变,可以准确评估肿瘤反应,并可能检测治疗下的进展(及其进展机制)。然而,ctDNA的进一步研究需要证明其在临床实践中的有效性。因此,我们的研究结果强调了cfDNA总浓度在评估化疗反应方面的不良表现,尽管cfDNA仍然是一个潜在的有趣的生物标志物,如果关注其肿瘤特异性部分。gydF4y2Ba
据我们所知,我们的研究是肺癌(肿瘤反应和生存)领域最大的研究。此外,在治疗方面,它包括一个均匀的人群,根据临床实践中对非小细胞肺癌的推荐,使用RECIST标准评估治疗反应,这里分析的人群是晚期非小细胞肺癌患者的典型人群。早期进展(n=6)或死亡(n=25)的患者未在Pharmacogenoscan中进行研究,因此未纳入我们的研究[gydF4y2Ba16gydF4y2Ba]。由于病例数量较少,这种排除可能导致的潜在偏差预计可以忽略不计。还应该指出的是,在本研究中,cfDNA定量使用PicoGreen进行,这是一种易于在临床实践中实施的简单方法。虽然大多数其他研究使用定量(q)实时PCR定量,但我们选择PicoGreen方法,因为在PicoGreen和qPCR检测之间观察到良好的正相关[gydF4y2Ba27gydF4y2Ba]。虽然qPCR具有高灵敏度和高精度,但它需要特定的自动化系统并且价格昂贵,而PicoGreen方法是一种快速、有效、可靠和廉价的cfDNA定量方法。它还显示出较高的检测限,使该技术适用于血浆cfDNA分析[gydF4y2Ba27gydF4y2Ba,gydF4y2Ba28gydF4y2Ba]。gydF4y2Ba
通过该方法获得的cfDNA中位数浓度与先前发表的NSCLC数据一致,尽管平均浓度低于其他系列报道,包括我们团队的一项研究[gydF4y2Ba13gydF4y2Ba,gydF4y2Ba14gydF4y2Ba]。这种绝对浓度的差异可能来自血液样本处理、血浆分离和储存或DNA定量方法,以及所研究人群的异质性。在这项工作中,血浆分离在抽血后4小时内按照所有参与中心相同的标准程序进行,以限制血细胞DNA可能的污染。此外,cfDNA的提取和定量在一个实验室集中进行,采用标准方案,以限制各中心之间的定量偏差。关于样品保存时间的潜在影响(长期冷冻可能会改变cfDNA的质量和数量),我们检查了样品保存时间与cfDNA浓度之间没有相关性。gydF4y2Ba
总cfDNA浓度似乎是肺癌的独立预后因素。尽管事实上总cfDNA浓度不能作为评估化疗有效性的信息,而且其他已证实的预后因素(如疾病分期或表现状态)已经存在[gydF4y2Ba3.gydF4y2Ba,gydF4y2Ba4gydF4y2Ba]), cfDNA在这种情况下仍然很有趣。事实上,在使用激酶抑制剂治疗期间,对生物标志物(如EGFR)的突变cfDNA部分进行随访,对于评估TKI反应和检测早期疾病进展似乎特别有希望[gydF4y2Ba26gydF4y2Ba]。cfDNA作为液体活检的使用在无创体细胞分子谱分析中也非常有前景,无论是在基线还是在随访中重新采样[gydF4y2Ba26gydF4y2Ba,gydF4y2Ba29gydF4y2Ba,gydF4y2Ba30.gydF4y2Ba]。gydF4y2Ba
总之,我们的数据表明,从血浆中定量cfDNA可能是一种有用的无创临床实践技术。在晚期NSCLC中,血浆中cfDNA基线浓度高与不良预后相关,与年龄、运动状态、分期和反应无关。然而,总cfDNA与化疗反应无关。cfDNA的效用,特别是肿瘤特异性cfDNA的效用,应该在更大规模的常规试验中进行评估。gydF4y2Ba
脚注gydF4y2Ba
有关编辑评论,请参阅gydF4y2BaEur呼吸器gydF4y2Ba2015;46: 1548-1550 [doi: 10.1183/09031936.01482-2015]gydF4y2Ba
本文的补充资料来自gydF4y2Bawww.qdcxjkg.comgydF4y2Ba
本研究已在clinicaltrials.gov网站注册,并附有识别码gydF4y2BaNCT00222404gydF4y2Ba.gydF4y2Ba
支持声明:Pharmacogenoscan研究得到了法国卫生部(2008年国家医院临床研究计划(PHRC))的支持。克莱尔·蒂索得到了里昂平民收容所(annaceme Recherche)的资助。gydF4y2Ba
利益冲突:可以在以下网址找到与本文在线版本一起披露的信息gydF4y2Bawww.qdcxjkg.comgydF4y2Ba
- 收到了gydF4y2Ba2015年4月30日。gydF4y2Ba
- 接受gydF4y2Ba2015年7月5日。gydF4y2Ba
- 版权所有©ERS 2015gydF4y2Ba
参考文献gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba















