摘要
宿主免疫对非小细胞肺癌(NSCLC)预后的影响存在争议。我们研究了非小细胞肺癌淋巴浸润模式与预后之间的关系。
肿瘤和间质浸润CD3+, CD8+叉头盒P3 (Foxp3)+使用免疫组织化学和一种新的图像分析算法分别评估196例NSCLC患者的总t淋巴细胞计数、细胞毒性t淋巴细胞计数和调节性t淋巴细胞计数。选择中位细胞计数作为定义患者亚组的切点,并确定相应的肿瘤胰岛:间质(TI/S)计数的比率。
总生存率与CD8升高呈正相关+TI/S比值(死亡危险比(HR) 0.44, p<0.001)与Foxp3呈负相关+TI/S比和总生存率(HR 4.86, p<0.001)。CD8高的患者+胰岛(HR 0.48, p<0.001)和Foxp3+间质(HR 0.23, p<0.001)计数有更好的生存,而高CD3+和CD8+基质数量和高Foxp3+胰岛浸润生存率较差(HR分别为1.55,2.19和3.14)。多变量分析,CD8高+TI/S比值提高了生存率(HR 0.48, p=0.002),但Foxp3较高+TI/S比与较差的生存率相关(HR 3.91, p<0.001)。
浸润t淋巴细胞的微定位是切除NSCLC预后的有力预测指标。
摘要
淋巴细胞微定位强烈影响肺癌患者接受治疗性手术的生存http://ow.ly/QUwbD
简介
炎症与恶性肿瘤之间的联系已被证实[1].从癌症发展的早期阶段开始,就会引起全身和局部的炎症反应。然而,现在已经确定,发展中的肿瘤能够适应这种宿主免疫反应,以创造一个有利于其生存和发展的微环境[2].
先前的研究人员报道,在上皮性癌症中,调节性t淋巴细胞(treg)的积累在不同类型的肿瘤中会导致更糟糕的结果[3.- - - - - -5].treg代表一种独特的t淋巴细胞群,其特征是叉头盒P3 (Foxp3)标记物的表达,Foxp3标记物是成熟和免疫抑制功能所需的转录抑制因子[6].积累的证据表明,肿瘤内特定的Treg募集有助于癌细胞通过各种机制逃避免疫介导的破坏,包括抑制效应t淋巴细胞增殖和形成免疫抑制细胞因子网络[7].相反,上皮内CD8增加+肿瘤浸润淋巴细胞计数与几种癌症的生存率提高有关,这表明这些细胞具有细胞毒性抗肿瘤细胞的作用[8,9].进一步,测定CD8的比率+肿瘤样本中的t淋巴细胞/ treg已被发现在许多癌症类型中具有额外的预后相关性[9- - - - - -12].
以前对非小细胞肺癌(NSCLC)淋巴网状浸润临床意义的定义产生了相互矛盾的结果,有证据支持有益的[13],中性的[14]和负面影响[15].然而,炎症细胞的精确微定位,而不是绝对细胞计数的评估本身,在分析与预后的关系时,似乎是至关重要的[16- - - - - -18].在这篇文章中,我们展示了手术切除的NSCLC中不同浸润淋巴细胞群的预后相关性,特别关注其准确性原位细胞微定位和亲肿瘤和抗肿瘤淋巴亚群之间的相互关系。
方法
研究人群
回顾性分析了圣詹姆斯医院(爱尔兰都柏林)2001年1月至2005年1月间接受非小细胞肺癌治疗的所有患者的病例记录。我们确定了197例接受完整肿瘤切除和系统淋巴结清扫的患者,病理证实(p)-根据国际肺癌分期系统进行研究的I至IIIA期非小细胞肺癌[19].在回顾临床记录和组织病理学报告后,收集基线人口统计学、临床病理特征和手术方式的信息。预后数据,包括围手术期死亡率和长期生存期,进行前瞻性更新。无患者接受辅助细胞毒化疗。当地医院伦理委员会批准了这项研究。
免疫组织化学
存档的196例患者肿瘤标本可用于组织病理学评估。从福尔马林固定、石蜡包埋的组织块中连续切下5 μm厚的切片,并干燥过夜。每组取一张切片,用苏木精-伊红染色,进行光镜检查,确认切片中有肿瘤边缘进展。
我们使用BondMax自动染色机器人平台(Vision BioSystems, Newcastle, UK)根据制造商的说明进行免疫组化染色。脱蜡后,用BondMax抗原表位提取液预处理20 min后,应用稀释后的一抗。切片用抗人CD3孵育(1:30;Novocastra,米尔顿凯恩斯,英国),抗人CD8 (1:30;Novocastra)和抗人Foxp3 (1:100;eBiosciences, San Diego, CA, USA)抗体,能够分别检测总t淋巴细胞群、细胞毒性t淋巴细胞群和调节性t淋巴细胞群。使用Bond Polymer Refine Kit (Vision BioSystems, Newcastle, UK),以3,3 ' -二氨基联苯胺为染色原,对染色细胞进行检测和可视化。组织用哈里斯苏木精反染色。所有试验均采用适当的阳性(人阑尾)和阴性(省略一抗)对照。
图像采集和炎症细胞定量
使用Aperio ScanScope CS切片扫描仪(Aperio Technologies, Vista, CA, USA)系统获取20倍物镜的组织切片全切片高分辨率数字化图像。使用Spectrum软件(Aperio Technologies)管理数字图像。采用免疫组化核定量算法软件开发自动化图像分析程序,检测和定量淋巴细胞(细胞质免疫组化CD3染色)+和CD8+Foxp3细胞和细胞核染色+先前所述的肿瘤及间质区域的细胞)[20.)(详情请参阅网上补充资料)。
为了比较不同肿瘤区室内的淋巴细胞计数,从五个随机选择的高能场中对肿瘤胰岛和间质的所有区域分别进行注释,以创建两个不同的对应“层”(详情请参阅在线补充材料)。采用新型细胞检测算法测定免疫组化染色淋巴细胞的绝对数量,并报告为细胞数·mm-2肿瘤和间质区。然后计算所有患者每种标志物对应的肿瘤胰岛和间质(TI/S)计数之比。患者分为CD3型+高或CD3+低取决于CD3+TI/S比值高于或低于中位数。同样,CD8+高, CD8+低,具体+高和具体+低他们建立了小组。在不了解临床结果的情况下进行淋巴细胞浸润分析。
EGFR和KRAS突变分析
研究人群中表皮生长因子受体(EGFR)酪氨酸激酶结构域和V-Ki-ras2 Kirsten大鼠肉瘤病毒癌基因同源物(KRAS)的基因突变/缺失也通过直接Sanger测序进行筛选,以测试这些突变是否与不同的淋巴细胞浸润模式有关。所使用的方法的完整描述包含在在线补充材料中。
统计分析
选取中位数作为切点,根据免疫组织化学标记物来定义亚组。各淋巴细胞亚型的浸润模式与生存率的相关性使用log-rank统计进行评估。采用SPSS 15.0软件(SPSS, Chicago, IL, USA)进行统计分析。使用Spearman ρ相关、r平方变化和线性回归来检验自动分析和人工分析之间的关系。采用Cox回归分析、Kaplan-Meier分析和log-rank检验来说明各项临床特征的显著性。采用卡方分析检验临床病理特征与不同淋巴细胞浸润模式之间的显著相关性。对所有协变量进行了比例风险假设检验。所有p值均为双侧,值<0.05为显著。
结果
研究人群
研究人群的临床病理特征在表1.均值±sd患者手术时年龄为65.5±8.8岁(41-86岁)。手术后30天内死亡的10名患者被排除在分析之外。整个队列的总体5年生存率为41.3%。在单因素分析模型中,肿瘤大小、肿瘤切除边缘是否受累、淋巴结分期和总体分期与总生存率相关(表1).11例EGFR突变患者和11例KRAS突变患者术后存活30天。EGFR和KRAS突变状态均不影响患者的预后。
自动图像分析算法的验证
每一种免疫组织化学标记物的染色都是明显的,很容易与周围的肿瘤和间质区分开。淋巴细胞浸润模式在患者之间有很大差异(图1).使用手动方法和自动化方法记录的淋巴细胞计数之间存在高度显著的相关性(Spearman ρ=0.849, p<0.001),证实了自动化系统的有效性。
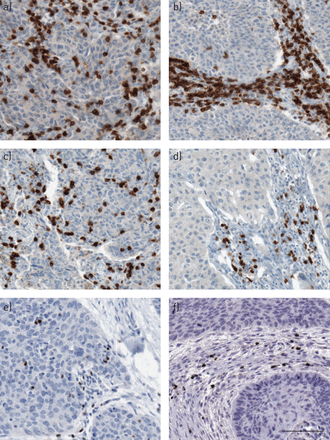
免疫组化淋巴细胞浸润模式。显微照片显示主要肿瘤胰岛浸润a) CD3+, c) CD8+e)叉头盒P3 (Foxp3)+t淋巴细胞和主要间质b) CD3浸润+, d) CD8+f) Foxp3+淋巴细胞)。比例尺=100 μm。
淋巴细胞浸润与预后的相关性
CD3的分布+, CD8+和具体+淋巴细胞呈阳性偏斜,不呈正态分布(数据未显示)。单因素分析显示,总生存率与CD8升高呈正相关+观察TI/S比值(HR 0.44, 95% CI 0.29-0.67;死亡P <0.001;图2).CD8患者的5年生存率+中位数计数以上和以下的TI/S比值分别为59%和34%。因为超过一半的病人有CD8+高模式存活5年后,该组的中位生存期无法计算。CD8患者的中位生存期+低模式为30.8个月。相比之下,Foxp3基因和Foxp3基因之间呈现出惊人的反向关系+Treg TI/S比值和总生存率(HR 4.86, 95% CI 3.11-7.59;p < 0.001;图2).Foxp3患者的5年生存率+中位数计数高于和低于中位数计数的TI/S比值分别为20%和69%。Foxp3患者的中位生存期+低模式无法确定,而Foxp3基因携带者的中位生存率+高模式为21.2个月。高CD3患者生存率提高的趋势+观察TI/S比值,但未达到统计学意义(HR 0.68, 95% CI 0.99-2.23;p = 0.058;图2).
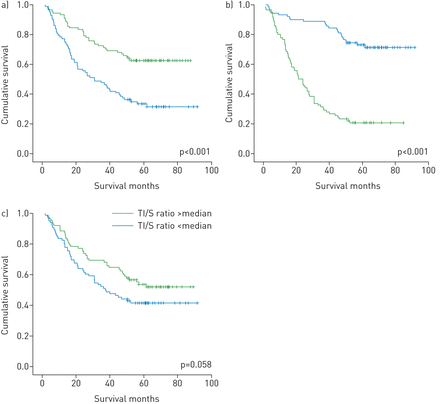
根据肿瘤胰岛/间质(TI/S)比率浸润a) CD8的Kaplan-Meier生存曲线+, b)叉头盒P3 (Foxp3)+c) CD3+淋巴细胞)。
接下来,我们检查了淋巴细胞计数在单个肿瘤区室和患者预后之间的关系。CD8浸润计数高于中位数的患者具有显著的生存优势+t淋巴细胞位于肿瘤胰岛内(HR 0.48, 95% CI 0.33-0.72;p<0.001)和Foxp3+肿瘤周围基质中的treg (HR 0.23, 95% CI 0.15-0.36;p < 0.001)。相比之下,CD3间质计数高与预后明显较差相关+t淋巴细胞(HR 1.55, 95% CI 1.03-2.3;p=0.034)和CD8+t淋巴细胞(HR 2.19, 95% CI 1.48-3.27;p<0.001)和Foxp3的高肿瘤胰岛计数+t淋巴细胞(HR 3.14, 95% CI 2.06-4.78;p < 0.001)。肿瘤胰岛CD3与肿瘤胰岛CD3无显著相关性+t淋巴细胞浸润与预后的关系。
不同CD8组合的预后意义+/ Foxp3+基于CD8的四种可能组合,通过分析患者的生存模式来评估TI/S浸润+和具体+t淋巴细胞浸润率(图3).四组患者联合浸润模式的生存差异具有高度统计学意义(p<0.001)。以CD8为特征的患者+高/ Foxp3+低CD8基因型患者的5年生存率最长(77%),而CD8基因型患者的5年生存率最高+低/ Foxp3+高Pattern的预后特别差(5年生存率为8%)。因为两组中有一半以上的人具有Foxp3基因+低存活时间为5年(即。CD8+高/ Foxp3+低和CD8+低/ Foxp3+低组),中位生存期无法计算。CD8的中位总生存率+高/ Foxp3+高和CD8+低/ Foxp3+高各组分别为31.0个月和17.2个月。
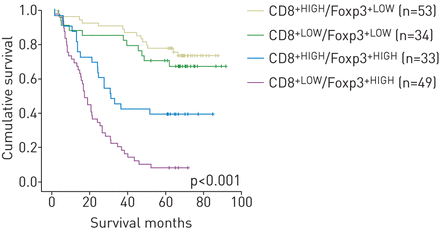
根据联合CD8的Kaplan-Meier生存曲线+/叉头盒P3 (Foxp3)+t淋巴细胞肿瘤胰岛/间质(TI/S)比值浸润模式。
采用比例风险假设来评估不同淋巴细胞亚群的TI/S比值是否为生存的独立预测因子(表2).临床病理变量包括肿瘤大小、肿瘤分期、淋巴结分期p -分期、手术边缘和CD3+, CD8+和具体+t淋巴细胞TI/S浸润比。通过单因素分析,选择这些参数是因为它们的相对预后意义(p<0.1)。高CD8+TI/S比与生存改善独立相关(HR 0.48, 95% CI 0.30-0.76;p=0.002),而高Foxp3+TI/S比值是较差生存的独立预测因子(HR 3.91, 95% CI 2.33-6.55;p < 0.001)。有趣的是,两者都是CD8+和具体+TI/S比是较强的预后变量p -多变量分析阶段。
EGFR和KRAS突变患者在不同的淋巴细胞浸润模式组中几乎均匀分布,表明突变状态与任何一种淋巴细胞浸润模式之间缺乏相关性,无论是单独的还是联合的淋巴细胞比例(在线补充材料)。
作为用于确定与t淋巴细胞TI/S比率评估相关的预后价值的方法的内部验证,研究人群被分为测试组和验证组。中位数TI/S值来自CD8的前100例患者(试验队列)+和具体+建立标记。然后应用这些新的切点值对其余研究人群(验证队列)进行二分,以检查方法的可重复性(图4).采用这种方法,Foxp3+在两项试验中,TI/S比值仍然是一个具有统计学意义的预后变量(HR 3.5, 95% CI 2.01-6.13;p<0.001)和验证队列(HR 8.05, 95% CI 3.33-19.47;p < 0.001)。CD8+t淋巴细胞TI/S比值在试验队列中呈统计学意义趋势(HR 1.60, 95% CI 0.95-2.70;p=0.076),在验证队列中显著(HR 5.70, 95% CI 2.01-16.15;p = 0.001)。
CD8试验和验证队列的Kaplan-Meier生存曲线+叉头盒P3 (Foxp3)+t淋巴细胞肿瘤胰岛/基质(TI/S)比值。一)CD8+测试组;b) FoxP3+测试组;c) CD8+验证组;d) FoxP3+验证队列。
免疫浸润与临床病理变量的相关性
采用卡方分析检验临床病理特征与不同淋巴细胞浸润模式之间的显著相关性。在本分析中,细胞计数数据按中值进行了二分。CD8之间显著相关+和具体+TI/S浸润模式确定(卡方3.97,p=0.04)。淋巴细胞标记物与任何检查的临床病理变量之间没有关联。病理分期与CD8无相关性+或Foxp3+TI/S浸润模式。总体分期与CD8组合之间存在弱统计学意义相关性+/ Foxp3+显示了浸润比;然而,这种关联仅在IA期和IB期以及IIA期和IIB期合并时才被证实。
讨论
在本研究中,我们对NSCLC手术标本中的肿瘤微环境进行了详细评估。尤其关注细胞微定位,我们的研究结果表明,t淋巴细胞亚群的区域分布是手术切除NSCLC患者大群体预后的一个强有力的预测因子,与肿瘤分期和其他临床病理变量无关。Foxp3比例较高的患者+肿瘤胰岛内的t淋巴细胞与周围瘤周间质内的t淋巴细胞相比,预后明显较差。CD8则相反+t淋巴细胞,这样,相对较高的肿瘤内浸润的免疫人群给予良好的预后,而间质CD8增加+计数与预后不良有关。
实体肿瘤中淋巴细胞的存在对肿瘤侵袭、生长、转移和临床结果的积极和消极影响都有关联。这一发现表明高水平的肿瘤胰岛Foxp3+treg预测NSCLC的结果明显更糟,这与其他研究人员的观察结果一致。在他们里程碑式的论文中,W面向对象et al。[21显示CD4细胞百分比增加+CD25+非小细胞肺癌和卵巢癌中的treg。采用半定量评分系统,Petersenet al。[22]随后显示,肿瘤内Treg积累相对于总浸润淋巴细胞计数增加的I期NSCLC患者疾病复发的风险增加。年代himizuet al。[23]也表明瘤内Treg浸润可以缩短NSCLC手术切除后的无复发生存期,这可能是由于这些细胞对免疫抑制酶环氧合酶-2的作用。treg的一个关键特征是它们能够抑制其他免疫群体(包括CD8)+t淋巴细胞)通过直接细胞接触,treg主动招募到肿瘤微环境,从而促进癌细胞逃避免疫检测和破坏[7].
不同的研究者已经证明了表达CD8的t淋巴细胞的瘤内浸润+标记物在结直肠癌中具有生存优势[24],卵巢[25]和cervical [26癌症,以及其他疾病。有效的抗肿瘤活性已被提出作为这些发现的生物学解释,这一现象也可以解释我们系列中肿瘤内CD8高的患者的显著生存增加+早期最重要的。的确,我们的结果与其他研究人员评估NSCLC浸润淋巴细胞免疫机制的结果有一些相似之处。Kawaiet al。[13]检查了IV期疾病患者的活检标本,发现CD8占主导地位+肿瘤胰岛内t淋巴细胞浸润与生存率提高相关。相比之下,Al- shibliet al。[27]发现间质CD8的数量很高+t淋巴细胞是一个独立的有利预后标志物,上皮细胞CD8的增加+淋巴细胞与生存率低相关,尽管仅在单变量分析中。然而,用于量化肿瘤和间质淋巴细胞计数的评分系统是基于淋巴细胞占每隔室总有核细胞的近似百分比。相比之下,在目前的研究中,每个区域的淋巴细胞的绝对数量是自动计数的,并表示为单位面积,以得出每个患者的确切值。这是特别重要的,因为评估不同免疫群体的精确微定位,而不是确定绝对的细胞计数本身在描述白细胞表型以研究炎症细胞浸润模式与预后之间的关系时,这似乎是至关重要的[16,18].
我们的数据还表明效应细胞和抑制细胞比例与预后之间存在相互关系。合并低TI/S CD8患者的5年生存率+高TI/S Foxp3+治疗性手术后的比率仅为8%,而相反模式的患者为77%。有趣的是,这两种Foxp3的TI/S比值都较低的患者+和CD8+t淋巴细胞比相应比例高的细胞表现更好。这些结果表明,虽然CD8的微定位+t淋巴细胞数量是术后生存的重要决定因素,treg的存在与否对预后影响最大。因此,尽管浸润NSCLC的不同淋巴细胞群的绝对数量很重要,促瘤(Tregs)和抑瘤(CD8)的平衡也很重要+细胞毒性细胞)的机制可能有更大的相关性。Foxp3的出现+在我们的人群中,使用多变量分析模型,TI/S比作为结果的独立预测因子,在内部验证后,该参数仍然与预后相关,进一步支持了这一假设。此外,我们的结果与CD8在患者预后中的变化有关+/ Foxp3+NSCLC中的t淋巴细胞浸润率与研究其他肿瘤类型的研究人员一致,表明肿瘤内调节t淋巴细胞亚群和细胞毒性t淋巴细胞亚群的平衡是预后的独立预测因子。低CD8之间有明显的联系+/Treg瘤内浸润率与不良预后的关系,此前已在颈椎[10]和gastric [11]癌,而卵巢癌浸润率越高,生存率越高[9]和结直肠[12癌症。
有几种可能的生物学解释可以解释CD8明显的相反作用+和具体+NSCLC中的t淋巴细胞。一个简单的假设是CD8+肿瘤胰岛内的细胞被功能性激活,并通过细化靶向和杀死癌细胞的细胞因子来控制肿瘤生长,而Tregs表现出一种免疫抑制表型,促进癌细胞的生存和增殖。因此,treg在瘤内积累的相对增加可能足以克服细胞毒性t淋巴细胞功能[28].多种机制被认为可以促进这种抑制功能,包括细胞间的接触、生长因子的局部竞争和抑制性细胞因子的分泌[29].事实上,有令人信服的证据表明Tregs抑制有效的CD8+t淋巴细胞毒性活性通过转化生长因子-β信号通路[30.].通过这种方式,肿瘤胰岛内过量的treg可能会钝化宿主效应机制,使癌症进展。同样地,在不同时调节细胞毒性t细胞活性的情况下消耗Treg群体的免疫治疗策略也不足以恢复有效的抗肿瘤免疫[31].相反,在对新辅助化疗有完全病理反应的患者中,细胞毒性t淋巴细胞浸润增加并伴有Tregs的完全消除是其特征[32].在这方面,需要强调的是,我们队列中没有患者接受术后化疗。这是特别相关的,我们相信我们的研究的一个优势,因为辅助癌症治疗可以从根本上改变免疫功能,并可能在结果方面成为一个混杂因素。
在我们的研究人群中,与不同肿瘤淋巴细胞浸润模式相关的可变预后支持了肺癌中可能存在不同肿瘤免疫原性表型的假设。事实上,最近的数据表明,肿瘤免疫逃避是有调节的通过两种不同的宿主炎症细胞和细胞因子模式。第一种类型的肿瘤表现出大量的适应性和先天性炎症细胞浸润。该亚群能够通过对免疫系统抑制途径的主要抑制作用和上调肿瘤促进细胞因子谱来抵抗宿主的抗癌努力,这种抑制作用由treg与其他炎症细胞群(如M2交替激活的巨噬细胞和树突状细胞(dc))共同介导[7,18,33]等。尽管CD8+效应t淋巴细胞是肿瘤内细胞流入的一部分,它们受到免疫抑制细胞因子环境的功能抑制。第二种主要表型表现为少免疫模式,低水平的免疫细胞浸润和趋化因子表达。这种肿瘤似乎能够通过免疫系统排斥和/或“无知”来抵抗宿主防御机制。
现在已经认识到,适应性免疫抗肿瘤细胞元件可能起源于经典的初级和次级淋巴器官以外的区域。在这方面,基质三级淋巴结构(TLS)的存在,包括成熟树突状细胞和被滤泡b淋巴细胞包围的t淋巴细胞的聚集物,也对不同癌症的预后产生影响。在早期NSCLC中,先前有报道称TLS中成熟树突状细胞的密度是死亡率的一个强有力的预测因子[34].而且,类似于我们观察到的低CD8+一组法国研究人员观察到,低水平的TLS衍生的b淋巴细胞和树突状细胞以及低密度的成熟树突状细胞和CD8的组合预示着不利的结果+t淋巴细胞鉴定非小细胞肺癌患者亚组死亡风险显著增加[35,36].这些发现强调肿瘤抗原特异性体液反应也是宿主抗癌防御的关键组成部分。然而,完全了解CD8之间复杂的相互作用+和具体+t淋巴细胞、b淋巴细胞和树突状细胞在NSCLC中的研究不足,值得进一步研究。
我们的观察支持了基于t细胞炎症模式的相对存在或不存在的不同免疫表型的累积证据,这对临床转译也具有潜在的关键意义。例如,无法支持活化的细胞毒性t淋巴细胞进入肿瘤微环境的肿瘤可能固有地对免疫治疗干预具有耐药性,并给予较差的临床反应。
我们的发现可能与发展中的NSCLC免疫治疗领域相关,特别是那些作用于免疫检查点通路抑制分子细胞毒性t淋巴细胞相关抗原(CTLA)-4和程序性细胞死亡蛋白(PD)-1的药物,以及后者的结合伙伴PD- l1。最近已批准单克隆抗体PD-1抑制剂nivolumab用于化疗失败的转移性鳞状NSCLC,并且由于Tregs高表达PD-1 [37],具体检查nivolumab(和其他PD-1/PD-L1抑制剂)对表现出高剂量的患者的相对影响将是有趣的与瘤内Foxp3低+淋巴细胞浸润。此外,最近的数据强调,抗ctla4抗体会耗尽瘤内Treg种群[38人们可能会推测,根据我们研究中淋巴细胞浸润特征,那些预后最差的患者可能会从单独或联合抗pd -1/PD-L1抗体抑制CTLA-4的方法中获益最大。测试这一假设也可能有助于确定是否有可能更好地选择患者参与未来针对免疫检查点通路的已批准和/或研究性药物的临床研究。
最近关于Foxp3表达的可塑性及其与Treg功能的关系存在争议[39].事实上,我们发现的一些细胞可能只有短暂的Foxp3表达。然而,这种可能性并没有改变我们发现的重要性。对不同淋巴细胞浸润模式患者肿瘤和间质区域细胞因子谱的彻底评估可能有助于阐明与我们的发现相关的生物学机制,特别是考虑到对非小细胞肺癌肿瘤特异性疫苗治疗的新兴趣[40].
总之,我们的数据表明,评估t淋巴细胞微定位可能有助于识别尽管明显完全手术切除,但仍有早期疾病复发风险的个体。内部测试和验证研究表明,Foxp3+可能还有CD8+TI/S比值可以帮助确定哪些患者应该接受辅助治疗。未来的免疫治疗策略能够下调瘤内Treg反应,同时增强相应的效应子CD8+t淋巴细胞活性可能值得研究。
脚注
有关编辑评论,请参阅呼吸呼吸J2015;46: 1541-1543 [doi: 10.1183/09031936.00159515]。
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:由爱尔兰都柏林皇家城市医院信托基金(D.S. O’callaghan)、Nycomed Pharma (D.S. O’callaghan)和爱尔兰健康研究委员会(在乳腺癌转移:生物标志物和功能介质研究计划的赞助下)(E. Rexhepaj和W.M. Gallagher)提供资助。本文的资助信息已存入FundRef.
利益冲突:可以在本文的在线版本中找到信息披露www.qdcxjkg.com
- 收到了2015年1月27日。
- 接受2015年7月14日。
- 版权所有©ERS 2015