文摘gydF4y2Ba
血浆循环(cf)游离DNA是肿瘤学的兴趣,因为它已被证明含有肿瘤DNA,并可能因此被用作液体活检。在nonsmall细胞性肺癌(NSCLC), cfDNA量化提出了监测和随访的患者。然而,可用的研究是有限的,需要有大量的样本证实了研究,包括病人获得更均匀的治疗。我们的目标是评估等离子cfDNA浓度的预测和预后价值与非小细胞肺癌患者的一大系列和处理标准的化疗方案。gydF4y2Ba
我们包括肺癌患者招募到Pharmacogenoscan样本研究。cfDNA的218名患者被荧光测定术提取并量化之前和之后的两个或三个周期以铂为基础的化疗。基线和治疗化疗后浓度和反应之间的关系,评估RECIST(响应评估标准固体肿瘤)或患者生存分析。gydF4y2Ba
cfDNA浓度高(最高tertile)患者在基线明显差无病和整体生存比低浓度(最低和中间tertiles)(中位总生存期10个月(95% CI 10.7 - -13.9)gydF4y2Ba与gydF4y2Ba分别为14.2个月(95% CI 12.6 - -15.8);p = 0.001)。在多变量分析中,cfDNA基线浓度的增加是一个独立的预后因素。然而,我们没有发现任何cfDNA浓度和对治疗的反应之间的联系。gydF4y2Ba
cfDNA可能是一个生物标志物在非小细胞肺癌预后的评估。然而,总浓度cfDNA没有出现预测化疗反应。gydF4y2Ba
文摘gydF4y2Ba
总DNA不是游离与先进nonsmall细胞肺癌化疗反应gydF4y2Bahttp://ow.ly/QpqyxgydF4y2Ba
介绍gydF4y2Ba
肺癌是全球癌症死亡的主要原因gydF4y2Ba1gydF4y2Ba]。诊断通常是在一个高级或转移阶段,因为当地和地区传播仍在大多数患者无症状很长一段时间。先进的肺癌的预后很差,5年生存的转移阶段不超过5%gydF4y2Ba2gydF4y2Ba]。预后的主要因素是疾病阶段,性能状态、诊断、年龄应对一线化疗,血浆乳酸脱氢酶水平和存在体细胞突变或重组的基因和通路靶向治疗是可用的(如表皮生长因子受体(EGFR)或间变性淋巴瘤激酶)(gydF4y2Ba3gydF4y2Ba,gydF4y2Ba4gydF4y2Ba]。晚期的治疗方法都是基于细胞毒性化疗和靶向治疗(gydF4y2Ba5gydF4y2Ba]。对治疗的反应是评估使用计算机断层扫描(CT)使用RECIST(固体肿瘤反应评估标准)标准(gydF4y2Ba6gydF4y2Ba]。到目前为止,没有可靠的生物标志物的评价标准化疗治疗肺癌和需要更多的患者预后因素管理先进nonsmall细胞性肺癌(NSCLC)。gydF4y2Ba
循环(cf)游离DNA最近收到的兴趣对其作为生物标志物在肿瘤的潜在gydF4y2Ba7gydF4y2Ba]。cfDNA对应于DNA片段游离在血液中循环,可以从血浆或血清中提取。据信被释放在血液中通过坏死、凋亡或由有核细胞如淋巴细胞主动分泌。cfDNA主要是由本构基因组DNA。几个条件可能与cfDNA浓度的增加有关,包括炎症、组织损伤和癌症(gydF4y2Ba8gydF4y2Ba,gydF4y2Ba9gydF4y2Ba]。对于癌症,cfDNA很大一部分来自肿瘤细胞和cfDNA浓度反映了肿瘤负担(gydF4y2Ba10gydF4y2Ba]。此外,cfDNA可能源自循环肿瘤细胞,从而可能反映了micro-metastatic疾病和疾病的潜在攻击性(gydF4y2Ba9gydF4y2Ba]。gydF4y2Ba
有人提出,cfDNA可能是一个预测因素的肿瘤预后因子的响应和良好的候选。在肺癌患者,一些研究已经表明,cfDNA浓度可能是预测因素的肿瘤手术和放射治疗(gydF4y2Ba11gydF4y2Ba,gydF4y2Ba12gydF4y2Ba),但很少有研究调查cfDNA浓度作为肿瘤化疗反应的预测因素。这些研究包括少量的样品,结果是矛盾的gydF4y2Ba13gydF4y2Ba- - - - - -gydF4y2Ba15gydF4y2Ba]。研究的预后价值cfDNA也显示冲突的结果(gydF4y2Ba11gydF4y2Ba,gydF4y2Ba13gydF4y2Ba]。gydF4y2Ba
我们评估了预测和预后价值的肿瘤反应和生存cfDNA浓度与铂类化疗治疗非小细胞肺癌患者。gydF4y2Ba
材料和方法gydF4y2Ba
人口gydF4y2Ba
患者纳入本研究从法国Pharmacogenoscan研究。Pharmacogenoscan是六医院进行的一项前瞻性群组Rhone-Alpes-Auvergne地区的法国。其目的是确定生物和组织学NSCLC患者预后的相关因素。的主要目标是识别特定的生物标志物和疾病控制率之间的联系。二级目标是识别生物标志物与患者生存有关。所有患者签署知情同意书。首先Pharmacogenoscan研究结果已报告在别处(gydF4y2Ba16gydF4y2Ba,gydF4y2Ba17gydF4y2Ba]。gydF4y2Ba
Pharmacogenoscan研究的入选标准如下。1)连续患者诊断为非小细胞肺癌的一个六参与中心2005年7月和2010年8月之间;2)癌症可能的任何阶段,但愿意接受铂类治疗双重新辅助治疗或化疗一线治疗转移性或复发性疾病(双重药物在调查员的选择);和3)东部合作肿瘤组(ECOG)性能的地位在包含0 - 2 (gydF4y2Ba18gydF4y2Ba]。gydF4y2Ba
所有患者接受血液采样在任何癌症治疗,第一反应评估之前,发生在两个或三个周期以铂为基础的化疗的调查员的选择。对化疗反应是评估使用RECIST标准(gydF4y2Ba6gydF4y2Ba]。gydF4y2Ba
从Pharmacogenoscan数据集,我们限制包含非小细胞肺癌患者化疗前后血浆样品和可以RECIST反应的评估(gydF4y2Ba19gydF4y2Ba]。此外,我们选择限制包含IIIB-IV阶段。事实上,我们先前已经表明,cfDNA浓度与分期有关(gydF4y2Ba10gydF4y2Ba]。gydF4y2Ba
Pharmacogenoscan研究伦理委员会批准的格勒诺布尔大学医院(法国格勒诺布尔)(gydF4y2BaNCT00222404gydF4y2Ba)。目前的辅助研究批准的国际癌症研究机构(IARC)伦理委员会(IEC 14-04)。gydF4y2Ba
等离子体cfDNAgydF4y2Ba
在无菌EDTA-coated瓶静脉血液收集基线(第一个化疗周期之前),CT扫描响应评估(发生的第二个或第三个周期化疗后,根据中心,但最后一个周期3周后在任何情况下)。样本离心机(∼590×gydF4y2BaggydF4y2Ba在室温下15分钟)内4 h(采血。血浆分离和储存在−80°C。所有血浆样本存储集中在格勒诺布尔大学医院。样品用于本研究从格勒诺布尔运往IARC在干冰根据国际标准。gydF4y2Ba
cfDNA从血浆中提取样品使用QIAamp循环核酸工具包(美国试剂盒,瓦伦西亚,CA)制造商的指示。洗脱了50µL超纯水(分子生物学级无菌水;埃普多夫,汉堡,德国)和孤立cfDNA量化之前一直在−20°C。gydF4y2Ba
量化的cfDNA是由荧光测定术使用PicoGreen dsDNA工具包(分子探针,尤金,或者美国)制造商的指示。盘子被读Fluoroscan提升FL荧光计(热费希尔科学Oy,万塔、芬兰)的波长538 nm和485 nm emisison和激发,分别。标准曲线是通过连续稀释λ-DNA证券(生产商提供的)。空白值减去和血浆DNA含量测定的标准曲线。gydF4y2Ba
研究人员进行DNA定量失明患者的临床结果。gydF4y2Ba
统计方法gydF4y2Ba
正态分布的假设测试使用Kolmogorov-Smirnov测试连续变量。正态分布变量均值±gydF4y2BasdgydF4y2Ba;非正态分布的变量作为中位数(四分位范围(差))。非正态连续变量的比较,我们使用了Wilcoxon测试两个相关样本和Mann-Whitney u测验和克鲁斯卡尔-沃利斯测试两个或两个以上独立的样本,分别。分类变量表示为百分数。相关性评估使用枪兵的ρ。gydF4y2Ba
生存分析我们使用kaplan meier方法和中位数生存(和相应的95%置信区间)使用生存率较比较。然后,我们使用Cox回归模型(输入方法),以评估变量与生存相关。在单变量分析模型是第一组,然后我们调整了模型与相关变量和/或变量在单变量分析发现是重要的。gydF4y2Ba
所有测试都是双面的,p < 0.05被认为是显著的。Cox模型,使用了p < 0.1。统计分析了使用SPSS(19.0版本;、IBM、美国纽约Armonk)。gydF4y2Ba
结果gydF4y2Ba
人口gydF4y2Ba
的537名患者招募Pharmacogenoscan研究2005年至2010年,218例患者符合本研究的入选标准(在线补充图S1)。本系列的患者包括147例腺癌,43例鳞状细胞癌和28大细胞癌病例(gydF4y2Ba表1gydF4y2Ba)。平均随访时间为12.3(15)个月。总体而言,176名患者有四期疾病和42名患者希望疾病阶段。在响应评价没有病人显示一个完整的响应,51部分反应,132一个稳定的疾病和35累进的疾病,根据RECIST标准。gydF4y2Ba
患者纳入研究的主要特点gydF4y2Ba
cfDNA浓度和临床相关gydF4y2Ba
cfDNA浓度测定血浆样品之前收集的荧光测定术(基线)和218年与非小细胞肺癌患者化疗后的治疗。cfDNA浓度范围从2.54 ng·毫升gydF4y2Ba−1gydF4y2Ba6451.36 ng·毫升gydF4y2Ba−1gydF4y2Ba。基线cfDNA浓度(化疗之前)中值为29.5 (37.0)ng·毫升gydF4y2Ba−1gydF4y2Ba和化疗后cfDNA浓度中位数是28.9 (38.1)ng·毫升gydF4y2Ba−1gydF4y2Ba(p = 0.421)。基线和化疗后浓度都显著相关(枪兵的ρ= 0.459,p < 10gydF4y2Ba−4gydF4y2Ba)。gydF4y2Ba
没有样本之间的相关性保护时间(从2006年至2010年)和基线或最终cfDNA浓度(枪兵的ρ=−0.022,p = 0.746;和ρ=−0.045,p = 0.507,分别为基线和最终浓度)。此外,我们没有发现显著差异根据年平均浓度采样(没有显示)。gydF4y2Ba
之间没有显著关联cfDNA浓度(基线和化疗后)和肿瘤患者或特征,包括诊断、身体质量指数TNM(肿瘤、节点和转移)阶段(希望gydF4y2Ba与gydF4y2Ba(四)或组织学类型(数据没有显示)。然而,我们发现了一个积极的协会之间的基线cfDNA浓度和ECOG性能状态诊断(中位数(差)24.19 (21.86)ng·毫升gydF4y2Ba−1gydF4y2Ba34.76 (61.74)ng·毫升gydF4y2Ba−1gydF4y2Ba和108.44 (3307.37)ng·毫升gydF4y2Ba−1gydF4y2Ba性能状态0、1和2分别;p = 0.001)。有趣的是,这两个变量是相关的,尽管适度(ρ= 0.239,p < 10gydF4y2Ba−4gydF4y2Ba)。gydF4y2Ba
cfDNA浓度和晚期NSCLC肿瘤反应gydF4y2Ba
考虑到三组肿瘤反应(部分反应gydF4y2Ba与gydF4y2Ba稳定的疾病gydF4y2Ba与gydF4y2Ba进步的疾病),中等浓度无显著差异的cfDNA(基线和化疗后浓度)之间的观察组(gydF4y2Ba表2gydF4y2Ba)。此外,没有显著差异的变化cfDNA治疗期间化疗后和基线浓度(区别)肿瘤三组之间的响应(gydF4y2Ba表2gydF4y2Ba)。当考虑客观的反应,因此比较稳定的疾病+局部反应gydF4y2Ba与gydF4y2Ba进步的疾病,没有发现协会。此外,我们将人口分成三tertiles根据基线cfDNA浓度(截止值≤22.26 ng·毫升gydF4y2Ba−1gydF4y2Ba,22.27 - -42.12 ng·毫升gydF4y2Ba−1gydF4y2Ba和> 42.12 ng·毫升gydF4y2Ba−1gydF4y2Ba)。基线之间没有显著差异,根据肿瘤化疗后cfDNA浓度响应在tertiles (gydF4y2Ba图1gydF4y2Ba)。最后,我们还用RECIST响应作为连续变量(百分比),没有发现重要的协会或相关基线和化疗后cfDNA浓度(枪兵的ρ= 0.17,p = 0.806−0.12, p = 0.861 RECIST(百分比)和基准之间的相关性或化疗后,分别)。gydF4y2Ba
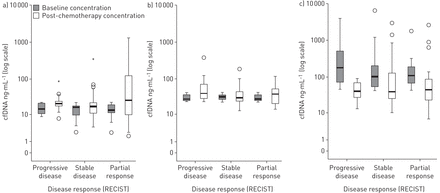
箱形图显示基线和化疗后(cf)游离DNA浓度根据tertile基线浓度和反应评估标准固体肿瘤(RECIST)响应类别。1)首先tertile;b)第二tertile;第三tertile c)。gydF4y2Ba
(cf)游离DNA浓度和肿瘤反应根据反应评估标准固体肿瘤RECIST标准gydF4y2Ba
预后价值cfDNA浓度gydF4y2Ba
中位无进展生存(PFS)是6.9个月(95% CI 6.1 - -7.7个月)和总生存期是12.3个月(95% CI 10.7 - -13.9个月)。tertile组基线cfDNA浓度最高显示比其他两个显著缩短PFS tertiles综合起来(5.7个月,95% CI 4.5 -6.9个月gydF4y2Ba与gydF4y2Ba分别为7个月,95% CI 6.3 7个月;p = 0.034)。的预后价值基线cfDNA浓度也显著时以总体存活率为结果变量:10个月(95% CI 10.7 - -13.9个月)在tertile最高gydF4y2Ba与gydF4y2Ba14.2个月(95% CI 12.6 - -15.8个月)在低/中间tertile组(p = 0.001) (gydF4y2Ba图2gydF4y2Ba)。gydF4y2Ba
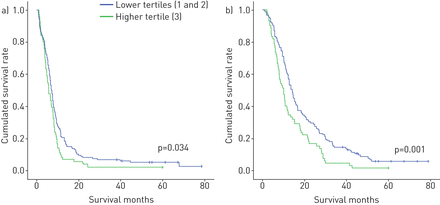
生存曲线显示无进展和b)总生存期的患者通过游离DNA浓度(最高机密gydF4y2Ba与gydF4y2Ba两个最低tertiles)。gydF4y2Ba
在单变量分析中我们发现疾病阶段,性能状态诊断和响应速度与整体生存和PFS(在线补充表S1)。这些变量和患者年龄是用于多变量Cox回归模型(gydF4y2Ba表3gydF4y2Ba)。基线cfDNA浓度仍然是重要的预后价值在这个多变量分析,重大协会总生存期和PFS的趋势的意义。总生存期,相应的调整风险比是100 030 (95% CI 100 003 - 100 057, p = 0.028),也就是说,死亡的风险增加了0.003%每增加1 ng·毫升gydF4y2Ba−1gydF4y2Ba在基线cfDNA浓度、独立的阶段,性能状况、年龄和响应速度。gydF4y2Ba
单变量和多变量Cox回归模型对无进展生存(PFS)和总生存期有关基线和化疗后(cf)游离DNA血浆浓度gydF4y2Ba
然而,我们没有发现重要的生存结果之间的联系和化疗后的浓度cfDNA (gydF4y2Ba表3gydF4y2Ba)。gydF4y2Ba
讨论gydF4y2Ba
在这项研究中,基线cfDNA浓度在NSCLC等离子体具有一个独立的预后价值。这是与之前的报道相一致。事实上,尽管一些研究没有发现任何cfDNA水平和生存之间的相关性(gydF4y2Ba11gydF4y2Ba,gydF4y2Ba15gydF4y2Ba,gydF4y2Ba20.gydF4y2Ba),大多数报告显示等离子cfDNA升高浓度之间的相关性和贫穷的生存gydF4y2Ba13gydF4y2Ba,gydF4y2Ba21gydF4y2Ba- - - - - -gydF4y2Ba24gydF4y2Ba]。GgydF4y2BaautschigydF4y2Baet al。gydF4y2Ba(gydF4y2Ba13gydF4y2Ba发现一个基线cfDNA浓度升高(> 10 ng·毫升gydF4y2Ba−1gydF4y2Ba)在多变量分析与总体存活率显著相关,独立于年龄、治疗阶段和历史。此外,三个研究[gydF4y2Ba14gydF4y2Ba,gydF4y2Ba22gydF4y2Ba,gydF4y2Ba25gydF4y2Ba)我们发现了非常相似的结果,使用tertile子组。因此我们的研究结果提供进一步的证据,从一个大系列的患者,预后价值的基线cfDNA浓度。gydF4y2Ba
相比之下,cfDNA浓度(基线,治疗期间化疗后或其变化)与化疗反应无关。先前的研究已经报道重大cfDNA浓度之间的联系和对治疗的反应,cfDNA水平下降的有效手术治疗或治疗放疗后(gydF4y2Ba11gydF4y2Ba,gydF4y2Ba12gydF4y2Ba]。在这里,我们发现cfDNA浓度不与RECIST响应两个或三个疗程的化疗治疗后。只有三个研究包括患者化疗已报告在肺癌(gydF4y2Ba表4gydF4y2Ba)。我们的研究结果是一致的两个(gydF4y2Ba13gydF4y2Ba,gydF4y2Ba14gydF4y2Ba]。lgydF4y2BaeegydF4y2Baet al。gydF4y2Ba(gydF4y2Ba14gydF4y2Ba]人口分析也分为tertiles,发现结果与我们的相似。考虑个人cfDNA变化治疗期间,GgydF4y2BaautschigydF4y2Baet al。gydF4y2Ba(gydF4y2Ba13gydF4y2Ba),我们发现cfDNA是不够可靠的响应预测:在某些病人cfDNA水平降低可能发生尽管疾病进展,而增加cfDNA水平可能发生尽管化疗反应。因此,这似乎证实cfDNA浓度不预测化疗治疗在非小细胞肺癌治疗的反应。gydF4y2Ba
(cf)游离DNA作为一种工具来监视对治疗的反应gydF4y2Ba
cfDNA不是特定肿瘤条件。也可能升高的炎症和感染状况。因此,高浓度的cfDNA和不良预后之间的联系可能与肿瘤负担和/或并存病(gydF4y2Ba6gydF4y2Ba]。然而,我们的研究结果强调的局限性的分析cfDNA的总量。事实上,cfDNA整体浓度的变化可能反映不仅改变循环肿瘤(ct) DNA,但其他医疗条件可能导致cfDNA的增加,包括化疗诱导裂解在正常细胞,从而促进正常cfDNA的释放到血液中。这或许可以解释为什么总浓度cfDNA可能不是化疗反应的预测。关注ctDNA(可检测到存在的遗传和表观遗传改变特定于原发性肿瘤)可能是一个更适当的替代标记。例如,NgydF4y2BaewmangydF4y2Baet al。gydF4y2Ba(gydF4y2Ba20.gydF4y2Ba)最近报道的方法称为CAPP-Seq(癌症个性化分析的深度测序),允许多个类的敏感检测体细胞变化和ctDNA的量化。另一项研究中,由MgydF4y2BaarcqgydF4y2Ba等gydF4y2Ba。(gydF4y2Ba26gydF4y2Ba]表明,监测EGFR突变等离子体的患者进行有针对性的EGFR-tyrosine激酶抑制剂(TKI)准确地评估肿瘤治疗反应和可能检测进展和发展机制下治疗。然而,进一步的研究需要ctDNA在临床实践证明其有效性。因此,我们的研究结果强调cfDNA总浓度的糟糕表现评估化疗治疗的反应,尽管cfDNA仍然是一个潜在的有趣的生物标志物如果专注于其肿瘤特异分数。gydF4y2Ba
据我们所知,我们的研究领域是最大的肺癌肿瘤反应和生存。此外,它包括一个同质性的治疗,治疗反应是评估使用RECIST标准根据建议NSCLC的临床实践和人口分析这是一个经典的晚期NSCLC患者的人口。患者早期发展(n = 6)或死亡(n = 25)没有研究Pharmacogenoscan,因此并不包括在我们的研究(gydF4y2Ba16gydF4y2Ba]。从这个排斥潜在的偏见,可能结果预计将可以忽略不计,因为小数量的情况。它还应该指出,在目前的研究中,使用PicoGreen cfDNA量化了,一个简单的方法,可以很容易在临床实践中实现。尽管大多数其他研究使用了定量(q)实时PCR定量,我们选择了PicoGreen方法之间因为一个良好的和积极的相关性一直观察PicoGreen和qPCR化验gydF4y2Ba27gydF4y2Ba]。尽管qPCR灵敏度高、精度高,它需要一个特定的自动化系统和仍然是昂贵的,而PicoGreen方法是一种快速、有效、可靠和廉价cfDNA量化的方法。它还展示了高检测的局限性,使这项技术适合等离子cfDNA分析(gydF4y2Ba27gydF4y2Ba,gydF4y2Ba28gydF4y2Ba]。gydF4y2Ba
cfDNA浓度中位数通过这种方法在非小细胞肺癌和以前公布的数据是一致的,尽管平均浓度低于其他系列报道中,其中一个从我们的团队gydF4y2Ba13gydF4y2Ba,gydF4y2Ba14gydF4y2Ba]。这种差异在绝对浓度可能来自血液样本处理、等离子体隔离和存储或DNA定量方法,以及人口的异质性进行了研究。执行在这个工作中,等离子体隔离在4 h血图,根据相同的所有参与中心的标准程序,限制污染来自血液细胞的DNA。此外,cfDNA提取和量化集中表现在一个实验室标准协议来限制偏差量化的中心。关于样品的潜在影响保护时间(长期冻结可能改变cfDNA)的质量和数量,我们已经检查,没有样本之间的相关性保护时间和cfDNA浓度。gydF4y2Ba
总cfDNA浓度似乎是肺癌的一个独立的预后因素。尽管总cfDNA浓度不是信息评估化疗和其他的有效性验证预后因素已经存在(如疾病阶段或性能状态(gydF4y2Ba3gydF4y2Ba,gydF4y2Ba4gydF4y2Ba]),cfDNA仍然是有趣的在此设置。的确,跟踪的分数变异等生物标志物cfDNA EGFR激酶抑制剂治疗期间似乎特别适合用来评估TKI响应和早期检测疾病进展(gydF4y2Ba26gydF4y2Ba]。使用cfDNA液体活检也非常有前途的非侵入性体分子剖析在基线或后续对重采样gydF4y2Ba26gydF4y2Ba,gydF4y2Ba29日gydF4y2Ba,gydF4y2Ba30.gydF4y2Ba]。gydF4y2Ba
总之,我们的数据表明,量化cfDNA从等离子体可能是一个有用的非侵入性技术,临床实践。在晚期非小细胞肺癌,高基线cfDNA浓度在等离子体与预后不良相关独立于年龄、性能状况、阶段和响应。然而,总cfDNA不是与化疗反应。cfDNA的效用,特别是肿瘤特异cfDNA,应该在较大和routine-based试验评估。gydF4y2Ba
脚注gydF4y2Ba
社论评论看gydF4y2Ba欧元和JgydF4y2Ba2015;46:1548 - 1550 (DOI: 10.1183/09031936.01482 -2015)gydF4y2Ba
可以从本文的补充材料gydF4y2Bawww.qdcxjkg.comgydF4y2Ba
本研究在clinicaltrials.gov注册标识号gydF4y2BaNCT00222404gydF4y2Ba。gydF4y2Ba
支持声明:Pharmacogenoscan研究得到了法国卫生部(国立医院临床研究计划(PHRC) 2008)。克莱尔天梭被授予从济贫院支持公民里昂(Annee矫揉造作的)。gydF4y2Ba
利益冲突:披露可以找到与本文的在线版本gydF4y2Bawww.qdcxjkg.comgydF4y2Ba
- 收到了gydF4y2Ba2015年4月30日。gydF4y2Ba
- 接受gydF4y2Ba2015年7月5日。gydF4y2Ba
- 版权©2015人队gydF4y2Ba
引用gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba
- ↵gydF4y2Ba















