摘要
一些特发性肺纤维化患者呼吸状态急性加重,导致大量发病率和死亡率。胃内容物的隐匿性误吸被认为是导致这些急性加重的一种可能机制。我们试图确定从特发性肺纤维化急性加重期患者获得的支气管肺泡灌洗液中胃蛋白酶(胃误吸的标记物)与疾病稳定期患者获得的胃蛋白酶是否升高。
在一项特征良好的患者的病例对照研究中获得灌洗样本。急性加重的定义采用标准标准。比较病例组和对照组灌洗胃蛋白酶水平,并与临床特征和病程相关。
急性加重24例,稳定对照30例。两组间基线人口统计学无显著差异。胃蛋白酶水平是急性加重状态的一个指标(p=0.04)。平均而言,急性加重患者的胃蛋白酶水平高于稳定对照组。这种差异是由8名胃蛋白酶水平≥70 ng·mL的患者(33%)组成的亚组引起的−1.胃蛋白酶水平不是生存时间的独立预测因子。
这些结果提示隐匿性误吸可能在某些特发性肺纤维化急性加重的病例中起作用。
特发性肺纤维化(IPF)是特发性间质性肺炎最常见的形式,患病率为14-42.7 / 10万[1].目前尚无成熟的治疗方法,诊断后的中位生存期为~ 3年[2,3.].IPF的自然史在历史上被认为是一个渐进的过程,其特征是肺功能随着时间的推移稳步下降。最近已认识到,许多病人在一段相对稳定的时期后,其呼吸状况可能出现急性恶化[4].当没有发现明显的诱因时(如。感染或肺栓塞),这些急性恶化被称为IPF的急性加重。IPF急性加重的特征是高分辨率计算机断层扫描(HRCT)显示新的磨玻璃影,外科肺活检显示弥漫性肺泡损伤(DAD) [4- - - - - -6].
胃食管反流继发的胃内容物隐匿性误吸被认为是IPF急性加重的一个可能原因[4,7].先前的研究表明,大多数IPF患者有胃食管反流[8- - - - - -10].胃食管反流被怀疑是肺误吸的危险因素[11].胃内容物误吸可引起急性肺损伤,肺活检DAD表现为急性肺损伤[12].
胃蛋白酶是由胃主细胞和粘液颈细胞分泌的一种蛋白水解酶,是一种非活性胃蛋白酶原。支气管肺泡灌洗(BAL)胃蛋白酶已被证明是肺移植后胃误吸的有用生物标志物[13,14]、儿科[15],气喘[16]和机械通风的人群[17].特别是,BAL胃蛋白酶已被证明是诊断儿童胃食管反流相关误吸的高度特异性(100%)和敏感性(80%)方法[15].一些正常健康人BAL中胃蛋白酶含量很低(可达2.6 ng·mL)−1) [18].我们假设,与稳定IPF相比,一些IPF急性加重患者的BAL胃蛋白酶水平会升高,这表明胃内容物误吸导致了急性加重的一个亚组。
材料与方法
研究设计和患者群体
这是一项针对2000年至2009年在韩国首尔峨山医疗中心就诊的IPF急性加重和IPF稳定患者的病例对照研究。受试者被纳入机构审查委员会批准的调查IPF的纵向队列研究。所有患者均获得知情同意。
IPF的诊断是根据修改的共识标准进行多学科回顾[19].稳定IPF定义为IPF患者在BAL时没有加重。BAL是在初次IPF诊断前后获得的(IPF诊断与BAL之间的中位时间差为-1天,四分位差(IQR)为-9-13天)。这些患者是从一个较大的队列中随机选择的作为对照人群。IPF急性加重的诊断依据已发表的标准[4].简单地说,急性加重的定义是:30天内呼吸道症状恶化,HRCT上出现新的双侧磨玻璃影,没有其他病因的证据。入院后不久进行BAL(入院与BAL时间的中位差为1天,IQR为1 - 4天)。所有IPF急性加重患者和可用的BAL液均纳入本研究。
记录患者的人口统计学、烟草使用史(分为从不吸烟、以前吸烟和现在吸烟)、身体质量指数(BMI)和肺功能值。根据患者或医生对疾病的报告,将合并症记录为存在或不存在。利用患者病历获取患者特征和生命状态。
支气管镜检查和BAL胃蛋白酶测定
按先前报告进行BAL [20.].对于急性加重病例,进行BAL作为患者急性呼吸道症状诊断评估的一部分。对于IPF稳定的对照组,进行BAL作为其间质性肺疾病初步诊断评估的一部分。对于病例和对照组,在右侧中间叶或舌叶的单个子节段进行BAL,并注入至少100 mL无菌盐水。BAL液在冰上保存,并在收集后1小时内进行处理,然后在-80°C冷冻。BAL胃蛋白酶水平使用市售酶联免疫吸附测定(USCN生命科学,武汉,中国)。
放射学检查
所有HRCT扫描均由一名对所有受试者的状态(病例或对照组)和临床病程不知情的放射科医生进行复查。测定毛玻璃影、实变、蜂窝状和网状的程度,以及整体计算机断层扫描(CT)评分[21].裂孔疝的存在和大小(颅侧长度和直径)是胃食管反流的已知危险因素[22),也下定了决心。从最上面的裂孔疝图像到食管裂孔的水平测量颅侧尺寸。在裂孔疝胸内部分的最大横向尺寸处测量直径。
统计分析
描述性统计以均数±表示sd或中位数(IQR)。组间比较采用非配对t检验、Mann-Whitney秩和检验、卡方检验或Fisher's Exact检验。采用Logistic回归分析来确定急性加重状态的预测因素。采用线性回归分析方法分析各自变量与BAL胃蛋白酶水平的关系。Cox比例风险模型用于确定急性加重队列中生存时间的预测因素。生存时间计算从BAL时间到死亡或审查时间。分析也使用胃蛋白酶作为一个二分类变量,使用稳定IPF组的第95百分位值作为阈值。所有数据分析均使用Stata版本11 (StataCorp, College Station, TX, USA)进行。所有试验均为双侧,显著性水平为0.05。
结果
病例和对照组的临床、放射学和BAL特征
共确定了24例IPF急性加重病例和30例稳定的IPF对照。两组之间的基线人口统计数据没有显著差异,包括年龄、性别、吸烟状况、BMI和报告的合并症(表1).
两组间毛玻璃不透明评分(p<0.01)、实变评分(p<0.01)、网状评分(p<0.01)、CT总评分(p<0.01)差异均有统计学意义(表2).两组间蜂窝评分差异无统计学意义。两组间在放射学鉴定的裂孔疝的患病率和大小上没有差异。
BAL液清晰,大体检查均无明显血液。急性加重组BAL红细胞(RBC)计数明显高于稳定组(p<0.01)。两组间BAL细胞总数无差异(表2).急性加重组BAL中性粒细胞百分比高于稳定组(p=0.02), BAL巨噬细胞百分比低于稳定组(p<0.01)。
急性加重状态的指标
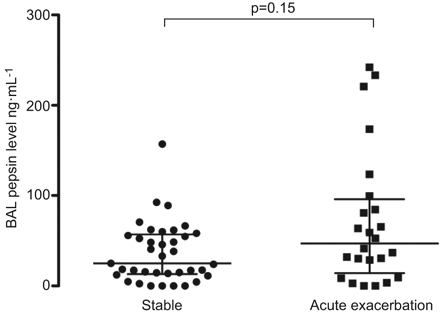
IPF急性加重期BAL胃蛋白酶中位水平为46.8 ng·mL−1为35.4 ng·mL−1在稳定IPF对照组中(p=0.15) (图1).在双变量回归中,BAL胃蛋白酶增加1个单位是急性加重状态的指标(OR 1.02, 95% CI 1.001-1.03;p = 0.04)。BAL胃蛋白酶水平增加1个标准差(24.8 ng·mL)−1)的比值比为1.46 (95% CI 1.03-2.09;急性加重状态P =0.04)。
没有与急性加重状态相关的临床变量(表3).放射性裂孔疝的患病率或大小与急性加重状态无相关性。BAL中性粒细胞百分比升高和肺泡巨噬细胞百分比降低是急性加重状态的指标。调整BAL中性粒细胞百分比后,BAL胃蛋白酶水平仍然是急性加重状态的指标(OR 1.02, 95% CI 1.002-1.03;p = 0.03)。
稳定型特发性肺纤维化(IPF)患者支气管肺泡灌洗(BAL)胃蛋白酶水平与IPF急性加重期比较水平线代表中位数,第25百分位和第75百分位。
BAL胃蛋白酶水平与急性加重
IPF急性加重期8例(33%)BAL胃蛋白酶水平高(即。高于稳定对照人群的95百分位,70 ng·mL−1).高胃蛋白酶急性加重组和低胃蛋白酶急性加重组在基线临床特征(包括胃食管反流或误吸史、使用强的松或抗反流药物、生存时间)方面无显著差异(表4).急性加重组的两名受试者在BAL时插管。BAL胃蛋白酶水平低组(36.8 ng·mL)−131.8 ng·mL−1分别)。两组间在放射性裂孔疝的存在、磨玻璃样混浊的百分比、实变或网状方面也无显著差异。高BAL胃蛋白酶组BAL淋巴细胞百分率高于低BAL胃蛋白酶组(p<0.01)。BAL胃蛋白酶水平低和高组红细胞计数无显著差异(p=0.24)。
急性加重队列中的7名受试者在诊断IPF时也曾接受过BAL (即。相应的稳定样品)。在这个小的亚组中,稳定(中位数为17.3 ng·mL)与无总体关系−1, IQR 0-92.5 ng·mL−1)和急性加重(中位数为52.5 ng·mL−1, IQR 8.5-63.6 ng·mL−1) BAL胃蛋白酶水平(p=0.61;图2).然而,7名受试者中只有1人在急性加重期间BAL胃蛋白酶水平较高(220.8 ng·mL)−1);这表明与受试者的稳定值(23.8 ng·mL)相比,BAL胃蛋白酶水平增加了大约10倍−1).
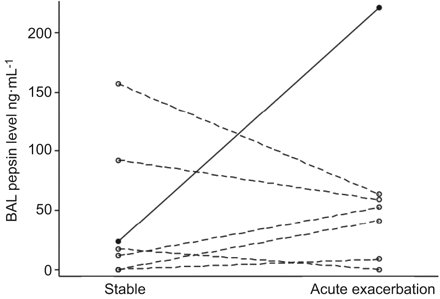
7例特发性肺纤维化稳定期和急性加重期患者的支气管肺泡灌洗液胃蛋白酶水平。每条线代表一个研究对象。闭圈和实线代表急性加重期BAL胃蛋白酶水平高的受试者。开圈和虚线表示急性发作期间BAL胃蛋白酶水平低的受试者。
BAL胃蛋白酶水平的预测因子
在病例和对照组的联合组中,临床变量包括年龄、性别、胃食管反流史、吸烟史、BMI、抗反流药物使用、强的松使用和插管状态与BAL胃蛋白酶水平无关(数据未显示)。急性加重状态和HRCT上网状增加与较高的BAL胃蛋白酶水平相关(p=0.01和p=0.02)。没有其他放射学变量是重要的指标,包括放射性裂孔疝。BAL淋巴细胞百分比增加与BAL胃蛋白酶水平升高相关(p<0.01)。BAL胃蛋白酶水平与BAL RBC计数无相关性(p=0.79)。在稳定的IPF队列中,BAL胃蛋白酶水平与%预测总肺活量(TLC)之间无相关性(p=0.83;图3)或% pred用力肺活量(FVC) (p=0.39)。
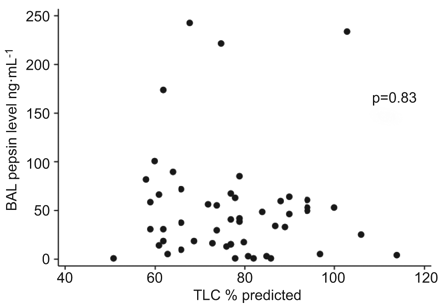
支气管肺泡灌洗(BAL)胃蛋白酶水平与%预测总肺活量(TLC)的相关性。
讨论
本研究探讨IPF患者隐匿性误吸与急性加重的关系。在双变量和多变量分析中,BAL胃蛋白酶升高可预测急性加重状态,这是由胃蛋白酶水平显著升高的病例亚组(33%)的存在所驱动的。尽管这种关系不大,但这一发现提供了证据,表明神秘的渴望可能在IPF急性加重中起作用。
人们对IPF患者胃食管反流和隐匿性误吸的作用越来越感兴趣[7].据推测,胃内容物的隐匿性吸出可能与IPF的自然史有关。一个病例系列描述了4例IPF患者在接受胃食管反流药物治疗后临床病程稳定(基于肺功能测试)[23].另一项研究回顾了14例等待肺移植的IPF患者,并显示这些患者在腹腔镜尼森基金复制术中氧需求稳定[24].这些研究支持IPF中胃食管反流和隐匿性误吸与疾病进展的可能关联。
我们的研究从两个方面扩展了这种关系。首先,我们在大多数稳定IPF患者中发现了可测量的BAL胃蛋白酶,这表明IPF中隐匿性误吸是常见的。其次,BAL胃蛋白酶升高与急性加重状态的关联提供了证据,表明隐匿性误吸可能在IPF的自然史中发挥作用,可能是通过引起一些急性加重。这种联系的另一种解释可能是急性呼吸失代偿导致吸入量增加(因此BAL胃蛋白酶水平升高)通过增加胸内压力波动。在我们稳定的IPF队列中,我们发现用% pred TLC和FVC测量的疾病严重程度与BAL胃蛋白酶水平之间没有相关性。然而,我们没有急性加重组的肺功能测试结果,在急性呼吸失代偿的情况下有可能发生微吸。
在本研究中,在病例和对照组之间没有BAL胃蛋白酶水平的临床预测因素。这一发现与已知的胃食管反流的体征和症状之间的不一致以及食管pH值测试中存在病理性反流是一致的[8,9].重要的是,我们没有功能性食管数据(如。24小时pH监测和测压),因此BAL胃蛋白酶水平升高的病例是否改变了食管功能尚不清楚。我们发现高BAL胃蛋白酶组和低BAL胃蛋白酶组在放射性裂孔疝方面没有差异,这可能有助于识别患者存在吸气相关急性加重的风险。在IPF急性加重病例中,BAL胃蛋白酶水平与生存率之间也没有相关性。这并不出乎意料,因为IPF急性加重的特征是DAD,其自然史可能与潜在的病因无关。
BAL差异细胞计数与IPF急性加重和BAL胃蛋白酶水平相关。BAL中性粒细胞百分比增加是急性加重的一个指标,提示生存率较差。这些发现与先前发表的数据一致,即BAL中性粒细胞与IPF 1年生存率降低有关[25].有趣的是,BAL胃蛋白酶水平高的IPF患者急性加重期BAL淋巴细胞比例较高。这一发现的意义尚不清楚,但它可能表明更显著的吸入与淋巴细胞募集到肺有关。
本研究的目的不是确定急性加重发展的危险因素,因此没有确定“高危”人群。我们配对样本中有限数量的急性加重患者(n=7)表明基线BAL胃蛋白酶水平不能预测未来的急性加重,但这个亚组不足以解决这个问题。我们的数据不支持从稳定的患者中获得BAL胃蛋白酶水平。基线胃食管反流和误吸与未来急性加重的关系应成为未来纵向研究的基础。
我们认识到这项研究还有其他局限性。首先,BAL胃蛋白酶不是一种直接的测量方法。然而,鉴于胃蛋白酶在下呼吸道中通常含量不高,其在BAL中的测量应该是一种有用的误吸生物标志物[15,18,26].其次,BAL胃蛋白酶水平可能受吸痰以外的因素影响,如支气管镜被上气道分泌物污染、BAL液浓度变化、患者的床位或近期插管。通过纳入稳定的IPF对照组和标准化的BAL技术,部分控制了这些因素。第三,有一个理论上的担忧,即我们可以从非胃源检测胃蛋白酶原(即。血液)由于抗体的交叉反应。然而,我们发现BAL RBC计数与BAL胃蛋白酶水平之间没有相关性。第四,BAL的位置在右脑中叶或舌部,HRCT扫描不一定是病变最严重的区域。这是可能的BAL胃蛋白酶水平可能已经较高,有最病变的区域取样。最后,考虑到使用图表回顾来确定医学合并症,我们很可能低估了胃食管反流病和其他合并症在这一人群中的患病率。
总之,这项研究表明,在IPF急性加重患者亚组中BAL胃蛋白酶升高。这些发现支持了胃内容物隐匿性误吸在IPF急性加重中起作用的假设。未来的研究应该在更大的、多中心的研究中证实这些结果。
致谢
作者贡献如下。参与研究的概念、假设和设计(J.S. Lee, T.E. King Jr, H.R. Collard);患者的选择和样本的获取(D.S. Kim),数据的获取(J.S. Lee, J.W. Song, B.M. Elicker, P.J. Wolters, D.S. Kim);数据分析和解释(J.S. Lee, P.J. Wolters, T.E. King Jr, D.S. Kim, H.R. Collard);大量参与了文章的写作和/或修改(J.S. Lee, P.J. Wolters, T.E. King Jr, D.S. Kim, H.R. Collard)。所有作者都赞成这个版本的手稿。
脚注
有关编辑评论,请参见242页.
支持声明
本研究由美国国家心肺血液研究所(Bethesda, MD, USA)的HL 973832和HL 086516资助。
权益声明书
D.S. Kim和H.R. Collard的兴趣声明可以在www.www.qdcxjkg.com/site/misc/statements.xhtml
- 收到了2011年3月22日。
- 接受2011年10月31日。
- ©2012人队