抽象
不可分型流感嗜血杆菌(NTHi)是原发性纤毛运动障碍(PCD)患者最常见的病原体。我们推测,PCD患者的纤毛运动异常和气道上皮细胞上的低气道一氧化氮(NO)水平可能有利于NTHi的定植和生物膜的发展。
我们使用原代上皮细胞共培养模型来研究NTHi感染。采用气液界面培养方法将PCD患者和非PCD患者的原代气道上皮细胞分化为睫状上皮细胞,并与NTHi共培养。
与非PCD细胞相比,NTHi在PCD上皮细胞上的粘附更大(p<0.05), PCD上皮上NTHi的分布显示生物膜中更多聚集的NTHi (p<0.001)。除了纤毛运动缺陷外,PCD细胞与非PCD上皮细胞在父子关系程度、上皮完整性、细胞因子、LL-37和NO的产生方面均无显著差异。与单独使用抗生素治疗相比,外源性NO和抗生素治疗PCD上皮显著降低了生物膜中的NTHi存活能力。
受损的纤毛功能是在PCD气道上皮细胞与非PCD上皮相比底层易感性的NTHi生物膜发展的首要缺陷。虽然NO的反应是类似的,采用有针对性的NO用抗生素在生物膜中增强的杀的NTHi的,提示有新的治疗方法。
抽象
体外研究表明PCD航空风险NTHi生物膜定植;新无药克服抗生素耐受性http://ow.ly/GrXC30e4Tqv
介绍
气道中运动的纤毛有助于清除粘液纤毛(MCC),这是保护宿主免受呼吸道感染的基础。原发性纤毛运动障碍(PCD)是一种遗传异质性的疾病,其特征是纤毛功能异常,MCC受损。患者从小就以反复发作的慢性窦肺感染、慢性中耳炎(OM)和进行性化脓性肺病为特征[1]。
不可分型流感嗜血杆菌(NTHi)是一种革兰氏阴性的coccobacillus,它与肺炎球菌属属从患有PCD的儿科病人的上、下呼吸道分离出来的最常见细菌病原体[2]和慢性OM [3.]。NTHi生物膜存在在活的有机体内(4,5),体外OM患儿的腺样上皮或中耳上皮活检[6,7]。
生物膜是在与呼吸粘膜表面相关联的exopolymeric矩阵包膜细菌的自组织聚集体8−10],并在OM慢性上、下呼吸道感染中出现[6,囊性纤维化(CF) [11]、慢性鼻窦炎[12和非cf型支气管扩张[13]。生物膜的形成增加了细菌对抗生素治疗的抗拒和宿主先天免疫反应,从而有助于慢性化脓性呼吸道疾病的病理生理[14,15]。虽然已经在细菌-病毒共感染的动物模型中研究了纤毛功能异常对呼吸道感染的影响[16,17,细菌感染尚未在PCD中得到广泛研究。
对于未了解的原因,患者的PCD与非PCD患者[相比具有低的气道的一氧化氮(NO)的水平18,19]。NO,通过宿主上皮细胞和先天免疫细胞产生的,可以响应于由感染有些呼吸菌是低的[20.,21]。我们以前观察到的感染原代培养的PCD和非PCD上皮,平均NO水平无差异与基础NO水平相一致报道他人[20.,22]。然而,我们发现无论是促炎细胞因子刺激还是NTHi感染,PCD上皮细胞都显著增加NO产量,与非PCD细胞相似[22]。由于呼吸道感染的NTHi与PCD儿童的敏感性,我们假设患者PCD上皮细胞可能是在允许增加的NTHi的坚持和后续生物膜发展。为了解决这一假设,我们开发了使用纤毛PCD或非PCD气道上皮细胞,在空气 - 液体界面(ALI)和分化感染了PCD临床分离株NTHi的人类初级共培养模型。在本研究中,我们使用了ALI-上皮细胞的NTHi共培养模型[22更广泛的研究:1)气道细胞对NTHi的反应,包括NO的产生,和2)生物膜靶向NO供体增强NTHi抗生素治疗的能力。
材料和方法
研究参与者
我们招募了15例PCD的诊断,根据2009年欧洲指南[23, 10名健康志愿者和9名非PCD引起的呼吸系统症状患者(表S1)。我们之前已经公布了我们国家PCD中心采用的诊断方法的细节[24]。该研究得到了英国国家卫生服务研究伦理委员会批准(06 / Q1702 / 109和08 / H0502 / 126),我们获得书面知情同意书。
PCD患者临床NTHi分离株的培养和生物膜的形成
NTHi的四个儿科患者PCD(HI1-HI4)从冷冻储备传代培养分离[25,并经革兰氏染色、V、X诊断盘检测和聚合酶链反应验证[6]。的NTHi在脑心脏浸液培养基中培养,在37℃在补充有氯高铁血红素和烟酰胺腺嘌呤二核苷酸(sBHI)至OD6000.1(〜2×108CFU·毫升−1) [25]。测定生物膜的生长情况在体外在用结晶紫(CV)染色和集落形成单位,一式三份实验(CFU)对巧克力血琼脂计数(CBA)[26,27以及使用荧光的扫描电子显微镜和共聚焦显微镜原位杂交(鱼)7,28]。
上皮细胞与NTHi共培养模型
关于上皮细胞恢复和后续分析的详细信息可在补充材料中找到,并已在其他地方发表。简单地说,最初的人鼻上皮细胞在ALI中培养,直到分化和纤毛化[29,30.]。We used ALI-cultured cells within 1 month. NTHi was co-cultured on the apical surface of epithelial cells from five PCD and nine non-PCD subjects and compared with five non-infected non-PCD controls. We inoculated approximately 1×108CFU·毫升−1用500 L无抗生素ALI培养基(感染多重性100)在transwell膜上ALI培养细胞上。共培养37℃/5% CO2for 72 h with daily medium changes and washed with Hanks' buffered salt solution (HBSS) to remove non-adherent bacteria prior to analyses [25]。
每天测量跨上皮电阻(TEER),并减去背景以确认上皮完整性(EVOM 2上皮伏特计,世界精密仪器公司,佛罗里达,塞拉索塔)[31]。纤毛运动频率(CBF)和能动的面积百分比到非运动纤毛上之前和NTHi的共培养期间ALI培养的细胞用全场测量快速傅立叶变换分析(ImageJ的https://imagej.net/与内部编写的插件)高速视频显微视频。简单地说,样本在37℃下使用装有40倍物镜的倒置Olympus IX71显微镜(Olympus, southdown -on- sea, UK)(1场=90×95视位m)和以每秒250帧的速度记录睫状体运动的PC2 Photron FASTCAM高速视频[29]。
气道纤毛细胞上NTHi的特征
从transwell膜上刮取细菌和上皮细胞入sBHI,连续稀释,涂布于CBA上,37℃/5% CO孵育2前CFU枚举(一式三份实验)。我们还利用共聚焦显微镜通过与16S的Hinf FISH探针确定的NTHi对ALI的文化样本[6,7]和在纤毛β微管蛋白通过免疫荧光共标记[32]。(;珀金埃尔默考文垂,UK版本6.0.1)穿过膜直径连续字段是通过使用一SP5共焦激光扫描显微镜(Leica Microsystems公司,米尔顿凯恩斯,UK)和每场的NTHi体积通过Volocity 3D图像分析软件,计算成像。选定的transwell膜中除去并处理和成像的使用FEI广达200扫描型电子显微镜(FEI,荷兰埃因霍温)25,28]。
细胞因子和LL-37对NTHi感染的反应
ALI培养的基底外侧培养基接种前冷冻,然后每天与NTHi共培养。我们测量纤维母细胞生长因子β(FGF -β),粒细胞集落刺激因子(g - csf)、粒细胞−巨噬细胞集落刺激因子(gm - csf)、白细胞介素- 6 (il - 6)、interleukin-1受体拮抗剂(IL-1Ra)、单核细胞趋化蛋白1 (MCP-1)、巨噬细胞炎性蛋白1α(MIP-1α),肿瘤坏死因子-α(TNF -α)和血管内皮生长因子(VEGF) fluorokine人类multianalyte分析(MAP)测定Bio-Plex 200分析仪检测(研发系统,阿宾顿,(英国)上清液(每96口井50厘升一式两份)(补充材料)[33]。白细胞介素-8分别由人IL-8 DuoSet ELISA试剂盒(DY208, R&D systems)检测,辣根过氧化物酶(HRP)底物由温度计微板阅读器(Molecular Devices, Sunnyvale,美国加利福尼亚州)按照说明书检测。
从ali培养的细胞中提取的顶端上清液(100滴L PBS)在共培养前冷冻,然后每天接种NTHi。样品点置于硝酸纤维素膜上,用1:1000 rabbit anti-LL-37 antibody (AB64892;随后是1:10 000 HRP标记的山羊抗兔二抗。洗涤后,使用VersaDoc成像仪检测Immuno-star鲁米诺化学发光底物,并使用Quantity One v4.6.9软件(Bio-Rad Laboratories, Watford, UK)进行定量。将LL-37浓度(重复实验)与连续稀释重组LL-37肽(AB140725;Abcam)。
NO产量气道上皮细胞和治疗外源性NO
Transwell membranes of live ALI-cultured epithelial cells were treated with 10 µM 4-amino-5-methylamino-2′,7′-difluorofluorescein diacetate (DAF-FM) to assess the presence of NO [34]。在固定上皮细胞培养物中免疫荧光标记物用于本地化NO合酶(NOS)(神经元(nNOS的),诱导型(iNOS)的和内皮型(eNOS)同工酶[32使用共焦显微镜。
ali培养的上皮细胞nthi共培养(72小时)用HBSS清洗以去除非附着菌[25),then treated with either 4 mg·mL−1阿奇霉素,50µM cephalosporin-3ʹ-diazeniumdiolate没有供体药物前体PYRRO-C3D,或两者的结合阿奇霉素和PYRRO-C3D 2 h。所有处理均采用含1% DMSO的HBSS(也用作未处理对照),NTHi CFUs在CBA中按上述(n=4)列举[25]。
统计方法
经t检验和曼 - 惠特尼U检验用执行的GraphPad Prism软件(6.0a版本,2012年,格拉夫派得软件公司)。使用了Sidak-Bonferroni法用于多重比较的t-检验适应的p值。P <0.05表明具有统计学意义。
结果
研究参与者
15 PCD和19个非PCD参与者的人口和临床细节介绍表1。所有PCD患者均表现出睫状功能异常(表S1)。
临床NTHi分离的PCD患者生物膜的发展
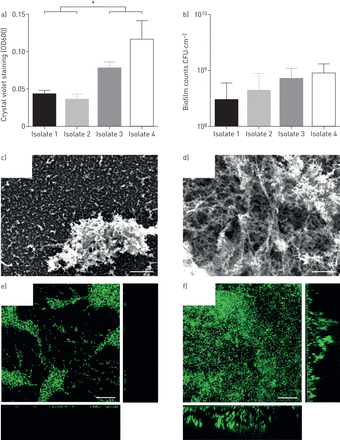
我们评估四个PCD的NTHi的能力分离,以形成通过标准测定法(CV,CFU计数),并通过扫描电子显微镜和共聚焦显微镜使用的Hinf特异性16S FISH探针(辅助材料)的生物膜(图1)。与首次培养NTHi的儿童分离株(HI1和HI2)相比,临床分离株(HI3和HI4)显示生物膜发育,外聚物基质的CV染色明显更明显(图1一个)。然而,CFU计数不菌株之间显著不同(图1 b)。分离株HI4用于以后的实验。
生物膜形成由原发性纤毛运动障碍(PCD)不可分型流感嗜血杆菌菌(NTHi)分离物(HI1-4)。条形图显示结晶紫染色(a)和平均值±SEM日志生物膜集落形成单位计数的平均值±SEM光密度(OD600)(CFU·厘米2(b) pcd -临床NTHi分离株(HI1-4)培养72 h (*: p<0.05)。扫描电子显微照片(x 4000) (c, d)突出了HI1和HI4的细菌聚集物和外聚物基质。共聚焦显微照片(e, f)描绘了72 h HI1和HI4生物膜与cy3标记杂交的代表性最大投影(z -堆叠)和正交切片(x/z右和y/z底部图像)流感嗜血杆菌特殊的荧光原位杂交探针(绿色)。年代cale bars=10 µm (c, d); 40 µm (e, f).
上皮细胞与NTHi共培养
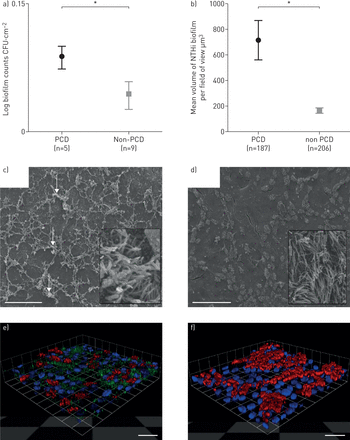
无论PCD患者还是非PCD患者,NTHi粘附于纤毛气道上皮细胞。然而在72 h时,NTHi的存活率明显高于3.8×106的CFU(±7.5×105)上PCD与2.0×10上皮相比6的CFU(±4.8×105)对非pcd上皮细胞(p<0.05)图2一个),符合扫描电子显微镜的数据(图2 c, d)。PCD细胞内有细菌细胞(生物膜)的不连续粘附聚集物(图2 c而NTHi细菌细胞在非pcd上皮细胞(图2 d)。
描述的non-typeable流感嗜血杆菌(NTHi)与气液界面(ALI)分化和纤毛化的气道上皮细胞共培养。均值±扫描电镜日志生物膜CFU·厘米2after 72 h of NTHi co-culture on ALI ciliated primary ciliary dyskinesia (PCD) (n=5), and non-PCD (n=9) epithelial cells (*: p<0.05). Representative scanning electron micrographs (×4000) (c, d) demonstrate increased bacterial aggregates and exopolymeric matrix formation (arrows) on PCD ALI-cultured ciliated epithelial cells in contrast to non-PCD cells. NTHi co-cultured on ALI ciliated PCD and non-PCD epithelial cells were labelled for confocal analysis. Bacterial cells were labelled with the CY3-流感嗜血杆菌特殊的荧光原位鱼杂交探针(绿色),纤毛用抗微管蛋白抗体(红色)标记,胞核用SYTOX blue(蓝色)反染。b)均值±扫描电镜PCD上每个视野的生物膜体积(鱼探针标记)(由共聚焦显微镜z堆叠的Volocity软件分析确定)与非PCD纤毛ALI培养物(*:P <0.05)。Confocal micrographs (e, f) are represented as three-dimensional opacity views of ciliated PCD (e), and non-PCD (f) cells co-cultured for 72 h with NTHi. Scale bars=20 µm.
我们使用共聚焦显微镜对共培养进行成像,使用FISH标记NTHi和抗管蛋白抗体标记纤毛。正交切片图像分析共聚焦显微镜z堆显示平均值±扫描电镜在PCD细胞培养的上皮细胞中,NTHi生物量(每视野)是其4倍(710±150个单位面积)3.),而非pcd原代细胞ALI培养(160±20 ampm)3.)(P <0.001)(图2 b)。聚集的NTHi在PCD上主小区上皮生物膜即有不正常的或静态的纤毛是明显的(图2 e)。相反,在纤毛功能正常的非pcd上皮上NTHi标记较少(图2 f)。
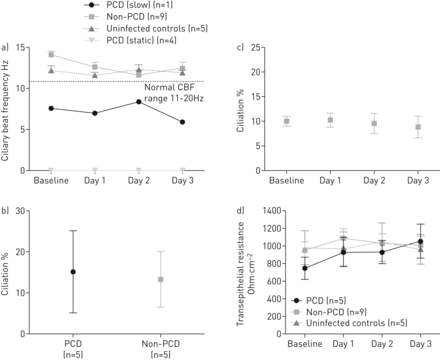
PCD细胞显示静态(N = 4)或慢运动障碍(N = 1)纤毛。The CBF of non-PCD epithelial cells remained within normal ranges (11–20 Hz) throughout the 72 h of NTHi co-culture, indicating that NTHi did not impair ciliary motility (图3a)。光镜和扫描电镜观察到,PCD和非PCD细胞与ali培养的上皮细胞的父子关系相似(图3b)。在非pcd气道细胞共培养期间,非pcd细胞每视野运动纤毛面积百分比未发生变化(图3c)。TEER用于测量之前和心尖的NTHi接种到纤毛ALI-培养的原代气道细胞后上皮细胞屏障功能。The TEER plateau reached prior to NTHi infection was the same for PCD and non-PCD cells and was maintained for 72 h in co-culture, demonstrating epithelial integrity (p-values ranged from 0.35 to 0.93) (图3D)。
比较原发性纤毛运动障碍(PCD)和非PCD空气-液体界面(ALI)培养的气道上皮细胞的睫状上皮百分比、睫状上皮功能和跨上皮电阻(TEER),以及不可分型效应的特征流感嗜血杆菌(NTHi)纤毛共培养。均值±扫描电镜ciliary beat frequency (CBF) (in Hz) of PCD (n=4 static cilia and n=1 slow dyskinetic cilia) and non-PCD (n=9) measured before (baseline) and daily during 72 h of NTHi co-culture, compared to uninfected non-PCD controls (n=5). The normal CBF range is 11–20 Hz at the Southampton PCD Centre and infection did not modify CBF in any group. b) The mean±扫描电镜分化ALI培养基上的鳞茎免疫细胞纤毛的覆盖率与鳞茎分化百分比相对应。每个样品随机选择10个显微镜视野进行比较,PCD (n=5)和非PCD (n=5)样品的父子关系百分比没有差异。c)均值±扫描电镜percentage ciliation calculated from whole field fast Fourier transform analysis of CBF where the ratio of motile to not-motile pixels (15 360 data points per total field of view from a video recorded at a resolution of 512×480; analysis box size 4×4 pixels). The mean±扫描电镜NTHi共培养后,非pcd (n=8) ali培养细胞的父子关系百分比在72小时内没有变化。d)均值±扫描电镜三通在欧姆·厘米2of NTHi-infected PCD (n=5) and non-PCD (n=9), measured before (baseline) and daily during co-culture for 72 h was compared to uninfected non-PCD controls (n=5). TEER remained stable and was not significantly different between groups.
细胞因子和LL-37对NTHi感染的反应
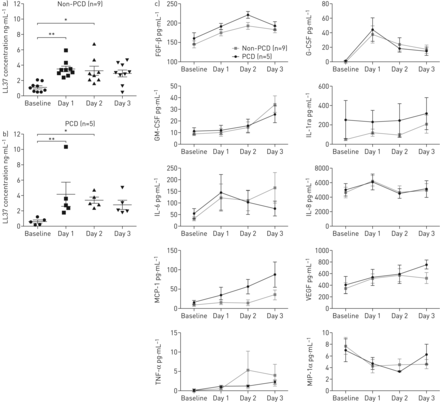
平均±年代EM concentration of cationic LL-37 peptide secreted from epithelial cell ALI-cultures peaked 24 h following NTHi inoculation, where an 8.8±2.9-fold increase in PCD and 3.8±0.6-fold increase in non-PCD samples was observed, but values remained within group variation at baseline and after inoculation (图4 a, b)。NTHi共培养72小时前或每日取样的PCD或非PCD细胞基底侧培养基中FGF- inhibitor、G-CSF、GM-CSF、VEGF或IL-1Ra、IL-6、IL-8、MCP-1、MIP-1、TNF- TNF-的水平(图4 c)没有显著差异,表明PCD气道细胞产生的细胞因子和趋化因子与非PCD细胞相似。这些数据表明,PCD和非PCD上皮细胞对NTHi产生类似的防御反应。
原发性纤毛运动障碍(PCD)和非PCD上皮细胞LL-37和细胞因子反应到不可分型流感嗜血杆菌(NTHi)感染。点和在(a)和(b)中须图展示了中位数(四分位数间距)阳离子型抗微生物肽的浓度,导管素LL-37(NG·毫升−1),在非PCD (a)和PCD (b)患者的气液界面(ALI)培养上皮细胞的根尖上清液中测量,在NTHi共培养72小时之前(基线)或每天之后。(c)均值±扫描电镜浓度(pg·毫升−1)的10种细胞因子:碱性成纤维细胞生长因子-细胞生长因子(FGF- gh)、粒细胞集中性刺激因子(G-CSF)、粒细胞巨噬细胞集中性刺激因子(GM-CSF)、白细胞介素-6 (IL-6)、白细胞介素-8 (IL-8)、白细胞介素-1受体拮抗剂(IL-1ra)、单核细胞趋化蛋白-1 (MCP-1)、巨噬细胞炎性蛋白-1 (MIP-1)在NTHi共培养72小时之前(基线)和每天之后,在PCD (n=5)和非PCD (n=9)上皮细胞ALI的基底外侧培养基中,对肿瘤坏死因子- TNF- TNF和血管内皮生长因子(VEGF)进行共培养。*: p<0.05, **: p<0.01。
NO产量气道上皮细胞和治疗外源性NO
PCD患者气道内NO水平极低[18,19]。然而,通过对上皮细胞进行免疫荧光标记,我们发现在PCD纤毛细胞和非PCD细胞中均存在nNOS、iNOS和eNOS同工酶(图5)。此外,我们没有检测到在PCD和非PCD ALI培养样品使用DAF-FM,强烈荧光在NO的存在(图5)。
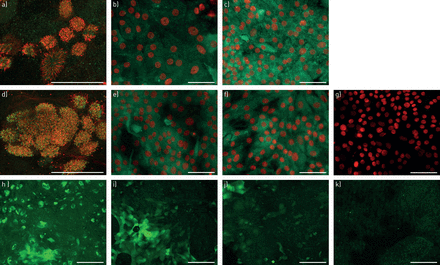
比较了纤毛原发性纤毛运动障碍(PCD)和非PCD在气液界面(ALI)培养的气道上皮细胞一氧化氮合酶(NOS)同工酶和一氧化氮(NO)。典型的阿里分化上皮细胞显微图显示,在非PCD (a - c)和PCD (d - f)受试者中,荧光标记了神经元性NOS (a, d)、诱导性NOS (b, e)和内皮性NOS (c, f)抗体,以及Alexafluor488共轭二抗(绿色)(每组n=3个重复)。消极的控制主要抗体被省略了,确认没有非特异性二级抗体标签non-PCD ALI-cultured上皮细胞(g),代表显微图显示的存在不通过4-amino-5-methylamino-2 ', 7 ' -difluorofluorescein二乙酸(DAF-FM)标签(绿色)在一个non-PCD (h)和金刚石(i, j)在两个科目(n = 4 non-PCD金刚石受试者和n = 3测试)。非PCD和PCD阿里培养的NOS同工酶或DAF-FM标记没有明显差异。非常低的自发荧光背景中可以看到一个未经处理的人类支气管上皮细胞系(16 hbe)负控制(k),细胞核染色与赫斯特(红色)(b, c, eg)和纤毛与一个反co-labelledβ微管蛋白抗体(红色所示)(a, d)。合并后的最大的预测共焦(a, d, h-k)或epifluorescent (b, c, eg)显微镜图片使用100×40×目标(40µm规模酒吧)。
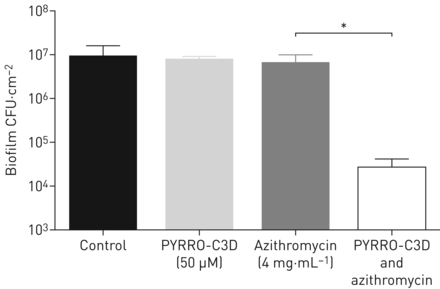
我们之前已经证明,没有调节NTHi代谢在体外(25]。因此,我们测试了外源性NO治疗的影响的NTHi对PCD纤毛上皮细胞成长。上皮细胞的NTHi共培养物用头孢菌素-3'-二醇二氮烯NO供体的前药,吡咯-C3D,其释放NO以下通过β内酰胺酶[活化处理25]。我们发现4毫克·毫升−1阿奇霉素治疗,超过浮游最低抑菌浓度(1磅·毫升)−1),未能杀死PCD上皮细胞上的生物膜NTHi。相比之下,当吡ro - c3d与阿奇霉素同时使用时,NTHi存活率下降了近3 log (图6)。这些结果表明,在NTHi的PCD上的生物膜纤毛上皮细胞是抗生素治疗的宽容和容忍被从药到NTHi的NO的β内酰胺酶介导的递送废止。
抗生素和一氧化氮(NO)供体前药治疗原发性纤毛运动障碍(PCD)空气-液体界面(ALI)分化的气道上皮细胞。图中显示平均值±扫描电镜log生物膜菌落形成单位计数(CFU·cm)2),用于贴壁(生物膜)不可分型流感嗜血杆菌(NTHi)在ALI处培养并纤毛的PCD气道上皮细胞上共培养72 h (n=4)。共培养孵育2小时,无论是没有(对照组)或没有供体前药吡rro - c3d(50粒粒M), 4 mg·mL−1阿奇霉素,或两者兼而有之。经吡喃- c3d /阿奇霉素处理后,NTHi存活率降低了近3 log。*: p < 0.05。
讨论
Our principal finding was that NTHi formed adherent biofilms on ALI-cultured PCD ciliated airway cells significantly more than on non-PCD controls over 72 h of co-culture, with the only attributable difference being ciliary dysfunction of PCD samples. Since host–pathogen interactions have not been widely studied in the context of PCD, these results are novel. NTHi is prevalent in PCD and other diseases in children associated with impaired mucociliary clearance, such as CF [35]和慢性OM [36]。在慢性或反复呼吸道感染的两个CF和慢性OM [病理生理的NTHi生物膜的发展特点6,4,13],但鲜为人知的是,NTHi的感染PCD。我们假设从PCD患者的气道上皮细胞不正常的纤毛运动可能是在允许的NTHi定植和生物膜的发展。据我们所知,我们的极化气道上皮ALI文化感染模型是首次检验的NTHi的从PCD患者和非PCD的主要捐助者呼吸道纤毛细胞的影响。生物膜发展以前从年轻CF患者的NTHi分离证明了使用的Calu-3细胞共培养[11]。但是,因为将Calu-3细胞不具缘毛,这种模式没有评估纤毛的NTHi的粘附和生物膜发展中的作用[37]。
我们比较PCD和非PCD上皮细胞的反应,包括分泌炎症和抗微生物蛋白和上皮完整,纤毛和纤毛功能下的NTHi共培养。细胞因子的产生,包括促炎细胞因子和参与白细胞募集的趋化因子,和抗微生物肽LL-37的分泌水平,分别为PCD和非PCD共培养物之间相称。上皮的完整性也是在气道上皮细胞与相媲美的NTHi共培养。虽然所有PCD ALI-培养的上皮细胞具有功能失调纤毛运动,而相比之下,功能正常的非PCD上皮细胞(表S1),总的纤毛感染前是相似的,通过扫描电子显微镜和免疫荧光标记β-所证明微管蛋白利用共聚焦显微镜纤毛。重要的是,感染的NTHi没有不利正常纤毛功能影响对非PCD ALI培养气道细胞在实验期间(运动纤毛的CBF和面积百分比)。综上所述,我们发现PCD和非PCD之间的唯一区别是在纤毛运动,支持在PCD异常纤毛功能增加NTHi的生物膜发展的风险的假设。
PCD患者表现出不正常的气道(特别是鼻)NO水平低,其原因仍在争论中[18]。先前已发现ALI培养PCD初级上皮细胞不能增加感染后早期NO水平肺炎链球菌,提示PCD上皮细胞没有生物合成和iNOS诱导异常[20.]。相反,本文的工作扩展了我们之前的研究,并证明了PCD和非PCD上皮细胞的生物合成在组成和NTHi感染后都不相似[22]。我们现在已经还评估使用互补的方法和显示NO的水平,PCD和非PCD细胞表现出类似的NO生物合成和NOS同工酶表达该共局部化与纤毛标记β微管蛋白,共培养期间。这些研究支持我们以前的数据显示,PCD上皮细胞能够biosynthesising NO的。初级上皮细胞NO的反应可能,但是,变化与细菌的类型,和特别是PCD的NTHi分离株不诱导与观察到的细胞毒性作用肺炎链球菌(38]。
我们的结果表明的NTHi存在于矩阵封闭聚集体粘附到偏振纤毛PCD上皮细胞[8]。众所周知,生物膜的发展会降低抗生素治疗的效果。我们的数据表明,气道上皮细胞培养物上的NTHi生物膜对阿奇霉素处理具有耐受性,可轻易杀死浮游NTHi [25],因为它是在减少的NTHi生存能力无效的。与此相反,用新的前体药物吡咯-C3D,设计用于靶向NO以下β内酰胺酶激活特异性释放细菌阿奇霉素的共同施用,通过在PCD上皮细胞近3日志减少的NTHi生存能力。这些结果支持最近与研究肺炎链球菌(28]及NTHi [25]表示NO在这些呼吸道细菌调节代谢活性,导致增加的抗生素敏感性的作用。重要的是,我们的呼吸道上皮细胞共培养模式允许的抗NTHi的生物膜处理与人原代细胞生理相关的上下文中的翻译研究。这些结果表明,与抗生素联合治疗感染需要进一步的研究给予该辅助外源性NO治疗。
这项研究有一定的局限性。First, because PCD cases are rare (≈1:10 000), the co-culture experiments are challenging to replicate in high numbers. Secondly, we examined a limited number of clinical NTHi isolates in co-cultures. Thirdly, our studies focused on epithelial cells and did not investigate other innate cell responses that are important in host defences to NTHi, or may contribute to disease progression. Despite these limitations, our studies suggest that NTHi biofilms play a role in the chronicity of respiratory infections in PCD and provide hypothesis-driven research questions for further work assessing mechanisms of pathogenesis.
综上所述,本研究报告了PCD患者原发性纤毛上皮细胞NTHi感染的主要观察结果。首先,与具有正常运动能力的非PCD气道细胞相比,PCD中异常的纤毛功能似乎更有利于NTHi生物膜的发育。其次,ali培养的PCD患者的原代气道细胞在NTHi感染后表现出了多种防御反应,与非PCD气道细胞表现出类似的细胞因子和LL-37的产生。第三,尽管大多数PCD患者鼻部NO水平异常低,但经阿里培养的PCD患者气道细胞在NTHi共培养后与非PCD细胞产生了相似水平的NO。第四,本研究表明,我们的共培养模型为研究抗感染治疗提供了一个稳健的分析方法。最后,我们证明了靶向外源性无增强抗生素杀伤生长在PCD上皮上的生物膜中的NTHi,提示了一种新的治疗PCD NTHi感染的方法。
补充材料
披露的信息
补充材料
S.N.浮士德erj - 00612 - 2017 - _faust
M.J.凯尔索erj - 00612 - 2017 - _kelso
J.S.A.卢卡斯erj - 00612 - 2017 - _lucas
确认
我们要感谢南安普敦大学生物医学成像部门的Anton Page和Patricia Goggin,感谢他们在电子显微镜技术方面的建议和帮助。我们也要感谢James Thompson和Janice Coles对细胞培养的帮助和支持,以及那些提供从我们的初级纤毛运动障碍中心(英国南安普敦大学医院NHS基金会信托)获得的鼻刷样本的患者。
脚注
这篇文章有补充材料可从www.qdcxjkg.com
支持声明:UHS的国家PCD中心是由英国国民保健署委托和资助的。南安普顿的PCD研究由NIHR南安普顿呼吸生物医学研究组和南安普顿NIHR Wellcome信托临床研究机构支持。W.T. Walker, C.L. Jackson, S.A. Collins, J.S.A. Lucas和L. Hall-Stoodley是成本行动BEAT-PCD (BM1407)的参与者。M.J. Kelso感谢来自澳大利亚囊性纤维化研究信托基金(ACFRT)的资助。本文的资金信息已存入Crossref资助者注册表。
利益冲突:披露可以在这篇文章旁边找到www.qdcxjkg.com
- 收到2017年3月23日。
- 接受2017年6月4日。
- 版权所有©ERS 2017年