抽象的
吸入含有糖皮质激素的药物可降低慢性阻塞性肺病(COPD)急性加重的频率(主要是感染源),同时反而增加了其他呼吸道感染的风险。目的是确定吸入糖皮质激素对慢性阻塞性肺疾病患者气道微生物负荷的影响,并评估潜在炎症谱对气道定植和微生物组的影响。
这是一项概念验证前瞻性、随机、开放标签、盲终点研究。60例稳定期中度COPD患者随机接受沙美特罗50 μg +丙酸氟替卡松500 μg联合吸入或沙美特罗50 μg连续吸入12个月,每日两次。主要结果是治疗过程中痰细菌载量的变化。
与沙美特罗相比,沙美特罗加氟替卡松治疗1年显著增加了痰细菌负荷(p=0.005),改变了痰微生物组成,增加了潜在致病菌的气道负荷。仅在吸入糖皮质激素治疗的基线痰液或血液嗜酸性粒细胞(≤2%)水平较低的患者中观察到细菌负荷增加,但在基线嗜酸性粒细胞水平较高的患者中没有观察到细菌负荷增加。
长期吸入皮质类固醇治疗会影响稳定COPD中的细菌负荷。降低嗜酸性粒细胞计数与呼吸道细菌负荷增加有关。
抽象的
长期吸入皮质类固醇增加了低嗜酸性粒细胞计数的COPD患者的气道细菌载荷http:///wly/8no530emsza.
介绍
慢性阻塞性肺病(COPD)的恶化对疾病的生活质量,预后和进展产生重大影响[1].
吸入皮质类固醇(ICSs)联合长效β2激动剂(LABAs)是COPD加重高风险患者的推荐治疗方法[1].有趣的是,最近的分析表明,血液嗜酸性粒细胞可预测ICS / Laba组合在预防Laba的加剧中的更大疗效,从而提供了可能的生物标志物,以确定更有可能受益于这种治疗的患者[2-4.].
有一个明显的悖论与COPD中的ICS治疗有关:一方面,IC / Labas有效地防止与感染性Aetiology通常相关的COPD恶化[5.另一方面,相同的组合增加了肺炎的风险[6.那7.].
许多COPD患者具有慢性细菌定植的气道,稳定COPD中的气道细菌载荷与加重频率有关[8.]肺功能下降[9.].以前曾观察到,在主要使用含ics药物治疗的人群中,一年多的气道细菌负荷增加[9.].也有报道称,在接受高剂量ICSs的COPD患者中有更大的痰细菌负荷[10.].这些观察报告中没有控制组。
在此背景下,我们进行了概念验证预期,随机开放标签,盲目的终点(探测),研究专门用于测定与Laba或Laba / ICS组合的12个月治疗的对痰细菌负荷的影响COPD患者。此外,通过痰/血液梭中分层分层的探索性分析进行了评价潜在的炎症性曲线对慢性气道殖民化和微生物组的影响。
方法
学习规划
连续COPD患者,根据全球慢性阻塞性肺病定义的倡议[1],于2009年5月4日至2012年5月7日举办的资格,参观了意大利费拉拉大学哮喘和COPD研究中心的门诊诊所的患者队列。60例类固醇 - 诺维患者患者稳定疾病(支气管扩张剂FEV1≥50和<80%预测)招募了Laba Salmeterol(Salm)治疗,以参与该探针研究[11.].
这是一个探索性概念验证研究,旨在探讨长期治疗与吸入的皮质类固醇(氟替卡松丙酸盐)的效果加入稳定COPD患者的痰细菌载体上的吸入皮质类固醇。出于道德原因,我们不允许注册患者患有更严重的疾病,仅用Laba治疗,作为比较器臂,被认为是不恰当的,患者将被治疗。
患者被随机地接受单独接收SALM(每日50μg一次吸入,N = 30)或IC / LABA吸入的固定组合(Salmeterol50μg加氟代滴水500μg(Salm / Fp每日一次吸入,N = 30))12个月。在基线评估和随机化后(访问0),患者在门诊设定中每3个月内看到。在恶化症状的情况下,指示患者联系中心进行联络员访问。用抗生素和全身皮质类固醇治疗加剧发作[1].该研究符合《赫尔辛基宣言》,工作得到了机构伦理委员会的批准,并获得了每个受试者的知情书面同意。补充材料中报道了研究设计、随机化和掩蔽程序、加重定义、肺功能测量和生活质量评估的详细描述。
这项研究注册于Clinicaltrials.gov., 数字NCT01213693。
随机化和掩蔽
患者随机地接受SALM / FP(每日50 /500μg;研究组,N = 30)或SALM(仅为每日50μg;对照组,n = 30)12个月(图1).根据使用随机数发生器编制的列表,患者被随机分配到治疗组。
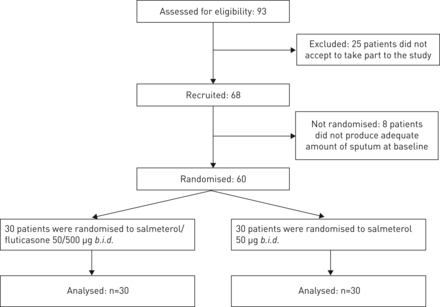
试用简介。
进行医疗评估和患者临床和功能数据收集的医生无权访问预定访问的微生物数据。以盲方式评估细菌和病毒的微生物载荷。因此,以盲化的方式获得用于评估初级和二次结果的数据(探测研究)[11.].
微生物化验
在补充材料和补充表S1和S2中,详细说明了痰收集和分析,定量细菌学,呼吸道病毒和非典型细菌检测和微生物鉴定和分析测定。
嗜酸性粒细胞计数和细菌负荷
由于先前据报道,血液中血液中≥2%的差异计数是在诱导的痰中预测嗜酸性粒细胞计数≥3%[12.我们表演了后HOC根据基线血液(≥2%或<2%)和痰嗜酸性粒细胞的水平评估细菌负荷变化的分析。复发间痰嗜酸性粒细胞症定义为高嗜酸性粒细胞计数(高于截止值),≥50%的可用样品在至少四次访问(在基线时,在治疗结束时,至少在研究期间的预定访问中)。
分析
主要结果是评估使用SALM/FP治疗12个月后COPD患者痰中的细菌负荷与使用SALM治疗的COPD患者痰中的细菌负荷。次要结果包括病毒检测评估;临床和炎症结果在补充材料中有详细说明。
在以前的研究中[9.,细菌负荷平均增加0.46 log10.菌落形成单位(CFU)ML-1在30例稳定COPD患者的痰样品中观察到1年。这些受试者的绝大多数(93%)被含有药物的IC治疗。基于这些场所:1)我们假定在不接受含有ICS药物的COPD患者1年内的痰细菌载量没有变化,2)我们计算出细菌负荷将增加到约0.5日志的平均值。10. CFU mL-1在含有ICS药物治疗的COPD人群中,含有含IC的药物。随着我们只招募类固醇 - 天真的主体,我们认为预期痰细菌载荷的增加比被认为是参考的[9.],增加20%的0.6 log值10. CFU mL-1是我们主要分析的假设。这种变化的共同标准偏差被假定为0.8。I型误差设置为0.05,功率至少为80%。在这些假设下,每个治疗组的样本量必须为30名患者用于分析。同样数量的受试者被纳入该研究,在超过1年的时间里观察到痰细菌载量增加[9.].
用于统计比较的测试在补充材料的方法部分中详述。P值为0.05或更小被认为是表示统计学意义。
结果
研究设计和患者特征
共有93名患者达到包含的标准;然而,25名患者拒绝参加该研究。招募了68名患者,但八名患者没有随机化,因为它们在基线上没有产生足够的痰液(图1).三十名患者随机以每天两次接收一次吸入Salm / FP50/500μg的组合,并随机选择30分钟以每天两次接受50μg。两组患者的人口统计特征没有发现差异(表格1)和合并的条件(补充材料)。进一步的患者在补充材料中详述了患者的临床和功能特性。
痰液取样
根据纳入标准,所有患者在基线(每组n=30)和1年研究治疗结束时采集痰标本(用于本研究的初步分析)。在3个月、6个月和9个月的研究访问中,90%、80%和83%的ICS/LABA治疗患者获得了痰液,86%、73%和83%的单独使用LABA治疗的患者获得了痰液。24例(80%)接受ICS/LABA治疗的患者和22例(73%)单独接受LABA治疗的患者可获得所有来访的样本。在所有研究来访的样本患者与整个研究人群之间没有发现人口统计学特征和/或肺功能的差异。
稳定状态下的细菌和病毒载量
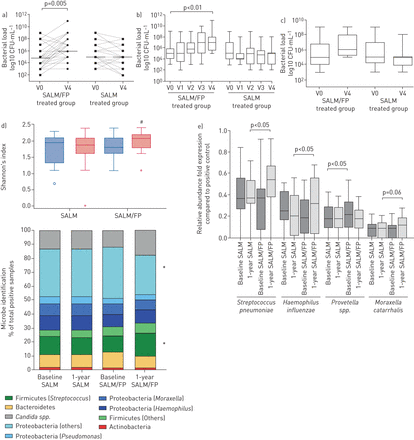
两组间的基线细菌负荷相似(图2A和2C)。
气道细菌载荷和微生物组分析。a)总细菌载荷显示为每mL的菌落形成单位(CFU),并在基线(V0)和12个月的痰液中的疗效(v4)中评估来自萨尔梅勒/氟丙酮(Salm / Fp)的痰液中和单独的鲑鱼。b)在每次访问时获得并评估痰样品的患者的总细菌负荷。c)在基线(V0)和12个月的治疗后(V4)后,致病气道细菌(PPB)的气道细菌负荷。d)痰微生物组合物(Shannon指数评估的α多样性)限制为通过多重16S RNA QPCR测定检测到的41个细菌或真菌病原体(*:P <0.05与基线形式的植物诱导术中,在盐糖醇/氟替卡松治疗的盐酸盐中团体;#:P <0.05相对基线)。e)通过多重16S RNA QPCR测定在痰液样品中的微生物定量。
在Salm / FP组的研究结束时,在样品中培养物中生长的任何类型的细菌的总细菌载荷显着增加,而最终研究总细菌的末端将显着增加(p = 0.005)LOAD没有从SALM组中的基线改变(图2A).在Salm / FP组中,当分析限制在每次访问时,在Salm / FP组中确认了Salm / FP组中的慢性细菌载荷的增加,每次访问图2B.).
补充表S3列出了通过研究中的常规培养测定检测到的潜在致病气通路(PPB)。对于来自访问1(基线)的患者观察到特定潜在病原体的检测的高变异性,在两种治疗组中访问4(12个月)。在ICS处理和检测特异性个体病原体之间没有发现任何相关性。在稳定的条件下,痰液中PPB的检测速率在整个研究中没有显着变化(PPB在每次研究访问中约三分之一的痰样品中鉴定)(补充表S3)。相反,在Salm / FP组的研究结束时观察到PPB载荷的增加(图2C.)虽然在考虑的样本数量相对较少的样本中的变化并没有达到统计学意义。这些数据通过在痰液中进行的PCR测定来确认用于选定的细菌病原体(补充图S1)[10.].
在基线和基团之间和之间的研究期间没有观察到呼吸道病毒检测的差异。通过实时PCR分析,在辅助材料中详述的研究中发现了低病毒检测率。检测到的病毒在补充表S3中详述。
痰微生物鉴定
痰微生物分析在120种成对的痰液样品中进行(基线上的60个样品相对60个样本在1年治疗结束时)单独使用SALM (n=30)或SALM/FP联合治疗(n=30)的患者。采用多重定量PCR方法检测41种细菌或真菌病原体(补充材料)的细菌16S rRNA和真菌核糖体rRNA基因序列。总体而言,我们发现ICS/LABA组的微生物数量显著增加(+12%;p<0.05),但在LABA治疗组中没有(−3%;p = 0.23)。在基线和1年时,两组的微生物谱图没有发现不同成分(图2D,补充表S6)。然而,在使用SALM/FP治疗的患者中(但在单独使用SALM治疗的患者中没有),我们发现平均α多样性显著增加(图2D1年后1年后,补充表S7和表S8)。微生物组合物也朝向更高的静脉(+ 6%; P <0.05)的检测增加念珠菌SPP。(+ 5%; p = 0.10),其平行于植物体外检测的显着降低(-9%; p <0.05)(图2D).
相对丰富增加肺炎链球菌肺炎料(P <0.05)和流感嗜血杆菌SALM/FP治疗1年后发现(p<0.05),而单独使用SALM没有发现(p<0.05)。在仅接受LABA治疗的患者中,我们发现相对丰度显著增加Fvootella.SPP。(P <0.05)。未发现痰微生物组合物的其他显着变化(图2E.).
临床结果
尽管该研究不是旨在评估治疗组对COPD临床结局的影响,但我们发现,在相关临床结局方面,ICS/LABA患者比单独使用LABA患者有小幅改善(如。SGRQ)详述补充材料(补充图S2)。与去年相比,Salm / FP组中发现了一种不显着的趋势,在加剧率的减少时发现了恶化率。在SALM组(补充材料)中没有观察到加剧频率的变化。
稳定状态下的气道炎症
在基线和在稳定条件下的研究组内和研究组之间的研究期内没有记录总和差异炎症细胞计数的差异(补充表S4)。
COPD加重期间的气道炎症和微生物学
在单独使用Salm / Fp和Salm处理的患者中发生二十二和28例恶化,其中没有任何需要住院治疗。
在加剧的中性粒细胞计数和总细菌载量之间发现显着的相关性(P = 0.041; r = 0.29图3.).与稳定状态相比,与稳定状态相比,在加剧中的气道炎症和细菌(包括PPB)和病毒载量的详细描述可在补充材料中获得(补充图S3)。
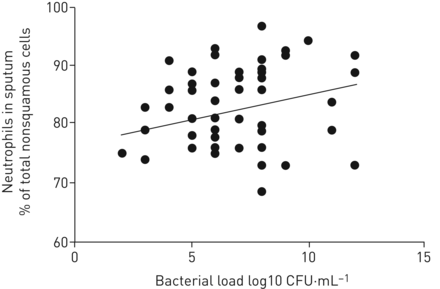
急性加重时痰中性粒细胞计数与气道总细菌负荷的相关性。
ICS/LABA联合治疗患者细菌负荷变化的预测因子
SALM / FP组中的细菌载荷的变化与任何基线人口统计学特征,功能参数和/或SGRQ值以及整个研究(补充材料)的变化不相关。
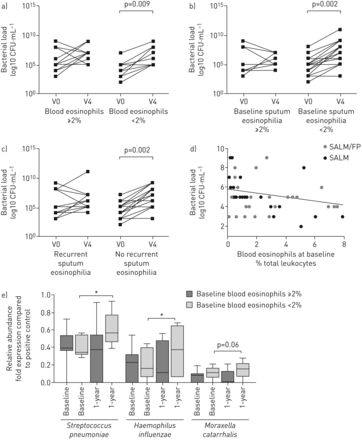
血嗜酸性粒细胞细胞计数分别在Salm / Fp和Salm组中的87%和83%的患者中获得募集。在基线的血嗜酸性粒细胞计数和痰嗜酸性粒细胞计数之间发现了显着的相关性(P=0.004;r = 0.37;补充图S4)。当患者基于血嗜酸性粒细胞分层时,1年的IC / Laba治疗导致显着增加(+ 2.47±0.44原木10. CFU·ML.-1)在患有基线的血嗜酸性嗜酸性血粒细胞的患者的总细菌载荷中,但在≥2%基线血液粒细胞水平的患者中(+ 0.91±0.37原木10. CFU·mL-1)(图4A).后者组由53%的IC / Laba治疗患者组成,在该研究中评估的患者。由于少数患者(10%)报道了基线的痰嗜酸性粒细胞水平≥3%,我们进行了分层分析,其截止值为2%痰嗜酸性粒细胞。含有ICS的一年治疗导致总细菌负荷的显着增加,这些细菌负荷限于患有<2%基线痰嗜酸性粒细胞(+ 2.14±0.31原木的患者10. CFU·mL-1)细菌载荷没有变化(+ 0.34±0.42日志10. CFU·mL-1)≥2%的基线痰嗜酸性粒细胞患者(后者组包含37%的IC / Laba治疗的人群)(图4B.).多元回归分析证实了基线治疗方案和痰嗜酸性粒细胞水平之间的相互作用作为增加的细菌载荷(补充材料和表S9)的预测因子。
a)基线(v0)的总细菌负荷和在用基线血液粒细胞(Salm / Fp)处理的患者的痰液中的治疗(V4)痰液中的痰液嗜酸盐(Salm / FP)计数≥2%或<2%的全白细胞。b)基线(V0)的总细菌载荷和在用基线痰液嗜酸钇患者治疗的患者的痰液中的治疗(V4)后(V4)≥2%或<2%的总炎症细胞的乳糖样品。c)基线(V0)的总细菌载荷和12个月的治疗(V4)在痰液中,用或没有复发痰嗜酸性粒细胞瘤治疗的患者的痰液≥2%在预定访问时获得的可用样品中的至少50%(至少2次访问)在1年的研究期间。d)基线血液嗜酸性粒细胞和细菌载荷之间的相关性。e)痰微生物定量Salm / FP处理的基线血液粒细胞患者水平<2%或≥2%。*:P <0.05。
同样,微生物分析表明,在用Salm / FP处理的COPD患者中,相对丰度增加S.肺炎和H.流感仅限于血液粒细胞的人<2%。在这些患者中,我们还发现了相对丰度的数值增加moraxella catarrhalis.1年后的Salm / FP治疗与基线相比(图4E.).
此外,1年ICS治疗没有改变复发性痰嗜酸性粒细胞增多患者的总细菌负荷(+0.75±0.39 log)10. CFU·mL-1),而观察到与基线相比观察到显着的细菌负荷增加(+ 2.15±0.32日志10. CFU·mL-1)在没有复发性痰嗜酸性粒细胞症的患者中(后者组包含60%的IC / Laba治疗的患者,在研究期间测试至少四个痰样品)(图4C.).
值得注意的是,在血嗜酸性粒细胞计数和总痰细菌载量之间的基线下发现了显着的负相关(P = 0.003; r = -0.28;图4D.).
与基线血嗜酸性细胞计数≥2%(85%)的患者相比,基线血嗜酸性细胞计数<2%的患者在病情加重期间更容易检测到PPB相对分别为61%;p = 0.082)。
讨论
本研究以受控的方式设计,以评估1年治疗的效果与吸入的皮质类固醇FP加入到Salm(Laba)中作为主要结果,在痰微生物载量上。Corticsteroid-NaïvePopd患者仅招募到该研究。
通过常规的痰培养物,并通过分子技术证实,我们发现FP加入到Salm中,来自中等气流限制的中度COPD患者的痰液中的痰液中增加的细菌负荷。相反,在呼吸道病毒的检测频率下没有发现任何变化。观察到IC治疗对细菌和病毒载体的差异效应的原因尚不清楚。涉及用于对抗细菌和病毒感染的机制之间的差异可以解释对类固醇治疗的不同易感性。此外,病毒检测在稳态疾病中相当低,[13.].
我们的研究结果表明,除了Salm之外,还具有高剂量FP的治疗增加了稳定状态COPD患者气道中的气道细菌负荷。与之前的偶尔报告的差异[9.那10.],这是第一次前瞻性研究,为我们的最佳知识,支持将此假设测试为主要结果。几项研究调查了IC对细菌病原体肺宿主防御的影响。通过干扰先天抗微生物活性的关键要素,例如1)抑制巨噬细胞抗菌活性的关键要素,FP可以损害细菌间隙[14.], 2)抑制巨噬细胞释放TNF、IP-10等细胞因子[15.3)下调MHC II类分子在巨噬细胞中的表达[16.]减少自适应免疫应答[17.].然而,关于细菌免疫应答的ICS对细菌免疫反应的调节效果的对比数据,一些研究表明FP强调人类气道上皮细胞中的PPB间隙[18.增强气道黏膜中参与固有免疫反应的分子的上皮表达[19.].需要进一步的研究来探讨吸入的皮质类固醇对针对细菌感染的宿主防御机制的影响,特别是在COPD患者中患有气道细菌定植的患者,并记录了对感染的免疫应答受损的免疫应答[20.].我们的研究证明,在这种临床条件下,与IC的长期治疗的最终结果是气道细菌负荷的净增加。
关于炎症标志物与细菌载荷变化的相关性检查,我们发现含ICS的治疗导致嗜酸性粒细胞计数低的患者的细菌载荷显着增加。已知嗜酸性粒细胞有助于对病原体的免疫应答。它们可以作为CD4的抗原呈递细胞+T细胞,从而促进T细胞增殖和极化[21.].此外,嗜酸性粒细胞通过嗜酸性粒细胞阳离子蛋白(ECP)和主要碱性蛋白质(MBP)表现出有效的杀菌活性[22.].因此,它们可以在先天和适应性免疫反应中发挥重要作用。实际上,嗜血糖病症被认为是严重感染缺乏临床结果的独立预测因子,例如菌细菌[23.]和COPD加剧[24.那25.].符合这些概念,并与最近的出版物[26.[我们发现基线COPD患者的嗜酸性粒细胞和气道细菌载量之间的负相关性。
ICS / Laba在嗜酸性患者中仅比Laba更有效地更有效[2那3.],其中最常发生的嗜酸性激素加剧[12.],细菌性病学不太可能[12.那27.].在这种嗜酸性环境下,我们的研究表明,慢性ICS治疗不能改变细菌负荷。相反,低嗜酸性粒细胞组不太容易从慢性ICS治疗中获益,除了LABAs之外,还可以预防病情加重,因此气道细菌负荷和感染性增加,从而增加感染事件的风险[7.].与这些概念一致,我们的发现还具有低血液粒细胞水平的患者在恶化时具有较高的PPB检测率。
虽然样本量小,但足以检验本研究的基本假设。我们承认该研究存在明显的局限性,即未能捕获临床结果并调查所进行的亚分析的分层;特别是增加的细菌载量是否会导致感染事件的增加。尽管缺乏动力,这项评估得出了一个重要的结果,这与最近的一项荟萃分析的结果相一致,该荟萃分析报告了在经ics治疗的低血嗜酸性粒细胞计数的COPD患者中肺炎风险增加[28.].我们知道学习的人口(前一年的〜1加剧)(表格1)没有资格接受常规ICS/LABA治疗[1].出于道德原因,这是唯一可以进行这种概念验证研究的人口。值得注意的是,我们的研究人口与先前在一些随机对照试验中进行的人口相似,评估SALM / FP固定组合和单组分的影响[6.那29.]平均符合欧洲COPD中的Salm / FP批准的批准适应症(每日50 /500μg一次吸入)。
以前的研究表明,健康,吸烟和COPD患者之间的肺部微生物组成的组成(主要是由植物的植物和压力的特征)[30.-32.].此外,已经记录了肺部微生物组的变化与COPD发热事件有关,并且可能涉及介导宿主炎症反应,并且植物间体外植物学主要表达于细菌性病学和迫使SPP的加剧。在嗜酸性加剧中[33.].为了我们的最佳知识,我们的研究是第一个纵向评估在痰微生物组合物上在COPD中添加吸入皮质类固醇的效果。我们认识到,我们的微生物分析有限,因为它不会涵盖整个气道生态学。然而,由于它包括属于气道微生物学的主要文学的最代表性病原体[30.-33.],它可以被认为是气道微生物组合物的代表。我们证实,COPD中的痰微生物组的组成相对稳定[33.].SALM / FP(但单独的SALM)治疗导致微生物组多样性的特异性扰动,随着机构的相对表达和减少的植物细菌的相对表达。此外,符合来自痰细胞培养物的数据,我们发现将IC添加到Laba导致潜在病原体微生物的丰富量增加(肺炎球菌那嗜血杆子和Moraxhella)仅对基线嗜酸性粒细胞水平<2%的COPD患者有效。在COPD中,这些不同微生物群落与上皮细胞相互作用和/或影响免疫系统的机制几乎是未知的。
总之,我们的随机对照试验结果表明,在稳定疾病期间,ICS增加了总细菌负荷,以及潜在致病性细菌负荷,但不增加病毒负荷,并改变了微生物组组成。是否增加的细菌负荷[8.[气道微生物组合物的变化[34.]在治疗ICS / Laba治疗的COPD患者中,必须通过适当设计的研究评估传染性临床后果的结果。细菌负荷的增加似乎仅限于血液和/或痰液粒细胞水平的患者。需要较大的随机对照试验来评估这种生物标志物驱动的药理学方法是否会导致COPD中临床结果的显着改善。
补充材料
披露
补充材料
N. Barnes.ERJ-00451-2017_Barnes.
G. Caramori.ERJ-00451-2017_CARAMORI.
m . ContoliERJ-00451-2017_CONTOLI.
G. Curradi.erj - 00451 - 2017 - _curradi
G. Forini.ERJ-00451-2017_forini
g . GnesiniERJ-00451-2017_GNESINI
b . MarkuERJ-00451-2017_Marku.
A. Papierj - 00451 - 2017 - _papi
A. Paulettierj - 00451 - 2017 - _pauletti
组织者一个RizziERJ-00451-2017_RIZZI.
确认
我们感谢Elisa Veratelli(Ferrara大学,意大利Ferrara,意大利)寻求稿件准备。我们感谢Giulia Zardi(Cros Nt,Verona,Italy)为统计分析的支持和修订。
脚注
2017年10月5日在线发表;2017年10月12日重新发布,修订作者的隶属关系细节。
本文提供了补充材料www.qdcxjkg.com
这项研究是注册Clinicaltrials.gov.数字NCT01213693。
支持声明:该研究得到了葛兰素史克公司不受限制的研究经费的支持。本文的资金信息已存入Crossref资助者注册表。
利益冲突:可以在本文中找到披露www.qdcxjkg.com
- 已收到2017年3月3日。
- 公认2017年7月10日。
- 版权所有©2017