文摘
基本原理严重的病毒性呼吸道感染通常的特点是广泛的骨髓细胞浸润和激活和持久的肺组织损伤。然而,免疫机制推动过度炎症肺仍然知之甚少。
目标识别机制,推动在肺部免疫细胞招聘病毒性呼吸道感染和确定新的药物靶点减少炎症和疾病严重程度。
方法临床前甲型流感病毒的小鼠模型和严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)感染。
结果氧化胆固醇和oxysterol-sensing受体GPR183被当成司机单核细胞/巨噬细胞浸润,肺在甲型流感病毒(IAV)和SARS-CoV-2感染。IAV和调节酶胆固醇25-hydroxylase SARS-CoV-2感染(CH25H)和细胞色素P450的家庭7亚科成员B1 (CYP7B1)在肺部,导致当地生产的氧化胆固醇25-hydroxycholesterol (25-OHC)和7α,25-dihydroxycholesterol(7α,25-OHC)。功能丧失的突变Gpr183或治疗Gpr183拮抗剂减少巨噬细胞浸润,肺的炎症细胞因子的生产IAV——或者SARS-CoV-2-infected老鼠。GPR183拮抗剂明显减毒的严重性SARS-CoV-2感染和病毒载量。数据分析单细胞RNA-sequencing支气管肺泡灌洗健康控制和COVID-19样本显示,中度和重度患者疾病CH25H,CYP7B1和GPR183在巨噬细胞在COVID-19显著调节。
结论这项研究表明oxysterols驱动肺部炎症通过GPR183并提供第一个临床治疗中获益的证据定位GPR183在严重的病毒性呼吸道感染。
文摘
病毒感染引发肺癌、oxysterol生产吸引巨噬细胞通过GPR183。激怒GPR183减少炎症和疾病严重程度SARS-CoV-2感染,使GPR183公认的治疗干预的目标。https://bit.ly/3DXlJCY
介绍
严重的病毒性呼吸道感染包括流感和COVID-19与广泛的骨髓细胞招聘到肺,从而导致严重的组织损伤和急性呼吸窘迫综合征的发展(1]。肺巨噬细胞组成和功能的转变与COVID-19严重程度相关。> 600住院病人的一项研究发现,在严重的情况下居民肺泡巨噬细胞被耗尽,取而代之的是大量的炎性monocyte-derived巨噬细胞(2]。快速的单核细胞/巨噬细胞浸润肺在严重急性呼吸系统综合症冠状病毒的急性期2 (SARS-CoV-2)感染是复制动物模型(3,4]。
氧化胆固醇最近成为肺部炎症的标志。Oxysterols增加在支气管肺泡灌洗液(BALF)过敏原后红肿的航空公司的挑战和与浸润白细胞(5]。他们也增加了在慢性阻塞性肺疾病患者的痰,关联与疾病严重程度6,7后,小鼠的肺中lipopolysaccharide-induced肺部炎症(8]。然而,oxysterols的角色在病毒性呼吸道感染肺还没有调查。
Oxysterols有一系列受体共享一个共同的炎症作用[9]。一个oxysterol途径导致的生产7α,25-hydroxycholesterol(7α,25-OHC),通过胆固醇25-hydroxylase (CH25H)和细胞色素P450的家庭7亚B成员1 (CYP7B1) [9,10]。7α,25-OHC可以随后被hydroxy-Δ-5-steroid脱氢酶代谢,3β-和steroid-Δ异构酶7 (HSD3B7) (图1一个)。7α,25-OHC内生高亲和力的受体激动剂oxysterol-sensing G protein-coupled受体GPR183 [11,12]。GPR183表达细胞的先天和适应性免疫系统,包括巨噬细胞、树突细胞,先天淋巴细胞、嗜酸性粒细胞和T和B淋巴细胞(5,13,14]。oxysterol配体,GPR183促进免疫细胞的趋化现象的分布二级淋巴器官(9,11,13,15]。在体外GPR183协调人类和小鼠巨噬细胞的迁移对7α,25-OHC梯度(16,17]。
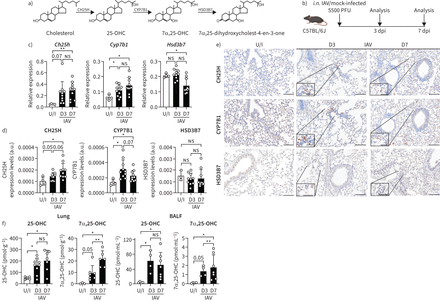
甲型流感病毒(IAV)感染导致胆固醇upregulation 25-hydroxylase (CH25H)和细胞色素P450的家庭7亚科成员B1 (CYP7B1)表达的肺癌和生产oxysterols 25-hydroxycholesterol (25-OHC)和7α,25-dihydroxycholesterol(7α,25-OHC)。一)25-OHC的生物合成途径和7α,25-OHC。b)实验设计:C57BL / 6 j小鼠感染鼻内(i.n。),5500年点状IAV的单位(PFU)。c) mRNA的表达Ch25h,Cyp7b1和Hsd3b7测量定量逆转录PCR在感染后的3天(dpi) (D3)和7 dpi (D7)正常化产生Hprt。CH25H d)定量分析,CYP7B1通过免疫组织化学方法和HSD3B7蛋白质标签(包含IHC)。e)代表包含IHC CH25H的图像,CYP7B1 HSD3B7肺部分未感染或IAV-infected老鼠。酒吧规模:100µm(主要)和50µm(插图)。f)的浓度25-OHC和7α,25-OHC肺部(左)和支气管肺泡灌洗液(BALF)在3 dpi和7 dpi(右)。数据意味着±sd(n = 4未感染的每个时间点,n = 6 - 10受感染的老鼠。ns:不重要的;U / I:模拟感染。*:p < 0.05;* *:p < 0.01。
在这项研究中,我们提出,病毒性呼吸道感染导致肺oxysterols的生产,导致过度的免疫细胞浸润和炎症。我们表明,oxysterols开车GPR183-dependent单核细胞/巨噬细胞浸润的临床前模型流感病毒和SARS-CoV-2感染和识别GPR183作为治疗干预的目标主机减轻病毒性呼吸道感染疾病严重程度。
方法
伦理和生物安全
所有实验动物伦理委员会批准(MRI-UQ / 596/18, AE000186)和机构昆士兰大学的生物安全委员会(IBC / 465 b / MRI /三/ AIBN / 2021)。
病毒株
奥克兰A / H1N1病毒股票/ / 1/2009 (H1N1),称为甲型流感病毒(IAV),在鸡胚蛋就做好了准备。一个mouse-adapted SARS-CoV-2应变是通过串行通道SARS-CoV-2 (B.1.351;加入hCoV-19 /澳大利亚/ QLD1520/2020 GISAID EPI_ISL_968081,收集2020年12月29日,请提供由昆士兰州卫生法医和科学服务)。的描述mouse-adaption SARS-CoV-2应变和基因组测序数据中可以发现补充方法和图S1。IAV病毒滴定度测定斑块化验Madin-Darby犬肾脏和SARS-CoV-2斑块化验州立E6细胞中描述补充材料。
小鼠模型
Gpr183tm1Lex从词汇获得药品,back-crossed C57BL / 6 j背景和培育内部。8-10-week-old C57BL / 6 jGpr183tm1Lex(Gpr183−−/)老鼠犀牛和4%异氟烷和鼻内感染了5500个点状单位(PFU) IAV奥克兰/ / 01/09 (H1N1)。SARS-CoV-2感染C57BL / 6 j和Gpr183−−/老鼠犀牛与氯胺酮和甲苯噻嗪(80 mg·公斤−1/ 5毫克公斤−1与8×10)和鼻内感染4空斑形成单位的mouse-adapted SARS-CoV-2。肺收集在指定的时间点为后续下游分析中描述补充材料。GPR183拮抗剂NIBR189 (7.6 mg·公斤−1)汽车(0.5%羧甲基纤维素/ 0.5%渐变- 80)或车辆只被口头管理填喂法在感染后的1天(dpi),每天两次每隔12 h,直到实验结束。
隔离和RNA逆转录酶定量PCR
总RNA分离使用隔离II RNA迷你包(Bioline试剂有限公司),(如前所述)(18,19]。提供了引物列表补充表S1。每个基因的相对表达正常参考基因hypoxanthine-guanine phosphoribosyltransferase (产生Hprt2)确定使用−ΔCt方法。
细胞因子量化使用ELISA
细胞因子在肺匀浆测定DuoSet ELISA(干扰素(IFN)β(DY8234-05) IFNγ(DY485) IFNλ(DY1789B)、白介素(IL) 6 (DY406)、肿瘤坏死因子α(TNFα)(DY410) IL-1β(DY401), IL - 10 (DY417)和CC趋化因子配体2主题(CCL2) (DY479);研发系统)根据制造商的协议。
流式细胞术
流式细胞术进行单细胞悬浮体从消化肺部和血液的详细描述补充材料。
免疫组织化学
免疫组织化学(包含IHC)上执行deparaffinised /患者肺部分通过与抗体immunolabelling SARS-CoV-2核衣壳蛋白(40143 - r040;嘉汉生物),离子钙结合适配器分子1 (IBA1) (019 - 19741;NovaChem)、CH25H (bs - 6480 r;bios抗体),CYP7B1 (bs - 5052 r;bios抗体)和同形像控制(兔免疫球蛋白;31235;热费希尔科学)稀释达芬奇绿色稀释剂(PD900;Biocare医疗),其次是孵化与辣根peroxidase-conjugated山羊anti-rabbit Ig抗体(1:200)(ab6721;Abcam) (补充材料)。同形像统计图所示的控制补充图S2。
统计分析
数据分析GraphPad棱镜软件。数据评估使用Shapiro-Wilk测试正常。斯皮尔曼等级相关的被用来分析相关性。两组比较,参数双尾学习任务通常被用于分布式数据而非参数Mann-Whitney U测试是用于数据偏离了常态。
结果
IAV感染增加CH25H CYP7B1表达式和肺oxysterol生产
调查是否IAV感染诱发的生产氧化胆固醇,老鼠感染IAV (图1 b)和mRNA的表达oxysterol-producing酶测定肺组织。Ch25h和Cyp7b1信使rna增加肺的IAV-infected老鼠和未受感染的动物相比,而Hsd3b7肺癌中表达下调7 dpi (图1 c)。同样,CH25H和CYP7B1蛋白质也增加HSD3B7保持不变时,通过免疫组织化学标记的肺部分与抗体检测CH25H CYP7B1和HSD3B7 (图1 de)。oxysterol-producing酶的诱导与浓度的增加有关oxysterols 7α,25-OHC和25-OHC肺匀浆图1 f左面板)和BALF (图1 f右面板)IAV-infected动物3 dpi和7 dpi。在未受感染的肺部,7α,25-OHC察觉在大多数样品测试。Ch25h和Cyp7b1信使rna中增加支气管肺泡灌洗(BAL)细胞颗粒IAV-infected小鼠相比,未受感染的动物Hsd3b7保持不变(补充图S3a)。
符合oxysterols的增加,Gpr183信使rna增加3 dpi和7 dpi BAL细胞(补充图S3a)和肺组织(补充图S3b),建议增加表达和/或招聘GPR183-expressing免疫细胞的肺感染。Gpr183表达呈正相关,Ch25h和Cyp7b1(补充图S3c)。
Gpr183−−/小鼠巨噬细胞浸润减少IAV后进入肺部感染
调查是否oxysterol-mediated免疫细胞招聘依赖于oxysterol-sensing GPR183,我们进行了实验小鼠基因缺乏Gpr183(Gpr183−−/)。Gpr183−−/总值老鼠表现出正常的表型(20.),正常循环单核细胞巨噬细胞集落形成单位的和类似的号码C57BL / 6小鼠的骨髓(补充图S4),这表明可比monopoiesisGpr183−−/老鼠。然而,在感染IAVGpr183−−/老鼠IBA1较低+在肺巨噬细胞数量3 dpi和7 dpi比感染C57BL / 6 j控件(图2一个)。Gpr183信使rna表达呈正相关,促炎细胞因子的表达白介素、肿瘤坏死因子和Ccl2在C57BL / 6 j小鼠(补充图S5),减少巨噬细胞浸润Gpr183−−/老鼠与减少有关白细胞介素6和肿瘤坏死因子,但不是Ccl27点,dpi (补充图S6)。身体重量和病毒滴定度通过IAV感染过程中整个基因型(补充图S7)。这些结果说明缺乏GPR183减少巨噬细胞渗透到肺IAV感染,这是与减少促炎细胞因子的表达有关。
删除的Gpr183基因或政府GPR183拮抗剂减少巨噬细胞浸润的甲型流感病毒(IAV)来华的肺。C57BL / 6 jGpr183−−/老鼠感染鼻内5500点状IAV的单位(PFU)。)代表免疫组织化学(包含IHC)离子钙结合的图像适配器分子1 (IBA1)在肺段IAV-infected C57BL / 6 jGpr183−−/老鼠(左)(右)和定量分析。b)实验设计:C57BL / 6 j小鼠Gpr183−−/老鼠感染鼻内(i.n。)与IAV 5500微升。老鼠和7.6毫克·公斤随后口服治疗−1NIBR189或车辆控制每天两次在感染后的1天(dpi),直到结束的实验。c)代表图像包含IHC IBA1 C57BL / 6 j和肺部分Gpr183−−/与各治疗组小鼠3 dpi (D3)和7 dpi (D7)(左)和IBA1染色(右)的定量分析。数据意味着±sdn = 6 - 12感染的老鼠每个基因型和时间点。酒吧规模:100μm。a.u。:arbitrary units; U/I: mock infected;ns:不重要的。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001;* * * *:p < 0.0001。
GPR183对抗减少巨噬细胞浸润
调查是否GPR183是公认的治疗目标,减少炎症,GPR183拮抗剂NIBR189 [11,17)是用于C57BL / 6 j小鼠每天两次从24小时后感染直到实验结束(图2 b)。就像Gpr183−−/小鼠C57BL / 6 j动物对待NIBR189显著降低巨噬细胞渗透到肺3 dpi和7 dpi由包含IHC (图2 c)。
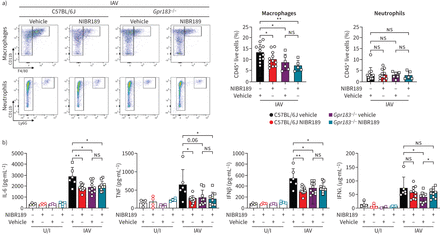
此外,流式细胞术分析进行肺从C57BL / 6 j和单细胞悬浮体Gpr183−−/老鼠接受NIBR189和车辆,分别使用以前公布的控制策略(补充图S8)[21]。NIBR189-treated C57BL / 6 j小鼠Gpr183−−/小鼠低百分比的招募/巨噬细胞渗透(F480高/ CD11b+/ Ly6G−/ SigF−)(图3一)相比,vehicle-treated C57BL / 6 j IAV后动物感染。NIBR189治疗并没有改变其他免疫细胞的百分比在肺子集,包括中性粒细胞(B220−/ CD3−/ Ly6G+/ CD11b+)(图3一),CD4+CD8 t细胞,+t细胞、b细胞、树突细胞和肺泡巨噬细胞(S9 / S10补充数据)。身体重量和肺病毒载量不受基因型或治疗(补充图S11)。
GPR183拮抗剂NIBR189减少巨噬细胞浸润和炎性细胞因子的生产。C57BL / 6 jGpr183−−/老鼠感染鼻内5500点状单位(PFU)甲型流感病毒(IAV)。老鼠和7.6毫克·公斤随后口服治疗−1NIBR189或车辆控制每天两次在感染后的1天(dpi),直到结束的实验。巨噬细胞浸润(F480频率高/ CD11b+/ Ly6G−/ SigF−)和中性粒细胞(B220−CD3−Ly6G+)是由相对于总可行CD45流式细胞术+免疫细胞在3 dpi(左)。图表显示巨噬细胞和中性粒细胞(右)的频率。b)细胞因子的测量白介素6 (il - 6)、肿瘤坏死因子(TNF)、干扰素β(IFNβ)和干扰素λ(IFNλ)7 dpi用ELISA。数据意味着±sd每个基因型n = 5 -感染小鼠和时间点。U / I:模拟感染;ns:不重要的。*:p < 0.05;* *:p < 0.01。
这些结果说明NIBR189显著降低巨噬细胞浸润,肺而不影响其他免疫细胞的招募子集。
GPR183对抗减少IAV-induced促炎细胞因子浓度
我们下一个决心,如果能减少由NIBR189导致巨噬细胞浸润减少肺部炎性细胞因子的生产。3 dpi、细胞因子无显著差异生产观察治疗组(补充图S12)。然而,IAV-infected C57BL / 6 j小鼠接受NIBR189 il - 6浓度显著降低,TNF和IFNβ(图3 b在7 dpi)。这是与IAV-infected的表型Gpr183−−/老鼠,NIBR189治疗在老鼠缺乏GPR183没有额外的效果。此外,没有观察到显著差异在两个时间点(IFNλ图3 b和补充图S12),证明GPR183拮抗剂治疗不会产生负面影响的生产类型III干扰素,它是重要的病毒控制在肺22]。没有观察到治疗组之间的差异在时间点对蛋白质的浓度IL-1β,CCL2或IFNγ治疗组(补充图S12和向)。因此,可以抑制药物GPR183减少促炎细胞因子在IAV严重感染。
GPR183对抗减少SARS-CoV-2感染严重程度
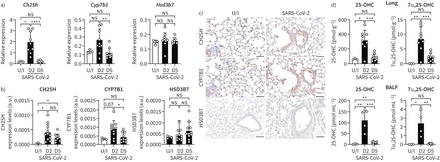
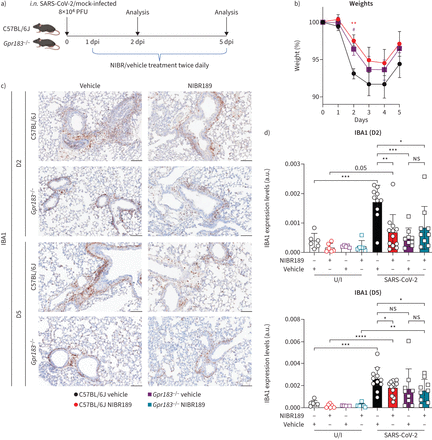
过度的巨噬细胞浸润和激活是一个严重的标志COVID-19 [2,23]。评估是否抑制GPR183扩展SARS-CoV-2感染的好处,我们建立了一个mouse-adapted SARS-CoV-2应变通过使β的变体SARS-CoV-2 (B.1.351)在C57BL / 6 j小鼠四倍。这导致了一种包含突变的病毒引起的非结构性蛋白5 (NSP5)和临床体征(减肥)感染小鼠(补充图S1)。与IAV感染结果一致,mRNA的表达Ch25h和Cyp7b1显著调节SARS-CoV-2-infected肺的老鼠相比,未受感染的老鼠Hsd3b7保持不变(图4一)。这也证实了在蛋白质水平包含IHC (图4 bc)。此外,25-OHC和7α,25-OHC肺匀浆浓度(图4 d、前面板)和BALF (图4 d,底部面板)显著增加2 dpi,回到未感染水平5 dpi届时动物开始从感染中恢复过来。Ch25h和Gpr183也增加了BAL SARS-CoV-2-infected老鼠的细胞Hsd3b7保持不变(补充图S14系列)。NIBR189或车辆是C57BL / 6 j或管理Gpr183−−/老鼠每天两次从24 h post-SARS-CoV-2感染直到实验结束(图5一个)。NIBR189-treated C57BL / 6 j小鼠体重显著减少和恢复速度比vehicle-treated老鼠(图5 b和补充图S15)。同样的,Gpr183−−/老鼠那么严重SARS-CoV-2感染。总的来说,这些数据表明oxysterols SARS-CoV-2后肺部感染和产生GPR183对抗显著降低SARS-CoV-2感染严重程度。
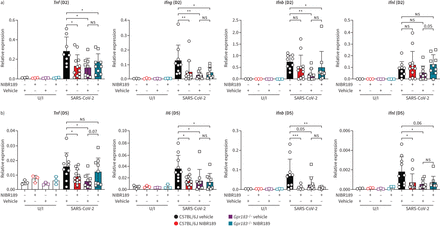
严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)感染导致胆固醇upregulation 25-hydroxylase (CH25H)和细胞色素P450的家庭7亚科成员B1 (CYP7B1)表达的肺癌和生产oxysterols 25-hydroxycholesterol (25-OHC)和7α,25-dihydroxycholesterol(7α,25-OHC)。C57BL / 6 j小鼠感染鼻内约8×104点状单位(PFU) mouse49-adapted SARS-CoV-2。信使rna表达的)Ch25h,Cyp7b1和Hsd3b7测量定量逆转录PCR在感染后的2天(dpi) (D2)和5 dpi (D5)正常化产生Hprt。CH25H b)定量分析,CYP7B1和HSD3B7蛋白免疫组织化学(包含IHC)标签在D2和D5和c)包含IHC CH25H的形象代表,CYP7B1和HSD3B7肺部分在未受感染的老鼠D2。d)的浓度25-OHC和7α,25-OHC肺(上)和支气管肺泡灌洗液(BALF)在D2和D5(底部)。数据意味着±sd(n = 3未受感染的老鼠和n = 9感染老鼠每个时间点。酒吧规模:50μm。U / I:模拟感染;a.u。:arbitrary units;ns:不重要的。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001;* * * *:p < 0.0001。
GPR183对立导致那么严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)侵染诱导的减肥和减少巨噬细胞浸润。C57BL / 6 jGpr183−−/老鼠感染鼻内约8×104点状单位(PFU) mouse-adapted sars - 63 CoV-2。老鼠和7.6毫克·公斤随后口服治疗−1NIBR189或车辆控制每天两次在感染后的1天(dpi),直到结束的实验。实验设计。b)权重的老鼠显示为接种时重量的百分比。c)代表免疫组织化学(包含IHC)离子钙结合的图像适配器分子1 (IBA1)在C57BL / 6 j和肺Gpr183−−/与各治疗组小鼠2 dpi (D2)和5 dpi (D5)。酒吧规模:100μm。d) IBA1 D2和D5的定量分析。数据意味着±sdn = 9 - 12感染的老鼠每个基因型和时间点。a.u。:arbitrary units; U/I: uninfected;ns:不重要的。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001。
GPR183对抗减少巨噬细胞浸润,肺的炎症细胞因子表达SARS-CoV-2被感染的老鼠
接下来,我们调查是否GPR183对抗减少肺巨噬细胞浸润、炎性细胞因子。SARS-CoV-2-infected C57BL / 6 j小鼠接受NIBR189显著降低巨噬细胞渗透到肺2 dpi和5 dpi (图5 cd)。NIBR189治疗与减少有关肿瘤坏死因子,Il10和Ifng在2 dpi (mRNA表达图6和补充图S16),减少肿瘤坏死因子,Il1b和白细胞介素6表达式在5 dpi (图6 b和补充图S16)。早期的干扰素反应不受NIBR189,具有可比性Ifnb和Ifnl表达在C57BL / 6 j小鼠2 dpi,但干扰素反应(dpi) 5日晚些时候在NIBR-treated动物相比显著降低控制(图6)。没有观察到治疗组之间的差异对mrna编码Ccl2,Il1b或白细胞介素62 dpi和Ccl2,Il10和Ifng在5 dpi (补充图S16)。这些结果说明减少NIBR189-treated小鼠巨噬细胞浸润与减少促炎细胞因子表达的肺癌,而早期抗病毒干扰素反应保持不变。
GPR183对立导致减少炎性细胞因子。C57BL / 6 jGpr183−−/老鼠感染鼻内约8×104点状单位(PFU) mouse-adapted严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)。老鼠和7.6毫克·公斤随后口服治疗−1NIBR189或车辆控制每天两次在感染后的1天(dpi),直到结束的实验。相关的表达肿瘤坏死因子,Ifng,Ifnb和Ifnl)2 dpi (D2)和b) 5 dpi (D5)在肺部以逆转录定量PCR,正常化产生Hprt。数据意味着±sd(n = 3未受感染的老鼠和n = 9 - 12感染小鼠基因型和时间点。U / I:模拟感染;ns:不重要的。*:p < 0.05;* *:p < 0.01;* * *;p < 0.001。
GPR183对抗减少SARS-CoV-2负载
最后,我们调查是否NIBR189治疗与改变病毒载量。SARS-CoV-2核衣壳蛋白表达减少在NIBR189-treated C57BL / 6 j小鼠相比管理车辆2 dpi (图7b),核衣壳蛋白表达没有检测到5 dpi,当动物从感染中恢复过来。然而,在mRNA水平,病毒MproRNA加载NIBR189-treated小鼠显著降低肺的dpi(5点图7 c)。确凿的,病毒空斑形成单位明显降低2 dpi和5 dpi NIBR-treated动物(补充图肌力)。总之,我们在这里展示,GPR183对抗降低病毒载量,巨噬细胞浸润和生产的促炎细胞因子SARS-CoV-2感染。
老鼠用GPR183拮抗剂治疗较低严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)负载。C57BL / 6 jGpr183−−/老鼠感染鼻内约8×104点状单位(PFU) mouse-adapted SARS-CoV-2。老鼠和7.6毫克·公斤随后口服治疗−1NIBR189或车辆控制每天两次在感染后的1天(dpi),直到结束的实验。)代表免疫组织化学(包含IHC)图像的病毒核衣壳蛋白(N)表达在2 dpi (D2)和5 dpi (D5)。b)病毒N蛋白表达的定量分析治疗组在D2。c)病毒载量在肺的检测评估MproRNA逆转录定量PCR在D5正常化产生Hprt。数据意味着±sdn = 9 - 12感染的老鼠每个基因型和时间点。酒吧规模:50μm。a.u。:arbitrary units; U/I: mock infected;ns:不重要的。*:p < 0.05;* *:p < 0.01。
肺巨噬细胞从COVID-19移植的病人CH25H、CYP7B1 HSD3B7和GPR183
确定oxysterol-producing酶是否增加在人类SARS-CoV-2感染,我们分析了单细胞RNA-sequencing (scRNA-seq)数据从健康控制和COVID-19中度和重度患者疾病(23]。我们发现CH25H,CYP7B1和HSD3B7明显调节COVID-19和几乎完全表达在巨噬细胞(图8)。而GPR183表达显著增加COVID-19期间在巨噬细胞和髓系树突状细胞,其在其他免疫细胞类型的表达式保持不变。
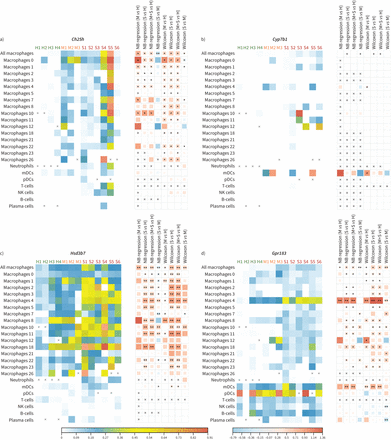
单细胞RNA-sequencing表达分析的细胞收集的支气管肺泡灌洗和健康对照组COVID-19病人。总结的热图在左边的面板显示平均正常基因的表达水平)Ch25h,b)Cyp7b1c)Hsd3b7和d)Gpr183每单个细胞类型集群。总结的热图的面板显示平均日志褶皱变化(logFC)在每个基因的表达在24细胞类型之间的集群温和COVID-19例和健康对照组(MvsH)、严重COVID-19例和健康对照组(SvsH), COVID-19例和健康对照组(M + SvsH),严重的和温和的COVID-19病例(Svs米)。
logFC值估计使用负二项广义线性模型应用到原始UMI计数,调整总UMI计数每个细胞,每个细胞的基因检测数量,每分每细胞线粒体数量(NB回归);或非参数Wilcoxon等级和测试应用于正常计数。重要的协会有一个星号标出如果他们超过Bonferroni意义(p < 1.30×10−4)或两个星号如果他们进一步表达了至少5%的两组细胞的绝对值logFC > 0.25。logFC > 0表明基因的表达水平更高的焦点小组(如。温和COVID-19例)相比其他组(如。健康对照组),反之亦然。争取民主变革运动:骨髓树突状细胞;pDC:血浆树突细胞;NK:自然杀手。
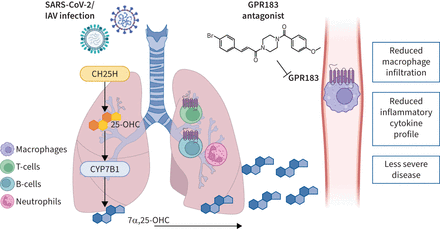
抽象图形的作用GPR183免疫反应的严重急性呼吸系统综合症冠状病毒2 (SARS-CoV-2)和甲型流感病毒(IAV)感染。SARS-CoV-2和IAV感染导致胆固醇的upregulation 25-hydroxylase (CH25H)和细胞色素P450的家庭7亚科成员B1 (CYP7B1),导致生产7α,25-dihydroxycholesterol(7α,25-OHC)。这oxysterol chemotactically吸引GPR183-expressing肺巨噬细胞产生促炎细胞因子。药物抑制GPR183减弱GPR183-expressing巨噬细胞的浸润,导致降低炎性细胞因子的生产没有负面影响抗病毒反应。
讨论
我们报告25-OHC和7α,25-OHC产生肺部IAV或者SARS-CoV-2感染、吸引单核细胞/巨噬细胞在GPR183-dependent方式。减少巨噬细胞浸润和炎性细胞因子的生产Gpr183−−/老鼠和NIBR189-treated C57BL / 6 j小鼠显著提高SARS-CoV-2感染严重程度。拮抗剂减毒SARS-CoV-2但不是IAV负载。是否这是由于pathogen-specific影响或导致更严重的疾病在IAV模型相比SARS-CoV-2模型还有待调查。然而,巨噬细胞浸润和炎性细胞因子的生产减少病毒模型。
在动物模型中IAV SARS-CoV-2,髓细胞迅速渗透到肺部(3,4,24]。患者严重COVID-19 GPR183的比例更高+激活巨噬细胞和巨噬细胞在BALF23),强烈暗示巨噬细胞作为关键贡献者COVID-19-associated hyperinflammation。严重COVID-19患者BALF中丰富趋化因子CCL2, CCL7招募单核细胞的肺通过趋化因子受体主题趋化因子受体2 (CCR2) [25]。从历史上看,趋化因子被认为是免疫细胞迁移到肺的主要动力;然而,我们的工作表明,oxysterols nonredundant单核细胞/巨噬细胞浸润。我们进一步证明COVID-19患者肺巨噬细胞表达高水平的oxysterol-producing酶和GPR183,表明该机制在人类是守恒的。类似于我们的观察Gpr183−−/老鼠,老鼠缺乏CCR2已经推迟了在肺巨噬细胞浸润21];然而,CCR2也是需要t细胞迁移。因此,动物缺乏CCR2推迟了t细胞浸润和更高的病毒滴定度(26]。尽管GPR183 t细胞表达,它不是必不可少的t细胞迁移到肺(27)和激怒GPR183没有负面影响t细胞室和其他免疫细胞的子集。
我们最近在小鼠模型的显示结核分枝杆菌(Mtb)感染GPR183和7α,25-OHC-producing酶CYP7B1需要快速巨噬细胞渗透到肺在分枝杆菌感染(18]。在结核分枝杆菌的模型中,嗜酸性粒细胞浸润[所需GPR183也14]。我们确定了肺泡巨噬细胞和巨噬细胞浸润主要细胞类型表达结核分枝杆菌CH25H和CYP7B1感染(18)和证实这个scRNA-seq COVID-19患者的数据。
删除Ch25h曾被证明是保护小鼠模型的流感(28]。25-OHC增加急性肺损伤模型;然而,房子是减少灰尘mite-induced哮喘模型(8]。气管内的管理25-OHC改善炎症标记物在急性肺损伤模型中,而它恶化哮喘模型的特点。在这两个模型,Gpr183表达不受影响。这表明25-OHC特定生产模型。
在这里,我们表明,减少巨噬细胞浸润Gpr183−−/老鼠和NIBR189-treated C57BL / 6 j小鼠与减少促炎细胞因子的生产,可能由于低数量的巨噬细胞存在于组织中。虽然我们没有观察NIBR189-mediated减少肿瘤坏死因子,白细胞介素6或Ifnb表达IAV-infected或lipopolysaccharide-stimulated骨骨髓来源的巨噬细胞(S18补充图美国),我们不能完全排除NIBR189的直接影响细胞因子的生产由其他免疫细胞。无论的确切机制,降低炎性细胞因子的生产NIBR189-treated动物可以解释,至少部分疾病预后越好。
虽然促炎细胞因子可能损害宿主(29日),早期的I型和III干扰素是至关重要的在控制病毒复制IAV [30.,31日)和SARS-CoV-2感染(32,33]。第三NIBR189没有改变早期的I型或干扰素反应SARS-CoV-2-infected动物,这表明抗病毒反应是不损害的治疗。
几个oxysterols可以直接抗病毒效果(9]。CH25H / 25-OHC抑制SARS-CoV-2感染已被证明在体外通过阻断宿主细胞膜融合(34,35]。是否NIBR189 oxysterols结构不同,影响病毒入口/复制还有待阐明。
其他免疫抑制疗法用于严重COVID-19,如糖皮质激素、增加血管紧张素转换酶2 (ACE2)表达,促进病毒入口/复制[36,37)和延迟SARS-CoV-2间隙(38]。NIBR189没有增加Ace2信使rna (补充图S19),但Ace2表达下调NIBR189-treated动物在较小程度上,这是符合低病毒载量。
总之,我们提供的第一个临床前证据GPR183作为治疗干预的小说主机目标减少macrophage-mediated hyperinflammation, SARS-CoV-2负载和COVID-19严重性。
补充材料
可共享的PDF
确认
我们感谢昆士兰健康法医和科学服务,昆士兰州卫生部门提供SARS-CoV-2隔离。我们感谢Sumaira哈斯奈英板牙研究所——昆士兰大学共享抗体用于这项研究。我们承认的技术援助团队,运营和维护服务(澳大利亚星系https://usegalaxy.org.au/)。我们感谢大卫休谟,马赫甘地和杰克Gratten板牙研究所——昆士兰大学的评论的手稿。
脚注
61年发表在体积3的欧洲呼吸杂志2023年3月9日;转载:2023年3月24日改变结果的最后一段中提到的参考部分。
作者的贡献:范本:李从先Foo, s . Bartlett M.J.甜,投资者短,M.M. Rosenkilde, k . Ronacher。方法:K.Y.咀嚼,h . Bielefeldt-Ohmann B.J. Arachchige, b·马修斯里德。调查:李从先Foo, s . Bartlett K.Y.咀嚼,医学博士非政府组织,h . Bielefeldt-Ohmann B.J. Arachchige, b·马修斯里德,c . Smith, r . Wang l .毛刺k . Bisht s Shatunova J.E.辛克莱,r·帕里y, j]。答:Khromykh几何。写作(初稿):李从先Foo, s . Bartlett Ronacher。写作(审查和编辑):所有作者。资金收购:s . Bartlett投资者短,M.M. Rosenkilde, k . Ronacher。
利益冲突:s . Bartlett报道早期职业生涯种子从母亲基金会的资助,支持本研究。从范式生物制药h . Bielefeldt-Ohmann报告咨询费,昆士兰科技大学,科罗拉多州立大学,在提交工作。M.J.甜报告从澳大利亚国家健康与医学研究委员会资助,在提交工作。k . Bisht报告从美国血液学会授予(灰)全球研究奖,和转化研究Institute-Mater研究林肯格兰特,板牙基金会,在提交工作。y杨的报告从板牙基金会赠款,支持本研究。j]。几何报告赠款从国家卫生和医学研究委员会和美国国防部的;从GlycoMimetics Inc .和版税或牌照,在提交工作。M.M. Rosenkilde报告支持动物研究和育种在丹麦在这项研究中使用的鼠标应变从丹麦独立研究基金;授予独立研究基金丹麦诺和诺德公司的基础; donations from deceased Valter Alex Torbjørn Eichmuller (VAT Eichmuller)-2020-117043, and Kirsten and Freddy Johansens Foundation (KFJ) - 2017-112697; royalties from Antag Therapeutics and Bainan Biotech from patents made at the University of Copenhagen; travel support from Gordon Research Conference 2022; and is the co-founder of the following biotech companies: Antag Therapeutics, Bainan Biotech, Synklino, outside the submitted work. K.R. Short reports grants from National Health and Medical Research Council of Australia; and consulting fees from Sanofi, Novo Nordisk and Roche, outside the submitted work. K. Ronacher reports support for the present manuscript from Mater Foundation, Diabetes Australia, Australian Infectious Diseases Research Centre, Australian Respiratory Council; and grants from NIH R01 (5R01AI116039), outside the submitted work. All other authors have nothing to disclose.
支持声明:本研究从母亲k . Ronacher基金会赠款支持,使澳大利亚澳大利亚呼吸委员会、糖尿病和传染病研究中心。s . Bartlett是由早期职业种子从母亲基金会的资助。转化研究所是由澳大利亚政府的资助。丹麦独立研究理事会我医学科学支持M.M. Rosenkilde。M.J.甜,投资者短期和j]。几何支持澳大利亚国家健康与医学研究委员会的研究员格兰特(1194406),研究员格兰特(2007919)和高级研究奖学金(1136130),分别。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2022年6月28日。
- 接受2022年10月20日。
- 版权©2023年作者。
这个版本分布在创作共用署名非商业性许可证的条款4.0。商业生殖权利和权限接触权限在}{ersnet.org