文摘
背景特发性肺纤维化(IPF)是一种进行性纤维化疾病的特点是异常的成纤维细胞/ myofibroblast积累和过多的胶原基质沉积在肺泡肺。作为第一个批准IPF药物,pirfenidone (PFD)显著减慢肺功能下降而其底层anti-fibrotic机制仍然是难以捉摸的。
方法我们进行转录组和免疫荧光分析的主要人类IPF组织。
结果我们表明,myocardin-related转录因子(MRTF)信号被激活在IPF肺myofibroblasts积累。此外,我们表明,PFD抑制MRTF人类肺成纤维细胞活化在初级临床可行的浓度(50 - 150µM half-maximal抑制浓度,最大抑制> 90%,最大浓度的PFD的病人< 100µM)。从力学上看,PFD似乎发挥其抑制效应间接地通过促进MRTF之间的交互和肌动蛋白。最后,PFD-treated IPF肺部表现出显著减少MRTF激活比天真的IPF肺纤维母细胞焦点地区。
结论我们的研究结果表明MRTF信号作为PFD的直接目标和暗示,一些anti-fibrotic PFD的影响可能是由于MRTF肺成纤维细胞的抑制作用。
文摘
抑制MRTF激活是临床可行的anti-fibrotic pirfenidone的机制https://bit.ly/3jElNQu
介绍
特发性肺纤维化(IPF)是一种进步和致命的间质性肺疾病诊断后3 - 5年的中位生存(1- - - - - -4]。尽管IPF的病理学基础是复杂和知之甚少,提出这种疾病很可能引发的重复microinjuries气道和肺泡上皮细胞(5]。这些实质的侮辱导致的激活和积累myofibroblasts肺间质地区。因此,这些myofibroblasts合成和沉积过多的细胞外基质蛋白在牙槽区域,从而导致肺功能进行性下降,最终,病人死亡(6,7]。因此,IPF代表一个巨大的未满足的医疗需要对全球公共卫生系统(5- - - - - -8]。
众多实验IPF的疗法在临床试验中已经失败了,到目前为止,只有两种药物被批准用于治疗IPF患者,pirfenidone (PFD)和nintedanib(元),根据他们的能力来减缓疾病进展以降低肺功能下降(9,10]。而被忽视的热带病提出了针对纤维母细胞和myofibroblast扩散和激活强有力的多个受体酪氨酸激酶抑制剂(11,12),PFD的anti-fibrotic机制仍然是难以捉摸的。在这方面,应该注意的是,最近的研究有关PFD的广泛生物活性如针对pro-fibrotic生长因子和转录因子,抑制胶原原纤维的形成,与氧化应激(13- - - - - -18]。然而,这些研究的局限性是使用过度集中的PFD和/或缺乏人类的证据。因此,这些观察的临床相关性尚未完全建立和PFD的分子目标(s)病人尚未定义(19,20.]。
血清反应因子(SRF)是一种重要的转录因子,调节细胞骨架和细胞活性基因的表达通过相互作用的两个主要辅活化因子:myocardin-related转录因子A和B (MRTFA / B) [21- - - - - -26]。如果细胞,MRTFA主要由绑定到隐藏在细胞质中单体的肌动蛋白(G-actin)通过其氨基端arginine-proline-glutamate-leucine共识sequence-containing (RPEL)域(23,27- - - - - -29日]。当细胞受到刺激时,Ras同系物(ρ)gtpase激活引发聚合的G-actin丝状肌动蛋白(f -肌动蛋白),从而释放MRTFs G-actin和允许他们主要易位到细胞核诱导细胞骨架基因表达通过与SRF互动(23,27- - - - - -29日]。MRTF信号的关键作用细胞活性和细胞骨架重组进一步支持人类遗传学数据MRTFA功能丧失的突变会导致免疫系统对病毒感染的易感性和异常的伤口愈合反应由于妥协运动性免疫细胞和成纤维细胞17]。老鼠的研究也表明,MRTF信号导致组织纤维化在多个临床前模型(30.- - - - - -36]。
在这里,我们假设,某些特异表达的分子途径(s)在人类IPF肺部可能PFD的anti-fibrotic行动的目标。通过转录组分析人类的样本,我们发现MRTF信号是人类IPF诱导肺及其hyperactivation似乎是特定于间充质细胞,包括成纤维细胞和myofibroblasts。此外,补充免疫荧光分析显示,MRTF激活似乎主要来自α-smooth肌肉肌动蛋白(ACTA2)表达myofibroblasts积累在IPF肺。接下来,我们表明,PFD抑制MRTFA核易位,中央细胞MRTF信号激活,并MRTF目标基因表达剂量依赖性的方式。PFD的效力与MRTF信号进一步实验确定half-maximal抑制浓度(IC50)50 - 150µM和最大抑制> 90%。从力学上看,我们发现PFD促进MRTF之间的交互和肌动蛋白间接而不影响ρ家庭成员(RhoA)激活和肌动蛋白聚合。符合这些发现,PFD-treated但不是NTD-treated IPF肺部表现出少MRTF激活成纤维细胞比天真的IPF肺疫源地没有PFD治疗。总之,这些数据表明MRTF信号直接可以抑制分子通路PFD在生理浓度有关,这可能是一个新的药物和临床可行的anti-fibrotic机制。
材料和方法
病人群
所有的人类样本收购被批准的加州大学旧金山分校(美国旧金山,CA)机构审查委员会。IPF患者的临床资料和人口统计信息和健康对照组中提供补充表S1。IPF患者队列处理或者没有PFD和被忽视的热带病据报道之前37]。在这个群,PFD治疗的平均持续时间为22.7个月(范围9-60月)和被忽视的热带病治疗的平均持续时间为13.4个月(范围7-20个月)(37]。
人类肺样本
移植肺组织病理诊断的患者获得间质性肺炎和IPF交办的共识临床诊断多学科讨论和审查的临床资料。书面知情同意了所有学科和研究是加州大学旧金山分校的机构审查委员会批准。人类肺部不是北部使用的加利福尼亚移植捐赠网络被用作控制;研究表明,在生理和病理上这些肺正常(38]。灌注后肺动脉和支气管肺泡灌洗,新鲜肺外植体组织存储在一夜之间完成媒体湿冰在随后的消化。IPF肺活检或没有处理pdf或被忽视的热带病是前面描述的37]。
主要的人类肺细胞隔离
汉克斯的组织被缓冲盐溶液(hbs),然后彻底碎消化缓冲区(哈佛商学院、2.5 mg·毫升−1胶原酶D和100µg·毫升−1DNase)。剁碎组织了45分钟在37°C。残余组织材料转移到新鲜消化缓冲和冲击另一个45分钟在37°C。两轮的单个细胞消化相结合,然后通过70 -和40-µm过滤器过滤。红细胞被使用红细胞裂解缓冲(Sigma-Aldrich,圣路易斯,密苏里州,美国)。细胞准备沾反CD45-BUV395(摘要;美国新泽西BD生物科学,富兰克林湖),反EPCAM-PE(摘要;美国圣地亚哥BioLegend CA),反CD31 PerCP-Cy5.5(摘要;BioLegend)和可以解决的可行性染料eFluor 780 (1:20 00;热费希尔科学、沃尔瑟姆,妈,美国),按fluorescence-activated EPCAM细胞分类+、CD31+、CD45+和三阴性人群使用BD FACSAria和FlowJo分析。
细胞培养
A539, U937、MLE12 THP1和HL60细胞从写明ATCC购买(美国弗吉尼亚州马纳萨斯)。主要人类肺部动脉内皮细胞从ScienCell购买(美国加利福尼亚州卡尔斯巴德)。这些主要细胞培养所指示的供应商。主要人类肺成纤维细胞-原油全部肺单细胞悬液中分离培养与2毫米DMEM补充谷酰胺,100 U mL−1青霉素、μg·100毫升−1链霉素和10%胎牛血清的边后卫。细胞U937细胞分化成macrophage-like ng 20毫升−1phorbol-12-myristate-13-acetate (PMA)(开曼化学,安阿伯市,美国)治疗前24小时无血清培养基(SFM)饥饿和刺激的边后卫。HL60细胞分化成neutrophil-like细胞1.5% (v / v)二甲亚砜治疗SFM饥饿和前6天的边后卫刺激。THP1细胞分化为树突状细胞样的细胞ng 20毫升−1interleukin-4(研发系统,明尼阿波利斯,美国)和20 ng·毫升−1PMA SFM饥饿和前4天的边后卫刺激。
RNA序列
从肺成纤维细胞RNA提取使用RNeasy工具包(试剂盒、希尔登,德国)和DNase对待我(美国生活技术,卡尔斯巴德,CA)。TruSeq困mRNA的库生成工具(Illumina公司、圣地亚哥、钙、美国),测序HiSeq系统2500年的高输出模式。
核糖核酸测序分析
测序读为肺所公布的数据和先前发表的肝脏数据(欧洲核苷酸存档加入ERP109255)过滤和一致使用HTSeqGenie v3.4.1 [39]。通过HTSeqGenie GSNAP v2011-12-28用于对齐,包装,在GENCODE基本基因模型的人类基因组组装GRCh38。只有读取具有独特的基因组比对分析。
每百万总正常化每千碱基读取基因模型读取(nRPKM)值被用作衡量基因表达的正常化,按照之前定义的计算(40]。日志2nRPKM转换计算nRPKM + 1−4和z分数日志2nRPKM热图中显示被限制到±3sd的日志2nRPKM值用于可视化;热图集群使用病房执行的方法。差异基因表达计算使用轰+ limma [41)与多种假说假定值使用Benjamini-Hochberg执行方法的修正。MRTF响应基因集的测试意义与背景相比使用相机参数方法进行日志褶皱变化分布(42]。
差异基因表达和基因本体论(去)分析,调节基因被定义为基因有nRPKM褶皱变化> 0,p值< 0.05调整。去分析使用的分子签名数据库(MSigDB)基因集43]。MRTF响应签名来自重叠之前报道MRTF直接目标基因(24在IPF)和细胞骨架或motility-related基因调节肺。日志2nRPKM褶皱变化分布包括所有MRTF响应基因与其他基因(背景),不包括基因没有至少10读入至少10%的样本。示例签名得分MRTF响应基因集被定义为第一主成分得分计算主成分分析的日志2nRPKM MRTF响应基因的集合(eigengene)。所有的RNA序列(RNA-seq)分析了R(进行44]。
免疫荧光染色
部分(4µm) formalin-fixed和石蜡包埋标本deparaffinated紧随其后抗原检索使用目标检索(Dako、斯特鲁普、丹麦)。随后被阻塞的部分和彩色PBS加上1%牛血清白蛋白(美国Gibco,卡尔斯巴德,CA), 5%多发地驴血清(美国杰克逊ImmunoResearch西树林,PA)和0.1% Triton x - 100。以下主要被用于免疫荧光抗体:anti-MRTFA (1:10 0;Sigma-Aldrich), anti-ACTA2-FITC(摘要;Sigma-Aldrich), anti-EPCAM (1:50 0;细胞信号技术,丹弗斯,妈,美国),anti-CD45 (1:400;细胞信号技术)和anti-CD31 (1:1000;细胞信号技术)。人类部分20×计划Apo DIC M成像目标(NA: 0.75)尼康Ti-Eclipse(尼康、东京、日本)倒置显微镜配备了一个和或Neo scMOS相机(英国牛津仪器,阿宾顿),linear-encoded自动化阶段(应用科学仪器,尤金,或者美国)和苍井空LED灯引擎(美国Lumencor、比佛顿或)软件由NIS所有元素(尼康)。
小干扰rna的转染
转染是表示的浓度20 nM小干扰rna(地平线发现,剑桥,英国)使用RNAiMax转染试剂(热费希尔科学)。转染细胞培养没有扰动至少48小时前SFM饥饿和20%的边后卫刺激。
逆转录酶定量聚合酶链反应
原代人正常和IPF肺成纤维细胞培养与SFM挨饿过夜,然后接受20%的边后卫和PFD或被忽视的热带病表示浓度的另一个24小时。随后,细胞RNA提取的收获。总RNA纯化使用RNeasy工具包(试剂盒)和DNase对待我(生命技术)。互补的DNA合成进行了与iScript RT Supermix (Bio-Rad、大力神、钙、美国)。执行定量PCR技术使用SYBR绿色试剂(Bio-Rad)一式三份。相对标准曲线计算方法用于定量和表达水平正常化,次黄嘌呤phosphoribosyltransferase。
免疫印迹
免疫印迹进行全细胞提取物或核提取物如前所述45]。等量的蛋白质溶解产物通过sds - page分离,转移到硝酸纤维素和使用以下主要抗体进行免疫印迹分析:MRTFA (1:200;美国圣克鲁斯生物技术、达拉斯、TX), YY1 (1:1000;Abcam), GAPDH (1:1000;细胞信号技术)和ACTB (1:200;圣克鲁斯生物技术)。
细胞功能检测
原代人肺成纤维细胞增殖试验,在96孔板培养对待PFD 48小时后跟CellTiter-Glo表示浓度的测定(WI Promega,麦迪逊,美国)。RhoA活化试验,主要人类肺成纤维细胞被饿死在SFM 24 h,然后用20%的边后卫+ PFD表示浓度的2 h和胞内RhoA活动测量使用RhoA G-LISA活化分析工具包(美国丹佛市细胞骨架)。原代人肺成纤维细胞f -肌动蛋白形成试验,饿死在SFM 24小时接受20%的边后卫+ PFD(1毫米)或Latrunculin B (LanB)(100海里)2 h后在4%多聚甲醛固定,permeabilisation 0.1%皂素和染色0.33µM罗丹明phalloidin解决方案在一个顺序排列的。细胞被彻底清洗和绑定phalloidin被30分钟孵化与纯甲醇提取。f -肌动蛋白含量是决定通过测量罗丹明phalloidin使用537纳米荧光激发和发射576海里。
下拉化验
下拉化验使用细胞提取物,Ni-NTA琼脂糖(热费希尔科学)饱和与6×肽或His-RPEL融合蛋白大肠杆菌清洗和用作亲和树脂溶解产物,随后孵化与人类肺成纤维细胞,胞质提取物主要由溶解在低渗的缓冲区(10毫米玫瑰(pH值7.9),氯化钾10毫米,1.5毫米MgCl20.1毫米二硫苏糖醇(德勤)和蛋白酶抑制剂)通过叶面喷洒和离心除去不溶性材料。相当于一个支流10厘米的人类肺成纤维细胞主要是用于一个绑定的反应。重组系统下拉化验,亲和树脂饱和与6×肽或His-RPEL蛋白与肌动蛋白纯化蛋白(细胞骨架)孵化代替原代人肺成纤维细胞胞质提取物。结合反应化验都绑定缓冲(2 h的50 mM Tris-HCl (pH值7.5),250毫米氯化钠,MgCl 1毫米20.1毫米,0.2毫米ATP,德勤和蛋白酶抑制剂)补充Triton x - 100的0.5%。树脂被洗了三次绑定缓冲没有蛋白酶抑制剂和4 - 20% sds - page。高分子量(> 25 kDa)的凝胶用于肌动蛋白免疫印迹(4970;细胞信号技术)和低分子量凝胶的(< 25 kDa)部分Coomassie蓝染色显示诱饵输入。
量化和统计分析
自定义脚本在R版本3.5.1利用RNA-seq数据分析和绘图。棱镜(美国GraphPad拉霍亚,CA)是利用绘图和统计分析。统计实验的细节可以在图中找到传说,包括所使用的统计检验和n的值和定义。
结果
MRTF签名是富含IPF肺
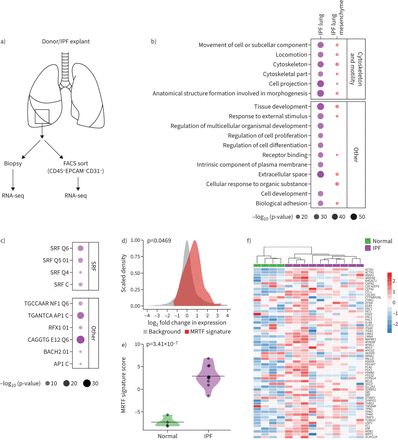
为了推进我们的理解人类肺纤维化的病理学,我们进行全基因组转录组分析新移植的人类肺IPF患者和nondiseased控制(46]。并行,转录资料也收集的间充质细胞直接从相同的肺部孤立通过三阴(CD45−EPCAM−CD31−)排序(图1一个和补充图S1)。去分析显示,生物过程,如细胞投影由cilium-associated基因和细胞运动是在IPF肺顶部的调节过程中,这与先前的报道是一致的(图1 b)[47- - - - - -52]。此外,细胞骨架及其相关细胞运动性通路也富含IPF肺的调节基因(图1 b)。然后我们试图确定浓缩细胞骨架和运动基因的失调引起的间充质细胞或基因的表达情况,另外,异常积累的间充质细胞数量如成纤维细胞/ myofibroblasts在肺纤维化。细胞分类后,我们发现细胞骨架和细胞活性仍在前调节生物过程在排序IPF间充质细胞(图1 b),这表明浓缩这些过程可能由于转录变化而非细胞结构的失衡。
myocardin-related转录因子(MRTF)签名是富含特发性肺纤维化(IPF)的肺。人类样本集合)原理的概述。b)顶级基因本体生物过程浓缩在纤维样品的基因调节。c)前10名独联体监管图案丰富的调节细胞骨架和细胞活性基因的启动子区域IPF肺。d)密度的日志2折叠IPF的变化分布与正常的肺。单独的分布显示MRTF响应基因(MRTF签名)和所有其他基因表达水平通过质量控制(背景)。显示的密度符合截断边界的观察日志2褶皱变化值在每个类别的基因。MRTF签名≠背景。e)小提琴的情节MRTF签名在正常(n = 4)和IPF肺(n = 10)。f)无监督层次聚类分析MRTF签名的基因表达在IPF (n = 10)和正常肺(n = 4)。流式细胞仪:fluorescence-activated细胞排序;RNA-seq: RNA序列;SRF:血清反应的因素。假定值计算使用未配对的双尾t检验。
识别潜在的转录渠道负责细胞骨架和运动基因表达,我们探索潜在的转录因子,可能导致细胞骨架和运动性重组通过MSigDB [53),发现SRF假定的目标基因在细胞骨架和运动基因调节高纯度IPF肺中点击率最高(图1 c)。为激发能动性和细胞骨架基因表达通过MRTFs [21- - - - - -26),我们下一个旨在确定MRTF信号是活跃在肺纤维化的通过生成MRTF响应签名来衡量其活动。的分布相对MRTF响应签名(IPF的表达式与nondiseased肺)显示一个明显的转变比所有其他基因分析(图1 d)。无监督聚类分析nondiseased控制和IPF患者使用相同的MRTF签名显示分离nonfibrotic和纤维化的样品(图1 e和f)。我们也进行了类似的分析MRTF签名在另一个之前报道IPF队列(54]。一致,我们发现一个重要的浓缩MRTF IPF肺与健康对照组相比签名(补充图S2a-c)。因此,观察从两个独立的IPF军团支持hyperactivation MRTF信号在IPF肺。
MRTF激活在IPF myofibroblasts肺
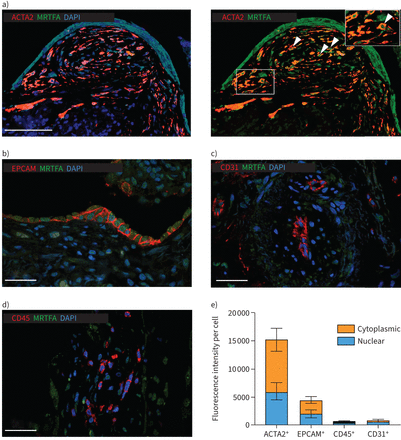
调查MRTF激活的细胞来源,我们进行免疫荧光化验检查MRTFA核本地化,MRTF激活的分子标志,IPF肺。在这方面,我们观察到著名MRTFA ACTA2的核本地化+myofibroblasts累积成纤维细胞疫源地,IPF肺组织学特性(图2一个和e),还应该注意分散MRTFA观察信号在EPCAM细胞质和细胞核+上皮细胞(图2 b和e),暗示MRTF激活这些细胞低于myofibroblasts。另一方面,我们只发现微不足道的细胞质和核MRTFA CD31的信号+内皮细胞和CD45+免疫细胞(图2 c- e)。因此,这些结果表明,myofibroblasts可能介导的主要细胞类型在IPF MRTF激活肺。
激活myocardin-related转录因子(MRTF)信号在myofibroblasts特发性肺纤维化(IPF)的肺。模拟)代表的免疫荧光图像MRTFA co-stained)α-smooth肌肉肌动蛋白(ACTA2), b) EPCAM, c) CD31和d) CD45 IPF肺部分。箭头:核MRTFA ACTA2+myofibroblasts。比例尺:a) 50µm;20µm罪犯)。e)核和细胞质MRTFA荧光信号恢复到正常水平的量化ACTA2细胞数量+,EPCAM+、CD45+和CD31+细胞IPF肺。IPF样本(n = 10)被用于MRTFA EPCAM信号量化+、CD45+和CD31+细胞,IPF样本(n = 8)被用于在ACTA2 MRTFA信号+细胞由于缺少纤维母细胞病灶在两个IPF样本。数据代表的意思是±sd。DAPI: 4′, 6-diamidino-2-phenylindole。
PFD抑制MRTF激活肺成纤维细胞的临床相关的剂量范围
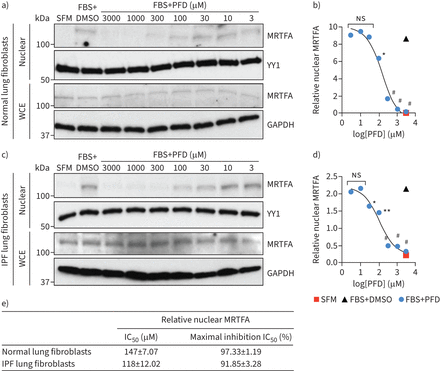
MRTF信号的hyperactivation IPF肺间质细胞,特别是肌成纤维细胞,提示我们推测PFD可能实现目标这个途径,至少,它的一些anti-fibrotic行动。因此,来测试这种可能性,我们检查了PFD能否抑制serum-induced MRTFA核易位在两个独立的主要人类肺纤维母细胞行从正常和IPF人类肺部孤立,分别。正如所料,PFD减毒serum-induced MRTFA核易位剂量依赖性的方式在不影响整体MRTFA蛋白质水平(图3一和c)。此外,我们没有观察到任何重大影响PFD的纤维胶原基因表达和肺纤维母细胞生存能力补充图S2和S3),一致,最近的一份报告建议MRTF信号不需要这两个过程在成纤维细胞(55]。的集成电路50对PFD MRTF核易位∼100∼150µM每个纤维母细胞,最大抑制达到> 90% (图3 b,d和e)。值得注意的是,集成电路50PFD抑制MRTFA核易位在临床上观察到浓度的范围(< 100µM) (56- - - - - -58),这表明部分抑制MRTF信号为PFD在人类IPF患者是可能实现的。我们也决定PFD在nonfibroblastic MRTF激活细胞的影响如肺泡上皮细胞,免疫细胞(如。中性粒细胞、巨噬细胞和树突细胞)和肺部动脉内皮细胞。数据显示PFD展品小影响serum-induced MRTF激活这些细胞即使在1毫米的浓度(补充图S4),表明PFD可能选择性地抑制MRTF肺成纤维细胞的信号。
Pirfenidone (PFD)抑制serum-induced myocardin-related转录因子(MRTFA)核积累在人类肺成纤维细胞在临床相关的浓度。a, c)代表西方滴核(顶面板)和全细胞提取物(WCE)(底板)MRTFA人类)正常和c)特发性肺纤维化(IPF)肺成纤维细胞用20%胎牛血清(的边后卫)没有或存在PFD的浓度表示。杨应1 (YY1)加载控制核分数。WCE Glyceraldehyde-3-phosphate脱氢酶(GAPDH)加载控制。b, d)量化的核积累MRTFA b)正常和c) IPF肺成纤维细胞。e)的总结PFD核MRTFA积累力量。e)中的数据表示的意思是±sd三个独立的实验。SFM:无血清媒体;集成电路50:half-maximal抑制浓度。假定值计算的边后卫与用单向方差分析的边后卫+ PFD。*:p < 0.05;* *:p < 0.01;#:p < 0.0001;ns:不重要。
转录组的分析抑制PFD MRTF信号在肺成纤维细胞的影响
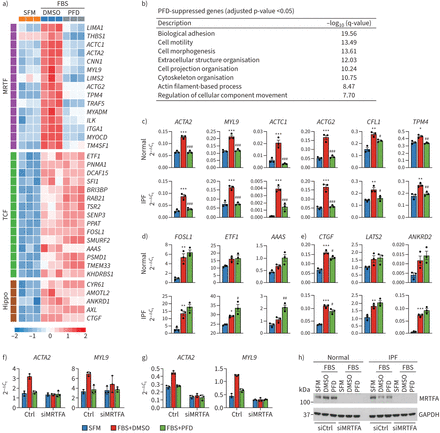
接下来,我们试图评估的系统性影响PFD的转录响应serum-induced MRTF肺成纤维细胞的信号。为这个实验我们选择1毫米PFD PFD的浓度可以达到≥90% MRTF两肺成纤维细胞抑制线路测试。RNA-seq serum-stimulated主要分析人类肺成纤维细胞显示PFD抑制一系列MRTF直接目标基因(图4一和补充图S5a)。一致,PFD表达下调的基因分析显示重要的功能性浓缩MRTF-related类别,包括细胞粘附、细胞活性、迁移和细胞形态发生(图4 b和补充图S5b)。
转录组分析pirfenidone (PFD)抑制影响myocardin-related转录因子(MRTF)信号。MRTF)的热图显示相对表达式,三元复杂因素(TCF)和河马目标基因在正常的人类肺成纤维细胞治疗或没有PFD。b)顶级基因本体生物过程丰富基因抑制PFD在20%胎牛血清(的边后卫)刺激正常的人类肺成纤维细胞。汉英)定量PCR验证中c) MRTF PFD抑制,d) TCF和e)河马目标基因表达在正常和IPF的人类肺成纤维细胞。f, g)ACTA2和MYL9表达式在无血清培养基(SFM)或20% FBS-stimulated f)正常和g)特发性肺纤维化(IPF)的人类肺成纤维细胞转染MRTFA或控制(Ctrl)小干扰RNA (siRNA) PFD的存在与否。h)代表免疫印迹的MRTFA全细胞提取物SFM或20% FBS-stimulated人类正常和IPF肺成纤维细胞转染MRTFA或控制核PFD的存在与否。Glyceraldehyde-3-phosphate脱氢酶(GAPDH)对全细胞提取的加载控制。PFD浓度:1毫米,n = 3生物复制。假定值计算单向方差分析。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001表明SFM的比较与的边后卫。#:p < 0.05;# #:p < 0.01;# # #:p < 0.001表示比较的边后卫与的边后卫+ PFD。
除了激活MRTF信号、血清可以强烈刺激其他途径,如三元复杂因素(TCF) [59和河马的信号60]。如果PFD选择性靶向MRTF信号,我们希望没有显著影响PFD TCF或河马下游靶基因的表达。为此,我们比较了几种行之有效的TCF和河马目标基因的表达血清刺激的缺乏或PFD的存在。正如预期的那样,我们观察到无显著的影响PFD在这些基因的表达(图4一,d和e补充图S5a)。此外,PFD似乎抑制serum-induced MRTF目标基因(例如ACTA2和MYL9)表达式通过MRTFA损耗的MRTFA完全废除PFD的拮抗作用(图4 f- h),支持作为MRTF PFD的特异性抑制剂。
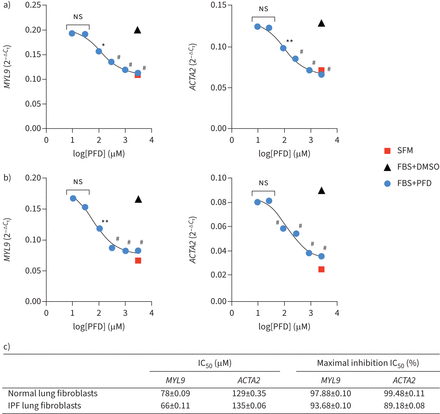
进一步调查如果临床相关的这些发现,我们确定两个MRTF目标基因的PFD剂量反应曲线:ACTA2和MYL9。同意其抑制活性MRTFA核易位(图3 e),PFD展品serum-induced类似的抑制能力ACTA2和MYL9表情:集成电路50范围在50到150µM最大抑制是> 90% (图5一个- c)。总的来说,这些结果表明,PFD的选择性抑制剂MRTF信号在肺成纤维细胞,至少,在体外。
测定pirfenidone (PFD)抑制效力在myocardin-related转录因子(MRTF)目标基因表达在人类肺成纤维细胞。a、b)剂量反应曲线的PFD抑制MRTF目标基因表达在人类)正常,b)特发性肺纤维化(IPF)肺成纤维细胞。c)的总结PFD抑制效力MRTF目标基因的表达。c)中的数据表示的意思是±sd三个独立的实验中,n = 3生物复制。集成电路50:half-maximal抑制浓度。假定值计算的胎牛血清(的边后卫)与用单向方差分析的边后卫+ PFD。*:p < 0.05。* *:p < 0.01;#:p < 0.0001;ns:不重要。
PFD MRTF肌动蛋白的间接促进了绑定
当我们观察到的抑制性影响PFD MRTF信号上,一个有趣的问题出现了:这可能是其机械基地的基础活动反对MRTF ?在这方面,我们认为以下三个关键上游MRTF核易位的细胞事件,都可能会影响到pdf: 1)ρGTPase / RhoA激活,2)肌动蛋白聚合和3)MRTF-actin交互。
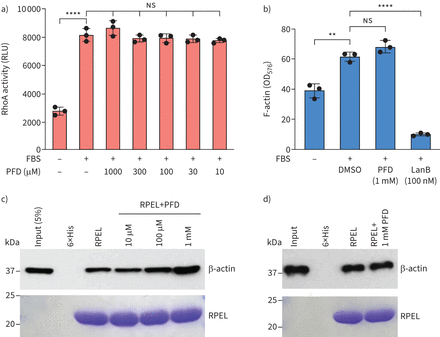
首先,我们探讨是否PFD抑制serum-induced RhoA激活和没有观察到显著影响的1毫米PFD RhoA激活(图6)。同样地,我们发现1毫米PFD并不影响G-actin聚合到f -肌动蛋白引起的血清,而LanB,有据可查的肌动蛋白聚合抑制剂,可以极大地扰乱这一过程(图6 b)。最后,我们测试了PFD的可能性可能调节物理MRTF和肌动蛋白之间的相互作用。我们融合MRTFA的肌动蛋白结合域,RPEL域(2 - 261),与6×他(His-RPEL)和执行下拉化验酝酿重组融合蛋白与胞质提取物治疗肺成纤维细胞有或没有PFD的浓度表示。结果表明,PFD增加内源性肌动蛋白的招聘His-RPEL重组蛋白剂量依赖性的方式(图6 c)。确定PFD直接促进这种交互,我们重复的下拉化验一个重组系统包括His-RPEL重组融合蛋白和肌动蛋白纯化蛋白质,而不是细胞提取物,1毫米PFD的存在与否。结果表明,PFD不能提高RPEL之间的交互和肌动蛋白重组系统即使在1毫米的浓度(图6 d)。总的来说,这些数据表明,PFD可能促进MRTF-actin物理交互以间接的方式,这可能成为PFD的拮抗作用的分子基础MRTF信号。
Pirfenidone (PFD)促进myocardin-related转录因子间接(MRTFA)和肌动蛋白相互作用。)Ras同系物家庭成员(RhoA)激活人类肺成纤维细胞刺激20%胎牛血清(的边后卫)没有或存在PFD的浓度表示。n = 3生物复制。b) f -肌动蛋白形成人类肺成纤维细胞刺激的边后卫在没有20%的1毫米PFD存在或100海里Latrunculin b (LanB)。n = 3生物复制。c)上面板:His-RPEL融合蛋白用于固定内源性肌动蛋白在细胞质溶解产物隔绝FBS-stimulated人类肺成纤维细胞治疗PFD表示浓度肌动蛋白免疫印迹紧随其后。底板:Coomassie蓝染色膜显示His-RPEL融合蛋白用于折叠式的化验。d)上面板:His-RPEL融合蛋白用于固定净化肌动蛋白缺失或存在的1毫米PFD肌动蛋白免疫印迹紧随其后。底板:Coomassie蓝染色膜显示His-RPEL融合蛋白用于折叠式的化验。数据在c和d)代表和类似的结果出现在三个独立的实验。 RLU: relative luminescence unit; OD: optical density. p-value calculated using one-way ANOVA. **: p<0.01; ****: p<0.01;ns:不重要。
PFD变弱MRTF IPF的肺成纤维细胞疫源地的核本地化
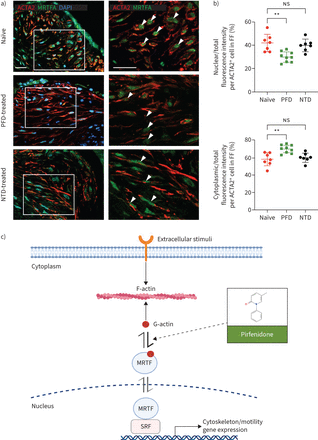
虽然我们的数据建立PFD MRTF抑制剂在体外,作为临床证据支持MRTF信号可实现的目标PFD在人类IPF患者缺乏。为此,我们分析了亚细胞定位的MRTFA纤维母细胞病灶区域发现一群由IPF患者有或没有pdf或被忽视的热带病37]。量化的MRTFA免疫反应性表明,纤维母细胞的核MRTFA信号病灶显著降低在IPF患者PFD比IPF患者没有接受PFD (图7和b)。相反,我们观察到,在纤维母细胞细胞质MRTFA信号病灶IPF患者PFD的显著高于在IPF患者不接受PFD (图7和b)。此外,我们确定的亚细胞定位MRTFA IPF患者成纤维细胞疫源地的被忽视的热带病从同一队列,并没有发现明显的变化与未经处理的IPF患者(相比图7和b),支持这一观点,我们没有找到任何的影响被忽视的热带病(1µM)在肺成纤维细胞MRTF目标基因的表达在体外(补充图S6)。另一方面,我们也注意到,pdf和被忽视的热带病影响MRTFA EPCAM的核/胞质分布+在IPF肺上皮细胞(补充图S7),支持PFD的观念可能特别抵销在肺成纤维细胞和myofibroblasts MRTF激活。总之,这些数据表明,pdf,但不是被忽视的热带病,抑制原位人类IPF MRTF激活肺。
Pirfenidone (PFD)抑制myocardin-related转录因子(MRTF)激活人类特发性肺纤维化(IPF)的肺。)代表的图像MRTFA纤维母细胞免疫荧光信号病灶(FF)地区的天真和PFD——或者nintedanib(元)治疗IPF肺部分。酒吧规模:20μm。箭头:核MRTFA ACTA2+myofibroblasts。核质分布的b) MRTFA ACTA2+myofibroblasts积累FF区域内(n = 8 IPF, n = 9为NTD-treated PFD-treated和n = 8;某些样本排除由于缺少FF)。c)示意图总结PFD的提议机制对MRTF通路的抑制活性。数据代表的意思是±sd。DAPI: 4′, 6-diamidino-2-phenylindole;ACTA2:α-smooth肌肉肌动蛋白;SRF:血清反应的因素。假定值计算单向方差分析。* *:p < 0.01;ns:不重要。
讨论
在过去的几十年里,生物医学社区多次治愈组织纤维化的动物。然而,只有PFD,以及被忽视的热带病,展品在IPF患者的临床好处(9,10]。因此,至关重要的是要理解这些药物如何工作IPF患者中获益。在此,我们第一次建立MRTF信号作为PFD的临床相关的和可实现的目标。这一发现是由一系列定量分析PFD的抑制性影响MRTF信号在体外和原位。在一个在体外成纤维细胞培养系统,我们测量PFD的抑制效力MRTF信号使用两种互补的读数:MRTFA核积累和MRTF目标基因的表达。这些独立的数据实验一致表明,集成电路50针对MRTF PFD的信号范围在50到150µM最大抑制是> 90%。我们所知,这是第一次效力的pdf报告。更重要的是,我们提出了人类的数据,PFD变弱MRTF信号∼30% IPF肺。考虑到临床可行的浓度对PFD < 100µM患者(56- - - - - -58),我们建议PFD的临床相关的抑制剂MRTF信号的患者。
PFD的拮抗作用的分子基础MRTF信号也调查了在当前的研究中。PFD的主要生物活性是抑制MRTF核积累,我们彻底PFD是否可以调节上游的细胞事件这一过程。令我们吃惊的是,我们发现PFD似乎促进MRTF之间的交互和肌动蛋白间接而不影响RhoA激活和肌动蛋白聚合。然后,直接分子PFD的目标可能是什么?在这方面,因为肌动蛋白是嵌入在一个复杂的细胞骨架网络,这是合乎逻辑的推测PFD可能目标特定分子接口(s) /管道(s)在细胞骨架网络间接调节MRTF-actin互动(图7 c)。这种可能性也可能有助于解释PFD在MRTF激活成纤维细胞的选择性影响细胞骨架,中央决定细胞的形状和形态,是唯一的亚细胞结构,区分成纤维细胞与其他细胞类型(61年,62年]。尽管如此,进一步的研究需要充分描绘了直接行动网站内的PFD (s)在成纤维细胞肌动蛋白/细胞骨架网络。
PFD的anti-fibrotic作用经常被与它的抗炎和anti-fibrotic活动等途径改变增长factor-β,肿瘤坏死factor-α和p38信号14,63年- - - - - -65年]。然而,主要说明在大多数研究是使用过度和临床上无法实现毫克分子浓度范围(主要)浓度的PFD展示其对这些通路的活动。从药理学角度来看,PFD的敌对活动在这些途径可能是临床上无关紧要,不得对PFD的患者的治疗效果。支持这一概念,但最近的研究报告说,转变增长factor-β信号不受PFD在患者样本15,37]。因此,在这种情况下,我们发现建立PFD作为MRTF抑制剂在临床上可实现的桥梁之间的差距PFD的药理作用浓度,床边。另一方面,由于MRTF信号的关键调节器mechano-transduction [22,28,29日)和新兴证据表明机械应力作为肺纤维化进展的关键驱动因素(66年,67年),有可能PFD的拮抗作用MRTF信号可能导致其治疗效果。
PFD的主要不良事件的患者包括皮疹、胃肠道事件,减少体重和海拔的丙氨酸、天冬氨酸转氨酶水平肝(9,68年]。然而,MRTF缺乏在人类和小鼠没有报道有关这些安全责任(23,69年,70年]。解释这种差异之一是机制PFD的副作用可能独立于其anti-fibrotic活动。鉴于小分子的化学性质,合理的PFD可以调节目标除了MRTF信号施加负面影响的病人。因此,未来的研究需要探索non-MRTF PFD的目标,这可能使潜在的PFD的修改来改善患者的治疗指数。
多达45%的死亡在发达国家可以归因于进行性纤维化疾病(5]。然而,直到最近,开发安全、有效的anti-fibrotic疗法已经被我们可怜的困惑的理解分子司机纤维化进展的患者。因此,我们目前的研究,建立了PFD作为临床相关MRTF抑制剂不仅可以阐明PFD的令人费解的anti-fibrotic机制也照亮MRTF信号作为一个制药司机慢性纤维化的进展。
补充材料
可共享的PDF
确认
我们感谢Genentech组织学和流式细胞仪实验室技术援助;基因泰克先进光学显微镜成像中心;并为RNA-seq Genentech挥动实验室。我们还要感谢琳达Rangell和黛博拉•邓拉普(美国基因泰克,南旧金山,CA)免疫组织化学支持。
脚注
数据和代码的可用性:RNA-seq一直存放在数据基因表达综合(GEO)数据存储库下加入GSE226249数量。样品制备的进一步信息,数据收集和数据处理方法中描述的细节,也可以针对铅接触。
作者的贡献:H-Y。马设计研究中,进行了实验,分析数据,并写了手稿。RNA-seq J.A.范德Heiden和美国Uttarwar进行分析数据,导致数据的解释。y Xi, r . LaCanna E-N。恩迪亚耶进行了实验。p . Caplazi导致纤维组织的组织学分析。美国Gierke帮助与免疫荧光成像。P.J. Wolters提供人类肺外植体和IPF肺活检。n丁设计的研究中,进行了实验,分析数据,与H-Y写的手稿。马和监督。
利益冲突:所有作者除了P.J. Wolters Genentech /罗氏公司或员工。
- 收到了2022年3月24日。
- 接受2022年12月14日。
- 版权©2023年作者。
这个版本分布在创作共用署名非商业性许可证的条款4.0。商业生殖权利和权限接触权限在}{ersnet.org