摘要
背景LIBERTY ASTHMA QUEST三期研究(ClinicalTrials.gov:NCT02414854)对无控制的中度至重度哮喘患者的疗效和安全性已经证明了dupilumab每2周200和300 mg的有效性和安全性与安慰剂。这事后分析评估了dupilumab对2型高哮喘患者一系列历史加重率的疗效结果和哮喘控制的影响。
方法52周治疗期间的年化严重加重率,支气管扩张剂前1 s用力呼气量(FEV)1),并在第24周和第52周评估前一年有≥1、≥2或≥3次发作的患者的哮喘控制问卷(ACQ-5)评分。按基线血嗜酸性粒细胞≥150或≥300个·μL分组−1或基线呼出一氧化氮分数≥25 ppb和基线吸入皮质类固醇(ICS)剂量。
结果在所有2型高亚组中,dupilumab与安慰剂显著减少了54-90%的严重发作,在研究开始前有更多发作的患者改善更大。同样,FEV的改善1(最小二乘(LS)表示差值与安慰剂:≥1次加重,0.15-0.25 L;≥2次加重,0.12-0.32 L;≥3次加重,0.09-0.38 L;多数p<0.05)和ACQ-5评分(LS平均差异范围:≥1次加重,−0.30 ~−0.57;≥2次恶化,−0.29至−0.56;≥3次恶化,−0.43 ~−0.61;所有亚组均观察到所有p<0.05),无论既往加重史如何。
结论Dupilumab显著减少严重恶化和改善FEV12型生物标志物升高患者的哮喘控制,与恶化史和ICS基线剂量无关。
摘要
Dupilumab减少了2型高哮喘患者的严重加重,改善了肺功能和哮喘控制,与加重史和ICS基线剂量无关。这些数据将有助于临床医生管理重症患者。https://bit.ly/2PjnSm6
简介
哮喘加重有时可能需要改变患者目前的治疗方法,导致大量的死亡率,并由于与其管理相关的医疗保健费用而造成相当大的经济负担[1,2].2型哮喘患者和/或接受高剂量吸入皮质类固醇(ICS)的患者病情更严重,需要更高剂量的类固醇来维持哮喘控制。因此,这些亚人群未来病情恶化的风险更大[3.].此外,哮喘加重史,特别是近期事件,已被证明是未来加重风险的一个重要独立预测因子[4,5].
Dupilumab是一种完全由人velocimmune衍生的单克隆抗体,可阻断白介素(IL)-4和IL-13的共有受体成分,从而抑制IL-4和IL-13的信号传导,这两种受体是多种疾病中2型炎症的关键和核心驱动因素[6- - - - - -9].这些细胞因子与IL-5一起在哮喘的发病机制中发挥重要作用[9,10].Dupilumab被批准用于≥12岁的中度至重度嗜酸性粒细胞性或口服皮质类固醇依赖性哮喘患者,用于控制不充分的伴有鼻息肉的慢性鼻窦炎成人患者,以及在美国和欧盟等国家用于治疗控制不充分的中度至重度特应性皮炎6岁成人患者[11- - - - - -20.].
在LIBERTY ASTHMA QUEST第三期研究中,dupilumab每2周200和300mg与匹配的安慰剂显著降低了严重加重率,并在1 s内改善了支气管扩张剂前用力呼气量(FEV)1)、哮喘控制和中度至重度哮喘患者的生活质量措施[15].2型炎症生物标志物(血液嗜酸性粒细胞≥150细胞·μL)基线水平升高的患者治疗效果通常更显著−1或呼出的一氧化氮(F伊诺)≥25 ppb) [15].
了解dupilumab等治疗在高疾病负担患者(近期频繁加重和大剂量ICS使用证明)中的疗效,对于临床医生治疗重症患者具有相当大的意义。这样做的目的事后LIBERTY ASTHMA QUEST研究的分析是评估dupilumab对2-高表型患者亚组中严重加重、肺功能和哮喘控制的影响,这些患者在前一年经历了一系列加重(≥1、≥2或≥3),并进一步按基线ICS剂量(高与介质)。
方法
研究设计与患者
自由哮喘任务(ClinicalTrials.gov:NCT02414854)是一项三期多国、多中心、随机、双盲、安慰剂对照研究,评估dupilumab对未控制的中度至重度哮喘患者的疗效[15].年龄≥12岁且医生诊断为12个月哮喘的患者(根据2014年全球哮喘倡议指南)有资格参加[21].该研究对所有患者开放,无论嗜酸性粒细胞状态或任何其他生物标志物要求。患者按2:2:1:1的比例随机分组,每2周皮下注射dupilumab 200 mg(加载剂量400 mg)或300 mg(加载剂量600 mg)或匹配体积的安慰剂52周。该研究的设计和方法的全部细节已在以前报道过[15,22];完整的患者资格标准,包括所有患者在登记前一年内有≥1次恶化的要求,可在原始稿件的补充附录中找到[15].
这项研究是根据《赫尔辛基宣言》、国际协调会议的良好临床规范指南和适用的监管要求进行的。一个独立的数据和安全监测委员会对患者安全数据进行了盲法监测。研究的进行和记录由当地机构审查委员会或伦理委员会监督,所有患者在参加试验前都提供书面知情同意。
研究终点和人群分析
本文分析的终点事后LIBERTY ASTHMA QUEST的分析结果为:52周治疗期间严重加重的年化率,支气管扩张剂使用前FEV与基线相比的最小二乘(LS)均值变化1(L)在第12和52周时,LS表示在第24和52周时哮喘控制问卷(ACQ-5)五项评分较基线的变化。严重哮喘加重被定义为哮喘恶化,需要全身皮质类固醇治疗3天,或因哮喘住院或急诊,需要全身皮质类固醇。ACQ-5是患者报告的哮喘控制充分性和哮喘控制变化的测量方法;得分越高,哮喘控制越差[23].
对患者进行亚组分析,按前一年加重次数(≥1、≥2或≥3)、基线血嗜酸性粒细胞(≥150或≥300细胞·μL)分层−1),基线F伊诺(≥25 ppb)和基线ICS剂量(中或高)。对基线时2型生物标志物水平未升高(嗜酸性粒细胞<150细胞·μL)的亚组患者也进行了分析−1而且F伊诺< 25磅)。
统计分析
以52周治疗期间发生的事件总数作为响应变量,4个干预组,年龄、地理区域、基线嗜酸性粒细胞层(<300或≥300个细胞·µL−1)、ICS基线剂量水平和前一年加重次数为协变量。与基线相比,支气管扩张剂前FEV的变化1ACQ-5评分采用重复测量的混合效应模型进行分析,包括指定的干预、年龄、基线嗜酸性粒细胞层数、随访、逐次干预交互作用、地区(合并国家)、相应的基线支气管扩张剂前FEV1或ACQ-5值和基线访视交互作用为协变量。性别和基线身高是FEV模型的附加协变量1.对于中断指定的干预并继续参与试验的患者,中断干预后的测量结果被纳入分析。
每个dupilumab剂量与安慰剂(在每个亚组内)之间的比较p值<0.05被认为具有统计学意义。
结果
病人的特点
1902例患者被纳入LIBERTY ASTHMA QUEST试验(1264例分配给dupilumab组,638例分配给安慰剂组),所有患者在前一年经历≥1次严重加重事件[15].尽管在研究开始前一年经历了≥3次发作的患者,其支气管扩张剂前FEV相对较低,但各亚组的基线特征无重大差异1基线时对ICS的使用要求也高于病情加重较少的患者。经历≥3次加重的患者也有较高的平均基线血嗜酸性粒细胞水平和F伊诺(表1).
严重哮喘加重年化率
Dupilumab每2周(联合治疗组)显著降低严重恶化率与基线血嗜酸性粒细胞升高的患者服用安慰剂,而不考虑加重史或基线时ICS剂量,既往加重≥2或≥3次的患者改善幅度更大(图1).降低恶化率与在意向治疗组(ITT)中,安慰剂为58% - 71%,而在基线嗜酸性粒细胞≥150细胞·μ L的ICS高剂量亚组中为54% - 65%−1基线嗜酸性粒细胞≥300细胞·µL的患者,ITT为66% ~ 75%,高剂量ICS为63% ~ 67%−1基线患者中63% ~ 80% (ITT)和62% ~ 75%(高剂量ICS)F伊诺≥25 ppb(所有p<0.001) (图1一个- c)。在基线时中等剂量ICS的患者中观察到类似的趋势(补充图S1a).在所有高2型生物标志物亚组中,dupilumab治疗后调整的年化加重率为0.16(在≥300细胞·LµL的患者中)−1dupilumab 200和300 mg联合治疗的中剂量ICS)到0.65(≥150细胞·µL−1和联合dupilumab 200和300 mg治疗的大剂量ICS)相比,安慰剂治疗患者的发生率在0.86到2.35之间。
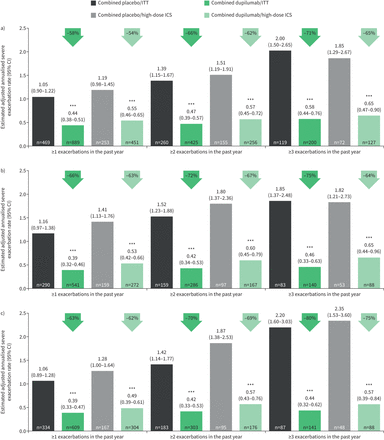
在52周干预期间,LIBERTY ASTHMA QUEST患者亚组严重加重的年化率(95% CI)降低(按a)基线血嗜酸性粒细胞≥150细胞·μL分类)−1, b)基线血嗜酸性粒细胞≥300细胞·μL−1c)基线呼出一氧化氮分数≥25 ppb(意向治疗(ITT)或高剂量吸入皮质类固醇(ICS))。* * *: p<0.001与安慰剂。
基线嗜酸性粒细胞<150细胞·µL−1和基线F伊诺<25 ppb,数值改进与观察到安慰剂的年化加重率,尽管这些在统计学上不显著(补充图S1b).
Pre-bronchodilator FEV1
Dupilumab 200和300 mg每2周(联合治疗组)与匹配的安慰剂改善了支气管扩张剂前FEV1在第12周,不论所有亚组的加重史如何(按基线嗜酸性粒细胞分层),F伊诺或ICS剂量(图2而且补充图S2);这些改善在大多数病例中具有统计学意义,改善水平随着先前恶化的次数增加而增加。在基线生物标志物水平(血液中嗜酸性粒细胞≥150或≥300细胞·μL)升高的亚人群中−1或基线F伊诺≥25 ppb),根据基线ICS剂量组进一步分层,以及在前一年经历≥1次恶化的患者,LS表示第12周支气管扩张剂前FEV较基线的变化1dupilumab组为0.35 - 0.46 L,安慰剂组为0.20 - 0.23 L (LS均值差异与安慰剂范围为0.15 ~ 0.25 L;所有p<0.001) (图2一个- c,补充图S2a和b).dupilumab治疗的改善在既往恶化≥2和≥3的生物标志物升高亚组中也很明显。在前一组,dupilumab治疗增加了支气管扩张剂前FEV1与安慰剂组0.19 - 0.28 L的变化相比(LS平均差异与安慰剂范围为0.12 ~ 0.31 L;p均<0.01)(图2一个- c和补充图S2a).在生物标志物水平升高和既往发作≥3次的患者亚组中,dupilumab和安慰剂在第12周的改善分别在0.36 - 0.66 L和0.19 - 0.33 L之间(LS平均差异)与安慰剂范围为0.09 ~ 0.38 L;所有p < 0.01与基线血嗜酸性粒细胞≥150细胞·μL的患者除外−1高ICS剂量(p=0.0679) (图2一个)和基线血嗜酸性粒细胞≥300细胞·μL的患者−1和高ICS剂量(p=0.1717) (图2 b).在第52周持续改善(补充图S2a和b).
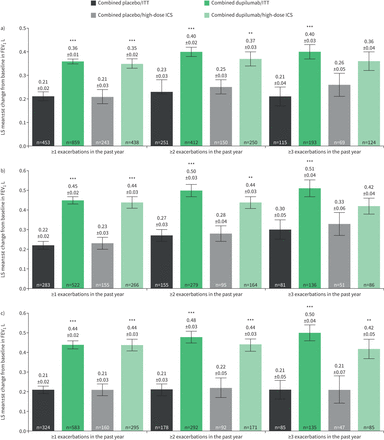
最小二乘(LS)为±se第12周支气管扩张剂前1 s用力呼气量(FEV)较基线有变化1),按a)基线血嗜酸性粒细胞≥150细胞·μL分类−1, b)基线血嗜酸性粒细胞≥300细胞·μL−1c)基线呼出一氧化氮分数≥25 ppb(意向治疗(ITT)或高剂量吸入皮质类固醇(ICS))。* *: p < 0.01;* * *: p<0.001与安慰剂。
在基线生物标志物未升高的亚组患者中(即。基线血嗜酸性粒细胞<150细胞·μL−1和基线F伊诺<25 ppb), dupilumab治疗的数值改善与在第12周和第52周观察到安慰剂,尽管这些在统计学上基本不显著(补充图S2c).
ACQ-5分数
每2周Dupilumab一次(联合治疗组)与在第24周,与安慰剂改善哮喘控制(ACQ-5评分)相匹配,而不考虑按基线嗜酸性粒细胞分层的所有亚组的加重史,F伊诺或ICS剂量(图3而且补充图S3).和FEV一样1这些改进的终点与安慰剂在大多数病例中具有统计学意义,在基线时生物标志物水平升高和既往发作≥3次的患者中观察到更大的改善。在这些在前一年经历过≥1次恶化的患者的亚组中,第24周ACQ-5评分的LS平均变化范围为dupilumab组- 1.47 - - 1.70,安慰剂组- 1.05 - - 1.24 (LS平均差异)与安慰剂的范围为−0.30 ~−0.56;所有p<0.001) (图3一- c,补充图S3a和b).在前一年有≥2和≥3次恶化的患者中,dupilumab治疗的改善范围分别为−1.51 ~−1.83和−1.58 ~−1.90;接受安慰剂的患者在哮喘控制方面的改善较低,分别为- 1.12 ~ - 1.45和- 1.07 ~ - 1.47与既往发作≥2次和≥3次的患者,安慰剂的范围分别为−0.29 -−0.56和−0.43 -−0.61;所有p < 0.05)。在第52周持续改善(补充图S3a和b).
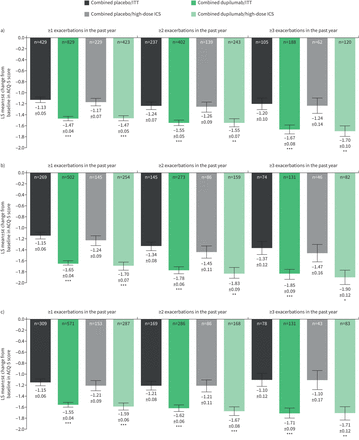
最小二乘(LS)为±se根据a)基线血嗜酸性粒细胞≥150细胞·μL的患者,哮喘控制问卷(ACQ-5)评分五项评分在第24周较基线发生变化−1, b)基线血嗜酸性粒细胞≥300细胞·μL−1c)基线呼出一氧化氮分数≥25 ppb(意向治疗(ITT)或高剂量吸入皮质类固醇(ICS))。*: p < 0.05;* *: p < 0.01;* * *: p < 0.001与安慰剂。
与加重率和FEV一样1终点,在基线生物标志物没有升高的亚组患者中,dupilumab的数值改善与在第24周和第52周观察安慰剂组(补充图S3c),尽管这些数据在统计上并不显著。
讨论
这事后LIBERTY ASTHMA QUEST 3期随机对照试验的分析评估了附加dupilumab治疗对严重发作年化率、肺功能(支气管扩张剂前FEV)的影响1)和哮喘控制(ACQ-5评分)。即。≥1、≥2或≥3次发作发生在研究入学前一年。这些亚群体进一步分层的基线水平升高的血液嗜酸性粒细胞(≥150或≥300细胞·μL)−1),F伊诺(≥25磅),即。2型炎症的两个生物标志物,以及进入时的ICS剂量(中或高)。选择这些地层的理由是基于以下知识:近期的恶化可以独立预测未来的恶化风险[4,52型生物标志物升高和/或接受高剂量ICS的患者病情更严重,因此哮喘加重的风险更大[3.,24].事实上,这些观察结果被患者的基线特征所证实,在研究开始前一年经历≥3次发作的亚组患者表现出相对较差的肺功能(支气管扩张剂前FEV)1)和对集成电路使用的更高要求。此外,既往发作次数与基线2型生物标志物水平之间似乎也有很强的联系,这表明2型特征较强的患者有更高的发作风险。
在所有亚组中,dupilumab每2周200和300 mg(联合用药)与匹配的安慰剂显著降低了严重的年化加重率,无论患者在研究开始前一年经历了多少次加重。此外,有一种趋势表明,与安慰剂相比,改善的幅度随着前一年经历的严重哮喘加重事件的数量而增加。因为病情加重的风险往往与近期病情加重的次数成比例增加[4,5],这一发现表明dupilumab抑制了这种增加的恶化风险,这一现象在其他哮喘生物制剂中也有报道[22,25].在所有高2型生物标志物亚组中,即使是在那些因既往高发生率的加重和高2型特征而被认为是最严重和最难治疗的组中,dupilumab治疗在改善肺功能方面表现出相当大的疗效,与安慰剂相比改善高达0.38 L。ACQ-5评分也有临床意义的改善[23],表明哮喘得到了更好的控制,无论患者在前一年经历过严重哮喘加重的数量,或他们的2型生物标志物的基线水平或ICS剂量。即使在最严重的高2型特征且在前一年经历≥3次加重的患者中,与安慰剂相比,dupilumab治疗第24周时ACQ-5评分也有临床意义和统计学意义的改善。
对于所有终点,在未显示2型表型的亚组患者中,观察到dupilumab治疗与安慰剂治疗相比在数值上的改善(即。基线嗜酸性粒细胞生物标志物浓度<150细胞·µL−1而且F伊诺< 25磅)。然而,与在2型高亚人群中观察到的效果相比,大多数这些改善在统计上不显著,治疗效果的幅度是最小的。在2型生物标志物升高的患者中观察到更大的治疗效果与dupilumab的作用机制一致,dupilumab通过与IL-4受体α结合,抑制2型细胞因子IL-4和IL-13,从而抑制这些患者表现出的2型炎症[9].在其他dupilumab哮喘研究中也报道了类似的发现[14- - - - - -16].
尽管本研究中所分析的数据是在一个大型的、随机的、严格控制的临床试验中收集的,但所提出的分析有一个局限性事后自然,因为母体研究没有能力专门调查所描述的亚种群的差异。因此,所分析和描述的许多亚组的样本量都很低。此外,本研究评估的许多加重的病因,无论是在研究开始前一年还是在研究期间,都是未知的。多种因素可导致病情加重,包括病毒或细菌呼吸道感染、环境过敏原、污染物和职业接触[26].事后看来,更好地描述所研究的病情加重的原因可以促进对dupilumab在这些表型中的疗效的比较检查。
总之,事后分析证实,使用dupilumab在LIBERTY asthma QUEST的ITT人群中观察到的严重加重率的显著降低、哮喘控制和肺功能的改善延伸到2型炎症生物标志物升高的患者,无论加重史和基线时ICS剂量如何。这些发现表明,既往的加重史对治疗临床医生的预后没有进一步的增加价值,但对临床医生了解dupilumab的疗效有相当大的价值,特别是在疾病负担非常严重的患者中。
补充材料
可共享的PDF
确认
我们感谢Nora Crikelair (Regeneron Pharmaceuticals, Inc., USA)和Colin Mitchell (Sanofi, USA)的贡献。医疗写作/编辑协助由Sinéad Holland(英国摘录pta Medica)提供。
脚注
本文的补充资料可从www.qdcxjkg.com
自由哮喘任务注册在ClinicalTrials.gov带有标识符号NCT02414854.有资格的研究人员可以要求访问患者级别的数据和相关研究文件,包括临床研究报告、研究方案(任何修订)、空白病例报告表格、统计分析计划和数据集规范。患者级别的数据将被匿名化,研究文件将被编辑以保护试验参与者的隐私。关于赛诺菲数据共享标准、合格研究和申请访问流程的更多细节可在以下网站找到:http://www.clinicalstudydatarequest.com.
利益冲突:J. Corren报告在提交的工作之外,赛诺菲对研究的非财务支持。
利益冲突:C.H. Katelaris报告在提交的工作之外,来自赛诺菲的非财务支持(顾问委员会成员和主要研究研究员)。
利益冲突:M. Castro报告了美国肺科协会、Gossamer、NIH、PCORI和Shionogi对研究的非财政支持,阿斯利康的个人讲座费和对研究的非财政支持,勃林格英格翰和赛诺菲的个人讲座费和咨询费,诺华的个人咨询费和对研究的非财政支持,波士顿科学和维达制药的个人咨询费,来自梯瓦的演讲和咨询的个人费用,来自基因泰克和再生制药公司的演讲的个人费用,来自爱思唯尔的个人费用(版税),在提交的作品之外。
利益冲突:J.F. Maspero曾担任阿斯利康、葛兰素史克、Menarini、诺华、赛诺菲、梯瓦和乌利亚的发言人;在提交的工作之外,还获得了诺华的研究资助。
利益冲突:L.B. Ford报告了来自阿斯利康、DBV、基因泰克、Gossamer、诺华和梯瓦的研究的非财务支持,以及来自赛诺菲的个人咨询费用,在提交的工作之外。
利益冲突:D.M.G.哈尔平报告了在提交的工作之外,阿斯利康、勃林格殷格翰、基耶西、CSL Behring、葛兰素史克、诺华、辉瑞、山德士和赛诺菲的演讲和顾问委员会工作的个人费用。
利益冲突:M.S. Rice是赛诺菲的雇员,可能持有公司股票和/或股票期权。
利益冲突:A. Radwan是Regeneron Pharmaceuticals, Inc.的员工和股东。
利益冲突:Y. Deniz是Regeneron Pharmaceuticals, Inc.的雇员和股东。
利益冲突:P.J. Rowe是赛诺菲的员工,可能持有公司股票和/或股票期权。
利益冲突:a .泰珀是赛诺菲的前雇员。
利益冲突:M. Djandji是赛诺菲的员工,可能持有公司股票和/或股票期权。
支持声明:研究由赛诺菲和Regeneron制药公司赞助。医疗写作/编辑援助由赛诺菲健赞公司和再生龙制药公司资助。本文的资助信息已存入Crossref基金管理人登记处.
- 收到了2020年12月11日。
- 接受2021年3月16日。
- 版权所有©作者2021。
本版本按照创作共用署名非商业性许可4.0的条款发布。商业复制权利及许可请联系权限在}{ersnet.org















