文摘
背景这个真实的研究旨在评估omalizumab治疗模式在成人和儿科哮喘病人,并描述哮喘控制和医疗资源使用(HCRU) omalizumab启动和停止。
方法法国医疗数据库系统(和国家des数据德桑特(snd))是用来确定≥6岁哮喘病人发起omalizumab至少16周从2009年到2019年。我们检查了omalizumab治疗模式使用分配记录。
结果我们确定了16 750名成年人和2453名儿童发起omalizumab。平均治疗持久化之前中止(T停止)为51.2 (95% CI 49.3 - -53.4) 53.7个月的成人和儿童(95% CI 50.6 - -56.4)个月。omalizumab暴露的2年,为哮喘住院率下降了75%,使用口服皮质类固醇(OCS) 30%,成人和儿童。在成年人停止omalizumab哮喘控制的时候,70%,39%和24%保持控制和没有简历omalizumab 1,分别为2和3年前中止。这些儿童的比例较高(分别为76%、44%和33%)。在停药后2年的随访中,在成人和儿童HCRU保持稳定,尤其是哮喘住院率(之前没有T停止、1.3%和0.6%,2年)和使用口服避孕药(在成人和儿童中,分别为:20.0%和20.2%之前,T停止在2年,33.3%和24.6%)。
结论这是第一次大规模的研究描述omalizumab实际接触模式在成人和儿科哮喘患者在法国> 10年的随访。我们显示的长期维护低HCRU成人和儿童停止omalizumab哮喘控制的时候,尤其是使用口服避孕药和哮喘住院治疗上。
文摘
这真实的研究显示长期维护低医疗资源使用在成人和儿科哮喘病人停止omalizumab治疗在哮喘控制https://bit.ly/3kzWH2d
介绍
尽管现实的研究提供了有价值的信息关于omalizumab治疗严重的哮喘病人,问题仍然存在关于omalizumab治疗的最佳时间1- - - - - -6]。虽然一些研究表明,大多数病人维持哮喘控制omalizumab停用后,其他人显示亏损哮喘控制(4,7,8]。迄今为止未知的有益作用是否omalizumab减少哮喘急性加重和医疗资源使用(HCRU)在现实生活中维持治疗后停药,也没有什么时间。最后,提供真实的数据主要关注成人患者中;较少的数据可供孩子,目前尚不清楚omalizumab有效性和曝光模式在现实生活中的两个种群之间的差异。
卫生行政数据库是有价值的数据来源检查药物接触模式和定量评估HCRU在现实生活中9,10]。解决上述问题的第一步是描述治疗模式在现实生活中的一个长期后续识别长期停用,可认为是故意的,而不是临时或短期停用目前文献中描述(omalizumab政府之间的差距≥90天或中止≥60天(11,12])。在这种情况下,使用法国医疗数据库系统(和国家des数据德桑特(snd)),本研究旨在评估omalizumab治疗的持久性,从起始到长期停用,在成人和儿科哮喘患者在真实的环境中,和描述哮喘控制启动和停止治疗。我们还提供一个纵向动态分析的HCRU omalizumab启动和停止,包括药物、医疗和辅助医疗访问,和住院治疗上。
材料和方法
数据来源
snd聚集,在个体层面,信息对门诊和住院医疗报销费用,和原因住院(国际疾病分类和相关的健康问题,10日修订(icd - 10)),日期和相关成本(13]。到目前为止,snd涵盖∼99%的法国人(13]。这是一个宝贵的工具,探索现实HCRU在法国13- - - - - -15],包括哮喘HRCU [16,17]。
这项研究是国家批准的专业委员会(蜡膜;1294482)和法国的个人数据保护署(yann padova;ar - 203 - 292)。相关的数据处理公司,法国里昂)符合法国访问个人数据保护机构标准snd (RERC181009)。
研究人群
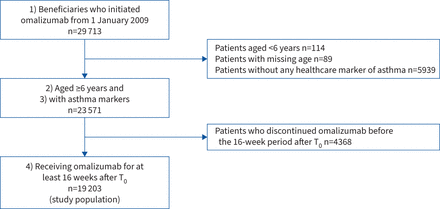
中可用的研究人群包括受益人snd 1)启动治疗omalizumab从2009年1月至2019年12月,2)≥6岁启蒙,3)HCRU标记的哮喘患者(排除为慢性荨麻疹omalizumab指示,另一个批准的迹象omalizumab疗法在那段时期;看到补充附录S2(18- - - - - -20.]),4)发起omalizumab最小累积暴露一段16周超过20周后启动(启动omalizumab治疗16周后对应的时间点治疗效果评估管理进一步omalizumab注射之前,如上所述在产品特征的总结21])。通过这种方式,我们旨在只包括那些病人可能受益于omalizumab治疗和为谁评估相关的治疗模式。
研究设计和设置
这是一个全国性的药物利用研究基于二次数据。该指数T日期0与第一个分配omalizumab (补充附录S1)。曝光模式描述了从T02019年12月31日或病人的死亡。
社会人口特征描述在T0。治疗历史评估在前年T0。并存状况确定使用映射算法基于T之前报销医疗保健支出的3年历史0(补充附录S2)。哮喘控制(即。没有哮喘恶化标记)和全球倡议的使用哮喘(吉娜)4 - 5步疗法,代表哮喘严重程度,评估基于今年的报销支出前T0(补充附录S2)。
HCRU在omalizumab起始评估患者发起omalizumab从2012年到确保住院次数的彻底性。他们从今年前T检验02年后T0,每6个月序列,其中只有病人的随访和治疗omalizumab整个序列都包括在内。HCRU omalizumab停用(T停止)是评估同样,从今年前T停止2年后T停止。
接触omalizumab
曝光模式建模分别基于分配的动态日期和盒子的数量和性质(es) [22]。以下假设是:1)一omalizumab豁免期限30天,2)最小周期没有任何omalizumab分配定义一个长期停用1年(补充附录S3)。指标来描述omalizumab曝光模式治疗的持久性和药物持有率(MPR)代替坚持。Omalizumab治疗持久性定义为持续时间从T0第一个长期停用,因此对应于第一个连续治疗omalizumab序列(23]。MPR定义为天数的比例覆盖量omalizumab分发的持续时间从T0长期停用;表示坚持MPR > 80%。
统计分析
kaplan meier方法被用来估计omalizumab治疗的持久性;审查病人与病人的随访期结束后,或去世,之前任何长期停用。追求omalizumab概率,即。在第一个连续暴露疗法序列之前长期停用,计算,每年,它使用对数转换95%置信区间。没有缺失值进行替换;没有代码表明snd中丢失的数据。分析使用SAS版本9.4.6.0 (SAS研究所卡里、数控、美国)。
结果
Omalizumab曝光模式和HCRU期间曝光
均值±sd整体随访期为59.4±37.0个月的成人和57.9±36.6个月的孩子。总共960名成人(5.7%)和八个孩子(0.3%)死于后续(242成人和三个孩子死于omalizumab曝光)。死亡原因没有在数据库中,但是574名成年人和五个孩子在住院期间死亡,其中27个成人和两个孩子住院了哮喘。
在研究人群,48.3% (n = 9282;48.9%的成年人和44.2%的儿童)至少有一个长期的中止。从kaplan meier分析,治疗的持久性中位数是51.2 (95% CI 49.3 - -53.4)个月的成人和儿童53.7 (95% CI 50.6 - -56.4)个月(补充附录S4)。追求成人omalizumab概率为0.78 (95% CI 0.77 - -0.79), 0.66 (95% CI 0.65 - -0.67), 0.40 (95% CI 0.39 - -0.41)和0.29 (95% CI 0.28 - -0.30) 1、2、6和10年从T0,分别。在儿童中,概率分别为0.89 (95% CI 0.87 - -0.90), 0.78 (95% CI 0.76 - -0.79), 0.31 (95% CI 0.28 - -0.34)和0.17 (95% CI 0.12 - -0.21),分别。中位数(四分位距(差))MPR对这个初始序列是99.7%(91.2 -100.0%)在成人和儿童(92.3 -100.0%)100.0%;14 (n = 794) 88.3%的成年人和89.5%的儿童(n = 2196)附着(MPR > 80%)。
关于omalizumab序列(即。曝光时间不间断长期停用),94.8%的病人(n = 18 200)只有一个接触序列(在成人中,94.7% 15 n = 866;95.1%的孩子,有两个n = 2334), 4.9%(5.0%的成年人,n = 830;4.5%的孩子,n = 111)和0.3%有超过两个(0.3%的成年人,n = 54;0.3%的孩子,n = 8)。
评估的HCRU omalizumab启动显示减少在2年随访在成人和儿童(表2和图2)。与之前相比起始([−6;T0(几个月),患者的数量HCRU年底降低了后续([18;24(月)73.8%和76.6%,分别在成人和儿童,为哮喘住院,27.9%和32.5%的大一消费,和吸入激素(ICS)的1.0%和11.6%。也观察意味着减少每日剂量ICS(分别为3.7%和21.2%,在成人和儿童)和口服避孕药的成年人(22.2%)(表3)。
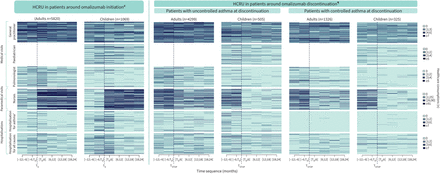
索引块医疗资源使用(HCRU)每学期约omalizumab启动(T0)(从今年前T02年后T0)和周围omalizumab中止(T停止)(从今年前T停止2年后T停止)。每人口指数情节了,每性质的医疗和时间序列(个月)在个体层面,为每个主题的人口。只有一个完整的患者随访2年之后T停止提出了。HCRU对于一个给定的病人在同一行表示对整个随访期。病人的任命从上到一个较低的线是相同的所有医疗在相同的人口。#:部分患者2年随访之后可用T0和暴露于omalizumab 2年;¶:部分患者2年随访之后可用T停止;+:作为主要的或相关的诊断。
哮喘控制和HCRU病人omalizumab停止
护理路径omalizumab长期停用后(T停止)在7761名成年人和1082名儿童进行评估后至少一年随访期间长期停用;其中,1829名成年人和442名儿童没有标记的不受控制的哮喘前中止,因此被认为是控制。均值±sd停药相似年龄是否哮喘控制在中止(分别为51.3±16.5,53.9±15.5年成人和儿童15.5±3.2,14.5±3.4年)。在成人和儿童中值(差)治疗的持久性在停药,分别为18.2(29.4)和36.8(33.0)个月如果哮喘控制在停药和12.8(23.8)和21.4(32.1)个月如果不受控制的哮喘。
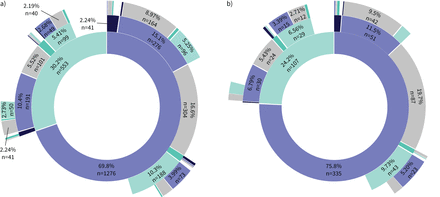
控制哮喘患者在停药,55.4%的成年人(n = 1013)和69.9%的儿童在T (n = 309)已经不受控制0(与82.1%的成年人和83.9%的儿童在T0治疗总群omalizumab发起者)(表1);43.2% (n = 791)和36.2% (n = 160),分别使用吉娜4 - 5步治疗(与66.5%的成年人和46.5%的儿童对整个队列)(表1和补充附录S5)。停止在1、2和3年后,69.8% (n = 1276), 39.4% (n = 720)和24.3% (n = 444)的成年人,分别仍然没有恢复omalizumab控制;38.9%的患者随访结束前3年(图3一)。的孩子,这是75.8% (n = 335), 44.1% (n = 195)和32.6% (n = 144),分别;随访结束前3年为40.7% (图3 b)。一些不受控制的成人和儿童收到其他生物疗法后停药(表4)。
暴露于阳光图表哮喘控制和omalizumab患者长期停用,停药后至少1年的随访中,在停药后3年随访)成年人(n = 1829)和b)儿童(n = 442)。患者已经被在一年的四个州(从中心第一层),2年(第二层)和omalizumab停用后3年(第三层):控制,和未曝光omalizumab(紫色)或恢复omalizumab(黑色)或不受控制的,远离omalizumab(浅绿色)或恢复omalizumab(深绿色)。最里面的环标志着国家在停药后1年,和第二个和第三个同心圆出口给美国的队列在停药后2和3年。患者不再改变的状态在后续继续保持下戒指。患者随访结束在灰色的。只有样本大小的> 2%。
年底omalizumab暴露([−6;T停止(),在控制哮喘患者HCRU T停止在那些不受控制的哮喘,低于所有研究项目(表4和5,图2)。此外,之前HCRU T停止在成人和儿童哮喘T控制停止低于HCRU T0([−6;T0()中观察到整个群omalizumab治疗发起人,为所有项目除了护理,符合omalizumab管理局(表2和3)。商务用户的比例在T0分别是75.3%和73.2%,成人和儿童;他们分别为20.0%和20.2%,T停止在成人和儿童哮喘控制。OCS意味着成人每日剂量分别为9.0±8.1毫克−1在T0和2.5±1.2毫克−1在T停止。停药后的纵向分析HCRU显示全球维修率,同时在成人和儿童哮喘控制T停止(表4和5,图2,补充附录S6)。值得注意的是,商务用户在成人T的比率停止在停药后2年,分别为20.0%和33.3%;在孩子们,分别为20.2%和24.6%。OCS意味着成人每日剂量分别为2.5±1.2 mg·−1在T停止和4.3±3.5毫克−1在2年。最后,为哮喘住院率2年1.3%的成年人和0.6%的儿童(与之前没有T停止)。
主要剂量口服皮质类固醇(OCS)和吸入激素(ICS)从安排报销医疗保险,患者接触omalizumab,每时间序列从今年前omalizumab中止(T停止2年后T停止
HCRU T之前停止在不受控制的哮喘患儿T停止也低于前T0整个群孩子omalizumab发起,大大为哮喘住院治疗上(分别为33.7%和18.4%,T0和T停止)和药物使用,除了ICS每日剂量(表2 - 5)。在成年人不受控制的哮喘患者T停止之前,尽管药物使用T停止与之前相比,T0在整体人群中,较低的哮喘住院率(17.2%之前,T0前的15.9% T停止)。的纵向分析HCRU停药后2年还显示全球利率维护控制哮喘患者T停止(表4和5,图2,补充附录S6)。
在死亡率方面,2.8%的成年人在控制哮喘T停止(n = 51)在后续去世与6.7%的成年人不受控制的哮喘患者T停止(n = 398)。35的51人死亡在成人哮喘控制T停止住院期间发生(68.6%)与240 398人死亡在成年人不受控制的哮喘患者T停止(60.3%)。没有一个35人住院,导致死亡是由于成人哮喘控制哮喘患者T停止,240人住院,导致死亡的成年人不受控制的哮喘患者T停止是哮喘住院治疗上(4.2%)。没有死在随访中确定控制哮喘患儿T停止,而六死亡发生在不受控制的哮喘患儿T停止(0.9%),其中包括四名住院期间,其中一个是由于哮喘。
讨论
我们的研究是第一个描述omalizumab实际接触模式在两个成人(n = 750)和儿童(n = 2453),基于snd数据库,> 10年的随访。这群哮喘患者中描述代表了有史以来最大的文学。snd数据库涵盖了几乎所有哮喘患者在法国,确保一个全面客观的评估。这个真实的研究侧重于omalizumab暴露和长期停用,停药后和哮喘控制提供信息持久化。最后,它描述了变化HCRU omalizumab患者和患者停止omalizumab,之前和之后的启动和停止,专注于医疗资源与哮喘相关包括药物治疗和住院治疗上视为代理的影响和好处。
Omalizumab曝光模式和HCRU期间曝光
在我们的人口中,大约有一半的成年人和儿童(分别为49%和44%)至少有一个omalizumab长期停用,平均处理持久性中止前4.5年(51个月成人和54个月孩子)。大多数患者附着:88%的成年人和89%的儿童有一个MPR > 80%。超过三分之二的患者(66%的成年人和78%的儿童)继续omalizumab治疗2年,超过三分之一仍omalizumab治疗6年(40%的成年人和31%的儿童)。很少有患者(< 5%)超过一个接触omalizumab序列。
其他真实的研究最近也检查omalizumab暴露在当前实践模式(3,5,6,11,12,27- - - - - -29日]。两种定义进行了使用数据库和报销的医疗保健支出omalizumab中止差距使用≥90天(11,12]。然而,与这些研究是不可能的,因为我们的研究是第一个定义长期停止使用≥1年而不是作为一个缺口≥90天,这样长期停用更可能是故意的。
我们捕获HCRU真实omalizumab启动之前和之后。除了护理,这可能反映了omalizumab管理访问,我们观察到减少评估HCRU omalizumab启动后,随着时间的推移,在成人和儿童。尤其明显为哮喘住院治疗上(在2年减少75%)和口服避孕药使用的使用数量减少(30%)以及成年人每日剂量的减少(20%),与文献[30.]。HCRU这相当大的减少可能是由于直接和间接omalizumab有益的影响,包括在反应者更好的哮喘控制。
哮喘控制和HCRU病人omalizumab停止
几个临床试验(31日- - - - - -33和小的现实研究27- - - - - -29日)表明,omalizumab减少哮喘发作的发病率。最近的一项随机、双盲、安慰剂对照的临床试验(XPORT)也评估了持久性omalizumab利益相比,成人哮喘患者长期omalizumab退出治疗患者持续omalizumab超过一年随访期间(34]。这些结果表明,病人追求omalizumab显著改善哮喘控制:67%的患者持续治疗没有恶化与48%的人停止(或0.45,95%可信区间0.24 - -0.83)。然而,作者强调了较大比例的患者在不加重中止的手臂,这表明omalizumab停药可能是一个安全的选择在治疗哮喘病人的一个子集。
我们的研究是第一个真实的报告,评估哮喘控制在停药,停药后和持久性的控制,在一个大的7761名成年人和1082名儿童在3年随访期。成年人控制哮喘患者在停药,70%,39%和24%仍控制和没有恢复omalizumab 1,分别为2和3年前中止。虽然这些哮喘控制的利率仅基于HCRU,他们确认的大部分患者仍控制omalizumab停用后1年,符合XPORT试验结果,还2和3年。值得注意的是,患者停止omalizumab治疗在哮喘控制有更少的标记不受控制的哮喘和吉娜4 - 5步治疗omalizumab启动之前,与整个群体相比,表明这些病人那么严重哮喘omalizumab启动。
的比较HCRU omalizumab前6个月期间中止与之前启动提供了三个主要发现:1)为成人和儿童哮喘控制停止,所有的速度研究HCRU年底曝光减少;2)减少HCRU也观察到儿童不受控制的哮喘患者在停药,与大量减少哮喘住院治疗上;和3)成年人不受控制的哮喘患者在停药率略高HCRU年底omalizumab暴露的研究药物,除了对哮喘患者住院的比例。这些结果可能反映了不同程度的对治疗的反应,有些不受控制的哮喘患者在停药可能部分反应或药品逃跑。最后,停药后HCRU水平维持在2年随访,在成人和儿童,不管哮喘控制omalizumab中止。稳定HCRU停药后可能反映了一个潜在的omalizumab对哮喘的影响自然历史教育,改变生活方式和更好的医疗随访与起始的生物有关。
主要结果在儿童与成人不同
一些临床试验显示的好处omalizumab疗法在儿童严重过敏性哮喘(30.]。我们的研究包括有史以来最大的儿科队列研究(2453名儿童),均衡比例的学龄儿童(11岁)和青少年。结果突出一些重要特性对幼年时期哮喘和HCRU的负担。与成年人相比,更多的孩子有哮喘住院相关omalizumab之前启动(37%与17%)。这反映出更严重的哮喘或儿童更有可能为严重哮喘住院管理。然而,严重发作住院是这个群体的主要特征(3,5,6]。最后,孩子们也会有一个稍长的治疗停药(中位数53.7之前持久性与在我们的研究51.2个月)。
我们估计,31%的儿童会追求omalizumab治疗开始后6年。最近,回顾锚的研究发现,21%的484名儿童发起omalizumab治疗6年(3]。作者记录发作减少86%和85%的大一课程在治疗的第一年。我们大现实研究证实,扩展了这些数据,降低77%住院治疗上减少哮喘和32%患者在口服避孕药omalizumab启动后2年。
Deschildre等。(4]发表的第一个大型现实研究评估儿童治疗停药。治疗停止了治疗医生因为稳定的良好控制在35 100名儿童(6 - 18岁)有严重的过敏哮喘(治疗持续时间25 - 72个月)。其中8个恢复omalizumab治疗哮喘恶化。一个嵌套病例对照研究报道omalizumab停用之间无显著差异(n = 30)与维修(n = 30)哮喘发作或哮喘控制的速度,与成年人的研究中观察到的结果。我们目前的研究表明,与成年人相比,更多的孩子与控制哮喘停止omalizumab保持控制和没有简历omalizumab治疗1、2和3年后停止(分别为76%、44%和33%的儿童和70%,39%和24%的成年人)。
限制
研究局限性主要源于报销医疗支出数据的使用。哮喘特点和并发症被确定通过映射算法可能导致选择和测量偏差。更具体地说,只有67%的成年人和46%的儿童被发现以前使用过吉娜步骤4 - 5 T0,就导致了这一假设可能被低估了。相同的假设可以使哮喘控制算法:使用吉娜定义为不受控制的哮喘(24),经常恶化哮喘、标准与口服避孕药使用和住院治疗上和糟糕的症状控制已经接近通过使用短效β2肾上腺素能受体激动剂。值得注意的是,大多数算法已经在先前的研究中使用;虽然这并不能保证其有效性,并确保他们的设计和优化与临床医生和专家讨论后的snd数据库和评论者。另一个限制是,测量omalizumab暴露是仅仅基于其豁免;这是减轻的事实,在大多数情况下,omalizumab注射的是医疗专业人员。然而,评估暴露于解剖R03化学类药物治疗(阻塞性气道疾病的药物)和口服避孕药受到测量偏差,鉴于哮喘病人依从性问题(35,36]。此外,最近年的曝光模式会影响可用性的新型生物制剂治疗严重的嗜酸性哮喘。Mepolizumab是第一个在法国从2015年6月在一个富有同情心的项目(“临时授权使用”)在商业化之前(2018年2月37]。最后,由于源数据的性质,omalizumab停用的确切原因仍不明。
结论
这项研究中,基于法国医疗数据库系统(snd),代表最大的omalizumab报告真实的使用几乎彻底治疗哮喘病人的人口在法国,包括数据从19岁203例和覆盖> 10年的随访。我们发现一个类似的中位数omalizumab治疗前4.5年长期停用的持久性成人和儿童。HCRU与哮喘有关,特别是人住院,口服避孕药的使用,减少在omalizumab曝光,而HCRU测量在治疗开始之前,在成人和儿童。此外,在患者停止omalizumab哮喘控制的时候,我们确认的大部分患者持续哮喘控制停药后1年在现实生活中,与以前公布的结果,而且2和3年。最后,我们显示出低的长期维护HCRU在成人和儿童停止omalizumab哮喘控制的时候,尤其是使用口服避孕药和哮喘住院治疗上。
补充材料
补充材料
请注意:补充材料并不是由编辑部,编辑和上传已由作者提供。
附录1:研究设计erj - 03130 - 2021. - appendix_1
附录2:并存状况主要映射算法用于识别和评估哮喘特征erj - 03130 - 2021. - appendix_2
附录3:调整omalizumab曝光erj - 03130 - 2021. - appendix_3
附录4:时间先omalizumab长期停用erj - 03130 - 2021. - appendix_4
附录5:哮喘特征omalizumab启动(T0)和中止(T停止)患者omalizumab停止erj - 03130 - 2021. - appendix_5
附录6:纵向演化HCRU omalizumab停用后在2年随访erj - 03130 - 2021. - appendix_6
可共享的PDF
确认
作者要感谢莎拉Guillemin从相关的(法国里昂)为她宝贵的意见和建议来提高论文的质量。
脚注
作者的贡献:所有作者的构思和设计研究。a . Rigault和a . Lajoinie执行统计分析。答:Lajoinie写的第一个版本的手稿。所有作者评论结果和导致了手稿。
利益冲突:这项研究是在诺华的支持下,研究数据控制器。d . Kamar和c Thonnelier是诺华公司的员工。诺华公司参与了研究设计、数据分析,决定发表和准备的手稿。d . Kamar另外报告咨询费和支持参加会议从Ividata生命科学为诺华提供服务。a . Lajoinie和a . Rigault是相关的员工。相关研究但没有基金负责设计和执行研究数据处理器。答:Rigault是法国医疗保险的员工,直到2020年9月1日。m·亨伯特布,c .身材Deschildre和m . Molimard收到酬金支付的诺华作为独立的科学研究委员会成员。m·亨伯特也报道从阿斯利康咨询费,基耶西,葛兰素史克,诺华公司和赛诺菲;演讲酬金从阿斯利康、葛兰素史克、诺华赛诺菲; outside the submitted work. A. Bourdin and C. Taillé also report lecture honoraria from AstraZeneca, Chiesi, GSK, Novartis and Sanofi; outside the submitted work. A. Deschildre also reports grants from Fondation du Souffle; Conseil Régional Hauts-de-France program 2014–2018 (grant ARCiR 2015-284); consulting fees from Novartis, ALK, GSK, Sanofi, Regeneron, Aimmune Therapeutics, DBV Technologies, Nestlé Health Science and Stallergenes Greer; lecture honoraria from Novartis, ALK, GSK, Sanofi, Aimmune Therapeutics, DBV Technologies, Nestlé Health Science and Boehringer Ingelheim; support for attending congresses from ALK, Sanofi, Boehringer Ingelheim, Stallergenes Greer, Novartis, AstraZeneca, Meda, DBV Technologies, Aimmune and Nutricia; acted on the Data Safety Monitoring Board (DSMB) for the BOOM study (ClinicalTrials.gov标识符:NCT04045301;首席研究员:菲利普开始,蒙特利尔,QC,加拿大);在提交工作。m . Molimard也报道从诺华和Stallergenes咨询费;参与Banook顾问委员会;在提交工作。
支持声明:这项工作是由诺华制药公司。资金信息,本文已沉积的Crossref资助者注册表。
- 收到了2021年12月10日。
- 接受2022年4月26日。
- 版权©2022年作者。
这个版本分布在创作共用署名非商业性许可证的条款4.0。商业生殖权利和权限接触权限在}{ersnet.org