文摘
背景:白介素6 (IL) trans-signalling (IL-6TS)正成为一个在慢性呼吸道疾病发病机理;然而,司机的IL-6TS航空和增加患者的表型特征IL-6TS途径激活仍然知之甚少。
摘要目的:我们的目的是识别和描述慢性阻塞性肺病患者增加气道IL-6TS并阐明生物司机IL-6TS途径激活。
方法:我们使用了一个IL-6TS-specific痰生物标志物概要(可溶性白介素受体(sIL-6R)、il - 6, IL-1β,引发,巨噬细胞炎性protein-1β)从COPD患者痰分层数据(n = 74;生物标记目标抗生素和系统性皮质类固醇治疗COPD恶化(BEAT-COPD))通过分层聚类。IL-6TS签名与临床特点和唾液微生物组配置文件。中性粒细胞胞外陷阱形成的诱导和IL-6TS (NETosis)流感嗜血杆菌研究了在人类中性粒细胞。
结果:层次聚类显示IL-6TS-high子集(n = 24)慢性阻塞性肺病的患者,与一个共同的表型性状IL-6TS-high子集之前发现哮喘。子集的特征是增加痰细胞计数(p = 0.0001),持续的痰液嗜中性(p = 0.0004),减少生活质量(慢性呼吸道问卷总分;p = 0.008),提高水平的促炎介质和基质金属蛋白酶的痰。IL-6TS-high COPD患者显示变形菌门的增加,嗜血杆菌作为主导的属。NETosis引起的流感嗜血杆菌被确认为一个潜在的机制增加sIL-6R水平。这是支持sIL-6R之间显著正相关,NETosis标记在支气管肺泡灌洗液从慢性阻塞性肺病患者。
结论:由于慢性殖民IL-6TS途径激活嗜血杆菌可能是一个重要疾病司机在慢性阻塞性肺病患者的一个子集。
文摘
肺白介素trans-signalling驱动流感嗜血杆菌全身NETosis是慢性阻塞性肺病患者慢性的病理特征嗜血杆菌中性粒细胞炎症感染,稳定和不受控制的疾病https://bit.ly/30vhgD5
介绍
慢性阻塞性肺病是一种异质性疾病,一种改进的理解分子表型的特点是特异性炎症途径可以帮助定义子集的慢性阻塞性肺病和指导靶向治疗(1]。白介素(IL) 6-trans信号(IL-6TS)途径是与慢性阻塞性肺病的病理生理学,包括肺气肿,肺纤维化,epithelial-to-mesenchymal过渡,增加上皮通透性和toll样受体(TLR)端依赖炎症反应2- - - - - -6]。分层的COPD患者基于IL-6TS-associated炎症可能使COPD病人的识别子集,受益于治疗针对IL-6TS。
IL-6TS通路激活细胞的能力,通常不会对il - 6的由于低表达il - 6受体(IL-6R),包括支气管上皮细胞和气管平滑肌细胞(2,7]。在这些细胞,途径激活是通过交互的可溶性白介素受体(sIL-6R) / il - 6与广泛表达复杂signal-transducing元素的细胞因子il - 6的家人,gp130 [8]。IL-6TS导致磷酸化统计家族转录因子(STAT3和/或STAT1)由Janus酪氨酸激酶家族(JAK1, JAK2 TYK2),而且也会使活化增殖作用的蛋白激酶,磷酸肌醇3-kinase和机械的雷帕霉素靶(mTOR)信号级联3,9]。几项研究提供证据表明IL-6TS可能活跃在肺癌和慢性阻塞性肺病的病理。例如,更高水平的sIL-6R被发现在COPD患者的痰而健康的吸烟者(10)和il - 6水平的提高,航空公司与慢性阻塞性肺病严重程度有关,急性加重,气道阻塞11,12]。此外,增加人类气性sIL-6R和il - 6水平与mTORC1通路hyperactivation肺组织显示正相关(3),STAT3和STAT1磷酸化是增加了与不吸烟者相比,慢性阻塞性肺病患者的肺组织(13]。
虽然sIL-6R可以被释放后IL-6R mRNA的可变剪接,大多数循环生成sIL-6R ADAM10和ADAM17-mediated脱落的膜结合IL-6R (mIL-6R) [14,15]。在当地网站的炎症,中性粒细胞已经被提议作为sIL-6R[的主要来源16],最近的一项研究表明,中性粒细胞的可能是一个重要来源sIL-6R肺部的慢性呼吸道疾病患者(17]。然而,病理生理过程,导致肺mIL-6R脱落在很大程度上仍未知。
在最近的一项研究中,我们使用聚类分析肺上皮细胞的转录组和痰液蛋白质组学数据强调协会IL-6TS-specific基因(TNFAIP6,PDE4B,IL1R2,S100A9,S100A8,S100A12,CHI3L1和SPP1)和蛋白质(sIL-6R il - 6,巨噬细胞炎性蛋白(MIP) 1β,IL-1β,引发,YKL-40和基质金属蛋白酶(MMP) 3)签名,与不同的哮喘患者表型(2]。这些签名在哮喘患者发作频繁,增加血液嗜酸性粒细胞,粘膜下浸润的t细胞和巨噬细胞,它没有重叠系统性炎症。痰sIL-6R和il - 6水平与标记相关的先天免疫激活,气道重构和增加痰中性粒细胞(2]。
基于IL-6TS sIL-6R水平和激活的增加下游通路在COPD患者中,我们假定IL-6TS-related签名中发现哮喘会增加慢性阻塞性肺病患者的一个子集。我们的目的是探讨这种慢性阻塞性肺病病人子集的存在,描述其临床特点和阐明IL-6TS的致病因素在慢性阻塞性肺病。为此,multi-omics数据的生物信息学分析从四个单独的COPD组与相关的补充在体外实验模型(图1)。
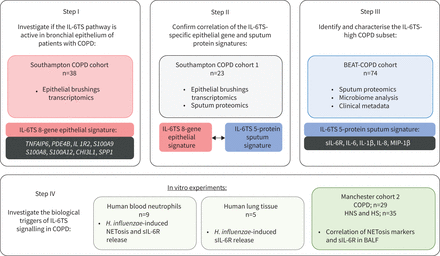
研究流程图。IL-6TS:白介素(IL) 6 trans-signalling;BEAT-COPD:生物标记目标抗生素和系统性皮质类固醇治疗COPD恶化;流感嗜血杆菌:流感嗜血杆菌;NETosis:中性粒细胞胞外陷阱的形成;接下来:健康不吸烟;海关:健康的吸烟者;BALF:支气管肺泡灌洗液。
材料和方法
详细描述的患者群,可以找到的材料和方法补充材料。
病人群
患者表现型是基于生物信息学分析上皮刷转录组数据和痰或支气管肺泡灌洗液(BALF)蛋白质组学数据从四个不同的组:南安普顿队列(COPD患者中,38例)18];生物标记目标抗生素和系统性皮质类固醇治疗慢性阻塞性肺病急性加重(BEAT-COPD) (COPD患者中,n = 74)19];曼彻斯特群1 (COPD患者中,n = 23) [20.];和曼彻斯特队列2 (COPD患者中,n = 29;健康不吸烟和健康的吸烟者,n = 35) (21]。
测量在痰
BEAT-COPD痰样本分析细菌(使用标准的常规文化)和加工生产cytospins细胞分析和浮在表面的流体相测量。大面板的血清和唾液生物标志物测定使用Meso-Scale-Discovery和单一ELISA在稳定和恶化的访问19]。从痰标本细菌基因组DNA提取和16 s rRNA基因测序进行如前所述[22,23和总结补充材料。
无人监督的层次聚类
层次聚类的基因表达数据和痰液蛋白质组数据都使用了平均链接和欧几里得度量方法,对每个变量正常化是0和方差1,使用Qlucore组学Explorer 3 (Qlucore,隆德,瑞典)。结果视觉系统树图热图的色标对应于一个范围从−2.0(蓝色),通过0.0(灰色)+ 2.0(红色)。
NETosis
人类血液中性粒细胞被处理流感嗜血杆菌3 h或4µM ionomycin氯化钙(CaCl和2毫米2)1 h。相关的细胞外DNA NETosis测量通过增加细胞不透水SYTOX绿色核酸染色(ThermoFisher科学)时中性粒细胞文化生活流感嗜血杆菌或ionomycin / CaCl2挑战。评估NETosis citrullinated表达式的组蛋白H3 (H3cit)免疫荧光染色的细胞被固定和分析。sIL-6R水平测量使用人类IL-6RαQuantikine酶联免疫试剂盒(研发)。
测量BALF中
代孕的水平NETosis标记和sIL-6R BALF中分析了慢性阻塞性肺病患者和健康志愿者从曼彻斯特队列2。(cf)游离DNA测量使用PicoGreen Quant-It化验(表达载体P7589)。髓过氧化酶(MPO)和sIL-6R水平测量使用人类髓过氧物酶工具包(MSD K151EEC)和IL-6RαQuantikine酶联免疫试剂盒,分别。
统计分析
基因表达和痰生物标志物数据日志2转换和使用基于一般线性模型的统计检验分析,调整了年龄和性别,使用Qlucore组学Explorer 3.3。Benjamini-Hochberg多个校正用于基因表达数据为误报率控制(称为核反应能量)。统计分析临床变量与克鲁斯卡尔-沃利斯和生物标志物数据进行测试,Mann-Whitney测试或卡方测试。比例的细菌被认为不是正态分布,并分析了Mann-Whitney测试。的统计分析在体外数据进行使用单向方差分析(图基的多个比较)和t。除了所有数据分析基因表达数据的分析被认为是基于假设和意义达到如果p≤0.05 (q)基因表达数据。Prism 6.0 (GraphPad软件)是用于数据分析和图形表示。
结果
支气管上皮的IL-6TS-specific基因签名定义了一个子集的COPD患者增加先天炎症的标志物
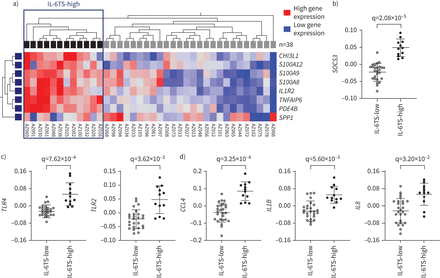
我们先前描述IL-6TS八个基因签名(TNFAIP6,PDE4B,IL1R2,S100A9,S100A8,S100A12,CHI3L1和SPP1),主要来源于IL-6TS-stimulated人类支气管上皮细胞(2)是用于调查IL-6TS通路是否活跃在COPD患者的支气管上皮细胞(南安普顿队列;n = 38) [18]。层次聚类识别病人的一个子集(IL-6TS-high, n = 12, 31.6%)的增加表达IL-6TS八个基因上皮签名(图2一个)。IL-6TS-high子集显示明显的表达增加SOCS3,主要STAT3-inducible基因(24),连接子集和JAK / STAT3通路激活(图2 b)。此外,IL-6TS-high病人显示TLR基因与其他基因的表达增加与天生的炎症,包括亚兰,IL1B和IL8(图1 c和d)。这个IL-6TS相关支气管上皮基因表达谱支持MIP-1β(亚兰),IL-1β和引发,连同途径触发il - 6和sIL-6R IL-6TS通路激活的蛋白质生物标记物在COPD患者中,这被称为“IL-6TS five-protein痰签名”。温和,但显著正相关(r = 0.49;p = 0.017)之间的IL-6TS八个基因上皮签名和IL-6TS five-protein痰签名确认额外的COPD组(曼彻斯特队列1;n = 23) (20.]成对支气管上皮刷和痰液样本(补充图S1)。
集群基于白介素(IL)的慢性阻塞性肺病患者6 trans-signalling (IL-6TS)八个基因上皮在南安普顿群签名。一)分层聚类通过使用IL-6TS八个基因上皮签名(TNFAIP6,PDE4B,IL1R2,S100A9,S100A8,S100A12,CHI3L1和SPP1)。增加患者的子集IL-6TS八个基因上皮签名(IL-6TS-high)突出显示。罪犯)之间的基因差异表达IL-6TS-high (n = 12)和IL-6TS-low (n = 26)患者。正常化和zero-centred基因表达值显示。Benjamini-Hochberg测试是用于q值。线表示意味着±sd。
IL-6TS five-protein痰签名il - 6、sIL-6 MIP-1β,引发和IL-1β标识一个中性的子集COPD患者控制不佳
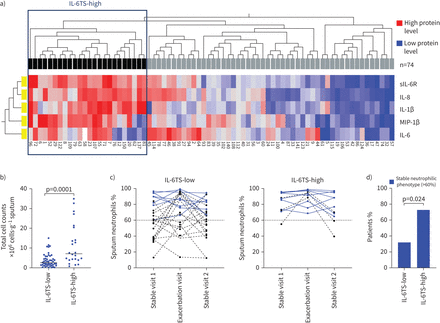
进一步探索在慢性阻塞性肺病IL-6TS通路的作用,我们研究了存在IL-6TS-associated表型BEAT-COPD队列(n = 74),临床特征明显队列唾液蛋白质组学和微生物数据(19]。分层的患者根据IL-6TS five-protein痰签名确认IL-6TS-high子集的大小(n = 24日32.4%)相似到南安普顿的一群(图3一)。没有明显差异在年龄、性别、吸烟状况、pack-year历史,身体质量指数,发作频率、皮质类固醇剂量或肺功能IL-6TS-high和低BEAT-COPD子集(表1)。然而,IL-6TS-high子集展出的增加总痰细胞计数(p = 0.0001;图2和3 b)和中性粒细胞比例显著增加(p = 0.0004)和提高水平的促炎介质和痰中基质金属蛋白酶(表1)。值得注意的是,IL-6TS-high病人子集是降低生活质量评估慢性呼吸道问卷(CRQ;总分13.64±0.98比16.72±0.63 IL-6TS-low子集;p = 0.008),显著降低分数掌握(p = 0.021)和疲劳(p = 0.049;表1)。IL-6TS-low患者相比,大多数IL-6TS-high病人保持了独特的中性表型痰中性粒细胞(> 60%)观察到基线访问恶化和6周post-exacerbation (图3 c和d)。
集群的COPD患者基于白介素(IL) 6 trans-signalling (IL-6TS) five-protein痰的签名BEAT-COPD(生物标记目标抗生素和系统性皮质类固醇治疗COPD恶化)队列和协会痰中性粒细胞。一)分层聚类通过使用IL-6TS five-protein痰签名(il - 6、可溶性il - 6,巨噬细胞炎症蛋白(MIP) 1β,引发和IL-1β)。高蛋白质含量是用红色和蓝色的低水平。增加患者的子集IL-6TS蛋白质签名(IL-6TS-high)突出显示。b)总细胞数的痰IL-6TS-high (n = 24)比较慢性阻塞性肺病患者的休息(IL-6TS-low;n = 50)。克鲁斯卡尔-沃利斯测试是用于假定值。c)的痰中性粒细胞比例(IL-6TS-high n = 11, IL-6TS-low n = 25)在基线访问(稳定访问1),恶化(恶化访问),6周post-exacerbation(稳定访问2)。虚线代表一个中性的下限表型痰中性粒细胞(> 60%)。患者维持一个稳定的中性表型,即。> 60%的痰中性粒细胞在所有三个访问,用蓝色突出显示。d)的患者比例稳定的中性表型。卡方测试是用于假定值。
慢性阻塞性肺病IL-6TS-high子集的特点是感染嗜血杆菌
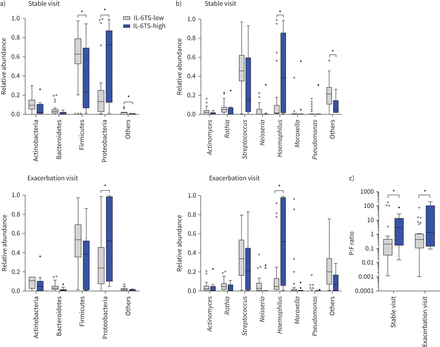
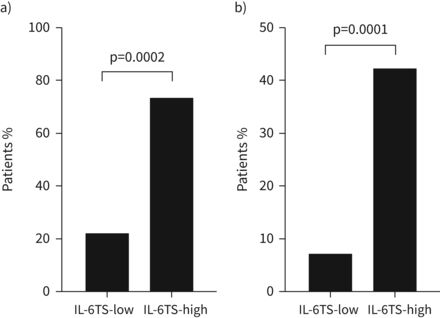
患者的痰液微生物BEAT-COPD队列是由16 s rRNA评估基因测序在稳定状态和急性加重(n = 39)。比较IL-6TS子集之间的微生物资料显示显著降低门壁厚菌门的相对丰度,增加了大量的变形菌门,嗜血杆菌最代表属IL-6TS-high子集在稳定状态(图4一和b)。一个相对大量的变形菌门和显著增加嗜血杆菌(图4一和b)和增加变形菌门:厚壁菌门(P: F)比例比(图4 c)保持在IL-6TS-high发作的病人。患者的百分比保持较高的相对比例(即。变形菌门和> 0.4)嗜血杆菌在两个访问中显著增加IL-6TS-high子集(补充图S2)。分析细菌生长的痰样本显示,更多IL-6TS-high子集(73.7%的病人与22.5%;p = 0.0002;图5一个病原微生物)是积极的(流感嗜血杆菌,莫拉克斯氏菌属复活,链球菌引起的肺炎,金黄色葡萄球菌和铜绿假单胞菌),尤其是流感嗜血杆菌(42.1%与7.5%;p = 0.001;图5 b)。
白介素6 (IL)的痰细菌分析trans-signalling (IL-6TS) -病人BEAT-COPD(生物标记目标抗生素和系统性皮质类固醇治疗COPD恶化)队列。相对含量最丰富的痰细菌类群和b)在临床疾病稳定,属恶化(IL-6TS-high n = 11, IL-6TS-low n = 28)。c)变形菌门:厚壁菌门(P: F)的比例比在稳定和恶化的访问。提出了数据图基的箱线图。*:p < 0.05 (Mann-Whitney)。
痰细菌生长的白介素(IL) 6 trans-signalling (IL-6TS) -病人BEAT-COPD(生物标记目标抗生素和系统性皮质类固醇治疗COPD恶化)队列。比例的患者(IL-6TS-high n = 19日IL-6TS-low n = 39)的显著增长)病原微生物(流感嗜血杆菌,莫拉克斯氏菌属复活,链球菌引起的肺炎,金黄色葡萄球菌和铜绿假单胞菌)和b)流感嗜血杆菌根据英国健康保护局评估标准操作程序。卡方测试是用于假定值。
流感嗜血杆菌全身NETosis导致sIL-6R人类中性粒细胞释放的主要
NETosis是一个过程,即中性粒细胞释放染色质细丝涂citrullinated组蛋白和抗菌蛋白以陷阱和杀死细菌25,26]。中性粒细胞胞外陷阱(网)曾被观察到在COPD患者感染的航空公司嗜血杆菌物种(27]。慢性阻塞性肺病IL-6TS-high子集的协会与持续的肺嗜中性和殖民流感嗜血杆菌建议NETosis引起的流感嗜血杆菌可能是一个司机sIL-6R释放的主要人类中性粒细胞。Citrullination组蛋白的酶肽基精氨酸deiminase (PAD) NETosis[4是一个要求28,29日),我们使用了一种新型小分子PAD4-inhibitor (PAD4i),由阿斯利康和描述的补充的方法和补充图S3专门阻止NETosis)。流感嗜血杆菌有效地诱导NETosis新鲜人体血液中性粒细胞,如图所示,增加细胞外H3cit的DNA和表达的积累,一个特征的标志PAD4-dependent净形成(25,26,30.),而这些过程被有效地抑制PAD4i (图6和b)。增加表达的细胞外H3cit colocalisation和细胞外DNA积极网被证实流感嗜血杆菌来华的中性粒细胞(图6 c)。Ionomycin,已知的和广泛使用的NETosis诱导物,作为一个积极的控制(25]。感应的NETosis流感嗜血杆菌一直与sIL-6R释放不同嗜中性粒细胞增加有关捐助者(n = 9;图6 d)。阻塞NETosis PAD4i显著降低sIL-6R的水平(图6 e)。一个潜在的殖民之间的功能联系流感嗜血杆菌和增加sIL-6R释放在肺部被确认的新人类的肺组织感染流感嗜血杆菌(补充图S4)。感染流感嗜血杆菌导致显著增加sIL-6R在周围介质。最高水平的细菌浓度诱导sIL-6R捐助者之间的不同,和sIL-6R的水平达到峰值后下降,可能由于过度引起的蛋白水解活性更高的细菌负荷。
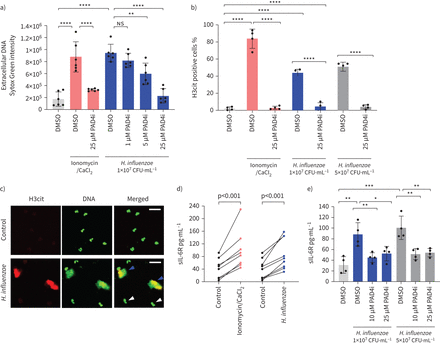
增加释放可溶性白细胞介素- 6受体(sIL-6R)在人类中性粒细胞流感嗜血杆菌全身的嗜中性粒细胞胞外陷阱(净)形成(NETosis)。新鲜的人类血液中性粒细胞被感染流感嗜血杆菌或刺激ionomycin /氯化钙(CaCl2)和细胞外积累的DNA分析,表达citrullinated H3 (H3cit),净sIL-6R形成和释放的。肽基精氨酸deiminase抑制剂(PAD4i)被用来专门阻止NETosis。a)的积累细胞外DNA(6捐助者)和b) H3cit-positive细胞的百分比(四个捐助者)进行分析。* *:p < 0.01, * * * *: p < 0.0001(单向方差分析)。c)代表H3cit和DNA-positive网的图片流感嗜血杆菌来华的细胞(蓝色箭头)和完整的中性粒细胞(白色箭头)。酒吧= 25μm规模。sIL-6R d)释放到周围介质与ionomycin / CaCl刺激后2和流感嗜血杆菌(1×108CFU·毫升1),分别(九个捐助者)。假定值采用配对t检验。e) sIL-6R释放显著抑制PAD4i(四个捐助者)。* *:*:p < 0.05, p < 0.01, * * *: p < 0.001(单向方差分析)。ns:不重要的;DMSO:二甲亚砜。
的水平sIL-6R积极与代理NETosis标记BALF中慢性阻塞性肺病患者
代理NETosis标记的水平,包括cfDNA和BALF中MPO增加慢性阻塞性肺病患者(n = 29;罕见的exacerbators n = 16和频繁exacerbators n = 13)相比,健康志愿者(n = 35;健康不吸烟者n = 27和健康吸烟者从曼彻斯特队列2 (n = 8)图7),而sIL-6R没有明显不同的两组(补充图S5)。cfDNA和MPO显著增加在慢性阻塞性肺病患者高水平的sIL-6R(上四分位数;> 165 pg·毫升1),而患者低sIL-6R(下四分位数;< 84 pg·毫升1)(图7 b)。此外,sIL-6R的水平与cfDNA呈正相关(r = 0.67;p < 0.0001)和MPO (r = 0.66;p = 0.0001) (图7 c)。一个近乎完美的相关性显示cfDNA和MPO (r = 0.99;p < 0.0001),表明我们是检测cfDNA-MPO复合物特定网络组件。这个观察加强了我们假设sIL-6R释放是一个NETosis-driven过程。sIL-6R cfDNA和MPO的正相关性是更加突出在慢性阻塞性肺病患者频繁发作患者罕见的急性加重(补充图S5)。
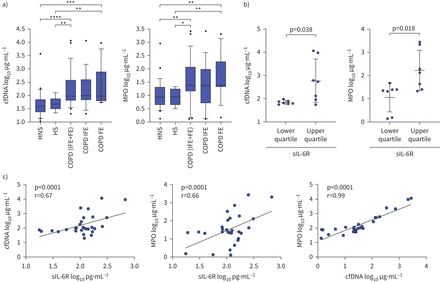
可溶性白细胞介素- 6受体(sIL-6R)和代理的相关性中性粒细胞胞外陷阱(净)形成(NETosis)标记在支气管肺泡灌洗液(BALF)慢性阻塞性肺病患者。)代理NETosis标记的水平,包括游离DNA (cfDNA)和髓过氧化酶(MPO)分析了在慢性阻塞性肺病患者BALF(罕见exacerbators(人生)n = 16,频繁exacerbators (FE) n = 13)相比,健康志愿者(健康的不吸烟者(hn) n = 27日健康吸烟者(HS) n = 8)从曼彻斯特队列2。数据提出了十箱线图,第90个百分位。b)代理NETosis标记增加的水平在慢性阻塞性肺病患者(机上娱乐系统+铁)高水平的BALF sIL-6R(上四分位数;> 165 pg·毫升1)相比,低水平的sIL-6R(下四分位数;< 84 pg·毫升1)。* *:*:p < 0.05, p < 0.01, * * *: p < 0.001, * * * *: p < 0.0001 (Mann-Whitney)。c)的相关性BALF sIL-6R, cfDNA和MPO COPD患者(机上娱乐系统+铁;n = 29)使用皮尔逊相关性测试检查。线代表一个线性回归健康。
讨论
虽然有一个IL-6TS之间建立联系和慢性阻塞性肺病的病理生理学2- - - - - -6),所知甚少的病理司机IL-6TS航空和慢性阻塞性肺病患者的表型特征增加IL-6TS途径激活。我们表明,增加IL-6TS-related生物标志物的表达与持续的中性气道炎症和感染变形菌门由属嗜血杆菌在慢性阻塞性肺病患者。此外,我们提供的证据之间的直接连接感染的肺部组织流感嗜血杆菌和增加sIL-6R的释放。与先前的研究一致(17),我们发现中性粒细胞代表sIL-6R的来源,我们表明,sIL-6R在中性粒细胞释放流感嗜血杆菌全身NETosis。提供新的见解COPD的异质性,通过识别一个新病人特征子集IL-6TS和阐明潜在的病理机制,将赋予特定的治疗和精密医学未来发展的方法。
在最近的研究中我们发现了一个IL-6TS八个基因上皮签名(TNFAIP6,PDE4B,IL1R2,S100A9,S100A8,S100A12,CHI3L1和SPP1)患者的哮喘和提议,它对应于一组IL-6TS-related痰蛋白质生物标记物,包括il - 6, sIL-6R, MIP-1β,引发,IL-1β,YKL-40 MMP3 [2]。这使我们的识别小说在哮喘、IL-6TS-high子集的特点是肺上皮IL-6TS途径激活显著缺乏系统性的il - 6的炎症。在这项研究中,我们证实IL-6TS之间的正相关关系八个基因和five-protein (il - 6、sIL-6 MIP-1β,引发和IL-1β)签名在同一病人在一个较小的COPD组上皮和痰液样本配对(补充图S1)。这支持的潜力IL-6TS八个基因上皮和five-protein痰签名识别可比IL-6TS-high子集的慢性阻塞性肺病患者。
IL-6TS的八个基因上皮签名是增加的一个子集从南安普顿COPD患者肺上皮刷群。IL-6TS-high COPD患者显示明显高于肺上皮细胞TLR2和TLR4的表达,复制结果IL-6TS-high子集的哮喘、高IL-6TS签名重叠TLR途径激活的增强标记(2]。一些证据显示IL-6TS和TLR通路之间积极的相互作用。IL-6TS已经证明可以增强TLR4-dependent炎症反应通过STAT3和特定的抑制IL-6TS完全保护小鼠免受脂多糖/ TLR4-mediated脓毒性休克(31日]。同样,hyperactivation STAT3基因表达调节TLR2在胃上皮细胞(32]。此外,IL-6TS显著放大TLR配体诱导产生炎症介质(IL-1β、引发、肿瘤坏死因子(TNF) -α,单核细胞化学引诱物蛋白1)由基质和先天免疫细胞(6]。相反,人类单核细胞诱导激活TLR2 IL-6TS通过促进il - 6的分泌和代sIL-6R [33之间),这表明相声IL-6TS / JAK / STAT和TLR通路作为一个更广泛的机制,增强IL-6TS-high表现型的炎症反应的严重程度。
的IL-6TS five-protein痰签名是调节在稳定的慢性阻塞性肺病患者的一个子集BEAT-COPD队列关联增加总痰细胞数量和更高的痰中性粒细胞百分比。重要的是,高水平的痰液il - 6与IL-6TS-high并不一定重叠子集。这意味着IL-6TS子集确定在本研究中明显不同于慢性阻塞性肺病子集将被单独il - 6。IL-6TS-low病人相比,大多数IL-6TS-high患者保持一个稳定的中性表型随着时间的推移,包括在恶化。类似于哮喘,IL-6TS-high子集IL-6TS签名与水平的提高气道重构生物标志物(MMP9 MMP8)和促炎介质(TNF-αMIP-1α),建议类似的分子表型的特点是增加了天生的炎症反应。在哮喘与IL-6TS表型,IL-6TS-high COPD患者没有表现出增加血液嗜酸性粒细胞和没有发作倾向增加,表明可能有不同的临床表现IL-6TS-driven病理学的哮喘和慢性阻塞性肺病。相反,慢性阻塞性肺病IL-6TS-high子集的特征是显著降低生活质量评估的CRQ相比其他的病人。
IL-6TS-high病人的特点是变形菌门的大量增加,特别是属嗜血杆菌,减少壁厚菌门。这个复制了之前的发现,增加变形菌门:厚壁菌门比观察到一群加剧COPD和哮喘患者中性粒细胞炎症和炎性介质增加痰(34]。肺部微生物在我们保持类似的子集构成发病时的临床稳定状态的恶化,这表明微生物在IL-6TS-high子集是纵向稳定并可能参与维护主机的慢性炎症反应,包括IL-6TS。支持这个假说的研究培养人类支气管上皮细胞的纯化内毒素准备孵化流感嗜血杆菌,这表明这些类毒素导致显著增加表达和释放il - 6 (35,36]。此外,流感嗜血杆菌强烈诱导il - 6生产由慢性阻塞性肺病患者肺泡巨噬细胞(37],痰液il - 6水平被发现在慢性阻塞性肺病患者细菌殖民化的航空公司流感嗜血杆菌最常分离出病原体与病人没有细菌殖民化和健康对照组(38]。演示IL-6TS通路和肺之间的直接机械连接殖民流感嗜血杆菌,人类的肺组织外植体感染流感嗜血杆菌,导致增加sIL-6R的释放。一个显著的限制我们的实验模型是一个高interdonor可变性的剂量流感嗜血杆菌引发sIL-6R释放,可能是由于不同细胞成分的检测肺组织(即。不同程度的免疫细胞代表sIL-6R)的主要来源。
人类中性粒细胞mIL-6R高水平表达的表面和被认为是sIL-6R的主要来源,释放炎症反应(17和凋亡刺激39]。在我们目前的研究显示,感染的中性粒细胞流感嗜血杆菌诱导NETosis恰逢sIL-6R释放的增加。在这里,我们使用了一种新型抑制剂能够特别块NETosis针对已知NETosis司机PAD4 [28,29日)确认的角色流感嗜血杆菌全身NETosis sIL-6R释放。NETosis更常见的航空公司中性粒细胞哮喘和慢性阻塞性肺病患者(40,41),与水平的提高有关嗜血杆菌物种(27]。这些发现,连同我们的新数据,建议嗜血杆菌可能是一个主要推动力的气道IL-6TS途径激活通过触发sIL-6R释放过程中中性粒细胞NETosis。重要的是,我们确认的水平sIL-6R积极与代理NETosis标记cfDNA和MPO水平BALF中慢性阻塞性肺病患者。尽管蛋白酶负责NETosis-mediated mIL-6R脱落不显示在这项研究中,主要的蛋白酶活性与网一直归因于中性粒细胞弹性蛋白酶、组织蛋白酶G和蛋白酶3 (42),暗示这些丝氨酸蛋白酶作为可能的候选人。其中,组织蛋白酶G,但不是中性粒细胞弹性蛋白酶或蛋白酶3,曾被证明在网站发布sIL-6R炎症(43]。
我们慢性阻塞性肺病患者表现型依赖患者群重叠蛋白质组学、转录组和微生物组数据。然而,相对较少的患者multi-omics COPD组代表了我们的一个主要限制这一研究中,特别是对于分子表型与临床表现的目的。此外,我们有限的信息并存病可以影响生活质量分数由CRQ评估。需要更大规模的研究深度与COPD患者的临床描述子集IL-6TS增加,中性气道炎症和嗜血杆菌感染。有趣的是,与我们的研究结果一致,大最近的一项研究,涉及253名慢性阻塞性肺病患者建立了变形菌门(主要是之间的联系嗜血杆菌)主导地位和更频繁的发作,用力呼气量下降1年代和死亡率上升44]。
总之,我们表明,慢性IL-6TS持续慢性阻塞性肺病患者中性粒细胞炎症的标志,而且它可能是与放大炎症反应和气道重塑。此外,我们的数据表明流感嗜血杆菌可以通过触发驱动肺部IL-6TS sIL-6R释放过程中中性粒细胞NETosis (图8)。这进一步加强了我们对微生物之间的相互理解,航空公司,打开潜在的新途径新生物标志物的发现和呼吸治疗。
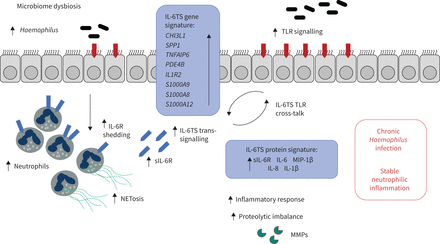
multi-omics识别的概述图白介素(IL) 6 trans-signalling (IL-6TS) -慢性阻塞性肺病患者和潜在的病理子集。TLR: toll样受体;MMP:基质金属蛋白酶。
补充材料
补充材料
请注意:补充材料并不是由编辑部,编辑和上传已由作者提供。
补充图S1。相关上皮刷IL-6TS签名的痰。IL-6TS 8-gene上皮和IL-6TS 5-protein痰签名从COPD患者(n = 23;曼彻斯特队列1)表示的分数计算上皮刷(8 gene-mean: TNFAIP6、PDE4B IL1R2, S100A9, S100A8, S100A12, CHI3L1和SPP1)和痰(5 protein-mean: il - 6、sIL-6R MIP-1β,IL-1β和引发)表达数据。皮尔森相关测试是用于关联IL-6TS签名的分数。参考线显示了理论绝对线性相关。erj - 03312 - 2020. - figure_s1
补充图S2。纵向稳定性的COPD患者的痰液微生物BEAT-COPD队列。痰液的相对比例)变形菌门和b)嗜血杆菌在基线访问(稳定的访问)和恶化(恶化访问)(IL-6TS-high n = 11, IL-6TS-low n = 28)。虚线代表高的相对比例的截止(> 0.4)。患者维持高的相对比例的变形菌门和嗜血杆菌,即。> 0.4在访问,都是用蓝色突出显示。的患者比例高的相对比例在访问都是显示在右边。卡方检验是用于假定值。erj - 03312 - 2020. - figure_s2
补充图S3。PAD4抑制剂(PAD4i)块NETosis人类主要的中性粒细胞。主要中性粒细胞与Ionomycin / CaCl刺激2诱导NETosis。的身份和纯度)证实了中性粒细胞髓过氧化酶(MPO)染色。酒吧25μm规模。b)代表剂量反应曲线PAD4抑制剂(PAD4i)剂量依赖性抑制NETosis量化评估的citrullinated H3 (H3cit)表达式。c)治疗的中性粒细胞10μM PAD4i完全阻塞NETosis,被缺乏细胞H3cit / DNA阳性铝型材(蓝色箭头)。酒吧25μm规模。erj - 03312 - 2020. - figure_s3
补充图S4。释放sIL-6R从新鲜人的肺组织感染流感嗜血杆菌。新鲜的人类肺组织外植体感染流感嗜血杆菌和积累sIL-6R周围的介质进行了分析。剂量反应的浓度流感嗜血杆菌的最高水平,感应sIL-6R(圆圈)。单向方差分析测试是用来计算假定值在每个浓度相比,控制(每毫升0 CFU)分别为每个捐赠者。*:p < 0.05;* *:p < 0.01;* * *:p < 0.001;* * * *:p < 0.0001。b)积累sIL-6R肺移植组织文化感染后从5捐助者流感嗜血杆菌。细菌的浓度诱导sIL-6R最高水平的个人捐赠者所示。假定值采用配对t检验。erj - 03312 - 2020. - figure_s4
补充图S5。sIL-6R的相关性和代理NETosis标记BALF中慢性阻塞性肺病患者频繁exacerbators。a)的水平在慢性阻塞性肺病患者BALF sIL-6R没有不同(罕见exacerbators(人生)n = 16,频繁exacerbators (FE) n = 13)相比,健康志愿者(健康的非吸烟者(hn) n = 27日健康吸烟者(HS) n = 8)从曼彻斯特队列2。数据表示为10 - 90百分位箱线图。b)相关性sIL-6R cfDNA和MPO的慢性阻塞性肺病患者铁和款项被皮尔森相关测试检查。线代表一个线性回归健康。erj - 03312 - 2020. - figure_s5
可共享的PDF
确认
我们感谢所有的肺组织捐助者。我们谢谢Thoraxkliniken的外科医生和护士,卡大学医院和哥德堡大学,瑞典哥德堡肺样本收集。我们感谢学生m . Marande和r . Dolgos(科技学院南希,南希,法国)在肺组织的帮助实验。也特别感谢职业卫生专家k Vesterlund(阿斯利康,哥德堡,瑞典)血液样本收集。我们感谢l·奥伯格p . Konings大肠穆罕默德和n范Zuydam(阿斯利康,哥德堡)为他们的帮助与生物信息学和统计学分析。
脚注
可以从本文的补充材料www.qdcxjkg.com
利益冲突:美国温斯洛是一种员工和分享/阿斯利康的股东。
利益冲突:l . Odqvist是一种员工和分享/阿斯利康的股东。
利益冲突:美国潜水员没有披露。
利益冲突:r·里瑟是一种员工和分享/阿斯利康的股东。
利益冲突:美国Abdillahi是一种员工和分享/阿斯利康的股东。
利益冲突:c . Wingren是一种员工和分享/阿斯利康的股东。
利益冲突:h . Lindmark是一种员工和分享/阿斯利康的股东。
利益冲突:a . 2亩是一种员工和分享/阿斯利康的股东。
利益冲突:美国必是一种员工和分享/阿斯利康的股东。
利益冲突:l . Yrlid是一种员工和分享/阿斯利康的股东。
利益冲突:e . Ax是一种员工和分享/阿斯利康的股东。
利益冲突:r .也有报告个人费用从TEVA和诺华讲座和咨询,个人费用从Synairgen咨询,个人费用从葛兰素史克公司参加会议,在提交工作。
利益冲突:美国bloom是一种员工和分享/阿斯利康的股东。
利益冲突:a .海厄姆没有披露。
利益冲突:d·辛格报告个人费用从阿斯利康,勃林格殷格翰的发言,基耶西,Cipla公司,基因泰克,葛兰素史克,Glenmark, Gossamerbio, Menarini, Mundipharma,诺华,Peptinnovate,辉瑞公司Pulmatrix,治疗先锋,维罗纳,外提交工作。
利益冲突:t Southworth没有披露。
利益冲突:石球Brightling报告个人费用从葛兰素史克,阿斯利康/美,勃林格殷格翰的发言,诺华,罗氏公司和基耶西,在提交工作。
利益冲突:香港奥尔森是一种员工和分享/阿斯利康的股东。
利益冲突:z Jevnikar是阿斯利康的员工和分享/股东。
支持声明:本研究是由阿斯利康。员工从阿斯利康参与研究设计、数据收集、数据分析、数据解释和写作的手稿。阿斯利康回顾了出版,不影响作者的意见,以确保医学和科学准确性和知识产权保护。相应的作者曾访问所有数据和最后的决定负责提交出版的手稿。其他融资机构没有参与任何部分的设计,研究分析或解释。e . Ax也是瑞典战略研究基金会支持的(SSF)。石球Brightling被落实的支持,医学研究委员会、国家健康研究所莱斯特生物医学研究中心(英国)和AirPROM (fp7 - 270194)之下。d·辛格是支持由国家卫生研究所(NIHR)曼彻斯特生物医学研究中心(BRC),西北肺慈善中心,曼彻斯特,英国阿斯利康,盖瑟斯堡,医学博士,美国。作者的观点是,不一定NHS, NIHR或卫生部。
- 收到了2020年8月28日。
- 接受2021年3月4日。
- 版权©2021年作者。生殖权利和权限接触权限在}{ersnet.org