抽象的
这项2期随机、双盲、安慰剂对照试验评估了lebrikizumab(一种白细胞介素(IL)-13单克隆抗体)单独或背景吡非尼酮治疗特发性肺纤维化(IPF)患者的疗效和安全性。
IPF患者≥40岁,强烈致力致命能力(FVC)为40%-100%预测和扩散能力,用于预测25%-90%的一氧化碳,均为治疗 - 天真(COHORT A)或接受PIRFENIDONE(2403毫克)·日−1;COHORT B)随机1:1每4周皮下接收lebrikizumab 250 mg或安慰剂。主要终点是FVC%的年度率预测下降52周。
在群组中,154名患者随机接受lebrikizumab(n = 78)或安慰剂(n = 76)。在Cohort B中,接受Pirfenidone的351名患者被随机化接受lebrikizumab(n = 174)或安慰剂(n = 177)。基线人口统计学在两个队列中的治疗臂均衡。在COHORT A(Lebrikizumab)中未达到主要终点(预测下降的年度化率预测下降)与安慰剂,−5.2%与-6.2%;p = 0.456)或Cohort B(Lebrikizumab与安慰剂,−5.5%与−6.0%;p = 0.557)。在队列B中,在倾向联合治疗的死亡率中观察到无统计学意义的不平衡(风险比0.42 (95% CI 0.17-1.04))。药效学生物标志物显示lebrikizumab活性。安全性与之前的lebrikizumab和吡非尼酮单药研究一致。
尽管药学动力学活动证据表明,单独或用Pirfenidone单独或与Pirfenidone的降低的FVC%预测下降无关。lebrikizumab具有良好的安全型材宽容。这些发现表明阻断IL-13可能不足以实现IPF患者肺功能效益。
抽象的
This phase 2 RCT found no benefit in FVC decline over 52 weeks in IPF patients for lebrikizumab与安慰剂作为单药治疗(n = 78与76)或与pirfenidone组合(n = 174与177);吡非尼酮治疗与以前的结果一致https://bit.ly/313NVR8
介绍
特发性肺纤维化(Idiopathic pulmonary fibrosis, IPF)是一种进行性、不可逆的纤维化肺疾病,其下降率不可预测,预后差,10年生存率≤15% [1- - - - - -3.].吡非尼酮是两种批准用于IPF的抗纤维化疗法之一。吡非尼酮减缓肺功能下降(以预测强迫肺活量(FVC) %衡量),改善无进展生存(PFS)和降低全因死亡率[4- - - - - -6].然而,在关键试验中,对呼吸困难、生活质量或其他临床有意义的结果没有显示出什么益处[4,5].因此,仍需要寻找新的治疗方法,可提供额外的临床益处IPF患者的需求得不到满足。
白细胞介素(IL)-13是成纤维细胞的有效活化剂,促进细胞外基质合成,纤维化潜在的致病作用[7- - - - - -10.].在小鼠模型中,IL-13缺乏或缺陷的IL-13信号传导降低肺纤维化,而IL-13的过度表达增加肺纤维化[11.- - - - - -15.].IPF患者肺活检标本中IL-13、IL-13受体和IL-13靶基因表达水平较正常对照组升高[16.,17.].在从IPF患者的支气管肺泡灌洗液,IL-13水平升高与对照组比较,和IL-13的水平呈负肺功能的关键措施,如%预计FVC和%预测一氧化碳弥散量(相关DLCO),表明IL-13在IPF患者中的致病功能[18.].C-C基序配体18(CCL18)和骨膜素是IL-13生物标志物通路与水平被升高IPF并与肺功能下降或死亡[相关联19.].
金珠单抗是人源化单克隆抗体,其特异性结合的可溶性IL-13中和其活性,并抑制随后的下游信号传导[20.].RIFF研究最初是为了评估lebrikizumab作为单药治疗,并在批准Pirfenidone之后,加入第二个队列研究以评估lebrizumab与Pirfenidone的组合用于治疗IPF患者。
方法
学习规划
即兴小段(NCT01872689)是一种随机的,多方形,双盲,安慰剂对照研究的lebrikizumab与安慰剂患者IPF患者。Riff最初设计为举办时间的时间审判,以评估Lebrikizumab对PFS的益处。样本大小计算,随机化,致盲和给药给药可以在其中找到补充材料.
一个fter the US Food and Drug Administration approved pirfenidone in October 2014, the RIFF protocol was amended in January 2015 to limit the number of patients (total 150 patients) and duration of blinded monotherapy assessment (52 weeks), designated as cohort A. Cohort B was added to assess the benefit of lebrikizumab与安慰剂患者接受患者患者疗法治疗。这两个队列是独立的并且顺序注册。患者在提供书面知情同意后进入了28天的筛选期。
In cohort A, patients were randomised 1:1 to receive lebrikizumab 250 mg monotherapy or placebo every 4 weeks for ≥52 weeks (图1).进行了研究治疗通过皮下注射,第一次注射在随机化时发生(第1天,参见2)。在安慰剂控制期后,未停止患者接受开放标签的lebrikizumab治疗52周。在最后剂量的研究治疗后,所有患者均遵循18周(安全跟进)。
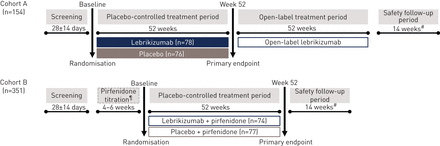
学习规划。#:安全随访18周结束后的最后一剂研究药物;¶:滴定期允许在入学时患者的患者患者。
在Cohort B中,患者每4周随机化1:1至lebrikizumab 250 mg或安慰剂,与pirfenidone组合(≤2403mg·日−1),为期52周(图1).Pirfenidone-naïve患者开始一个磨合期(4-6周),允许吡非尼酮滴定到2403 mg·天−1(每个处方信息),每个国家特定指南的最高剂量耐受或推荐剂量[21.].学习治疗和安全跟进与群组A的匹配。
本研究按照赫尔辛基宣言的原则进行,良好的临床实践进行了。在研究开始之前,从所有机构审查委员会获得批准。伦理批准可以在其中找到补充材料.
耐心
关键合格标准包括年龄≥40岁,根据2011年国际指南诊断为IPF,筛查前≤5年(由筛查期间高分辨率ct中央审查确认,或筛查前≤12个月,如有必要,可进行多学科评估),稳定(筛查和随机之间的FVC (L)差异<10%),%预测FVC≥40%和≤100%,%预测DLCO≥25%和≤90%和6分钟步行距离(6mWd)≥100m[3.].In cohort A, patients received no background IPF therapy for ≥4 weeks prior to randomisation and throughout the placebo-controlled period. In cohort B, patients received pirfenidone ≤2403 mg·day−1for ≥4 weeks prior to randomisation and throughout the placebo-controlled period. Key exclusion criteria can be found in the补充材料.
评估
血清趋化因子CCL13,CCL18和Periostin,IL-13途径的生物标志物在基线和数周4,24和52中测量。在嗜血酮中的嗜血酮的现有发展方案中,磷脂脂酶B样蛋白2(PLBL2)的抗体,在一些患者中检测到与过程相关的蛋白质杂质;观察到免疫原性和安全之间的关联[22.].在基线和规律的时间间隔收集用于检测和表征抗药物抗体(ADAS),以金珠单抗和PLBL2血液样品,以评估免疫原性。其他生物标记物的评估和免疫原性细节可以在找到补充材料.
不良事件,严重不良事件(SAE)和特殊利益(AESIs)的不良事件过程中两个同伙,并在金珠单抗曝光时间52周,安慰剂对照期间进行了评估(从金珠单抗的第一剂量,直到安全性随访结束-up)在队列A.不良事件由研究者报告,每个医学词典编码管理活动方面(版本20.1);没有进行裁决。AESIs包括过敏反应,局部注射部位反应,感染和恶性肿瘤。如在阶段确定的3个临床试验包括在内或光敏性皮疹,胃肠道相关的不良事件(AESIs涉及吡非尼酮例如恶心、腹泻、呕吐)及肝酶水平升高[4,5].
端点和分析
主要终点是ITT群体中的第52周预测FVC的年度下降率,这在跨治疗臂中使用了0.05个双面意义水平的随机斜率模型进行了比较。从模型中,每个处理臂的年度下降率的最小二乘意味着包括在基线,周1,4,12,24,36,44和52处收集的所有FVC测量,并提供了两个处理臂之间的差异95%的置信区间。由于死亡或其他原因,没有因缺失结果而估算。缺少数据由模型处理在缺失的AT-ATURATION(IE。假设预测的肺活量百分比随时间线性下降)。
群组A和COHORT B中的二次疗效终点包括PFS,%预测的年度下降率DLCOIPF生活质量评估工具(ATAQ-IPF)第52周总评分从基线到任意原因死亡的年化变化率[23.].收集Borg类别比例10比例(Borg Scale)作为探索终点。在COSHORT A中,Saint George的呼吸问卷得到了评估。在COHORT B中,还评估了时间终点,包括呼吸相关住院时间的时间,急性加剧或死亡,≥10%预测的FVC或死亡,≥15%的绝对下降DLCO或死亡。Kaplan-Meier估计、基线肺功能分层的log-rank检验、Cox回归模型估计风险比和95%置信区间用于比较时间-事件终点。
所有接受≥1剂量研究药物并有≥1个非缺失药代动力学观察的患者都被纳入药代动力学可评价人群。在ITT人群中评估了药效学生物标志物基线水平的变化。
结果
耐心
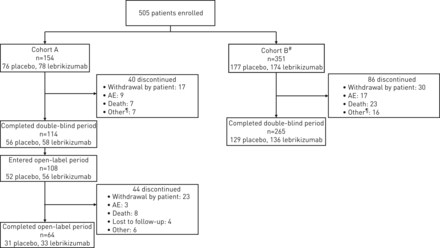
在COHORT A中,325名患者在13个国家的156个地点进行了筛选(图2)2012年10月和2015年4月之间.154名患者随机化(筛查失败率,53%),76名患者接受安慰剂和78名患者lebrikizumab;114名患者(74%)完成安慰剂控制期。完成安慰剂控制期的患者持续和接受开放标签的lebrikizumab,64名患者(59%)完成了开放标签期。在COHORT B中,在2015年5月和2016年5月之间筛选了623名患者。351例随机接受背景Pirfenidone治疗(筛查失败率,44%),174名患者接受lebrikizumab和177名接受安慰剂;265名患者(75%)完成安慰剂控制期。在两个队列中停止的最常见原因被患者,死亡和不良事件戒断。
耐心的性格。AE:不良事件。#:以吡非尼酮治疗为背景;¶:在安慰剂控制期间停用的其他原因包括缺乏疗效,失去后续行动,医师决策和议定书。
病人的人口统计概况参加群组A的两个治疗组和队列乙可比性(表格1;补充表S1).大多数患者均为雄性(分别为83%和81%),白色(82%和86%)。中位数(范围)年龄为群组队队队(51-88)岁(51-88)岁,在队列B.
基线疾病特征,包括预测FVC和%预测的%DLCO,两种队列中的治疗臂之间的相当。大多数患者(≥93%)具有≥1病史发现,包括有源合并条件和非活动的过去条件。群组中最常见的有针对性病史条件(≥20%)在群组中,是胃肠道反流疾病(GORD; lebrikizumab,39.7%与安慰剂,42.1%),关节炎(19.2%与冠状动脉疾病(29.5%)与15.8%),2型糖尿病(19.2%)与25.0%)和肺炎(20.5%)与11.8%)。在队列B中,最常见的条件是GORD(金珠单抗,52.3%与安慰剂,54.8%),冠状动脉疾病(24.1%与20.9%)和关节炎(19.5%)与24.9%)。大多数患者(≥98%)在安慰剂控制期间接受≥1兼容药物(补充表S2).任何治疗臂中最常见的(≥50%)伴随药物是质子泵抑制剂,他汀类药物,类固醇和水杨酸盐。
功效
两个队列均未达到主要终点(图3.).在年度率±中没有观察到差异±SEM.在队列中,%在52周内预测FVC的下降一个(lebrikizumab,-5.2±0.93%与安慰剂,-6.2±0.93%;差异,0.98±1.31%;p = 0.456)或群体B(lebrikizumab,-5.5±0.60%与安慰剂,−6.0±0.61%;差异,0.50±0.85%;p = 0.557)。
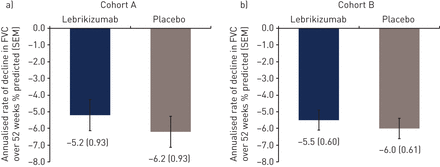
在52周内预测的强迫肺活量(FVC)年下降率%。队列B接受吡非尼酮背景治疗。
在队列A中,没有观察到对死亡率的影响,其他次要终点显示了有利于lebrikizumab (表2.).在COHORT B(HR 0.42(95%CI 0.17-1.04)中观察到有利于lebrikizumab加上pirfenidone治疗的死亡率的数值不平衡; p = 0.053)(图4.).事件率的差异差异(Lebrikizumab和Pirfenidone的七种死亡;安慰剂和Pirfenidone的15次死亡)受到Cohort B的安慰剂加上的急性加剧的影响而导致了更多的死亡。观察到类似的趋势,有利于lebrikizumab第一次急性加重或死亡的时间(HR 0.61(95%CI 0.29-1.25))(补充图S1).在队列B中,其他次要终点未观察到治疗获益(表2.).
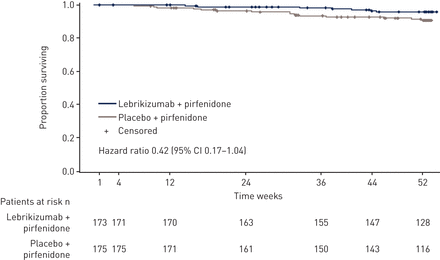
B组从随机到任何原因死亡的时间。
探索性生物标志物分析
血清CCl13,CCL18和Periostin的基线水平与每个群组内的臂之间相当(补充表S3).减小在所有三种生物标志物在金珠单抗治疗的患者为与它们各自的安慰剂或吡非尼酮治疗的对照相比,两个队列中观察到,这表明是金珠单抗活性阻断这些循环生物标志物的一个组件,它是IL-13(下游侧补充图S2).无论吡非尼酮治疗背景如何,lebrikizumab治疗患者之间的生物标志物调节水平是一致的。
药代动力学
每4周皮下注射250 mg lebrikizumab,伴吡非尼酮或不伴吡非尼酮,观察到的平均谷浓度在第4周相似(补充表S4).观察到的平均槽浓度从两周到第52周增加到2倍,对于两个队列。平均值SD.lebrikizumab的半衰期估计在两个队列中都是相似的(队列A和21.9±4.79天的队列23.5±5.36天)。在COHORT B中评估与FVC变化的暴露关系建议响应与暴露有关(补充图S3).在24周、36周和52周时,因呼吸原因住院的患者与非呼吸原因住院的患者或后来死亡的患者之间没有发现暴露关系。
安全
赤鲷治疗的持续时间相似,队列A和COHORT B(补充表S5).不良事件的总数与两个队列中的治疗臂(表3).在安慰剂受控期间,在75(96.2%)和71名(93.4%)和71名(93.4%)患者中报告了不良事件,分别为群组A的安慰剂臂,158(90.8%)和171(96.6%)lebrikizumab分别和队列B的安慰剂武器。群落A的治疗臂常见的常见不良事件的频率通常与lebrikizumab臂相似或更低,而不是在COHORT B的安慰剂臂中(补充表S6).lebrikizumab臂的光敏反应比在群组B的安慰剂臂中少频繁(3.4%与分别为12.4%)。在lebrikizumab暴露期间,队列A中96.9%的患者发生≥1例不良事件(补充表S7).
在安慰剂对照期,队列A的lebrikizumab组和安慰剂组中分别有23例(29.5%)和19例(25.0%)患者报告出现SAEs;在队列B的lebrikizumab组和安慰剂组中分别有56(32.2%)和47(26.6%)报告了SAEs (表3).在接受lebrikizumab的两名患者中报告了与治疗相关的Saes(调查员评估)报告了lebrikizumab的患者,其中一个接受了群组的安慰剂和接受lebrikizumab和六人在群组中接受的lebort b的六个患者有背景pirfenidone。最常见的SAE(≥2%的队列中的≥2%的患者)是IPF(调查员报告的恶化或加剧),呼吸道感染和肺炎。在群组中,肺炎植物,肺栓脂和心脏衰竭Saes也≥2%(在任一臂)中也发生。在Lebrikizumab暴露期间,57名患者(43.8%)在群组中经历了总共92个SAES,其中三个患有治疗相关的SAES,如研究人员评估。AESE的发生率在两个队列中的治疗臂之间相当表3).没有不良事件达到过敏反应的标准。
在群组中,19名患者在研究期间死亡;lebrikizumab暴露期间发生了15例死亡(补充表S8).在安慰剂对照期间,lebrikizumab组有3名患者(3.8%)死亡,安慰剂组有3名患者(3.9%)死亡。9例死亡发生在开放标签lebrikizumab治疗期间,4例死亡发生在安全随访期间。在A组中,IPF是最常见的死亡原因(10例患者)。研究人员认为队列A中有3例死亡与研究药物有关:IPF(双盲安慰剂治疗后安全随访期间)、急性呼吸衰竭(双盲安慰剂治疗后开放标签lebrikizumab治疗后5天)和肺栓塞(lebrikizumab治疗后安慰剂对照期间)。
在群B中,29例死亡;在安慰剂对照的期间22名死亡发生:在金珠单抗和安慰剂组,分别9(5.2%)和13(7.3%)(补充表S8).队列B中有7例死亡发生在安全随访期间。IPF是lebrikizumab组和安慰剂组中最常见的死亡原因(分别有5例和8例患者)。在队列B的29例死亡中,有1例在安慰剂对照组中使用吡非尼酮(由于IPF,在安慰剂对照期间),研究者认为与研究药物有关。
在两个队列中,Lebrikizumab治疗的患者中分别有5.7%(14 / 247)和24.7%(42 / 170)检测到Lebrikizumab ADAs和PLBL2抗体。lebrikizumab ADAs的中位起病时间为~ 12周。没有证据表明抗莱布单抗阳性抗体或抗plb2抗体的存在对接受莱布单抗治疗的患者的安全状况有不良影响(数据未显示)。
讨论
riff未能满足IPF患者的主要终点。lebrikizumab单药治疗(群组A)与肺功能,死亡率或其他相关结果的治疗益处无关。添加lebrikizumab以背景皮里芬酮治疗(Cohort b)也没有与肺功能的治疗益处相关。尽管在群组B中使用了背景Pirfenidone,但在群组A和B中观察到的FVC下降的总体率相似。然而,不能在单个方案下作为不同试验时代的单独研究进行直接比较。在Cohort B中,观察到有利于组合治疗的死亡率的非统计学上显着的不平衡(HR 0.42(95%CI 0.17-1.04))。由于患者与背景皮酮接待安慰剂的患者,由于急性恶化,事件率的差异受到更多的死亡。观察到有利于lebrikizumab的类似趋势,以时间急性加重或在群组中急性加重或死亡(HR 0.61(95%CI 0.29-1.25)))。降低死亡率是IPF的重要结果。在Pirefenidone和尼丁尼布的3阶段试验,该试验导致其批准治疗IPF,在各种研究中报告了对死亡率的影响,并在汇总分析中组合每项治疗的第3阶段数据[4- - - - - -6,24.,25.].在单独的审判中未观察到尼丁尼布未观察到死亡效益,也未观察到汇总分析[24.,25.].在吡非尼酮3期研究,在三分之一的3期临床试验,并在汇总分析观察到的死亡率益处[4- - - - - -6].因此,观察到的有限降低了急性加剧率和随后用联合治疗治疗的患者的死亡可能需要进一步调查,因为该研究得到了动力,只能展示肺功能变化。
其他在IPF中评估IL-13抗体的临床试验也显示在这一患者群体中缺乏疗效,这表明IL-13可能不是IPF的合适治疗靶点。一项2期随机、双盲、安慰剂对照试验终止,该试验评估了60例IPF患者抗il -13 QAX576治疗52周时FVC的安全性、耐受性和变化[26.].在302例IPF患者的72周内评估%预测的FVC在302例IPF患者中评估了IL-13 ralokinumab的72周内的变化的阶段2,随机的双盲,安慰剂对照试验在临时分析后缺乏疗效终止了终止[27.].一个phase 2, randomised, double-blind, placebo-controlled trial that assessed change in % predicted FVC at 52 weeks of the anti–IL-13/IL-4 SAR156597 in 325 patients with IPF showed no significant difference in the primary efficacy endpoint [28.].然而,在COHORT B中报告了急性加剧降低的类似趋势。由于研究人群的差异,急性加剧定义和统计,报告的IPF临床试验中的急性加剧率是可变的(4-28%)可能发生的可能性(4-28%)方法 [29.].在COHORT B中,Lebrikizumab Plus Pirfenidone Arm中的事件率为2.9%(五种急性加剧)与6.2%(11)安慰剂加上pirfenidone臂(HR 0.45(0.16-1.31); p = 0.1346)。虽然急性加剧的总体数量较低,急性加剧率的差异没有达到统计学意义,但有趣的是要注意,lebrikizumab加上皮苯胺酮手臂中没有与急性加剧相关的死亡,而11名患者中有7例在安慰剂加上Pirfenidone ARM去世,与报告的死亡率急性加剧≥50%均匀。虽然这些发现类似于SAR15697试验中报告的结果,但没有证据表明lebrikizumab和COHORT a中的安慰剂(HR 1.21(0.41-3.61); p = 0.73)。
药代动力学(例如lebrikizumab的半衰期估计和药效学在两个群组中都是相似的,这表明背景皮里涅酮治疗没有影响lebrikizumab浓度或活性。药效学措施支持lebrikizumab生物活性,既单独和在面包酮治疗的情况下。此外,疗效/响应关系通常横跨终点,并且没有表明增强的给药导致功效终点的提高。
这项研究有几个限制。每个独立的队列被供电以检测金珠单抗和安慰剂治疗组之间肺功能的差异,而不是在其他结果的差异。2种抗纤维化疗法的在2014年底批准促成了队列甲早期患者停止,这限制了捕获评估金珠单抗作为单一疗法的数据量。在队列A的招募阶段,屏蔽168例(51.6%)没有达到类似于其它抗IL-13 2012 2016和它之间执行试验的合格标准已提出许多病人中提到的抗IL-13试验可能已经从大相位筛选故障3个试验当时完成,因而可能不反映在现有3期试验研究了现实世界人口或群体。相比之下,FVC和DLCO测量使用标准化设备,培训和努力与中央过度读取;因此,标准化问题并不可能导致缺乏观察到的效果。
lebrikizumab作为单药治疗和与pirfenidone的组合耐受良好,具有良好的安全性剖面,与在2阶段2和3阶段临床试验中单独报道的lebrikizumab和pirfenidone的那些相一致[4,5,30.,31.].lebrikizumab和安慰剂治疗的患者的lebrikizumab或plbl2抗体的发病率似乎没有影响药代动力学或安全性。
总之,lebrikizumab单疗法或与背景吡法酮治疗的组合没有降低肺功能下降或为IPF患者提供其他临床显着的益处。
补充材料
可共享的PDF
致谢
我们感谢患者及其家属谁参加了这项研究。该RIFF研究由F.霍夫曼罗氏公司和Genentech公司资助我们感谢Genentech公司的贝卡生,为的药效学分析的贡献。第三方代写,卫生互动,公司的克里斯汀·古尔德提供支持由F.霍夫曼罗氏公司提供。
脚注
本文提供了补充材料www.qdcxjkg.com.
这项研究是注册Clinicaltrials.gov.作为NCT01872689.合格的研究人员可以通过临床研究数据的要求平台要求查阅个别病人级数据(https://vivli.org/)。罗氏的标准,符合条件的研究进一步详情,可浏览这里(https://vivli.org/members/ourmembers/)。有关罗氏的临床信息共享,以及如何申请获得相关的临床研究文献的全球政策的进一步详情,请参阅这里(https://www.roche.com/research_and_development/who_we_are_how_we_work/clinical_trials/our_commitment_to_data_sharing.htm)。
作者的贡献:所有作者有权使用所有数据的研究,并采取了数据和数据分析的准确性诚信责任;所有作者作出了重大贡献的研究设计,数据分析和解释,并在稿件的写作。
利益冲突:T.M.马赫在研究进行期间报告从葛兰素史克公司和加州大学伯克利分校(UCB),大学补助金;他担任顾问和扬声器Apellis,阿斯利康,拜耳,刀片治疗,勃林格殷格翰,Bristol Myers Squibb的,加拉帕戈斯群岛,葛兰素史克,Indalo酒店,诺华,绕指柔,ProMetic公司,Respivnat,罗氏,Samumed和UCB。
利益冲突:U. Costabel是吉利德研究评审委员会成员;曾担任拜耳、勃林格殷格翰和InterMune/Roche的顾问和发言人;曾担任Centocor、Fibrogen、Gilead、GlaxoSmithKline、UCB Celltech和Biogen的顾问。
利益冲突:M.K.Glassberg在研究期间报告Genentech / Roche的赠款;是上升研究指导委员会的成员;并曾担任Bellerophon,Boehringer Ingelheim,Bristol Myers Squibb,长期,Redx Pharma和Roche的顾问。
利益冲突:日本卫生,劳工和福利部的kondoh报告赠款在该研究中,曾担任Genentech的顾问,并担任Asahi Kasei,Boehringer Ingelheim,Eisai的顾问和演讲者,janssen,kyorin,三菱Tanabe Pharma,诺华和Shionogi。
兴趣冲突:T. Ogura报告Boehringer Ingelheim和日本卫生,劳工和福利部的赠款,在该研究中担任Asahi Kasei,Boehringer Ingelheim,Eisai,Nitto Denko的顾问或演讲者,shionogi和toray。
利益冲突:Scholand M.B. Scholand曾任职于Boehringer Ingelheim和InterMune/Roche/Genentech的顾问委员会。
利益冲突:D. Kardatzke是Genentech,Inc。的员工
利益冲突:M. Howard是Genentech,Inc。的员工
利益冲突:J. Olsson是Genentech,Inc。的员工
利益冲突:M.邻居是Genentech,Inc。的员工
利益冲突:P. Belloni是Genentech,Inc。的员工
利益冲突:J.J.Swigris报道了在研究期间,Genentech,Inc。的经常声费,个人费用的补助金;是上升研究指导委员会的成员;在科学咨询委员会担任长期,并担任Boehringer Ingelheim和Roche的顾问。
支持声明:本研究和手稿被F.霍夫曼罗氏公司和Genentech公司的赞助商促成研究设计,数据收集,数据分析,数据解释赞助,该报告的撰写。本文的资金信息已存入CrossRef Resder注册表.
- 已收到2019年12月18日。
- 接受2020年8月12日。
- 版权所有©ers 2021
此版本在Creative Commons归因许可证4.0的条款下分发。