抽象的
介绍结核性脑膜炎(TBM)往往是诊断挑战性。在常规临床实践中,尤其是欧洲环境中的干扰素-γ释放测定(IGRA)和分子测定的性能和分子测定的性能存在有限的数据。
方法这是一项多中心回顾性研究,涉及9个欧洲国家27家为结核病儿童提供护理的卫生保健机构。
结果118例患儿中,确诊54例(45.8%),疑似38例(32.2%),可能26例(22.0%);TBM 1级39例(33.1%),2级68例(57.6%),3级11例(9.3%)。在108例接受颅脑成像的患者中,90例(83.3%)至少有一项与TBM一致的异常发现。结核菌素皮肤试验在5毫米边界处的敏感性为61.9% (95% CI 51.2-71.6%),在10毫米边界处的敏感性为50.0% (95% CI 40.0-60.0%)。QuantiFERON-TB和T-SPOT的检测灵敏度。结核检测结果分别为71.7% (95% CI 58.4-82.1%)和82.5% (95% CI 58.2-94.6%) (p=0.53)。不确定的结果是常见的,发生在17.0%的QuantiFERON-TB检测。脑脊液(CSF)培养阳性率为50.0% (95% CI 40.1 ~ 59.9%),脑脊液PCR阳性率为34.8% (95% CI 22.9 ~ 43.7%)。同时行结核菌素皮试、IGRA、脑脊液培养和脑脊液PCR的患儿亚组中,84.4%的患儿至少有一项检测结果呈阳性(95% CI 67.8% ~ 93.6%)。
结论现有的免疫学和微生物结核病试验在TBM的儿童中具有次优敏感性,每次测试产生了大量比例的患者的假阴性结果。将基于CSF培养和CSF PCR组合的基于免疫基测试导致相当高的阳性诊断产量,因此应该是高资源环境中的标准临床实践。
抽象的
所有现有的免疫和微生物结核病检测方法对结核性脑膜炎儿童的敏感性都不理想。将基于免疫的试验与脑脊液培养和聚合酶链反应相结合可获得高得多的阳性诊断结果,因此应成为标准做法。http://bit.ly/2tsaarl.
介绍
在全球范围内,估计每年有100万儿童和青少年罹患活动性结核病,其中大多数疾病负担发生在资源匮乏的国家[1].在大多数欧洲国家,结核病的发病率近几十年来一直在稳步下降,但耐药结核分枝杆菌带来了新的挑战,特别是在东欧[2].
结核脑膜炎(TBM)是结核疾病的一种不常见表现,但即使在资源丰富的环境中,也与显著的发病率和死亡率相关[3.].TBM患儿通常表现为非特异性症状,且无结核接触史,因此诊断TBM往往具有挑战性[4- - - - - -6].重要的是,以前的数据表明,诊断延迟与差的结果有关[7].
在过去二十年中,常规临床实践中使用的TB诊断在过去二十年中显着发展,引入干扰素-γ释放测定(IGRA)和各种商业分子测定[8].最近的数据显示,IGRAs和分子结核病检测方法在欧洲广泛可用,并被儿科结核病专家广泛使用[9,10].
基于免疫的结核病检测,包括结核菌素皮肤试验(TSTs)和IGRAs,通常被用作疑似结核病儿童的辅助诊断工具[8],但关于IGRAs在TBM儿童中的具体表现的现有数据仍然非常有限[11,12].此外,虽然少数研究已经调查了使用疑似TBM的儿童的分子结核病测定,但大多数是小,限于单一的研究现场,或从低资源环境中的低资源设置可能更多常见于欧洲[4,13,14].此外,大多数研究是在协议的研究条件下进行的,因此与常规临床环境中的性能相比,易于估计测试敏感性。
本研究旨在确定欧洲常规临床护理中TBM患儿免疫、常规微生物和分子结核试验的敏感性。次要目的是描述临床特征和影像学表现,并评估欧洲TBM研究病例统一定义(UTRCD)评分。
方法
儿童结核病网络欧洲试验组(ptbnet)的欧洲成员,当时包括来自31个欧洲国家的214名临床医生和研究人员[9,10,15,16],被邀请回顾性报告在其机构接受医疗保健的患有TBM的儿童和青少年(0-16岁)。该研究于2016年2月开始,报告于2016年8月结束。数据通过一个基于网络的工具收集,为每个案例创建一个标准化数据集。该研究得到了Charité Universitätsmedizin柏林人类伦理委员会和ptbnet指导委员会的审查和批准。在进行这项研究期间,没有收集个人或可识别的数据。
案件分类
根据基于UTRCD得分的共识定义,案例被分类为明确的TBM,可能的TBM或可能的TBM(补充表S1)[3.],稍作修改,如下所示。“与肺结核或TST或IGRA阳性个体密切接触史”项目得分为2分 原始标准中的要点分为两个单独的项目:1)与肺结核患者密切接触史和2)TST阳性(≥10 mm)和/或IGRA,若存在,则各得一分。此外,“脉络膜结节”被添加到“其他地方结核病的证据”类别中,得分为1 点(如有);保留了最高类别分数4分。如果没有一个特定项目的数据可用,则相应项目的得分为0。简单地说,明确的TBM被定义为具有临床入组标准(头痛、易怒、呕吐、发烧、颈部僵硬、抽搐、局部神经功能缺损、,意识改变或嗜睡)加上以下一项或多项:脑脊液(CSF)中检测到抗酸杆菌,M肺结核脑脊液培养M肺结核脑脊液PCR检测。可能的TBM定义为存在临床输入标准加上总诊断评分≥12分,可能的TBM定义为存在临床输入标准加上总诊断评分6-11分。
疾病严重程度
根据修改后的英国医学研究委员会(BMRC)标准对疾病严重程度进行分级[17,18].简而言之,1级为格拉斯哥昏迷评分15分,无神经体征;2级为11-14分或15分,有局灶性神经体征;3级为≤10分。
统计分析
非参数双尾Mann-Whitney U-Tests用于比较连续变量。使用双尾Fisher的确切测试进行比较诊断测试的敏感性。在进行TST并报告为阴性的情况下,但没有以毫米为单位的毫米,它被认为是在5毫米阈值下缺失的数据,并且在10mm阈值下作为负结果;如果将TST报告为阳性而没有强化大小,则将其被认为是在10mm阈值下的阳性,因此在5mm阈值下也是正的。使用WALD方法计算比例的95%置信区间。对多变量逻辑回归分析进行阳性IGRA,阳性TST(处于5毫米和10mm阈值)的关联,并将IGRA不确定为结果变量,预测因子变量,性别,性别,Bacille Calmette-guérin(BCG)疫苗接种状态,TBM分期和明确的TBM诊断。使用Hosmer-Lemeshow评估模型的拟合良好测试和接收器操作特性曲线显示曲线下的区域≥0.7。主要结果措施是差异比例。针对每种差距计算的95%置信区间,P值<0.05被认为是显着的。 Analyses were done using Prism (version 8.0; GraphPad, La Jolla, CA, USA) and Stata (version 12.1; StataCorp, College Station, TX, USA). The study is reported in accordance with Standards for Reporting of Diagnostic Accuracy Studies guidelines.
结果
来自保加利亚(n=1)、芬兰(n=1)、德国(n=3)、希腊(n=1)、意大利(n=3)、斯洛文尼亚(n=1)、西班牙(n=12)、瑞典(n=2)和英国(n=3)的27家医疗保健机构为研究提供了病例。
118名儿童含量在最终分析中,包含54(45.8%)的确定,38(32.2%)可能和26例(22.0%)可能的TBM病例。关于疾病严重程度,39(33.1%)为BMRC TBM 1,68(57.6%)2级和11级(9.3%)3级。
人口统计细节显示在表1.中位数(四分位数范围(IQR))年龄为2.7(1.1-6.4)年。虽然大多数(89.8%)的儿童出生于欧洲,但其中几乎一半(48.3%)来自家庭,源自具有高TB患病率的国家。近一半(41.5%)有Tb接触的历史。对73名(61.9%)儿童进行艾滋病毒的考验;只有两个(2.7%)是阳性的。
最常见的症状是发烧。最常见的神经症状包括呕吐、头痛和意识水平改变(表1).
UTRCD评分在亚组间的分布
在明确TBM组中,平均±sd评分为12.8±3.1(范围4-19)。可能合并或可能合并TBM患者的平均评分为12.1±2.8(6-18)分。在明确TBM的患儿中,近三分之一(n=17, 31.5%)的评分<12 (图1).
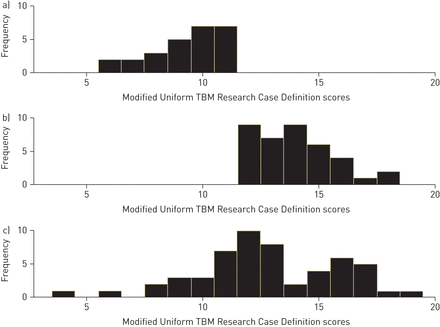
改性均匀结核性脑膜炎研究(TBM)案例定义分数的分布,a)可能,b)可能和c)明确结核性脑膜炎。
放射学调查
在112例接受胸片检查的患者中,81例(72.3%)有提示胸腔内结核病的变化,包括肺门淋巴结肿大、肺浸润、实变或空化(表2).26例(22.8%)检出粟粒浸润。
65名患者患有腹部超声扫描。在大多数(64.6%)中,没有检测到异常。最常见的异常发现是肝肿大,脾肿大和胚胎肉芽肿(表2).
108例患者进行了头颅ct和/或磁共振成像。其中90例(83.3%)有一项或多项与TBM一致的异常发现。最常见的发现是脑积水,其次是基底脑膜强化和颅内结核瘤(表2). 在剩下的18名(16.7%)患者中,未发现明显异常,其中包括6名患有明确TBM的儿童。
结核病免疫试验的执行情况
TST, QuantiFERON Gold assay和T-SPOT。分别有92例、53例和17例患者获得了结核检测(均对血液样本进行了检测)结果。在10例患者中,TST和IGRA结果均不可用。
表3总结了108名患者的结果,其中可以获得TST和/或IGRA结果。在TST和IGRA结果的54名儿童中只有六个(11.1%)一定的阴性TST(在10毫米阈值下)和IGRA结果;五(9.3%)有阴性TST和不确定QFT结果;在剩余的43中(79.6%),至少一个免疫测试结果是阳性的。
在5毫米截止的TST的敏感性为61.9%(95%CI 51.2-71.6%),10毫米截止50.0%(95%CI 40.0-60.0%)。QFT和T-Spot.tb测定的敏感性分别为71.7%(95%CI 58.4-82.1%)和82.5%(95%CI 58.2-94.6%)。统计上,在5 mm截止的TST和QFT测定的TST的灵敏度之间没有显着差异(0.27);然而,10毫米切断的差异有显着差异(P = 0.0143)。类似地,在5mm处的TST之间没有检测到显着差异,T-Spot.tb测定(p = 0.16),但在10mm切断时存在显着差异(p = 0.0167)。IGRA测定的敏感性(P = 0.53)之间没有统计学上显着差异。BCG接种疫苗和BCG非过催化儿童(47.1%)之间存在阳性TST结果(在10毫米截止)的比例没有显着差异与52.5%;p = 0.78);此外,在TST硬度大小(中位数为8mm)方面,两组之间没有显著差异与10毫米;p = 0.81)。
在53例QFT结果的患者中,九个(17.0%)具有不确定的试验结果(95%CI 9.0-29.5%)。在17例T-Spot.TB结果中,没有效果不确定。对于不确定的比例,两次IGRAS之间没有统计学差异与定(即。结果(p=0.10)。不确定检测结果的儿童平均年龄(中位数(IQR)年龄为2.0(1.4-3.0)岁)小于确定检测结果的儿童(2.7(1.0-6.5)岁),尽管这没有达到统计学意义(p=0.22) (补充表S2).
脑脊液微生物试验的表现
抗酸染色、分枝杆菌培养及M肺结核脑脊液PCR检测分别为75、94和69例。只有3例(4.0%)抗酸杆菌阳性(敏感性95% CI 0.9-11.6)。47例(50.0%)分枝杆菌培养结果为阳性(95% CI 40.1 ~ 59.9%),仅24例(34.8%)PCR检测结果为阳性(95% CI 22.9 ~ 43.7%),但差异均无统计学意义(p=0.06)。62例脑脊液分枝杆菌培养和PCR同时进行的病例中,17例分枝杆菌培养和PCR均为阳性,15例仅培养阳性,4例仅PCR阳性。在这个群,并行执行两个测试取得了更大的敏感性(62年36例(58.1%),95%置信区间45.7 - -69.5%)比执行要么文化(32 62(51.6%),95%置信区间39.5 - -63.6%)或独自PCR(21 62(33.9%), 95%置信区间23.3 - -46.3%),但只有仅与PCR比较具有统计学意义(p = 0.59, p = 0.0113,分别)。
结合免疫学和微生物试验
图3.总结了在CSF上进行免疫和分枝杆菌培养和PCR的患者亚组的结果(n = 32),表明TST阳性/ IGRA阳性/ CSF培养阳性和IGRA阳性仅是最常见的结果星座,但也是结果星座非常异质。在所有四次测试中只有五种(15.6%)案件存在负面结果;因此,所有四种测试的总灵敏度合并为84.4%(95%CI 67.8%-93.6%)。这五种案例中只有一个在另一个地点进行抽样,淋巴结活检是培养和PCR阳性的M肺结核.
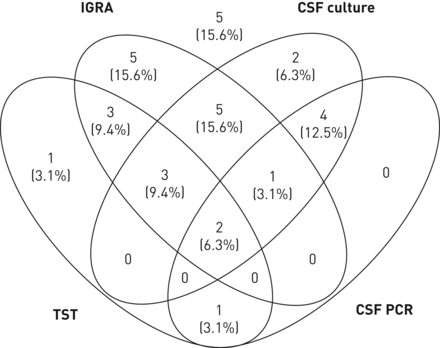
总结阳性结核蛋白皮肤测试(TST),干扰素-γ释放测定(IGRA)和脑脊液(CSF)测试结果(培养和PCR)在进行所有四个测试的患者中(n = 32)。在其中五名患者中(如图所示),所有四个测试都是阴性的。
讨论
据我们所知,这是迄今为止规模最大的关于低结核病发病率儿童结核病研究的多中心研究,通过建立完善的儿科结核病合作研究网络,欧洲各地的许多参与中心都参与了这项研究。
该研究在低TB入射环境中进行了与其调查结果的解释相关。近三分之一(33.1%)的病例具有BMRC TBM级疾病,而只有9.3%的疾病患者患病级,与来自高结核病发病国家的报告形成鲜明对比,其中绝大多数患者在演示时有2年级或3年级疾病[13].这表明在欧洲环境中,TBM患者患者早期呈现患者,患者较小。
此外,我们的队列与大多数患有TBM的儿童的群组不同于高结核病患病率,关于微生物学证实的病例的比例。在我们的队列中近一半(45.8%)确认,与来自高于四分之一的高流行环境的研究对比,确认了案例[14,19,20.].这可能是我们研究中召回偏倚和优先报告确诊病例的结果,也可能是参与这项研究的中心比资源较少的地区更容易获得诊断检测。后一种假设得到了以下事实的支持:在结核病高流行环境中可获得分子诊断的儿科研究报告了微生物确诊病例的相似比例[4,21].
以专家共识为基础的UTRCD评分系统的表现[3.],在我们的队列中次优。微生物学证实TBM的案例几乎三分之一(31.5%)具有评分<12,因此在没有阳性微生物结果的情况下将这些患者分类为“可能的TBM”。比较不良的性能可能涉及欧洲患者早期呈现的趋势(并且因此具有较少的特征,并且因此降低得分)比高TB流行环境中的患者更低。但是,在某些患者中,评分所需的某些数据(例如症状持续时间)未记录,可能导致这些患者倾斜较低值的患者的UTRCD评分。然而,重要的是,该评分系统是为研究目的而开发的,而不是用于临床决策。
暗示性Tb疾病的放射变化存在于案件的几乎四分之三(72.3%)。这种突出显示疑似TBM的患者应经常接受胸部成像,因为这可能提供有用的信息诊断。但是,我们的数据与来自其他研究的数据形成鲜明对比,报告胸部射线照相的变化相当较低的TBM比例,通常为40-60%[19,22,23].我们队列中有很高比例(83.3%)的儿童在颅脑影像学上出现异常,包括脑积水、基底脑膜强化和颅内结核瘤,这与既往报道一致[19,20.,22].
我们的数据突出显示所有现有的免疫学和微生物TB测试在TBM的儿童中具有次优敏感性。TST,QFT测定和T-Spot.TB测定具有〜80%或更低的敏感性,表明当进行单一免疫检测时,在进行单一的免疫检测时,在进行单一的免疫检测时,大约一个患有TBM的患儿。最近的几项研究,包括TBM患者,在血液中调查了新的免疫基础TB生物标志物,其患有有可能改善儿童TB的诊断,但需要额外的研究来确认他们的研究结果[24- - - - - -26]. 有趣的是,我们的多元逻辑回归分析表明,TST假阴性结果在患有更严重TBM的儿童中更为常见。此外,根据肺结核儿童研究报告的观察结果,我们发现大部分患者的TST和IGRA结果不一致[24,27,28].
令人震惊的是,相当一部分儿童的IGRA测试结果不确定。在接受QFT检测的儿童中,17.0%的儿童有不确定的结果,这比大多数研究肺结核儿童QFT检测的结果要高得多[24,27,29,30.].有趣的是,在加利福尼亚的一项研究中也观察到结核性中枢神经系统疾病和不确定的IGRA结果之间的关联,该研究仅包括17例确诊的中枢神经系统疾病病例[11].尽管这些观察的基础仍不确定,但考虑到我们队列的中位年龄为2.6岁,我们很容易假设年龄是一个影响因素,但在多变量logistic回归分析中,我们没有发现年龄和不确定的检验结果之间的关联。然而,包括我们自己在内的几项已发表的研究表明,年轻与不确定的IGRA结果有关[31- - - - - -33].或者,患有TBM的儿童和具有肺结核的人之间可能存在免疫差异,导致前者IGRA性能受损。
根据已发表的数据,我们的结果显示抗酸杆菌染色显微镜对TBM患儿的敏感性非常差[7,14,22].脑脊液分枝杆菌培养是敏感性最高的微生物试验,但仍只有一半的病例呈阳性。聚合酶链反应对M肺结核脑脊液检查的敏感性更低,只有大约三分之一的病例出现阳性结果。然而,不同医疗机构使用的各种内部和商业PCR检测限制了这一发现的解释。最近的一项研究包括23名感染艾滋病毒的成人TBM发现,最近发布的Xpert MTB/RIF Ultra试验比上一代Xpert MTB/RIF试验和培养具有更高的敏感性(敏感性70%)与(分别为43%和43%)[34],表明一些基于商业的PCR基测定可以表现和培养或甚至在TBM中具有优异的敏感性。然而,需要更大的前瞻性研究来确认这些结果。我们的数据表明,在CSF上进行培养和PCR并行地提高了诊断产量,同时在南非的儿科研究中的观察结果中的一致性[21].最近发表的一篇文章提出了新的希望,即下一代脑脊液宏基因组测序可能会改善现有微生物方法难以检测的CNS感染的诊断[35].
此外,我们的数据显示,如果TST,IGRA,CSF培养和CSF PCR并行进行,则在大多数患有TBM的儿童中产生阳性结果,只有15.6%的病例显示错误阴性结果在所有四个测试中。在儿科环境中,免疫试验通常用作疑似TB疾病的辅助测试[8],我们的研究结果支持的做法。虽然阳性免疫检测不证实TB疾病,但在伴有兼容的临床和放射发现的孩子中,它们对TBM的推定诊断提供了大量的支持。
在这一组的大量儿童中M肺结核在脑脊液以外的样本中检测到,有助于确定微生物学诊断。痰液、胃抽吸物、支气管肺泡灌洗液标本检出率均较高,普遍阳性检出率≥75%。然而,考虑到获得这些样本的决定是由管理患者的临床医生做出的,而不是根据标准化的研究方案,这些样本很可能优先在一组有胸部x光片改变或呼吸症状的患者中获得。然而,我们的数据强调,呼吸道/胃样本的检测应该在疑似TBM的儿童中进行常规检查,如M肺结核通常不能在脑脊液中发现,从而排除了微生物学确认和药敏试验。
与所有回顾性研究一样,关键限制是由于文件不完整,一些数据缺少。更大数量的患者进行了TST,但仅记录了分类而不是定量数据,导致这些患者必须被排除在某些分析之外。此外,只有少量的参与中心使用T-Spot.tb测定;因此,有关该测试性能的数据有限。没有对CSF进行IGRAS的情况;然而,最近的META分析表明,在CSF上表现IGRAS而不是血液不会导致更高的诊断产量[12].最后,与所有回顾性研究一样,存在回忆偏倚和优先报告的风险。
总之,我们的数据显示,在欧洲环境中,患有TBM的儿童倾向于呈现早期,严重疾病较小,而不是高结核病发生率。大部分患有TBM的儿童共存,并因此在所有疑似TBM的患者中考虑胸部成像和呼吸或胃样品的收集。免疫学(TST和IGRAS)和微生物结核病试验均具有TBM儿童的次优敏感性。通过培养和PCR对CSF的微生物检测进行TST和IGRA并行进行TST和IGRA,导致具有结核病感染的儿童比例的大幅增加,因此应该是医疗保健环境中的标准方法,具有足够的资源来执行这些测试。.
补充材料
可共享的PDF
承认
PTBNetTB脑膜炎研究组:Matthias Bogyi,Wilhelminenspital Vienna,奥地利;Carlotta Montagnani,Anna Meyer儿童大学医院佛罗伦萨,意大利;Laura Lancella,BambinoGesō儿童医院罗马,意大利;芬兰赫尔辛基大学埃瓦索罗;Angeliki syngelou,儿科学部第二部,国家&Kapodistrian大学雅典大学,P.&A. Kyriakou Childsher的医院,希腊;Uros Krivec,大学儿童医院卢布尔雅那,斯洛文尼亚;安德烈马丁纳达纳尔达和安东尼索里亚诺 - 亚兰斯,医院Vall d'hebron巴塞罗那,西班牙;Irene Rivero,HospitalClínico大学大学De Santiago de Compostela,西班牙;Marta Benavides Nieto,医院Infantil Virggen delRocío塞维利亚,西班牙;Mercedes Bueno,医院UniversitarioFundaciónAlcorcónMadrid,西班牙; Teresa del Rosal, Hospital Infantil La Paz Madrid, Spain; Luis Mayol and Borja Guarch, Hospital Universitari Dr Josep Trueta Girona, Spain; Jose Antonio Couceiro, Complejo Hospitalario de Pontevedra, Spain; Carmelo Guerrero Laleona, Hospital Miguel Servet Zaragoza, Spain; Rutger Bennet, Astrid Lindgren Children's Hospital Stockholm, Sweden; Karsten Kötz, Queen Silvia Children's Hospital Gothenburg, Sweden; Brittany Raffa, Evelina London Children's Hospital, UK; Fiona Shackley, Sheffield Children's Hospital, UK.
脚注
本文提供了补充材料www.qdcxjkg.com
作者贡献:S. Thee和R. Krüger构想了这项研究。R. Basu Roy, S. Thee, D. Blázquez-Gamero, B. Santiago-Garcia, M. Tsolia, R. Krüger和M. Tebruegge设计了这项研究,收集了数据并进行了数据分析。L. Falcón-Neyra, O. Neth, A. Noguera-Julian, C. Lillo, L. Galli, E. Venturini, D. Buonsenso, F. Götzinger, N. Martinez-Alier, S. Velizarova, F. Brinkmann和S. b . Welch贡献数据,审查数据并提供输入。所有作者和合作者都对论文进行了评审并提供了意见,并批准了最终的稿件提交。
利益冲突:R. Basu Roy于2014年至2016年担任非营利性组织日内瓦FIND的顾问。
利益冲突:S. Thee无需披露。
利益冲突:D.Blázquez-Pabero没有什么可披露的。
利益冲突:L.Falcón-Neyra无需披露。
利益冲突:O. Neth没有什么可透露的。
利益冲突:A. Noguera-Julian无意义。
利益冲突:C. Lillo没有什么可透露的。
利益冲突:L.加利没有什么可透露的。
利益冲突:E.Venturini没有什么可披露的。
利益冲突:D. Buonsenso没有什么可披露的。
利益冲突:F.Götzinger没有披露。
利益冲突:N.马丁内斯-阿利尔没有什么可透露的。
利益冲突:S. Velizarova没有什么可披露的。
利益冲突:F. Brinkmann无需披露。
利益冲突:S.B.韦尔奇没有什么可披露的。
利益冲突:Tsolia先生没有什么可透露的。
利益冲突:B. Santiago-Garcia为来自Cepheid的其他项目没有收到诊断测定,并支持Glaxosmithkline的会议。
利益冲突:R。克鲁格没有什么要透露的。
利益冲突:M. Tebuegge在减少的定价或对制造商(Cellestis / QIAGEN)的其他TB诊断项目免费获得Quantiferon测定,并得到了对Cepheid的会议的支持。
支持声明:此项目进行了无需专用资金。PTBNET由Deutsche GesellschaftFürInternationalezusammenarbeit提供支持。M. Tebuegge得到了英国国家卫生研究所(NIHR)提供的临床讲座的支持,以及通过技术战略委员会/创新英国的补助金。B. Santiago-Garcia由西班牙卫生部资助 - Instituto de Salud Carlos III(ISCIII)并由欧洲联盟(联邦联邦)共配(Contrato JuanRodés,Grant JR16 / 00036)。R. Basu Roy由伦敦卫生和热带医学院的NIHR学术临床讲座资助。A. Noguera-julian得到了“每个LaIntensificaciódeCocultatiussecialistes的”Subvelions“(Favicamente De Salut de La Generalitat de Catalunya)的支持得到了支持(Slt008 / 18/00193)。本文的资金信息已存入交叉参考基金登记处.
- 已收到2019年10月11日。
- 接受3月9日,2020年3月9日。
- 版权©2020人队
这个版本是在知识共享署名许可证4.0的条款下发布的。
















