抽象的
尼古丁通过α7-烟碱受体在人支气管上皮细胞(HBEPC)中诱导ACE-2过表达https://bit.ly/3ej5b35.
到编辑:
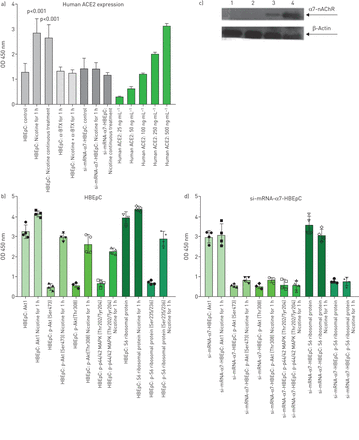
L.Eung.等等。[1]最近发表了欧洲呼吸杂志一篇关于吸烟者和COPD患者小型气道上皮细胞上皮细胞血管素转换酶II(ACE-2)表达的纸张,探讨了对2019年重症冠状病毒疾病风险的影响(Covid-19)。作者发现,具有COPD和当前吸烟者的受试者的气道中ACE-2基因的表达增加。实际上,最近系统审查关于感染严重急性呼吸综合征冠状病毒2(SARS-COV-2)的患者的吸烟习惯的报告数据得出结论,吸烟可能与疾病的负面进展相关和不利结果[2]。这些结论在C的通信中受到挑战AI.[3.在缺少解释这种关联的可靠机制的基础上。通过其他研究支持这些结果的需求非常清楚,但我们认为存在强大的机制解释。尼古丁对肾素 - 血管紧张素系统(Ras)的稳态有血管素 - 转化酶(ACE)/血管紧张素(Ang)-ii / Ang II型1受体轴的稳压影响,以及降低补偿ACE的下调-2 / ang-(1-7)/ mas受体轴,又转向心血管和肺部疾病的发展[4.]。不同的气道细胞,如支气管上皮细胞,II型肺泡上皮细胞和间质肺成纤维细胞,表达烟碱乙酰胆碱受体(NACHR),特别是α7subtype[5.]。所有这些细胞表达RA的组件[4.]。此外,尼古丁增加了肺中Ace的表达和/或活性[4.],也是在吸烟者血清中发现的增加,并且至少需要20分钟才能返回控制水平[4.]。ACE-2用作SARS-COV的生理相关的细胞入学受体,用于人类呼吸冠状病毒NL63,并且可能对于SARS-COV-2 [6.]。ACE结合SARS-COV-2 S蛋白,并且通过其组织表达介导定位和感染的效率[6.]。此外,尼古丁诱导上皮 - 间充质转换(EMT)[5.那7.],足以允许“正常”分化细胞获得干细胞状特征和性质的机制。我们计划从细胞应用公司获得的人支气管上皮细胞(HBEPC)进行实验(www.cellapplications.com/product.数字502k-05a)。将细胞保持为完全支气管/气管上皮细胞生长培养基中的粘附单层(www.cellapplications.com/product.)在95%AIR / 5%CO中的37°C2,以7.5×10的初始密度播种4. cells·cm-2并且当培养物达到80%汇合时,用0.25%胰蛋白酶-1mM EDTA溶液(Sigma-Aldrich,米兰,米兰,意大利)。HBEPC源自正常人支气管非患病的表面上皮(IE。哮喘,COPD或2型糖尿病)。形态与上皮起源一致,是上皮细胞标志性细胞角蛋白18的阳性。第四段的半汇合HBC(7.5×104. cells·cm-2)被治疗:1)1小时,零或1.0×10-7 M nicotine (Sigma-Aldrich, Milan, Italy) dissolved in saline in complete medium; 2) with 1.0×10-6 M α-Bungarotoxin (α-BTX; Sigma-Aldrich, Milan, Italy) dissolved in saline, in the continued presence of nicotine at zero or 1.0×10-7 M for 1 h; 3) treated continuously with nicotine for additional passages, 1 passage every 48 h for a total of 16 passages. We showed, for the first time, that nicotine at 1×10-7 M (the concentration present on the alveolar lining fluids after one cigarette is in the range 6×10-6到6×10-5 M [5.])能够增加ACE-2(图1A)在HBEPC中。用尼古丁治疗诱导磷酸-S6核糖体蛋白(SER235 / 236),AKT1,磷酸-AKT(SER473),磷酸-AKT(THR308)和磷酸-P44 / 42 mapk(Thr202 / Tyr204)(图1B.)。为了验证ACE-2通过γ-2通过α7-NACHR,HBEPC,第四通道,在指数生长阶段,以1×10的密度镀6. cells·mL-1,在100μlsiRNA转染培养基中孵育稀释的α7-NACHR siRNA(0.1μg)。如L所述进行转染一世等等。[8.[综合,成功,HBE16人气道上皮细胞系(未受影响的细胞)转染。经尼古丁治疗后,未表达α7-NACHR蛋白的转染HBEPC的克隆(图1C.),并且不能在尼古丁处理后诱导磷酸-S6核糖体蛋白(Ser235 / 236),Akt1,磷酸-AKT(Ser473),磷酸-AKT(Thr308)和磷酸-P44 / 42 mapk(Thr202 / Tyr204)(图1D)被选择用于进一步实验。尼古丁在该克隆中没有诱导ACE-2(Si-mRNA-α7-HBEPC)(图1A)。该观察结果支持ACE-2增加的假设由α7-NACHR特别介导。此外,当用尼古丁和α-BTX同时孵育HBEPC时,α7尼古丁拮抗剂[9.],未观察到ACE-2的诱导(图1D)。重要的是,用尼古丁治疗α-BTX或组合不是细胞毒性(数据未示出)。在这些基础上,我们建议吸烟可以促进SARS-COV-2至α7-NACHR信号传导的细胞摄取机制。可能的α7-NACHR下游机制可以是磷酸-AKT和磷光-P44 / 42 MAPK的诱导。这种机制是假设的,部分地通过o假设LDS.和K.aspbani.[10.[他们的原理图]解释尼古丁暴露如何增加SARS-COV-2进入肺细胞的风险。α7-NACHR在神经元和非神经元细胞中存在(IE。肺,内皮,淋巴细胞);因此,吸烟可能会影响若干器官系统中的Covid-19病理生理学和临床结果,包括大脑。
尼古丁对人支气管上皮细胞(HBEPC)或Si-mRNA-α7-HBPC的影响。a)血管紧张素转换酶II(ACE-2)检测。用人ACE-2 ELISA Kit AB235649测量ACE-2(www.abcam.com/human-ace2-elisa-kit-ab235649.html.)根据制造商的指示。数据是平均值±SEM.;使用T检验评估p-Vaule。绿色地块是人类ACE-2标准。实验一式三份进行两次。B)磷酸-S6核糖体蛋白(Ser235 / 236),Akt1,磷酸-AKT(Ser473),磷酸-AKT(THR308)和HBEPC中的磷酸-P44 / 42Mapk(Try202 / Tyr204)的诱导。使用pathscan®细胞生长多目标夹心ELISA套件N.7239(细胞信号)pathscan®细胞生长多目标夹心ELISA试剂师是一种固相夹心ELISA,其结合了检测S6核糖体蛋白的内源性水平所需的试剂。,磷酸-S6核糖体蛋白(SER235 / 236),AKT1,磷酸-AKT(SER473),磷酸-AKT(THR308)和磷酸-P44 / 42MAPK(THR202 / TYR204)。数据是平均值±SEM.;使用T检验评估p值。实验两份进行两次。c)α7-NACHR蛋白质检测。如前所述进行蛋白质印迹[11.]。人类α7-NACHR抗体NBP1-49348购自NOVUS生物学(www.novusbio.com.)。1-2 Si-mRNA-α7-HBEPC用零(泳道1)或1.0×10处理-7 M nicotine (lane 2) for 1 h. 3–4 HBEpC treated with zero (lane 3) or 1.0×10-7 M nicotine (lane 4) for 1 h. Experiments were performed twice. d) as in panel b, but treated cells are si-mRNA-α7-HBEpC.
可分享的PDF.
脚注
利益冲突:P. Russo没有什么可披露的。
利益冲突:S. Bonassi没有什么可披露的。
利益冲突:R. Giacconi无需披露。
兴趣冲突:M. Malavolta没有什么可以披露的。
兴趣冲突:C. Tomino没有披露。
利益冲突:F. Maggi无需披露。
- 已收到2020年4月10日。
- 公认2020年4月16日。
- 版权所有©ers 2020
此版本在Creative Commons归因非商业许可证4.0的条款下分发。