摘要
在南非夸祖鲁-纳塔尔省的耐药结核病和艾滋病毒患者中,在开始治疗前发现了与bedaquillin耐药性有关的基因突变,并在治疗期间获得。需要加快bedaquiline的常规耐药性测试。http://bit.ly/2vnL4VY
到编辑:
全球结核病控制受到耐药性的威胁,2018年有超过50万例对一线药物产生耐药性[1].Bedaquiline是一种高效的Tb药物,在试验和程序化环境中具有改善的耐药TB(DR-TB)结果[2那3.].世界卫生组织(世卫组织)建议将其包含在大多数DR-TB方案中[4.]并且在临床试验中进一步评估。有几个关于临床床型抵抗的报道[5.-8.].迄今所鉴定的临床分离株中的耐药相关变异(RAVs)几乎完全是由Rv0678可以提高的突变结核分枝杆菌贝达奎林和氯法齐明的最低抑菌浓度[9.].
南非夸祖鲁-纳塔尔省是艾滋病毒合并感染患者中广泛耐药结核病(XDR-TB)爆发的地方[10.那11.].尽管kwazulu-natal的使用广泛,但常规表型或基因型药物易感性测试(DST)未进行,留下未识别的贝壳型抗涂抹的潜力。
基线的临床意义Rv0678变体不清楚[12.].的出现Rv0678治疗期间的突变已被记录,但它们的发病率未知。我们在用床型和氯氟沙西胺处理的前瞻性DR-TB群体中报道了基线和新芽贝壳族RAV的频率和相关的临床结果。
在南非夸祖鲁-纳塔尔省一家公共结核病转诊医院就诊的耐药结核病和艾滋病毒成年患者在PRAXIS研究中开始使用bedaquiline两周内被纳入(nct03162107)2016年11月至2019年1月。抗逆转录病毒治疗的治疗是强制性纳入标准。在治疗的前6个月内每月访问临床资料,问卷和痰,随后的治疗结束。该研究得到了夸祖鲁 - 纳塔尔大学生物医学和哥伦比亚大学伦理审查委员会的批准。将所有熔化物接种到分枝杆菌生长指标管中,并在Bactec 960(BD,MD,USA)中培养。阳性培养物接受全基因组测序(WGS)和Bedaquiline MIC测试,用于分离株Rv0678采用7H11琼脂比例法进行变异。6个月时的文化转换定义为两个或两个以上连续的负月度文化。治疗结束时的结果按照标准定义进行分配[13.].
在研究期间就诊的965名成年结核病患者中,有297名有资格参加研究并同意参加。最常见的不合格原因是没有同时感染艾滋病毒(n=160)和2周前开始使用bedaquiline > (n=126)。本报告的92例患者的基线培养和WGS结果均为阳性。其余205例患者在基线时培养阴性(n=198)或有WGS失败的分离株(n=7)。测序队列51%为女性,中位年龄为36岁(四分位数范围(IQR) 30-43岁);66%以前有任何结核史,23%耐药结核患者。中位CD4计数为276 (IQR 134-452)。测序分离株的患者更有可能出现二线耐药(53/92;57.6%与82/205;40.0%;P =0.006),但其他方面具有相似的基线特征。
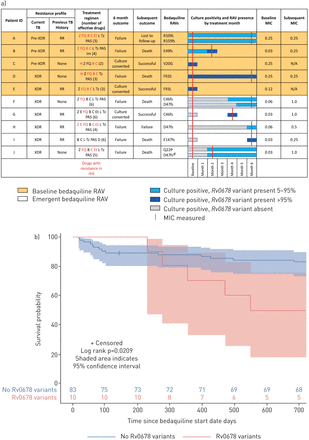
基线Rv0678在启动Bedaquiline治疗之前,在5.4%(5/92)患者中鉴定了5.4%(5/92)患者的患者(图1).虽然没有一个MICs为样本的基线Rv06783/5的mic值处于野生型范围的顶端(0.25µg·mL-1).有基线的B患者的bedaquiline MICRv0678变体,从0.03μg·ml增加-1在基线到0.25μg·ml-1在第2个月增加Rv0678变异等位基因频率从72%到96%。额外的紧急Rv06785.7%(5/87)患者在治疗期间出现变异(图1).新兴Rv0678变异与贝达奎林MIC增加8倍>相关。
a)患者Rv0678阳性结核病(TB)痰培养中的突变。电阻配置文件适用于当前和最近的前一TB剧集。指示治疗方案中使用的药物,由于阻力而无效。h:isoniazid;Z:吡嗪酰胺;E:ethambutol;FQ:氟质喹;B:Bedaquiline;C:Clofazimine;等:乙醇; L: linezolid; T: terizidone; PAS: p-aminosalicylic acid; D: delamanid; Im: imipenem; RAV: resistance-associated variant; XDR: extensively drug resistant; RR: rifampicin resistant. Patient A was phenotypically ethionamide resistant in the absence of ethionamide resistance-associated variants.Rv0678变体分为基线(橙色背景)或应急(白色背景)。变异位点上的氨基酸变化被指定(fs,移码突变)。条形图表示无变异体(灰色)、杂合子变异体(浅蓝色)和固定变异体(深蓝色)的培养阳性样本。最低抑菌浓度(mic)显示在基线和后续时间点,如果执行(红线)。#:在病人J,六个进一步低频率Rv0678变种出现在6个月(A57E, R72 T, D88fs, D88A, G121R, L122P)。b)开始bedaquiline治疗后的生存概率Kaplan-Meier曲线,并对随访损失进行审查。阴影区域表示95%置信区间。
所有基线或紧急的患者Rv0678变体具有对氟喹诺酮酮或二线注射剂(XDR-TB / XDR-TB)的耐药性,并以先前对DR-TB进行治疗60%。患者Rv0678突变更可能具有XDR-TB(60%)而不是没有(29%)(p = 0.07)。没有先前用Bedaquiline或Clofazimine治疗。不百分子或atpE突变被确定。在治疗期间,除bedaquiline/clofazimine外,没有出现进一步的表型或基因型耐药性。患者的基线耐药情况和方案Rv0678显示变体(图1).
在4/5例中,由于感染菌株的患者内部患者的患者进化而发生突出的Bedaquiline抗性,而在一种情况下(患者G)抗性是患者F患者F的耐床尿布菌株的抗性。两名患者在此期间住院同期,这似乎表示医院传输,因为没有交叉污染的证据。
整个队列的中位随访时间为12.8个月(IQR 6.0-18.9),死亡率为20.7%(19/92)。73/92例(79.3%)患者经6个月培养转化。患者没有Rv0678突变,70/82(85%)培养转化,而基线患者Rv0678转化2/5(40%)培养物。五个患者中的基线Rv0678变异患者中,3/5(60%)有不成功结局(2例死亡,1例失访),而非变异患者中,16/82(18.4%)有不成功结局Rv0678变异(p = 0.058)。患者紧急Rv0678突变体在6个月时更有可能是培养阳性(4/5;80.0%与12/82;14.6%;4/5(80.0%)死亡或失访,15/82(18.3%)未随访(P =0.007)。在有基线或紧急情况的患者中Rv0678变异,70%(7/10)有不成功的结局(死亡、治疗失败或随访失败),而18%(15/82)没有(p=0.001)。
患有患者麦克风的分布Rv0678本研究中的变体与其他报告一致,发现许多变体与低于或临界浓度的凸起麦克风相关[14.].所有隔离物与MICS>0.25μg·mL-1在该研究中,具有C46或D47帧突变突变,仅在获得的耐药性中看到。具有更高(但技术易感)MIC的菌株与其他TB药物的态度也与更高的复发风险有关[15.].关键问题是贝壳型麦克风在0.25μg·ml的临界浓度下方或均匀-1(7H11琼脂)对临床决策和监测抗性传播进行临床后果和破坏床型表型DST的临床后果和破坏指导。
值得关注的是,所有5名出现紧急耐药性的患者在他们的治疗方案中都有4种或更多的活性药物。有趣的是,随访期间未发现其他突发性耐药性。Bedaquiline可能是治疗方案中的关键药物,对Bedaquiline产生耐药性或根本不产生耐药性,由于其较长的半衰期,当依从性不佳时,长时间暴露于亚治疗水平可能导致耐药性的发生。bedaquiline和氯法齐明的联合可能也有助于耐药性的选择Rv0678突变带来交叉耐药性,所有患者都接受了两种药物的联合治疗[9.].
基线的百分比Rv0678我们研究中鉴定的变体类似于C208和C209 Bedaquiline临床试验中确定的6.6%[8.].C209报告> 4倍的MIC增加与Rv067812/205(4.4%)患者的变异性,类似于我们研究中的4/92(4.3%),但与结果没有关联[12.].基线的存在Rv0678突变可能表示群组中的贝壳和氯氟氮硫胺菌株的目前传播。
本研究的局限性包括相对少量的患者可评估。患者的数量Rv0678变异也很小,限制了临床结果差异的因果解释。虽然南非是Bedaquiline的重要早期采用者,但高艾滋病毒患病率和独特的TB流行病可能会限制我们的研究结果的概括。与差的结果相关的因素倾向于聚集(如。低药物粘附,次优艾滋病毒控制和物质滥用),使得易于解开贝基丝耐药性差异差的差异或仅是共变化的程度。本研究的优势包括其前瞻性设计,纵向随访和仔细收集的临床结果。
本研究鉴定了与临床结果不良相关的基线和新芽贝基丝氨酸RAV的重要亚型。我们突出了活性基因型监测的作用,以鉴定贝壳型抵抗力,以及再评估表型DST临界浓度。本报告还提高了围绕DR-TB的经验治疗方案的总体策略的担忧,即使用新型剂构建,也可能需要通过测序引导的个体化治疗方案来实现所有患者的最佳治疗结果,并防止BEDAQUILINE的出现抗DR-TB菌株。
可分享的PDF.
脚注
支持声明:C. Nimmo由Wellcome Trust (203583/Z/16/Z)支持。J. Millard由威康信托基金(203919/Z/16/Z)资助。M. O'Donnell得到了美国国立卫生研究院/国家过敏和传染病研究所(R01AI124413;R21TW011077),以及赫伯特和弗洛伦斯·欧文基金会。本文的资金信息已存入CrossRef Resder注册表.
兴趣冲突:C. Nimmo报告在研究期间从惠康信托提供赠款(203583 / z / 16 / z)。
兴趣冲突:J.Milard在研究期间,惠康信托的报告(203919 / z / 16 / z)在研究期间。
利益冲突:k·布莱恩没有什么可透露的。
利益冲突:S. Moodley没有什么可披露的。
利益冲突:L. Van Dorp没有什么可披露的。
利益冲突:K. LutchMinarain无需披露。
利益冲突:A.狼报告在研究期间,来自国家卫生卫生研究所的国家过敏和传染病研究所的赠款。
利益冲突:A.D. Grant无需披露。
利益冲突:F.巴洛克斯没有什么可透露的。
利益冲突:A.S.皮姆是杨森制药的雇员。
利益冲突:N.Padayatchi无需披露。
利益冲突:奥唐纳先生没有什么可透露的。
- 收到了2019年11月28日。
- 公认2020年2月6日。
- 版权所有©ers 2020
此版本在Creative Commons归因许可证4.0的条款下分发。