摘要
hsp60调控的PRMT1表达调控上皮-间质相互作用,调节气道重构,并通过支气管热成形术逆转http://bit.ly/2NDCKGW
哮喘被宽泛地定义为一组的临床症状与可逆呼气气流限制或支气管高反应性有或无气道炎症[1]。这些症状与气道重塑,尤其是严重哮喘患者,它的特点是组织结构的改变和细胞在气道内,包括增加黏膜下细胞外基质沉积,网状基底膜(元)增厚,气道平滑肌增生和肥大(ASM),支气管微血管改造和粘液细胞化生2- - - - - -4]。
支气管热成型术(BT)是一种内镜手术,通过局部传送射频波来加热气道组织(65°C) [5]。该过程已被描述为第一哮喘的治疗,目标气道通过调节气道炎症和气道高反应[重塑,而不是直接间接地6]。三项随机对照试验的长期随访研究指出,BT可减少患者在接受BT治疗5年后的哮喘发作、急诊就诊和住院治疗[7- - - - - -9]。这表明BT后肺功能的改善可能是一个长期的影响。BT确实降低了RBM内的ASM质量和I型胶原沉积[10]。此外,BT降低黏膜下神经密度,ASM相关神经密度和上皮神经内分泌细胞的数目。These results were associated with several clinical outcomes, including the Asthma Control Test (ACT) scores, the number of exacerbations and emergency department visits at 3 and 12 months after BT [11]。对气道重塑减少的影响可能不仅仅是由热损伤的直接急性效应来解释,而且一定是由于BT引起的另一种生物机制[12]。虽然这些临床和组织病理学的发现极大地扩展了我们对BT的认识,并揭示了它的作用模式很可能远远超出了最初提出的对气道平滑肌的选择性影响,但我们仍然缺乏对BT如何调节重塑过程的详细的力学理解。
上皮-间质沟通是调节气道重建的主要机制。在本期杂志中欧洲呼吸杂志,S联合国et al。(13他们假设,上皮细胞和成纤维细胞之间的相互作用将支持BT的有益作用。他们假设,上皮分泌的因子将控制成纤维细胞的表观遗传机制,从而驱动BT的持久作用。在他们的研究中,他们主要关注蛋白精氨酸甲基转移酶-1 (PRMT1)。PRMT1是哺乳动物细胞中主要的PRMT酶,它可以甲基化组蛋白和其他蛋白上的精氨酸残基。PRMT1已被证明在肺癌、肺纤维化、肺动脉高压、COPD和哮喘的发病机制中发挥作用[14]。在小鼠胚胎成纤维细胞导致DNA损伤的PRMT1缺失和减少细胞增殖15]。因此,有兴趣研究PRMT1的成纤维细胞增殖导致对气道之前和发生后BT患者重塑重症哮喘的作用。
在这项研究中,作者收集了8例患者的支气管肺泡灌洗液(BALF)和62例重症哮喘患者接受BT治疗前后的原代支气管上皮细胞(PBECs)。PBECs被种植和收集。将来自PBEC培养的上清液和来自患者的BALF应用于原代成纤维细胞。在这些气道成纤维细胞,他们发现PRMT1表达增加,细胞增殖和线粒体质量以应对BALF之前收集BT, BALF中没有观察到反应收集在平行BT。之后,他们的差别观察对这些miR-19a以及增加细胞外signal-regulated kinase-1/2 (ERK1/2)活动,以应对BALF BT之前收集,而BALF收集BT后没有显示这些变化。这很重要,因为miR-19a是ERK1/2活性和PRMT1表达的抑制因子[16]。CCAAT enhancer-binding protein-β(C / EBPβ)依次是负的调节器miR-19a [17]。
作者进一步报告,从BT后收集的气道上皮细胞的培养上清液中降低C /EBPβ表达,ERK 1/2活性,过氧化物酶体增殖物激活受体γ共激活因子1α(PGC1α),热休克蛋白60(HSP60),PRMT1气道成纤维细胞和线粒体的质量与来自BT之前获得的上皮细胞的培养物上清液。这些结果证实了上皮细胞和成纤维细胞之间的细胞串扰的关键是一些BT后观察到的持续变化。此外,通过siRNA PRMT1的下调降低C /EBPβ的表达和从上皮细胞BT前培养上清液的增殖作用,表明PRMT1的在此响应了至关重要的作用。总的来说,这些结果表明,无论是BALF和BT后上皮培养物上清液通过涉及的miR-19A导致ERK1 / 2,PRMT1和C /EBPβ下调的上调的机制降低成纤维细胞的增殖。
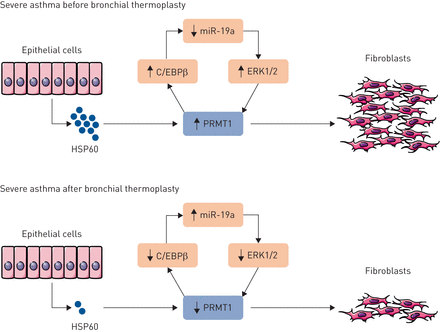
为了阐明引发这种交流的分泌因子,作者对BALF进行了蛋白组学分析,对上皮细胞进行了转录组分析。他们发现BT后HSP60的表达下调。HSP60是线粒体中表达的一种伴侣蛋白,参与蛋白从细胞质到线粒体基质的运输和重新折叠。此外,HSP60是一种蛋白质,是在细胞受到热等应激反应后诱导产生的[18]。释放到细胞外空间的HSP60被认为是一种危险信号,与自身免疫性疾病、癌症和炎症相关,并与各种细胞间隔内的分子直接相互作用[19]。肺成纤维细胞与人重组HSP60的直接刺激显著增加C /EBPβ,PRMT1和PGC1α的表达,证实此细胞间信号中间体的至关重要的作用。总之,这表明存在通过HSP60调节的PRMT1表达管辖上皮间充质相互作用是气道重塑起到了重要作用,并通过BT(逆转图1)。
本研究还发现,BT治疗后,哮喘患者的PBECs增殖明显快于BT治疗前,这与Pretolani等。(11他们没有观察到BT对再生上皮的影响。这种差异可能是由于测量方法和时间的不同造成的。Pretolani等。(11上皮]利用组织病理学评估在原地,而年代联合国et al。(13使用一种方法来量化上皮细胞的增殖体外。在临床研究中原位,第一次随访时间为3个月,远远超过了气道上皮细胞增殖的时间窗。因此,不可能从Pretolani等。(11研究捕获的上皮细胞增殖是否发生变化在体外的年代联合国et al。(13]。
用S研究联合国et al。(13是第一个显示BT对PRMT1表达的作用,突出其在气道重塑中的作用的研究。进一步的有趣的问题从这项研究中产生,需要探索。第一个与上皮分泌HSP60的机制和BT的作用有关。已有研究表明,H2O2诱导细胞内氧化应激增加HSP60表达上皮细胞进入细胞外介质通过NFκB-p65 [20.]。这将有兴趣研究这是否也与BT的刺激的情况下。它还有趣的研究上皮分泌的HSP60的信号传导途径作为这似乎是向成纤维细胞中表达PRMT1的初级调节路由。例如,该受体和信号效应都参与了成纤维细胞信号传导响应HSP60,并且是这些药物的潜在目标?
第二个问题是关于揭示PRMT1活性在调节成纤维细胞反应中的作用。其他研究表明,PRMT1通过组蛋白修饰H4R3me2调控ZEB1表达,调控上皮向间质转化[21],并通过精氨酸34的甲基化扭曲1,导致E-cadherin的抑制[22]。此外,PRMT1甲基化的表皮生长因子受体[23]。我们也有兴趣确定这些可能的通路和基质在成纤维细胞中被PRMT1甲基化,从而解释其对气道重塑的影响。
总的来说,S的研究联合国et al。(13他们报道了BT对上皮-间质相互作用的持续影响,其特征是HSP60-PRMT1信号通路下调。这些新发现不仅激发了对BT调控的通路和表观遗传机制的进一步研究,而且还激发了对这一信号通路的其他潜在治疗方法,如抑制HSP60或PRMT1,从而可能减少哮喘气道重塑相关的成纤维细胞反应。
支气管热成型术对气道上皮间质沟通影响的示意图。支气管热成型术减少释放热休克protein-60 (HSP60)上皮细胞,进而减少细胞外的表达signal-regulated kinase-1/2 (ERK1/2),蛋白质精氨酸methyltransferase-1 (PRMT1)和CCAAT enhancer-binding protein-β(C / EBPβ),而miR-19a恢复的表达。
可共享的PDF
脚注
利益冲突:S.F. Rahmawati没有什么要披露的。
利益冲突:R. Gosens报告来自Boehringer Ingelheim, Chiesi Farmaceutici和Aquilo的资助,在提交的作品之外。
支持声明:该作品由Lembaga Pengelola达纳Pendidikan /印尼捐赠基金用于教育(LPDP)的支持。本文资金的信息已交存Crossref资助者注册表。
- 收到2019年9月25日。
- 接受2019年的10月28日。
- 版权所有©ERS 2019