摘要
通过单细胞RNA测序,Morse和他的同事已经确定了特发性肺纤维化过程中肺巨噬细胞群体的深刻变化,并提出了一种针对这种致命疾病的新的治疗策略http://bit.ly/30Hb0Gl
阐明与特发性肺纤维化(IPF)的开始和进展相关的细胞和分子机制是一个巨大的挑战。更好地了解这些问题不仅对阐明IPF的致病机制至关重要,而且对诊断和预后提供新的治疗策略和选择。IPF的发病机制特别复杂,涉及与动态病理生物学过程相关的多种细胞类型,包括慢性炎症导致的伤口过度愈合、肺泡上皮和内皮细胞凋亡、由假分层和细支气管样上皮组成的蜂窝囊肿的形成、肌成纤维细胞效应细胞活化,形成成纤维细胞灶,最后,细胞外基质过度沉积,导致肺结构破坏和肺功能丧失。遗传易感性、衰老和吸入毒素都有助于纤维化过程的启动[1.–3.].
在本期的188bet体育备用网址欧洲呼吸杂志,米orse等.[4.]使用单细胞RNA测序(scRNA-seq)提供与IPF患者肺相比,正常肺新鲜样本中细胞群和相关基因表达变化的详细图谱。
单细胞分析和相关计算方法的最新进展为在特定病理生理学背景下表征细胞异质性提供了独特的机会。本研究中使用的基于液滴的scRNA-seq系统[5.]支持每次运行数千个细胞的捕获和基因表达谱分析。与传统的批量方法不同,scRNA-seq阐明了精确的细胞组成、发育和激活状态[6.–9],并已被用于识别新的罕见细胞类型,如最近描述的人气道壁离子细胞[10,11].强烈的协作努力,人类细胞阿特拉斯领导的财团,旨在描述所有人类细胞在人体的特定基因表达模式,生理状态,组织发展轨迹和空间分布,最近强调肺组织作为其优先级的项目之一(12]因此,这一完整的健康肺图谱将通过揭示细胞状态的变化以及与特定疾病相关的细胞-细胞相互作用的改变,为慢性肺疾病(如IPF)的研究提供一个独特的参考集。它还应指出表明这些细胞变化是否是旨在重新激活上皮-间质界面的发育途径或获得新的病理程序,并导致识别新的生物标记物以及治疗策略的进展。
Morse等.[4.]已经为IPF的发病机制提供了一些重要的新见解。有趣的是,他们的策略是在同一IPF患者的肺中选择两个特定位置,对应于严重纤维化的下肺叶和较少纤维化的上肺叶,以便在不同的进化点捕获疾病。作者比较了使用来自三名IPF患者和三名健康对照的新鲜消化肺样本,通过scRNA-seq从这些不同位置到正常肺的转移,提供了一组广泛的47个单细胞转录组 771个单元格,代表17个 231和30 分别来自健康肺和IPF肺的540个细胞。通过计算分析,可以识别出20多个细胞簇,这些细胞簇随后被识别为离散的细胞类型,包括炎性细胞、上皮细胞、血管细胞和间充质细胞类型。然后,作者使用先前描述的标记物进行了全面鉴定根据疾病状态(正常、上叶和下叶),IPF中细胞群和相关基因表达的变化如前所述,他们可以证实,在纤维化的下叶中,肺泡I型和2型上皮细胞明显缺失,基底细胞、杯状细胞、纤毛细胞和棒状细胞(包括蜂窝状囊肿)也相应增加[13].正如预期的那样,纤维母细胞的比例也显著增加在纤维化的叶中,增加了多个基质基因的表达,这与组织学分析显示增加的成纤维细胞灶一致。
值得注意的是,他们的数据还捕捉到了疾病过程中肺巨噬细胞群的深刻变化。最近,通过使用小鼠模型和人类样本,强调了在心脏、皮肤和肺等多个器官的纤维化过程中特定巨噬细胞亚群的重要性[14–19].Morse等.[4.],显示正常和IPF肺均含有三个分立的巨噬细胞亚群,其中只有一个具有单核细胞来源巨噬细胞的标记物,如FCN1 (FCN1)嗨).另外两个种群对应于居住者样巨噬细胞,一个高表达FABP4和INHBA (FABP4)嗨)和另一种高表达的SPP1/骨桥蛋白和MERTK (SPP1嗨) (图1).尽管单核细胞来源的巨噬细胞在IPF和对照肺样本之间保持稳定,但在疾病过程中观察到两个居民样亚群的切换情况,SPP1显著增加嗨纤维化下肺叶中的巨噬细胞(图1)。基于先前几项研究显示骨桥蛋白在IPF和小鼠肺纤维化模型中的关键促纤维化功能[20.,21],这些数据强烈指向SPP1嗨这一假说得到了额外的免疫荧光成像数据的支持,这些数据显示骨桥蛋白在IPF基质中显著沉积,以及高度增殖的SPP1共定位嗨在纤维化的肺叶下部有巨噬细胞伴成纤维细胞灶。此外,MER/AXL/TYRO3受体激酶家族成员MERTK在SPP1中的表达升高嗨细胞提示该激酶在细胞激活和存活中具有特定的关键功能。MERTK抑制与骨髓细胞存活相关[22]作者认为,MERTK抑制剂可能会耗尽IPF肺中促纤维化巨噬细胞和成纤维细胞的活化(图1).
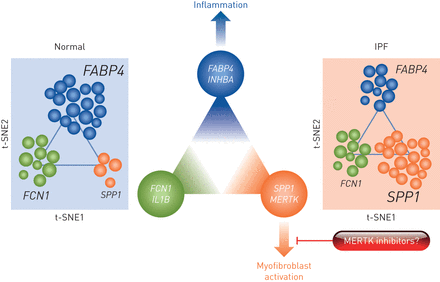
健康和特发性肺纤维化(IPF)患者的肺巨噬细胞亚群从正常或IPF患者的肺中鉴定的三个巨噬细胞亚群被可视化为t-SNE (t分布随机邻居嵌入)图。这三个群体的失衡与疾病进展有关。作者感谢弗兰克·阿奎拉的作品。
这项研究由Morse等.[4.与Reyfman等.[16].两项研究都指出SPP1的增加嗨IPF肺中存在促纤维化巨噬细胞,但他们的结论在健康肺中存在这个亚群方面存在差异。事实上,虽然Reyfman等.[16呈递最高检控官嗨Morse等.[4.支持这一观点,即该亚群是肺巨噬细胞自然异质性的一部分,已经存在于正常肺中。对两个公开的数据集进行比较分析,以及其他类似的研究,应该可以解决这个重要的问题。事实上,SPP的存在嗨健康肺中的巨噬细胞可能具有重要的治疗意义,这表明针对单核细胞/巨噬细胞迁移到IPF肺的治疗策略可能会失败,而针对mertk介导的巨噬细胞生存的治疗策略可能会对这种疾病显示出希望。
正如研究人员所指出的,还应开展进一步的工作,以回答几个关键问题,特别是破译IPF中组织内巨噬细胞增殖的分子机制,这可能涉及CSF-1、IL-4和/或IL-13。另一个重要问题涉及IPF患者样本的scRNA-seq数据集中某些特定细胞类型的比例相对较低,特别是间充质细胞,因为这些细胞在组织消化过程中选择性丢失。这一缺陷目前正在阻止与从小鼠模型中获得的数据进行比较[23,24以及对与疾病进展相关的特定间充质亚群(包括肌成纤维细胞或脂肪成纤维细胞)的可塑性的深入分析[25].这种分析可能确实揭示了参与肌成纤维细胞激活的新的治疗靶点,包括最近提出的TGF-β通路的间质特异性调节因子[26].关于这个具体问题,新技术的使用,如空间转录组学[27,可能提供了额外的精确层,通过捕捉特定位置的基因表达调节,包括蜂窝囊肿和成纤维细胞病灶。
总的来说,M的出色工作orse等.[4.已经有助于更好地理解这种致命疾病的发病机制,并为进一步的单细胞研究铺平了道路,这将扩大我们对在疾病进展中发生的细胞状态的多种变化和细胞间相互作用的改变的知识。
脚注
利益冲突:B. Mari没有什么可透露的。
利益冲突:B. Crestani报告了阿斯利康的讲座和差旅支持的个人费用、勃林格殷格翰和罗氏的拨款、MedImmune的拨款、赛诺菲的讲座和咨询费、Genzyme的顾问委员会工作的差旅支持等提交工作之外的费用。
- 收到了2019年6月26日。
- 认可的2019年6月26日。
- 版权©2019人队















