摘要
在钙激活的氯离子通道,TMEM16A,在IPAH患者的肺动脉的新研究识别的增加,提出了苯溴马隆的再利用,所述信道的非特异性抑制剂,作为用于所述疾病的治疗的新http://bit.ly/2ITN4ul
之一的肺动脉高压最完善的标志(PAH)的距离PAH患者的肺动脉平滑肌细胞(肺动脉平滑肌细胞)的独特的细胞表型。这种表型,这是由高收缩性,过度增殖,凋亡性和有氧糖酵解所定义的,紧密地与质膜去极化联和升高胞质钙浓度([钙2 +]赛特)[1-3]。
在过去的二十年里,多个研究已经确定的品种,有助于PAH此去极化肺动脉平滑肌细胞表型阳离子通道的表达改变或调节。这些变化包括池操纵Ca的表达增加2 +通道,包括典型瞬时受体电位(TrpC)通道,TrpC6 [4],并且在电压 - 门控钾通道(一个功能kv),例如Kv1.5 [五],这使得K的流出+细胞内的离子。一起,增加Ca2 +流入和减少K+流出有助于膜的去极化和的进一步升高的[Ca2 +]赛特通过电压依赖性钙通道的开放(图1)。最近,无论是遗传的PAH家庭和特发性肺动脉高压(IPAH)的患者群的遗传筛选启用丧失功能的杂合突变的鉴定KCNK3中,编码基因的TASK-1钾通道,在这两个患者群体[6,7]。KCNK3在多环芳烃的野百合碱大鼠模型中降低,并发现其抑制作用可诱导正常大鼠肺血管细胞的异常增殖[8]。此外,KCNK3沉默促进PASMC膜去极化体外,还提供PAH中的病变细胞表型的另一种介质[9]。
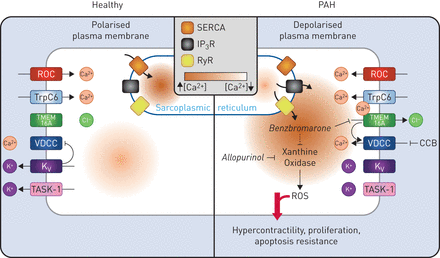
概述肺动脉高压(PAH)患者肺动脉平滑肌细胞(PASMCs)离子通道功能改变的示意图,以及苯溴马龙酮在逆转疾病细胞表型中的作用。在PAH中,储存操作的钙离子通道,如典型瞬时受体电位(TrpC)通道TrpC6上调,而钾离子通道,包括TASK-1和电压门控钾离子通道(Kv)被下调,导致增加的细胞内钙和PASMC膜的去极化水平。这些改变驱动电压依赖性钙通道(VDCCs)的活化。钙的升高的表达2 +激活的氯−通道,跨膜成员16A(TMEM16A),导致进一步的PASMC膜去极化,高收缩性,增殖和凋亡抵抗。苯溴马隆对多环芳烃细胞的治疗可以阻断TMEM16A,恢复膜极化,逆转多环芳烃细胞表型。然而,苯溴马龙和别嘌呤醇一样,也可能通过其对黄嘌呤氧化酶的作用发挥治疗作用。钙通道阻滞剂3R:肌醇三磷酸敏感受体;ROC:受体操作通道;RyR:阿诺定受体;ROS:活性氧;SERCA:肌浆/内质网atp酶钙。
与这种在多环芳烃中被彻底定义的阳离子处理作用相比,阴离子通道对疾病的潜在作用受到的关注相对较少。到目前为止,这项工作主要局限于Ca的研究2 +激活的氯−信道,TMEM16A,其在暴露于慢性缺氧或野百合碱大鼠的肺动脉平滑肌上调并作为临界贡献者PASMC去极化和肺动脉过强疾病的两种模型[10,11]。有趣的是,对气道上皮细胞的研究表明Ca2 +激活的氯−启用Cl的通道−亚微摩尔浓度增加时的射流反应[Ca]2 +]赛特在与TRPC6串联罐功能,提供TMEM16A活性增加并在PAH肺动脉平滑肌的去极化的公知的演员之间的可能联系[12]。尽管这样令人信服的证据,工作配套TMEM16A,或其他阴离子通道具有重要作用,在PAH的发病机制尚未超越动物模型。
在的当前问题188bet体育备用网址欧洲呼吸杂志,P应用程序等。[13]利用激光捕获IPAH患者和健康对照者肺微解剖肺动脉中阴离子通道和转运体基因表达的靶向筛选来解决这一局限性。作者认为TMEM16A是IPAH肺动脉中唯一显著上调的负离子通道,并证明了该通道在PASMC去极化中的中心作用。虽然这些研究为人类疾病的细胞病理生物学提供了重要的见解,但P应用程序等。[13]来自他们引进的苯溴马隆,一种非特异性的TMEM16A抑制剂,作为潜在的多环芳烃治疗。
苯溴马隆是一种尿酸剂和黄嘌呤氧化酶抑制剂,20世纪70年代首次被引入治疗痛风[14]。但直到2012,该药物也被确定,通过高通量筛选,因为在微摩尔浓度TMEM16A的抑制剂[15]. 第页应用程序等。[13]表明,苯溴马隆恢复膜极化和块PAH肺动脉平滑肌的血小板衍生的生长因子诱导的细胞增殖体外,同时防止肺动脉高压的发展体内在慢性缺氧小鼠和多环芳烃单辛他林模型大鼠。
通过这项研究,苯溴马隆成为现有药物中最新的一种,包括二氯乙酸[16],他克莫司[17),羟氯喹(18]等人,其正在考虑用于再利用作为PAH治疗。按P最近审查rin等。[19],药物再利用提供了罕见的致命疾病,如多环芳烃具有很大的优势通过允许监管机构批准的快速跟踪,同时尽量减少与新药开发相关的成本。值得注意的是,苯溴马隆的是,一直被认为是再利用的PAH,与秋水仙碱和别嘌呤醇沿着第三痛风治疗。重要的是,两个别嘌呤醇及苯溴马隆是黄嘌呤氧化酶的抑制剂,提高的可能性,至少的苯溴马隆的治疗益处的部分,超出上TMEM16A任何操作,可能是由于其对活性氧的产生(ROS)的影响[20.]。
在考虑多环芳烃中任何药物的潜在再使用时,候选药物在人类患者群体中表现出安全性和有效性是至关重要的。关于前者,苯溴马龙相对于其他重新利用的候选人可能处于不利地位。尽管苯溴马隆在一些国家仍可作为非专利药使用,但出于对肝毒性的担忧,Sinofi-Synthelabo于2003年将该药物撤出市场。随后的风险-收益分析表明,这些安全担忧可能被夸大了[21]。然而,为了在临床上可行,苯溴马隆还必须表现出足够的效力大于对患者安全的任何潜在风险。在这方面,必须承认,苯溴马隆在预防疾病多啮齿动物模型的发作有效是很重要的,但还没有被证明扭转建立疾病在这些模型中,或在PAH,的SUGEN缺氧大鼠模型,现已成为潜在PAH治疗的翻译[金标准的临床前模型17,22]。
尽管没有这些数据,P应用程序等。[13]做了检查,以诱导在一小群10名PAH患者的急性血管舒张响应苯溴马隆的容量。一世n these subjects, the administration of 200 mg benzbromarone, twice the standard daily dose for the treatment of gout, failed to reduce mean pulmonary arterial pressure or pulmonary vascular resistance and actually caused a small but significant increase in both values. Perhaps this result is not surprising when considering previous clinical experiences with L-type, voltage-dependent calcium channel blockers (CCBs). CCBs, such as amlodipine, nifedipine or diltiazem, only induce an acute haemodynamic response in a subset of IPAH patients [23],对其中一小部分人的慢性给药有效,代表5-10%的多环芳烃患者,对他们来说,过度和慢性血管收缩是其疾病的主要特征[24]。虽然苯溴马隆的长期给药可能需要实现在更广泛的人群PAH有利的影响,但也有可能是针对改变阴离子处理可能仅是PAH患者的一小部分可行的治疗策略。如果这后一种情况的话,还必须考虑这个子集是否将代表同一组已经在临床上广受城市商业银行服务的个人,或者,如果目标改变阴离子流将开辟新的治疗选择为当前未定义组患者。
与苯溴马龙作为一种治疗策略的最终临床价值无关,值得注意的是,随着CCBs和西地那非作为批准的治疗方法的采用,多环芳烃已经是一个重新利用药物的成功故事。此外,所有其他经批准的多环芳烃治疗方法都起源于指定的孤儿药,可追溯到1984年首次使用环氧丙烷醇[25]。这个历史例证药物再利用的优势,加快药物名称为机制来提供治疗的迫切需要一个相对较小的患者群的治疗选择。然而,这条赛道战绩也提醒人们领域尚未开发出了定制专为PAH的基础上,独特的分子病理学驾驶疾病进展的治疗批准。
随着高通量DNA测序技术的兴起,一些新的PAH相关基因最近被鉴定陪突变的初步鉴定BMPR2,the gene encoding the bone morphogenetic protein (BMP) type II receptor (BMPR-II), nearly 20 years ago [26-30.]. 这些基因有助于识别疾病中新的失调信号通路,并揭示控制多环芳烃起始和进展的细胞过程。更重要的是,这些新的靶点也为下一代量身定制的分子治疗提供了希望,这种治疗不仅建立在动物模型或已确诊多环芳烃患者的细胞表型上,而且还建立在人类疾病的遗传学基础上。有趣的是,这些新发现的基因包括BMPR-II信号通路的组成部分,如BMPR-II配体BMP9和BMP10[28-30.],强调该受体对疾病的重要性,支持寻求旨在恢复PAH中功能失调的BMP信号通路的治疗方法。随着这项针对下一代多环芳烃治疗的工作的进行,问题仍然是,是否需要这种定制疗法来真正改变临床环境,或者开发用于治疗其他不相关疾病的药物的回收是否代表了更可取的前进道路。
脚注
利益冲突:A.L. Theilmann有没有透露。
利益冲突:M.L.Ormiston无需披露。
支持声明:该作品是由健康研究加拿大学院(授予PJT-152916)的支持。本文资金的信息已经保藏交叉引用出资者注册。
- 收到2019年3月23日。
- 公认2019年3月28日。
- 版权所有©ERS 2019