抽象的
临床试验结果与现实世界结果之间的分歧主要是许多癌症类型的未知数。本研究总体上旨在评估效力效应差距(临床试验与现实世界之间的差异)在全身治疗中的转移性Nonsmall细胞肺癌(NSCLC)中。
研究了在2008年至2014年期间诊断出阶段IV NSCLC的患者,在七个荷兰大型教学医院(Santeon)网络中,所有患者均在七位荷兰大型教学医院(Santeon)之间进行了研究。对于每位患者,通过将来自临床试验评估的组合的中位数OS除以与各自的治疗评估的合并中位OS来计算疗效效率(EE)因子。
从2989例诊断为患者,1214(41%)开始使用一线治疗。对于所有学习的方案,现实世界OS短于临床试验中报告的OS短。总体而言,EE因子为0.77(95%CI 0.70-0.85; p <0.001)。现实世界患者常常完成治疗计划,并越来越频繁地进行进一步治疗。这些参数与东方合作肿瘤组性能状态一起解释了EE因子变化的35%。
在现实生活中,接受化疗或靶向治疗的转移性非小细胞肺癌患者的生存时间比试验中的患者短近四分之一。患者的表现状态、更早的停药和更少的后续治疗可以部分解释这种差异。
抽象的
在现实世界实践中治疗的化疗或靶向治疗患者的转移性NSCLC患者的存活率比临床试验所含的患者近四分之一。这些现实世界数据为临床医生提供了有用的信息。http:///wly/khd230minff.
介绍
在荷兰,非小细胞肺癌(NSCLC)占所有肺癌诊断的77% [1].大多数患者在确诊时已出现局部晚期或转移性疾病[2,3.].转移性NSCLC(第四阶段)的总体1年生存率仅为22%[1].为这些患者提供的姑息治疗可以包括症状缓解,通过最佳的支持护理或针对肿瘤组织的全身治疗。
众多第3期临床试验表明,在转移NSCLC患者中最佳支持性护理的系统性治疗的优越性2,4].然而,来自肿瘤学临床试验的数据虽然提供了临床活动的关键证据,但不提供足够的信息,以确定在真实世界中使用时治疗的影响。由于严格的患者含有标准,重要的患者特征在临床试验中常常预测治疗响应是不足的。这导致临床试验如何转化为现实世界人口的不确定性。然而,这些信息对于患者和医生来说是至关重要的,以决定选择什么类型的治疗,如果有的话,特别是在姑息的环境中,寿命质量可能超过全身治疗的可能延伸。
已经努力提供对具有肺癌的现实世界群体的治疗结果的洞察力与临床试验。例如,z胡等.[5]与东方合作肿瘤组(ECOG)4599审判的参与者相比,常规实践中的中位生存率估计较短。ungels等.[6]显示出可比的反应率,但在先前用化疗治疗的患者中,在现实世界中存活较短。另一个例子是加拿大研究,表明,临床实践中的中位生存率较短,导致欧洲毒素的二线治疗与在临床试验环境中[7].在几个单一的单一治疗比较之外,肺癌仍然缺乏临床试验和常规护理环境之间可能发散的全面概述[8].
考虑到大量转移性NSCLC患者在临床试验外进行治疗,目前的研究旨在整体探索现实世界实践中系统性治疗的有效性与来自临床试验的疗效数据(效力效率(EE)间隙),并研究可能解释差距的因素。
方法
数据源
这项研究的临床数据来源于荷兰七家大型(非大学)教学医院的网络,它们分布在荷兰的地理位置上,名为Santeon (在线补充附录4).Santeon成立于2007年,为12%的荷兰患者提供服务。
2012年,圣仁建立了结果登记处的护理,其中包括从2008年从2008年诊断出肺癌的所有患者的临床和结果数据。这些数据包括肿瘤特征,患者特征,治疗计划和临床结果。有关如何获取数据,标准化和验证的信息可以在其他地方找到[9].
Santeon于2010年从2010年接受了一家医院接受了一家医院的所有患者的个人患者水平,Santeon Farmadatabase并行,为Santeon Farmadatabase设立了Santeon Farmadatabase,该父母在各个患者中包含所有规定和分配的药物。对于每种处方,数据库包括药物名称,剂量,管理和行政途径。Santeon Farmadatabase的完整细节在别处描述[10.].
这项研究由医学研究伦理委员会讨论,豁免了对知情同意的必要性,因为该研究被认为免于审查。
研究参与者
在关注结果注册表中,为本研究选择了2008年至2014年间诊断的所有转移性(第四阶段IV)NSCLC(2008 - 2009年的分期是基于美国癌症TNM联合委员会的第六版(肿瘤,节点,转移)肺癌和2010年开始的分期系统基于第七版;在两个版本中,使用了阶段IV NSCLC的相同标准)。由于其未知的生存地位,不包括重要地位“移民”(2017年1月31日)的患者被排除在外。对于剩下的患者,收集了以下临床患者特征:诊断,性别,查理合并症指数(CCI)和单独的合并症(例如糖尿病),ECOG性能状态(PS),组织学和诊断年。
接下来,对于每个患者,我们搜查了Farmadatabase以确定它们是否接受了转移NSCLC的全身治疗。2008年和2009年,检查各个药房系统缺少有关系统性治疗的数据。
每位患者的全身治疗鉴定
对于每位患者,系统治疗的概述由记录的处方数据构建,包括鉴定方案以及它是第一,第二还是进一步的治疗方法。诊断日期后的初始全身治疗被定义为一线治疗。在前一个方案的理论结束日期(务实)被视为随后的治疗系列后,转换为另一个方案> 90天。在手动审查以前方案的理论结束日期后切换到另一个方案<90天,以确定由于疾病进展(后续线)或毒性(相同的治疗系列)来确定交换机。
基于所有已识别的方案,构建了一个列表,其中涵盖了所有第一线治疗方案的90%。出于实际原因,剩下的(很少应用)方案被置于“其他”类别中。
用于参考结果的系统文献综述
进行了系统文献搜索和荟萃分析,以获得来自上述列表的第一线治疗方案的汇集功效结果。首先,所有相应的第三阶段研究的概述是由PubMed,Embase和Cenchrane图书馆)数据库的广泛搜索构建的(在2017年9月1日搜索)。提供了此搜索的确切细节在线补充附录1.如果满足以下所有标准,则视为符合条件的文章。1)诊断出NSCLC的患者;2)III期的主要文章随机试验;3)研究下的干预是我们数据中确定的方案之一;4)患有阶段IV疾病的患者(可能与IIIB阶段组合);5)总体生存(OS)作为结果。要创建均匀的文章选择,我们排除了关于二级分析的文章(例如亚组分析,后HOC.分析或中间分析);本刊中包含相同全身治疗的变化之间的随机化的制品(例如时序,剂量或持续时间的差异);关于整体治疗的文章与放疗;本刊中包含疾病进展后随机化的相关文章;和既没有为卫生局部提供置信区间也没有生存曲线的文章。
通过两个审稿人(CC和EVDG或FS或BP)基于标题和摘要来筛选资格的第一次选择的文章。在审稿人之间存在差异的情况下寻求共识。随后,单一审阅人员(CC)审查了全文文章,其中第二次审查员在有关资格的不确定性(EVDG)的情况下。没有执行参考跟踪。在线补充附录2提供每个方案更详细的系统回顾和荟萃分析数据的产量。从所有纳入的文章中,提取结果(OS以月计)、纳入周期、纳入标准、治疗线、患者特征、治疗方案完整的患者百分比和接受后续系统性治疗的患者百分比。如果未描述中位OS,则该结果由生存曲线得出。
计算机程序审查经理(版本5.3;北欧Cochrane中心,Cochrane Collaborations,Copenhagen,丹麦; 2014年)用于将所有报告的OS结果与临床试验结合,以估计每个方案的“参考结果”(合并OS)所有包括文章。根据异质性水平(P <0.05级)计算固定效应或随机效应(倾向效果)措施。使用了等式计算了所需的标准错误SE.=(上限95% CI -下限95% CI)/2×1.96,或使用Kaplan-Meier曲线衍生的四分位区间(IQR),其中SD.≈(IQR)/1.35和SE.=SD./√N。
现实世界治疗结果
对于每个患者,根据系统治疗的开始日期与死亡日期之间的时间计算OS。仍然在2017年1月31日仍然活着的患者被赋予这一后续日期,作为死亡之日(n = 54)。随后,我们通过汇总临床试验OS为第一线治疗方案划分各个实际世界操作系统来计算每个患者的EE因素。这种EE因素应被解释为单个结果如何与相应的临床试验中的中位OS相关(例如情感表达因子为0.80意味着生存时间缩短20%)。除了生存,毒性评估使用治疗转换百分比、剂量减少(≤初始剂量的80%)和早期停药(少于4个周期或使用酪氨酸激酶抑制剂<1个月)作为替代。
统计分析
统计软件(Windows的SPSS版本24; IBM,ARMONK,NY,USA)用于统计分析。连续数据表示为平均值±SD.或适当时中位数(范围)。使用Chi-Square和使用T-Tests,Chare Tests和Ine-Way Anova进行分析分类数据。首先,为了评估ee间隙的存在,使用Wilcoxon签名秩检验相对于1.0测试计算的EE因子的分布。如果该分布没有中位数为1.0,则拒绝禁止缺失的假设(现实世界中的中位操作系统类似于临床试验中报告的内置)。后一种测试总体和每个方案进行。
接下来,在EE因子的对数转换(由于非正态分布)后施加多变量的线性回归分析,以研究患者特征与EE间隙的幅度之间的关联。所有可用的特征都被探索为潜在的预后因素。在该分析中,缺失值被回归避难所估算(单次运行模型中的所有可用特征)。通过方差分析评估了最终模型的解释性效果。
为了评估我们主要分析的稳健性,我们进行了四次敏感性分析:1)计算现实世界型号,从治疗开始,但基于诊断日期,并基于系统性治疗的开始日期减去14天(这2-选择周窗口,因为大多数临床试验方案需要在随机化后的2周内进行首次药物管理;2)2017年1月31日仍然活着的患者获得了1年的额外生存时间(暂缓的死亡日期:2018年1月31日)而不是后续日期;3)通过最高/最差值和最低/最佳值替换可变ECOG PS中的缺失值而不是避阻值;4)统计起动分析,以将不确定性纳入参考结果的估计汇总效果,以便与现实世界结果进行比较。因此,数据集是由基于计算机的采样(Excel 2010; Microsoft,Redmond,Wa,USA)创建的数据集,从原始观察中替换。重复采样和估计程序重复10 000次,从而提供EE因子的分布,其具有基于百分位的置信区间。
结果
在2008-2014年期间,通过Care for Outcome注册,我们确定了2989名IV期非小细胞肺癌患者。排除7名生命状态“移民”的患者后,最终样本量为2982例。在这些患者中,1214人(41%)接受了一线全身治疗。表格1概述每个方案和总体的基线患者特征。平均年龄为63岁;54%的所有患者的CCI为0(无可用性),大多数(84%)患者在诊断时有0或1的ECOG PS(5%缺失数据)。最常接受的化疗方案是顺铂 - 培养基(1214名患者中的347(29%)),其次是顺铂 - 吉西他滨(n = 214,18%)和卡铂 - 戊酰基(n = 213,18%)。表皮生长因子受体抑制剂(Gefitinib和Erlotinib)被5%的患者使用。总体而言,八个方案负责应用的一线治疗中的92%(n = 1122名患者)。
对于所有方案,真实环境中的中位OS都比临床试验参考OS短(表2.),根据方案,从1.3到77个月的范围内。总体而言,EE因子的分布与1.00的假设中值显着不同(EE因子0.77,95%CI 0.0.85; P <0.001),并且所有个体治疗方案的中位数因子<1.00(图1).
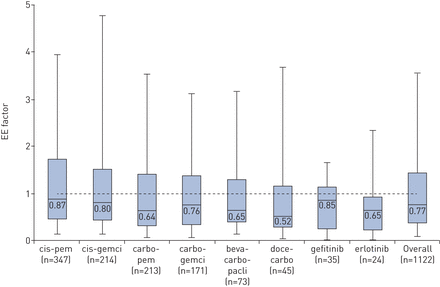
基于单程全面治疗开始日期的疗效效率(EE)因子的分布。对于所有方案,中值EE因子与试验值1.0(一种样品WILCOXON签名试验)显着不同,P <0.05的p值。CIS:顺铂;PEM:Pemetrexed;Gemci:吉西滨;Carbo:Carboplatin;Beva:Bevacizumab;帕里西:紫杉醇;doce:docetaxel。
多变量线性回归分析显示,患者的ECOG PS与EE因子的大小显著相关(B - 0.130, 95% CI - 0.163 -−0.098;p < 0.001)。阴性b值表明ECOG PS较高/较差的患者EE差距较大(0-4类)。ECOG PS为0-1的患者EE差为19% (EE因子0.81,p<0.001), ECOG PS≥2的患者EE差为61% (EE因子0.39,p<0.001;12%, n = 140)。模型中的其他变量(诊断时的年龄、性别、CCI(和单独的共病)、组织学和诊断年份)与EE差距无统计学意义的关联。然而,ECOG PS仅解释了5.2%的EE因子变异。
四种敏感性分析证实了我们的研究结果的稳健性。独立于如何计算真实世界操作系统,试验结果存在显着分歧(基于诊断日期的EE因子为0.89(P <0.001),以及基于全身治疗的开始日期的EE因子减去14 days was 0.82 (p<0.001)). Furthermore, giving an additional 1 year survival time to patients still alive at January 31, 2017 resulted in a similar significant overall EE gap (EE factor of 0.77, p<0.001). Replacing missing values in the variable ECOG PS by both the highest/worst value (PS 4) and the lowest/best value (PS 0) instead of the imputed value did not change the finding that ECOG PS is associated with the magnitude of the EE factor (B −0.083, p<0.001 and B −0.126, p<0.001, respectively). Finally, the EE factors per chemotherapy regimen derived from the bootstrap analysis agreed very closely with the ones derived from the main statistical analysis; the same regimens appeared to have a statistical significant EE gap and the largest (although small) difference was for gefitinib (absolute difference of 0.03 between the original and the bootstrapped EE factor).
在现实世界中,患者完成治疗计划的频率低于临床试验(56%)与61%, p=0.024),与临床试验患者(34%)相比,现实世界中接受后续化疗的患者更少(34%)与46%, p < 0.001) (表3).卡铂-吉西他滨的剂量减少水平高达39% (网上补充附录3).总体而言,12%的患者(n=131)因毒性而改用其他方案。通过将“早期停药(<4个周期)”和“后续化疗线”等变量加入到EE因子的预后模型中,模型的解释效果提高到35%。
讨论
该研究显示,在接受一线全身治疗的转移性NSCLC患者中,实际操作的中位OS比临床试验短近1 / 4 (EE因子0.77,p<0.001)。
为我们的知识,这是第一项研究,了解不同全身治疗(化疗和靶向治疗)在大型未选择的转移性NSCLC患者中的疗效效率差距的完全概述。我们观察到的减少效果的恒定模式增加了结论,即不管系统治疗方案如何存在差距是一般现象。它也存在于有针对性的疗法。
我们研究中发现的EE差距的大小符合先前对常规护理的研究与转移NSCLC中特定方案的试验。Z.胡等.[5]在IV阶段NSCLC患者常规实践中观察到Bevacizumab-Carboplatin-PACLitaxel中位数生存估计为9.7个月与ECOG 4599试验中的参与者中位生存率为12.3个月(相当于0.79的EE因数)。研究的研究heikh和C哈姆伯尔斯[7[临床实践中,患有Erlotinib的先进/转移性NMSCLC的二线治疗晚期治疗5.2个月,而参考临床试验报告了6.7个月(EE因子0.78)的中位OS。
在先前关于高级NSCLC中的预后因素的研究中,ECOG PS已被证明是一个重要的独立预后参数[11.].eCOGPS≥2的患者通常占患有先进疾病的一线治疗试验的一小部分患者,但当进行基于人口的调查时,代表比例显着更高(高达30-40%)[11.].然而,在我们的研究人群中,ECOG PS≥2的患者比例仅为12.5%,与我们meta分析的临床试验(15%)没有太大差异。这意味着,尽管我们的数据证实,行为状态是较差的生存结果的预后因素,但这可能不是观察到的情感表达差异的唯一驱动因素。因此,与临床试验相比,它需要与现实世界中更糟糕的结果相关,也需要与现实世界中更普遍的结果相关。这意味着还有其他因素在起作用。从我们的数据中可以得出两种可能的解释:在现实生活中,接受后续治疗的患者的频率较低,在真实人群中,完成4个或4个以上周期的患者比例更低(添加这两项测量将模型的解释效果从5%提高到35%)。这些措施可能反映了共病的差异,影响了在试验中对更积极的患者进行全身治疗和/或选择的活力。关于共病,在我们的数据集中,我们没有观察到早期停止或未停止全身治疗的患者之间的频率差异(网上补充附录3,表S11).然而,我们承认现有的共病数据在某种程度上是颗粒状的(例如慢性阻塞性肺疾病(COPD)是/否而不是COPD阶段),并且合并列表是有限的。后者由方差分析结果支持,表明涉及其他未测量的因素。与EE差距相关的其他因素是临床试验的许多排除标准,参与临床试验本身是有益的(Hawthorne Effect [12.])。不幸的是,这些因素无法在本项目中进一步评估,因为在Care for Outcome注册中没有所需的数据,也没有相应临床试验所需的个体患者水平数据。
本研究的强度是,它基于荷兰诊断阶段IV NSCLC阶段的大型未选择性患者,提供大多数应用全身治疗方案及其在西欧国家的结果,具有高标准水平卫生保健。此外,我们捕获了一个时间框架> 7年,从而降低了临时因素的偏见风险。最后,本研究基于高分辨率数据。结果注册表的护理包括具有非常低数量的缺失值(只有5%缺失数据的变量)的详细和验证的患者数据。
对这项研究的限制可能是我们计算真实世界操作系统的方法。由于大多数临床试验从随机化的日期计算OS,因此我们基于第一药物管理日期的计算具有低估OS的风险。但是,对我们对此事的敏感性分析确认我们的主要结论是令人放心的。此外,人们可以争论我们的方法,以比较现实世界和临床试验之间的中位操作系统。替代方法可能是基于危险比的方法,但我们认为这是不可行的,因为在提取来自发布论文的必要的代理数据时,各个患者数据和其他几种方法缺点的不可用的不可用。13.].关于不能在我们的方法中检查患者的后果,我们认为潜在的偏倚风险相当小,因为在随访时间结束时,队列中只有4%的人仍然活着。我们基于这些患者不同的估算死亡日期进行的第二次敏感性分析也证实了其没有任何实质性影响。第三,来自临床试验的参考中位数OS可能被高估,因为几乎所有纳入meta分析的试验都允许IIIB期患者。然而,将10%的IIIB期患者>排除在meta分析之外的试验,仅导致参考结果的很小变化,对EE因素的计算也几乎没有影响(总体为0.75,p<0.001)。最后,我们的研究结果的外部有效性可能会因最近引入的新治疗方案而改变(例如在研究中未涵盖的免疫疗法和其他有针对性的疗法。然而,目前,绝大多数患者接受了我们项目中学的一项方案。因此,我们的调查结果有可能通过对谈话中的真实效力数据进行洞察力来改善共享决策。例如,数据可用于通知男性患者与ECOG PS 1计划开始四个循环的顺铂-PemetRexed,他的操作系统可能比临床试验报告中的10周短,并且在他身上之前的患者完成了60%的病例中的四个周期。
总之,我们的结果表明,在现实生活中接受治疗的患者的生存期比临床试验的患者短近四分之一。有效性降低的持续模式表明,这种差距的存在是一种普遍现象,与系统治疗方案的类型无关。患者的表现状态、更早的停药和更少的后续治疗是造成这种差异的部分原因。临床决策应该更牢固地建立在真实世界的结果基础上。
补充材料
致谢
作者感谢M. van Hulst(荷兰格罗宁根Martini医院),M.J. Deenen(荷兰埃因霍温Catharina医院),S.F. Oude Wesselink (Enschede medich Spectrum Twente,荷兰),E.A.F. Haak (OLVG,荷兰阿姆斯特丹)和J. van der Mee (Nijmegen Canisius Wilhelmina医院,荷兰)。荷兰),感谢他们为完成和验证医院药房数据所做的努力。此外,我们感谢R.H.H. Groenwold(乌得勒支大学医学中心,荷兰)在引导程序方面的帮助,以及C. Sloof(乌得勒支圣安东尼奥斯医院/Nieuwegein,荷兰)在文献搜索方面的帮助。没有人因为这些贡献而得到经济补偿。
脚注
这篇文章有补充资料可从www.qdcxjkg.com.
Santeon NSCLC研究组(合作者)是:A.J.Polman,Medisch Spectrum Twente,荷兰Enschede;B.E.E.M.van den forne,Catharina医院,荷兰埃因霍温;J.W.G.Van Putten,Martini医院,格罗宁根,荷兰;A.A.J.SMIT,OLVG,阿姆斯特丹,荷兰;A. Termeer,Canisius Wilhelmina医院,Nijmegen,荷兰。
作者贡献:E.M.W. van de Garde、F.M.N.H. Schramel和H.J.M. Groen获得了研究资金。C.M. Cramer-van der Welle、E.M.W. van de Garde、B.J.M. Peters、F.M.N.H. Schramel和H.J.M. Groen参与了概念和研究设计。e。m。w。van de Garde为研究监督做出了贡献。C.M. Cramer-van der Welle、B.J.M. Peters、E.M.W. van de Garde和O.H. Klungel负责数据分析和解释。C.M. Cramer-van der Welle和B.J.M. Peters负责手稿的准备和撰写。所有的作者贡献了手稿,并批准了最终的手稿。
利益冲突:B.M.M.彼得没有任何披露。厘米。Cramer-van der Welle无需披露。
利益冲突:F.M.N.H. Schramel没有什么可披露的。
利益冲突:O.H. Klungel报告了葛兰素史克的拨款,在提交的工作之外。
利益冲突:H.M.M.Groen报告费用(支付给机构),用于BMS,Roche,Novartis,Merck和Pfizer的咨询工作,以及来自所提交的工作之外的Boehringer-Ingelheim的机构补助金。
利益冲突:e.m.w。在研究期间,Van De Garde报道了荷兰癌症协会和罗氏荷兰BV的赠款。
支持声明:本研究得到了荷兰癌症协会(批准号SAN2016-7942)的支持。本文的资金信息已存入CrossRef Resder注册表.
- 已收到2018年6月12日。
- 接受2018年10月13日。
- 版权©2018人队。
本文是开放式访问,并根据创意公约188滚球软件归因非商业许可证4.0的条款分发。















