抽象
一种可能用于治疗阻塞性睡眠呼吸暂停(OSA)的精确药物方法包括对选定的患者使用补充吸入氧来针对通气不稳定(循环增益升高)。在这里,我们测试通过临床多导睡眠图量化的环路增益升高和三个关键的内表型特征(溃散性、补偿性和觉醒性)是否可以预测补充氧气对OSA严重程度的影响。
36例(呼吸暂停-低呼吸指数(AHI) >20例)-1)完成补充氧气两个通宵多导睡眠图的研究(单盲随机对照交叉)(40%的启发)与假(空气)。OSA性状从空中夜多导睡眠图量化。应答通过在一个AHI≥50%减少(仰卧非快速眼动)所定义。次要终点包括血压和自我报告的睡眠质量。
九的36例(25%)对补充氧气(ΔAHI = 72±5%)。升高的环路增益不是反应者/非反应者状态的显著单变量预测因子(初步分析)。在事后分析,基于提高环路增益和其他特性(更好的可折叠性和补偿性;交叉验证的准确性为83%(交叉验证前为89%);预测反应表现出改善阻塞性睡眠呼吸暂停综合症的严重程度(ΔAHI 59±6%与在预测非应答者12±7%,p值= 0.0001)加降低血压晨和“更好的”自我报告的睡眠。
阻塞性睡眠呼吸暂停患者对辅助供氧有反应,可以通过多导睡眠描记术测量其鼻内型特征来识别。
抽象
的阻塞性睡眠呼吸暂停谁从稳定具有补充氧气的治疗通气控制受益的亚组可以通过从常规诊断睡眠研究估计病理生理学机制被识别http://ow.ly/yeVp30lewG4
介绍
周围的诊断患有阻塞性睡眠呼吸暂停(OSA)患者一半当前未处理的或非粘附到持续气道正压(CPAP)[1,2]。因此,我们需要新的治疗OSA的方法。在过去的几年里,个性化的OSA治疗的概念出现了,基于这样一种观点,即当OSA干预与患者的潜在病理生理学或“内表型”相匹配时,其影响最大[3-7]。这一概念的核心是人们认识到,OSA的出现是由于不同个体的不同内鼻型特征,即1)咽部塌陷增加,2)通气控制稳定性降低(环路增益升高,即一个夸大通气驱动响应于降低的气流和伴随的缺氧/高碳酸血症),3)减少呼吸唤醒阈值(在通气驱动小升终止睡眠)和4)降低代偿咽扩张肌活化8-11]。
个体化医学临床实施的一个主要障碍是,对导致OSA的特征的评估一直局限于研究实验室[9,12]。为了克服这个障碍,我们最近开发了一种自动评估四个关键特征的技术[13-15]使用常规的临床睡眠研究(多导睡眠图)。
在这项研究中,我们使用多导睡眠描记法对表型的预测价值进行了前瞻性检验,该研究是一种专门用于降低环路增益的治疗方法[16]和显着改进OSA的患者[亚组3]。我们测试了由临床多导睡眠图测量的环路增益升高预测单晚补充氧(40%激发)可优先降低OSA严重程度的主要假设。与随机单盲交叉研究(NCT01751971)。我们还与其他三个特征评估结合高架环路增益的预测值(事后分析)。
方法
参与者
Patients with a previous clinical diagnosis of OSA with an apnoea–hypopnoea index (AHI) >20 events·h-1有资格参加。使用呼吸兴奋剂或镇静剂(包括阿片类和苯二氮卓)患者被排除在外,因为是那些有心脏衰竭或肺部疾病的诊断,那些中央,而不是阻塞性睡眠呼吸暂停(多数中枢性呼吸事件),谁是孕妇。与会者签署知情同意书,并批准由合作伙伴机构审查委员会批准。
我们招收47名学员;8条评论不表现出OSA和三个没有参加第二届一夜,留下36例谁完成了协议(补充图S1)。
程序
患者完成两个通宵多导睡眠图的研究,相隔一周(随机顺序)。补充氧气或医用空气(假)递送通过一个文丘里面罩(40%吸入氧气,约为4 L·min)-1通过一个套管17];参见[3,4])。单盲设计启用实时监控的适当吸入氧水平(O2分析仪17625;VacuMed,美国加州文图拉)。患者主要仰卧睡觉,以减少体位的影响。测定仰卧位血压(Dinamap Pro 100v2;(在安装过程中休息≥1小时,以平卧位休息约10分钟),在除氧/假手术后再次亮灯(约10分钟)。在研究结束时,我们评估了自我报告的睡眠质量(“更好”、“相同”或“更差”)与以前的研究;每天早上打进1,0和-1,分别地)和警觉性(斯坦福嗜睡量表)。
多导睡眠描记术
使用标准临床多导睡眠测量仪器[18]。用鼻压和口鼻热敏电阻评估气流。我们优先记录高质量的鼻压信号。低氧血症的评分基于气流减少30%而无氧饱和度或觉醒标准(补充氧气否则会掩盖低氧血症)。
量化通过多导睡眠的病理生理特点
假夜多导睡眠图来定量使用自动化方法[基线OSA性状13-15] 如下面所描述的。
化学驱
表型特征通过首先估计“通气驱动”来量化,即预期通气,使用化学反射反馈控制模型(增益、反应时间、延迟、觉醒反应)符合通气数据[13]。简单地说,鼻压(平方根转换)提供了一种通气性流量代理,可集成产生呼吸-呼吸通气信号(未校准的潮气量乘以呼吸速率,平均正常化)。确定包含≥1个呼吸事件的7分钟窗口(非快速眼动(REM)),估计的通气驱动力(模型输出)最适合阻塞性事件之间(气道通畅时)的通气信号。
环路增益
对于每个窗口,循环增益由反馈模型计算;中位数用来代表夜晚[13]。两个参数进行量化:LG1(先天的predictor) is the ventilatory drive response to a 1 cycle·min-1减少通风及反映“超敏反应”(例如增加敏感性或降低的肺体积)。LGñ量化“不稳定性”,也包括循环延迟效应(LG)ñ>1.0产生周期性中央呼吸暂停)[3,19]。
兴奋阈值
觉醒阈取作中值估计通气驱动前述刻痕脑波觉醒[15]。
对治疗反应的定义
患者被认为是“反应”,如果他们的AHI减少了≥50%与治疗与假(先天的标准);患者除了认为“无反应者”。[Responses were considered “complete” if the AHI was also <15 events·h-1治疗[4,相当于在我们的人口中减少67%的AHI。如果无反应者表现出33%的AHI >降低,则被认为是“边缘性”。
预测值的评估
基于是否有在AHI降低的显著差异环路增益和其他性状的预测值进行了评估(作为基线值的百分比)定义的“预测的应答者”之间和“预测的非响应者”亚组(例如高与低环路增益)。预先指定的环路增益参数(LG)1)及截幅为0.7 (即定义高的门槛与LG低1)是基于现有的研究结果[13]。对所有事后子组的分类试验,包括多变量分析(见下文),选择临界值,以使灵敏度最大化加特异性[20.]。预测价值使用留一法交叉验证,其中每个受试者的响应是使用与对象的自己的数据相同的模型漏掉的修改版本的预测估计。
多变量模型分析
我们使用了使用表型变量的逻辑回归,即环路增益,溃散,唤醒阈值和肌肉补偿,以限定预测应答者的子组和预测的非应答者;二次模型,其中包括相互作用项和平方项基于交互的明确证据选择。条款使用向后消除(对去除的= 0.157)[选择21]。为了提高统计能力,我们纳入了之前一项使用补充氧(n=20)的研究的训练数据,以帮助建立一个更稳健的回归模型[4];预测值的患者在当前的研究中(独家报道补充材料)。
统计分析
非配对t-检验或Wilcoxon秩和检验用于比较反应者组之间的差异(与无;预测反应者与预测的非应答者)。对于比例的标准误差(阳性/阴性预测值,即所采用的正态近似二项式分布给出一个正/负预测)正确预测的比例;p值表示从机会价值观的差异。显着性为p <0.05接受。
结果
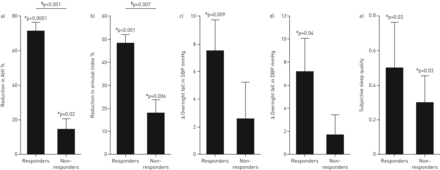
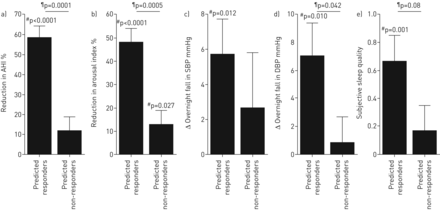
基线特征详见表格1。补充氧降低了AHI,约为30% (补充表S1)被唤醒指数(约25%)的降低所证实。反应者(n=9)的AHI指数降低了~ 70%,从睡眠中惊醒的频率降低了~ 50%,浅睡眠(第一阶段非rem)的时间减少了~ 50%,夜间血压的变化减少了~ 7 mmHg (图1)。这些变化并没有在非应答者(N = 27)进行观察。小号ix of nine responders also had an AHI of <15 events·h-1氧(即完全反应)。总体而言,大多数患者认为他们睡“好”上了氧气晚上(最好:同一个:氧气更糟与空气= 19:9:7)。对主观警觉性没有影响(改变斯坦福嗜睡量表评分:+0.1±0.2个单位,更高的值表示警觉性降低)。
补氧对有反应者(9例)和无反应者(27例)的一级和二级结局的影响。a)在反应者中,观察到呼吸暂停-低呼吸指数(AHI)的改善。此外,反应者在b)从睡眠中唤醒的频率(唤醒指数)以及c、d)血压(从晚上到早上的变化)和e)主观睡眠质量方面表现出改善。主观睡眠质量评分:1=睡眠质量较好;0 =睡同样的;−1 =睡更糟。斯坦福嗜睡量表(主观的早晨警觉度,没有显示出来)没有影响。误差线显示SEM。SBP:收缩压;舒张压:舒张压。#:氧与虚假的;¶:急救员与无。
环增益和氧气反应
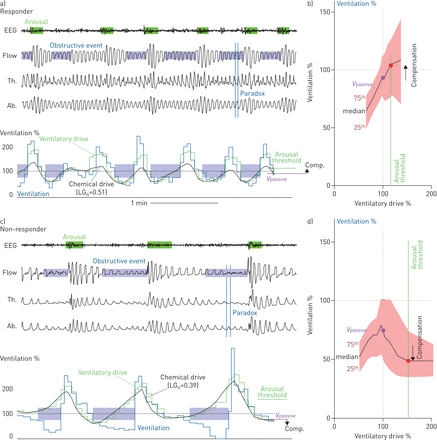
示例测量在一个响应和一个非响应显示图2。相反,我们的主要假设,升高的基线环路增益不具有补充氧气的对治疗的反应(还原%在AHI的显著单变量预测因子与假),即有患者之间的响应具有较高的无差异与基于LG较低的环路增益1(35.7±6.6%与25.2±9.0%,P = 0.4;预先指定的截止= 0.7;补充图S2)。然而,有对基于LG更高的环路增益在那些更大的响应走势强劲ñ(图3)。
例如,a、b、a应答者(假性呼吸暂停-低呼吸指数(AHI)=44.9,治疗AHI=9.7事件·h)的治疗内表型数据-1和c、d)无反应者(假AHI=42.8,治疗AHI=45.2事件·h-1)。a, c)睡眠呼吸暂停的说明性痕迹和通气性驱力的模型估计。注意,主题中的事件是自相似的。在应答者中,通气轨迹的变化估计了阻塞性事件期间的通气驱动力。相比之下,在无反应者中,通气量随着通气量的上升而下降。在通气驱动的模型估计中,注意到胸(Th.)和腹部(Ab.)偏移(压电式呼吸带)信号在两个受试者事件期间相位不一致(矛盾),与气流阻塞一致。通风和通气性驱动被表示为窗口平均通风的比例(“eupnoea”)。估计通气驱动(绿线)分为化学驱动(chemoreflex,即环路增益(LGñ以及对觉醒的通气性反应(觉醒贡献,绿线减去黑线)。b、d)通风系统总用地(即实际气流)与通气驱动(即(黑线:中位数;材质:四分位范围)。反应者环路增益较高,觉醒前通气驱动(觉醒阈值)较低,从正常通气驱动下较高的通气水平推断出的塌陷程度较轻(V被动)。脑电图:脑电图;流动:平方根变换鼻腔压力;比较:补偿。
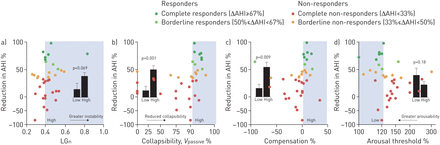
造成阻塞性睡眠呼吸暂停endophenotypic性状的预测值。一)环路增益(LGñ)表示通气不稳定,即易感性自发周期性呼吸。B)陷(V被动), c)补偿和d)觉醒阈值数据以eupnoeic水平的比例表示。详情见正文。阴影说明了预测响应的区域和高的定义与每个特征子组都很低。条形图显示治疗后呼吸暂停-低呼吸指数(AHI)的降低与低子组(意味着±SEM中,患者被分配给使用交叉验证子组)。请注意Y轴比例被压缩低于零,以便高于零值的视觉解释。各性状有显著阴性预测值:LGñ(降低AHI:37.6±6.9%与14.0±11.5%;阳性预测值(PPV)=35±10%,p=0.3;阴性预测值(NPV)=92±7%,p=0.02;V被动(49.3±6.9%与10.9±8.1%;PPV = 47±12%,p = 0.07;净现值= 95±5%,p < 0.001);补偿(53.0±8.9%与18.5±7.2%;PPV = 55±15%,p = 0.049;净现值= 88±6%,p = 0.046);兴奋阈值(39.7±12.8%与22.2±6.0%;PPV = 50±13%,p = 0.06;净现值= 91±6%,p = 0.009)。
其他生理特性和对氧的反应
减少溃散(高V被动)和更多的补偿性是对氧气反应的强有力的预测因子,并且在低唤醒阈值(图3)。
多变量模型分析
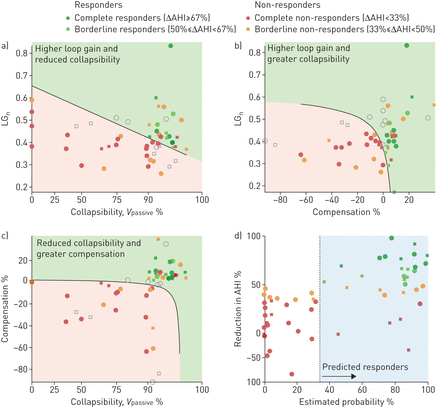
当综合考虑特征时(多变量logistic回归),更高的循环增益增加了成为反应者的可能性,特别是在补偿更好的患者中;较差的补偿和较差的可折叠性降低了成为响应者的可能性(表2,图4;另请参阅补充表S2,补充图S3)。整个回归模型表现出优秀的预测价值(ΔAHI预测反应者与预测的非应答者:62±5%与10±7%,P <0.0001;阳性预测值(PPV)= 69±13%,p值= 0.0005;阴性预测值(NPV)= 100±0%,P <0.0001;精度= 89±5%,P <0.0001);后交叉验证结果仍然强劲(ΔAHI= 58±6%与12±7%,P = 0.0001;PPV = 62±13%,p值= 0.007;NPV = 96±4%,P <0.0001;精度= 83±6%,p值= 0.0002)。
在预测应答次要终点
预测应答者(交叉验证的结果)显示出与觉醒指数,血压和主观睡眠质量的改善氧(睡得更好,相同或氧恶化与空气)对在预测非应答者观察到的(图5)。斯坦福困倦量表的评分在两个亚组中没有变化。
关于患者的病理生理学合适的伯和仲结局的补充氧气的效果,即“预测反应者”(n=13)和病理生理学不合适的患者,即“预测的非应答者”(N = 23),基于endophenotypic性状(逻辑回归,交叉验证;表2,图4)。一)在预测的应答者,治疗导致阻塞性睡眠呼吸暂停的严重程度(减少呼吸暂停 - 低通气指数(AHI))的改进;对比图1的,预测的应答者和非应答者之间的差异不是“通过定义”,因为亚组使用来自其他主题仅数据(指定即交叉验证)。预测应答者也b中展出的改进)从睡眠,C,d)血压(晚间减去上午水平)和e)主观睡眠质量觉醒的频率。主观睡眠质量评分:1=睡眠质量较好;0 =睡同样的;−1 =睡更糟。有在任一组(未显示主观早晨的警觉性,)在斯坦福嗜睡量表没有影响。SBP:收缩压;舒张压:舒张压。#:氧与虚假的;¶:急救员与无。比较的结果图1。
非生理变量的预测值
Predicted responder/non-responder status based on patients’ pathophysiology remained significantly associated with responses to oxygen (p=0.002–0.003) after adjusting for common clinical factors (age, sex, body mass index, neck circumference, current CPAP use and AHI off treatment; logistic regression with covariates added separately;补充图S4)。这些临床因素不是重要的预测因素。
讨论
目前的研究表明,使用定量诊断多导睡眠OSA患者的病理生理特点可以识别患者的病情很可能是可治疗的使用补充氧气,并能排除非应答。反观我们具体的假设,高架环路增益独显不应对氧气的一个强有力的预测。相反,在具有更大的咽通畅(不太严重的溃散和更大的补偿)组合升高环路增益预测改进的OSA;将合并的多变量模型准确地排除了对治疗(95%确定性)的积极响应,并确定了预测的应答者谁1)具有减半呼吸事件的频率和充分治疗OSA的46%的可能性的62%的可能性的子组(一个HI<15 events·h-1),和2)经历了早晨血压降低显著(相对于晚间值)和自我报告的睡眠质量的提高(比睡上一夜没有更好的治疗)。我们的研究表明,测量并结合睡眠呼吸暂停的关键endophenotypic原因的基础上,日常睡眠研究,提供了洞察响应干预,并打开个性化基于底层机制干预的大门。
生理洞察
高架环路增益
基于环路增益较高的患者在降低环路增益和改善阻塞性睡眠呼吸暂停(OSA)方面的作用范围最大的观点,我们假设环路增益较高的患者可以预测通过补充氧气降低环路增益的反应。例如,许多形式的中枢睡眠呼吸暂停,一种高环路增益的情况,可以通过补充氧气得到有效治疗[22,23]。此外,我们之前对OSA的研究(n=12)发现,高氧对患者更有效与较低的环路增益[3,13]。然而,在这里,我们发现单靠环路增益是不足以预测到补充氧气的反应,证实最近的研究说明该环路增益(或敏感性)本身不是强相关的(甚至是负相关[24通过降低环路增益的治疗降低OSA的严重程度(例如氧,乙酰唑胺)4,6,25]。目前的研究表明,成功地针对一种异常的病理生理特征来治疗OSA,不仅需要了解这一特征本身,还需要了解OSA的其他决定因素。
大咽开放
重要的是,我们的研究表明,更严重的咽塌陷和肌肉差补偿规则进行了积极的OSA响应补充氧气(使用多导睡眠图测量)。这些发现与OSA病理生理相一致;谁同时拥有高环路增益,并降低呼吸道通畅患者将继续减少通畅一旦环路增益降低,促进残留OSA无论有多高的环路增益在基线[4,16]。
基线严重阻塞性睡眠呼吸暂停综合症
[Remarkably, in the nine responders (25% of patients), oxygen lowered the AHI from an average of 57 to 18 events·h-1(约70%减少),说明即使在严重的阻塞性睡眠呼吸暂停(OSA)患者中,补充氧也有很大的影响。反应者在基线时没有轻度睡眠呼吸暂停,即较低的你好。因此,OSA的严重程度不太可能对临床决定使用降低循环收益的干预措施(表格1,补充表S1,补充图S4)。
排除与裁决
多导睡眠图表型分析准确地排除了对补充氧(高NPV)没有反应的患者,但在判断对治疗有反应的患者方面有些不准确。因此,一个具有适当病理生理的病人是否会对治疗产生积极的反应仍不确定。一个更确定的结果可能需要干预也能持续成功地改善患者的病理生理学(降低循环增益),但这种改善的程度差异很大[3,4,13,25]。无论如何,通过排除明确的无反应者,我们的方法有可能使临床医生和研究人员限制未来对病理生理学最有利的OSA患者亚组的补充氧(或其他降低环路增益的药物)试验。
临床意义
OSA患者中的大部分不能耐受CPAP的,并补充氧气目前用作OSA一个抢救治疗主要是为了保持夜间氧合作用。在未选择的患者中,氧合的改进是一致的,但在OSA的改进是温和的(在AHI减少~10-30%)[3,6,27-31];在一些个人,氧气甚至可能增加OSA严重性(图2-五)。然而,在患者的一组特定的表型性状,补充氧气可以具有临床相关的效应(>在AHI减少50%;图4和五)。此外,最近的一次试验表明,坚持补充氧气,而不完善,优于CPAP [27],提示补充氧气可以在这些个体被良好耐受的。
我们识别可能的反应方法是量化使用临床睡眠研究,并且不需要侵入性的设备或气道正压操作,并完全自动化的技术引起OSA的病理生理特征。因此,我们的方法可以很容易地在临床环境中实现。
具体的四个特征回归模型(图4)是根据现有资料(事后),使用留一法交叉验证方法,这使得有效地利用有限的数据的测试。我们强调,我们的具体型号需要确认通过前瞻性试验,最好是较长治疗期,以确认临床效用。因为我们的发现与生理学原理相一致,我们相信重现性的可能性很高。
我们的研究也提供了原则的证据,即有可能更普遍地识别出OSA患者对降低环路收益的治疗有反应。我们希望我们的结果也能用于预测当前和未来针对环路增益的OSA干预的反应,例如乙酰唑胺(25], H2年代抑制剂(32]和嘌呤拮抗剂33]。相结合的非侵入性特质测量的一般方法也可以帮助预测其他疗法,如咽部手术反应[34,35]。需要沿着这些路线的进一步调查。
方法论的注意事项
在目前的研究中,研究对象在一个晚上的补充氧治疗。因此,随着时间的推移,OSA严重程度可能的额外改善没有被发现[26,36]。然而,现有数据表明,氧气对OSA严重程度超出第一晚效应在OSA的严重程度没有大的影响,并观察到的改进立即中断治疗逆转[30.]。尽管如此,仍有必要进行长期研究,以检验氧气对预测反应者的OSA症状和血压的影响。为了科学的准确性,我们通过文丘里罩以中等浓度(40%激发,约为4 L·min)给氧-1通过鼻套管)中,在一个水平先前使用[3,4]。因此,我们1)避免了鼻插管气流测量和氧气/假手术给药之间的干扰,2)避免了可能影响患者致盲和减少最佳治疗夜晚的比例的滴定程序,3)尽量减少可能影响亚组间疗效评估的剂量差异。
我们解释了我们的多特征模型的结果(包括高环路增益和较轻的塌陷),作为证据,有一个可识别的患者亚群优先对氧疗作出反应。我们还考虑了这种表现型可能仅仅是一种较轻的OSA(尽管以前没有根据AHI或其他多导睡眠测量方法识别),这可能更容易治疗一般的OSA干预类型。虽然需要进一步的研究来证明氧治疗的特异性,但现有的证据反驳了这一观点。首先,预测反应者亚组在血压和自我报告的睡眠质量方面表现出选择性的改善,这表明OSA的反应者表型在临床上显得很重要,即是不平凡的。其次,使用多导睡眠测量更高的环路增益已被证明预测非应答者咽部手术,示出了在氧应答表型的高环路增益的贡献是不容易性治疗OSA的生物标记[35]。第三,我们最近的数据表明,较高的环路增益和不太严重的塌陷(氧应答表型)预测,口腔矫治器治疗失败[37,表明氧反应者可能对其他疗法没有反应;的确是高环路增益通过CPAP操作还预测口腔矫治器无反应[五]。研究正在进行进一步调查这个问题(NCT03189173)。
我们注意到,在从常规的多导睡眠监测当前的研究中获得的生理特征值是代理人,并可能从与专业生理学实验室中使用侵入性的“黄金标准”的措施获得的不同。然而,我们的措施相媲美金标准值(相关系数~0.7各性状)13-15]。
主要结果变量是AHI在仰卧非REM睡眠测量,呼吸事件使用改性条件的所述氧饱和度信号来避免依赖(呼吸事件需要在气流减少≥30%)评分。使用标准的标准得分呼吸事件,或包含所有睡眠状态和位置(与≥3%饱和或觉醒流量减少≥30%),产生类似的结果(补充表S1)。
患者仰卧睡,因为在最坏的情况,这会捕获OSA病理生理;治疗后外侧OSA的无机械干预将是一个不太艰巨的挑战。在一个病人谁睡完全横向,我们认为没有理由,同样的特质,同时横向也不会预测到氧疗也侧卧位响应。进一步的测试是必要的。
结论
我们首次证明,通过临床睡眠研究(非治疗)测量引起OSA的病理生理变量,可以预测哪些患者最适合补充氧治疗。一个多变量模型将增加的环路增益和改善的气道(更好的折叠性和补偿性)准确地预测了对治疗的反应者:预测的反应者不仅表现出OSA严重程度的改善,而且在血压和睡眠质量感知方面也有改善。我们认为,这种方式的表型将为无法耐受CPAP并可能继续治疗的患者提供个性化干预手段。
补充材料
脚注
这篇文章有补充材料可从www.qdcxjkg.com
本研究注册于ClinicalTrials.gov标识号NCT01751971。如有要求,将向合格的科学家提供数据。
作者投稿:概念与设计:S.A.金沙,学士学位爱德华兹,P.I.特里尔,A.马尔霍特拉,A威尔曼。方法开发:S.A.金沙,P.I.特里尔,A Azarbarzin。数据收集:S.A.金沙,学士学位爱德华兹,C.M。德梅洛,E.T.Smales。分析:S.A.金沙,L.B. Hess. All authors interpreted data, edited the manuscript for important intellectual content and approved the final draft.
利益冲突:S.A.金沙研究进行期间报告从NIH和AHA,补助金;从剑桥声音管理,NOX医疗默克,外提交作品的个人费用。
利益冲突:爱德华兹学士在研究期间从澳大利亚心脏基金会领取薪水。
利益冲突:P.I.特里尔在研究进行期间报告从澳大利亚国家卫生和医学研究理事会(1064163),补助金;从赫尔家庭捐赠,2014年,外提交的作品补助。
利益冲突:J.P.巴特勒有没有透露。
利益冲突:R.L.欧文斯从瑞思迈和伊塔马尔医疗,外面的工作提交报告从诺华公司的顾问个人的费用,以及酬金及差旅费。
利益冲突:L. Taranto-Montemurro报告了来自美国心脏协会的拨款,来自诺维恩制药公司和剑桥声音管理公司的个人费用,以及Apnimed提交的作品之外的其他费用。
利益冲突:A.阿扎巴津没有什么可透露的。
利益冲突:马奎斯没有什么可透露的。
利益冲突:L.B.赫斯没有透露。
利益冲突:E.T.Smales有没有透露。
利益冲突:C.M.德梅洛有没有透露。
利益冲突:D.P. White报告了来自飞利浦呼吸科(首席科学官)的个人费用,来自Night Balance的个人咨询费用,以及Apnicure(前首席医疗官)的个人费用。
利益冲突:A.马尔霍特拉放弃所有外个人收入在2012年的美国胸科协会的官员。瑞思迈支持睡眠中心提供的慈善捐赠给大学圣地亚哥分校。
利益冲突:A. Wellman报告了国家卫生研究院和飞利浦呼吸器在进行研究期间的拨款;来自Varnum睡眠和呼吸解决方案和剑桥声音管理的拨款,以及来自Bayer和Nox医疗的个人费用,在提交的作品之外;此外,a . Wellman公司还专利发布了气道和气流因子。
支持声明:这项工作由美国心脏协会(15SDG25890059 to S.A. Sands)、美国国家卫生研究院(R01HL102321, R01HL128658, P01HL094307和P01HL095491 to A. Wellman和S.A. Sands)、澳大利亚国家卫生和医学研究委员会(1053201 to S.A. Sands;1035115至学士爱德华兹;以及P.I. Terrill, S.A. Sands, A. Wellman和b.s. Edwards)、R.G. Menzies基金会(S.A. Sands)、美国胸科学会基金会(S.A. Sands)和澳大利亚心脏基金会(Future Leader Fellowship 101167;文学士学位爱德华兹)。A. Malhotra, NIH R01HL085188、K24HL132105和T32HL134632首席研究员,R21HL121794、R01HL119201和R01HL081823联合研究员。这项工作也得到了哈佛催化剂(国家研究资源中心和国家转化科学推进中心,NIH奖励UL1TR001102)的支持。本文的资助信息存储在Crossref资助人注册表中。
- 收到了2018年4月9日。
- 公认2018年7月29日。
- 版权©2018人队