摘要
特发性肺纤维化(Idiopathic pulmonary fibrosis, IPF)是一种致命的疾病,会降低预期寿命,对现有治疗反应有限。吡非尼酮已被批准用于治疗IPF,但对吡非尼酮给药后肺内发生的明显代谢变化知之甚少。
在此,我们使用高分辨率定量基质辅助激光解吸/电离傅立叶变换离子回旋共振质谱成像(MALDI-FTICR-MSI)进行了概念验证研究,以同时进行检测、显示和定量原位在小鼠的肺源性和外源性代谢物进行实验纤维化和人类IPF患者,并评估吡非尼酮治疗对代谢物水平的影响。
代谢途径分析和内源性代谢物的定量显示,吡非尼酮治疗还原氧化还原失衡和糖酵解在IPF组织,并且下调抗坏血酸和aldarate代谢,从而可能有助于原位胶原处理的调制。因此,我们检测到的代谢物途径特异性改变纤维化和,重要的是,代谢校准以下吡非尼酮治疗。
总之,这些结果凸显高分辨率MALDI-FTICR-MSI的适用性破译吡非尼酮的治疗效果,并提供吡非尼酮治疗期间发生的代谢变化进行了初步分析体内。因此,这些数据可能会有助于改善对IPF目前可用的治疗方法。
摘要
MALDI-FTICR质谱成像检测吡非尼酮在纤维化pharmacometabolic效果http://ow.ly/zKee30l1tNs
介绍
特发性肺纤维化(IPF)是一种慢性进行性和弥漫性实质性肺病,导致器官功能丧失。IPF的特征在于替换肺实质与纤维化组织,成纤维细胞异常-肌成纤维细胞的活化,上皮细胞增生和损伤,以及免疫失调[的1]。IPF被认为是一种无法治愈的致命疾病,中位生存期为2至3年,比许多癌症更糟。
吡非尼酮(5-甲基-1-苯基-2-(1H) - 吡啶酮)是口服活性的吡啶分子,其表现出抗纤维化和抗炎活性[2,3.]。它被批准用于治疗IPF全世界,包括欧盟和美国,在那里它是批准用于IPF患者使用[两种药物一个4]。尽管吡非尼酮用于治疗IPF的第一线药物[5],它的作用的确切机制尚未阐明迄今为止[6]。在此,为了更好地指导IPF的治疗,我们试图更好地了解吡非尼酮活性的具体机制。
原位代谢物成像是已精制通过超灵敏和高分辨率定量基质辅助激光解吸/电离质谱成像(MALDI-MSI)高通量,非靶向代谢物组学的技术,用傅里叶变换离子回旋共振(FTICR)与轨道阱[7- - - - - -11]。大质量分辨率MALDI-MSI使空间分布的同时映射对于宽范围的低分子量代谢物,包括中央代谢途径的代谢产物,氧化还原相关的代谢物,核苷酸衍生物,脂质和氨基酸,直接在形态上完整的组织部分。MALDI-MSI质谱通过测量以预定的光栅点横跨组织切片,从而产生二维分布图对每个测量分子获取[12,13]。因此,MALDI-MSI允许获得细胞表达谱,同时保持细胞和分子的完整性。这项技术擅长于成像组织特征内分子的空间组织[14],并能描述几个功能不同的通路的分子相互作用网络[15]。
IPF发病机制的代谢变化,特别是患者对药物治疗的特异性反应,仍然知之甚少。最近对IPF的液体代谢组学研究报道了几种中断的途径,包括鞘脂代谢、糖酵解、三羧酸(TCA)循环、精氨酸代谢、ATP、谷胱甘肽生物合成和鸟氨酸氨基转移酶[16,17]。我们最近报道说,高分辨率MALDI-FTICR-MSI可准确检测健康小鼠组织中的分布和吡非尼酮和吡非尼酮相关的代谢物(5-羟甲基吡非尼酮和5-羧基吡非尼酮)的药代动力学。值得注意的是,在这项研究中,我们没有观察到吡非尼酮,或其代谢产物的一贯作用,对已知的代谢途径[18]。
在这里,探讨肺纤维化时吡非尼酮治疗的内源性代谢动力学,我们使用高分辨率的MALDI-FTICR-MSI和基于组织的第一个执行原位初治和吡非尼酮治疗的IPF患者的代谢物成像,以及该疾病的实验性小鼠模型。我们为这项技术的使用提供了一个概念验证,以评估IPF和吡非尼酮治疗的患者发生的动态代谢变化。
材料和方法
肺纤维化的实验小鼠模型
所有动物实验使用8 - 10周龄的雌性C57BL/6N小鼠(查尔斯河实验室,威明顿,马,美国),并按照美国国立卫生研究院的实验室动物护理和使用指南的建议进行。建立小鼠肺纤维化(伦理批准TVA21-12) [19]。Briefly, bleomycin (3 U·kg−1)或PBS气管内施用作为单次剂量。从第7天至14后处理,既博来霉素处理动物和对照动物的一个子集被施用每日口服吡非尼酮(Selleckchem,休斯敦,TX,USA)(补充材料)。所有动物(PBS n = 3时,PBS +吡非尼酮n = 3时,博来霉素,N = 3和博来霉素+吡非尼酮N = 3)处死第14天。
人的肺标本
本研究经医院伦理和大学生物安全委员会在比利时鲁汶。从IPF患者外植的肺组织那名未处理或吡非尼酮下处理,或供体对照,在鲁汶大学(伦理批准ML6385)搜集。用于处理和采样肺标本协议已经详细描述20.]。简单地说,每个肺充气到30厘米的跨肺压力2O,然后放气到10厘米2O的同时在液氮中冷冻蒸气;冷冻的样品储存在-80℃。鲁ngs (IPF n=4, pirfenidone-treated IPF n=3 and donor n=4) were cut into slices 2 cm thick; cores with a diameter of 1.4 cm were excised and processed as described previously [21]。
免疫荧光冷冻组织
将含有冰冻肺切片的载玻片浸泡在2%多聚甲醛中固定5 min,然后用蒸馏水浸泡,然后用吐温20 (Tris-buffered saline, TBS-T)快速冲洗。用3%过氧化氢/蒸馏水溶液(10分钟)浸泡,然后用3%牛血清白蛋白(BSA)/TBS-T缓冲液(20分钟)浸泡,以防止非特异性结合。用型胶原(COL1)抗体(洛克兰免疫化学试剂,波特斯敦,PA,美国)染色,用抗体稀液(Zytomed Systems,德国柏林)稀释(1:50 0)。COL1抗体染色在4℃湿室中过夜。然后用TBS-T和1:50 0稀释的二抗(Alexa Fluor 568 donkey anti-rabbit;用Invitrogen(美国加利福尼亚州卡尔斯巴德市),室温(1小时)在黑暗中孵育。4’,6-二氨基-2-苯基吲哚(1:2500;美国密苏里州圣路易斯的Sigma-Aldrich公司)冲洗1分钟,然后用TBS-T缓冲液冲洗三次。然后将它们覆盖上荧光安装介质(德国汉堡达科),并使用AxioScan进行扫描。Z1数码载玻片扫描仪(Zeiss, Goettingen, Germany),配备20倍放大物镜。
MALDI-FTICR-MSI
内源性代谢的研究中,MALDI-FTICR-MSI(solariX 7T;布鲁克道尔顿,比尔里卡,MA,USA)测量在的质量范围进行米/z1000−在负离子模式下(MH−)在500赫兹的频率,使用50激光枪和70μm的空间分辨率。
吡非尼酮和其相关的代谢产物,5-羟甲基吡非尼酮和5-羧基吡非尼酮的药物成像研究中,MALDI-FTICR-MSI(solariX 7T)中选择的离子(CASI)模式的连续累积中进行。质量选择性四极杆设置为186.1米/z,窗口为130米/z。米ass spectra were acquired with a 70 µm spatial resolution in positive mode, using 100 laser shots, at a frequency of 1 kHz.
代谢物鉴定通过液相色谱 - 质谱和组织MS / MS,和路径分析
如所描述的进行通过液相色谱(LC)-MS靶向代谢物的鉴定[22]。使用组织串联MS对于代谢物鉴定互补实验/ MS分析用MALDI-FTICR-MSI(solariX 7T)使用CASI模式,它允许在四极目标离子选择来执行,并且使用碰撞诱导解离分段。代谢产物被鉴定或估计通过比较MS / MS谱与标准化合物或通过精确质量与数据库匹配,如在别处描述15,22,23]:METLIN(http://metlin.scripps.edu),MassTRIX (http://masstrix3.helmholtz-muenchen.de/masstrix3),元空间(http://annotate.metaspace2020.eu)[24]及人类代谢组数据库(www.hmdb.ca)[25]。这些数据库与MetaboAnalyst (www.metaboanalyst.ca)(26]和KEGG(www.genome.jp kegg)用于通路分析。关于MALDI-MSI组织的制备、数据处理和统计分析、内源性代谢物的相对定量以及LC-MS对代谢物的鉴定的详细信息载于本文补充材料。
结果
吡非尼酮和内源性代谢物的检测原位在实验性肝纤维化
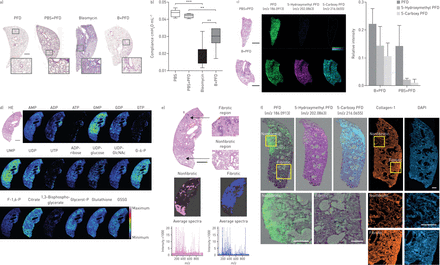
探讨吡非尼酮的纤维化肺组织的分布和影响,我们诱导大鼠肺纤维化小鼠使用博来霉素。吡非尼酮(500 mg·kg−1)通过口服强饲法每日一次给药7天至第14的基础上,以达到最大浓度所采取的先前确定的时间(t马克斯)在正常老鼠组织内[18]。On day 14, mice were sacrificed 45 min after final pirfenidone administration and lung tissue was harvested. Histological analysis of bleomycin-treated samples revealed destruction of normal tissue architecture, excessive accumulation of extracellular matrix (ECM) and decreased lung compliance compared with PBS-treated controls (图1a和b)。在博莱霉素+吡非尼酮治疗的小鼠中,我们观察较不显着肺纤维化和显著改善肺功能,这表现在更好地遵守,在博来霉素治疗的动物相比,观察(图1a和b)。吡非尼酮的代谢产物5-羟基吡非尼酮(米/z202.0863)和5-羧基吡非尼酮(米/z在全球范围内,用波莱霉素+吡非尼酮处理的小鼠的肺组织比用吡非尼酮处理的未受影响小鼠的肺组织更为丰富(图1c)。值得注意的是,我们观察到波莱霉素+吡非尼酮治疗的小鼠纤维化肺保守区吡非尼酮积累增加,对应于纤维化区域COL1含量较低的区域(图1F)。
吡非尼酮(PFD)检测博来霉素诱导的肺纤维化小鼠肺部。一)HE染色从用PBS,PBS + PFD处理的小鼠的肺切片的,博来霉素诱导的纤维化和B + PFD。年代cale bar: 1000 μm. b) Lung compliance measurements of mice from each treatment group. Data are shown as mean±sd。* *:p≤0.01;***:P≤0.001。C)左:PFD和其相关的代谢产物,5-羟甲基PFD和5-羧基PFD的质谱成像的分布,在从PBS + PFD-和B + PFD处理的小鼠的肺。年代cale bars: 1000 μm. Right: relative quantification of PFD and related metabolites in lungs from PBS+PFD- and B+PFD-treated mice. d) Heterogeneous distribution pattern of central pathway-related endogenous metabolites in lung tissue from B+PFD-treated mice. Scale bar: 1000 μm. e) HE images with zoomed regions of nonfibrotic and fibrotic tissue. Spatial segmentation of histological components through unsupervised hierarchical clustering reflects the histological components of fibrotic (blue) and nonfibrotic (pink) areas. Scale bar: 1000 μm. f) Immunofluorescence staining for collagen type 1 in sectioned lungs from the B+PFD-treated group. Scale bars: 500 μm. B+PFD: bleomycin+PFD; HE: haematoxylin and eosin; GlcNAc:N乙酰氨基葡萄糖;G-6-P:葡萄糖-6-磷酸;F-1,6-P:果糖-1,6-二磷酸;甘油-P:甘油单磷酸酯;GSSG:谷胱甘肽二硫化物;DAPI:4',6-二脒基-2-苯基吲哚。
为了确定内源性代谢物的变化,我们进行了原位波莱霉素+吡非尼酮治疗小鼠肺纤维化关键代谢通路主要成员的影像学研究。我们确定了核苷酸衍生物,以及中心代谢途径和氧化还原相关代谢物。对于一些(如。GMP,UMP和葡萄糖-6-磷酸),它们的分布模式与整个微纤维化区域的区域(相关图1D和e)。然后我们进行无监督的层次聚类[27,28]在由博来霉素+吡非尼酮治疗的动物的肺的代谢物,并生成基于不同的MSI光谱聚类的纤维化和nonfibrotic区域分割图(图1E)。这些数据与由组织病理学家进行显微镜检查协议。
糖酵解的MALDI-FTICR-MSI分析和吡非尼酮治疗后的TCA循环途径
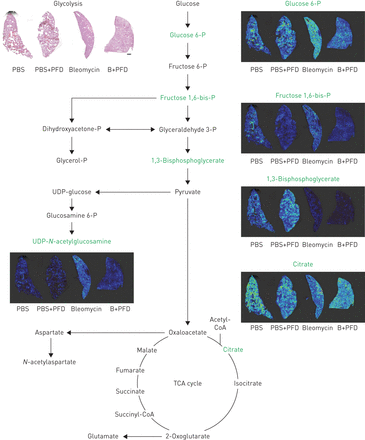
接下来,我们比较了来自糖酵解和TCA循环的几种代谢物在所有治疗组动物肺中的表达(图2)。我们观察到,在葡萄糖博来霉素处理的小鼠纤维化期间-6-磷酸增加,而1,3- bisphosphoglycerate在肺部从博莱霉素和博来霉素+吡非尼酮治疗的动物下降;果糖-1,6-二磷酸水平不变。当丙酮酸盐,其选自1,3- bisphosphoglycerate导出,进入己糖胺生物合成途径,它被转化为UDP-N乙酰氨基葡萄糖。UDP -N-乙酰氨基葡萄糖参与透明质酸合成[29],这是一种由博莱霉素诱导的纤维化和IPF中的肌成纤维细胞高度产生的ECM成分[30.]。在这里,我们发现UDP-的显著增强N-乙酰氨基葡萄糖在纤维化肺从博莱霉素治疗小鼠。但是,与UDP -N乙酰氨基葡萄糖,柠檬酸水平在各组相似。这些数据在小鼠博莱霉素致纤维化和吡非尼酮治疗期间发生的肺代谢变化提供了初步证据
由高分辨率的定量基质辅助激光分析糖酵解和三羧酸(TCA)循环的代谢解吸/电离傅里叶变换离子回旋共振质谱成像在纤维化小鼠。用PBS,PBS + PFD,博来霉素和B + PFD治疗肺的苏木精和曙红的部分被示出在左侧的顶部。年代cale bar: 1000 μm. Representative metabolite images of selected steps (in green) of glycolysis and the TCA cycle are shown. PFD: pirfenidone; B+PFD: bleomycin+PFD; P: phosphate; CoA: coenzyme A.
吡非尼酮治疗博莱霉素诱导的肺纤维化的代谢作用
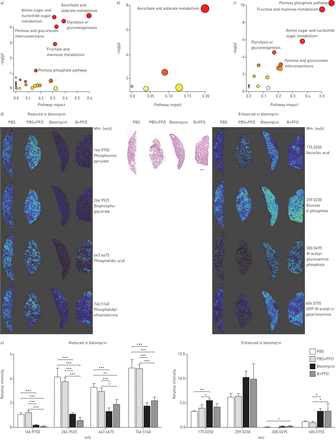
接下来,我们进行的代谢途径富集分析,比较PBS控制和博莱霉素诱导的纤维化(图3a)。通过从每个肺切片中选择健康的、未塌陷的区域,从pbs处理的小鼠中选择控制区。根据组织学特征和通过空间分割识别的纤维化簇(图1E)。总共发现1402个分子是控制和纤维化组织之间显著不同,与富集409个分子和993个分子在纤维化区域减小。此外,这些536在METLIN数据库中注释;这些被推定分配给57间脂质(24降低和富集在纤维化区域33),234种肽(223减小,并且在纤维化区域富集11)和其他245种代谢物。然后负责代谢分化代谢物进行富集途径分析(图3和表1)。管制的代谢产物驾驶途径意义中列出补充表S1。我们发现糖酵解/糖异生代谢在肺纤维化中显著降低,而抗坏血酸和醛糖代谢、氨基糖和核苷酸糖代谢、戊糖磷酸途径、戊糖和葡萄糖酸盐相互转换、果糖和甘露糖代谢在博莱霉素诱导的纤维化中显著增强(图3a,表1和补充表S1)。
在实验性纤维化有和没有吡非尼酮(PFD)治疗判别代谢改变的途径分析。代谢途径是根据从富集(纵轴)和使用MetaboAnalyst拓扑分析(途径的影响,水平轴)他们的分数表示为圆。一)在博来霉素诱导的纤维化判别途径用PBS对照组相比。b)如在PFD治疗博来霉素诱导的纤维化判别通路。c)如在PFD治疗博来霉素诱导的纤维化判别通路与PBS + PFD处理组进行比较。d)用PBS处理的肺的苏木精和曙红的部分,PBS + PFD,博来霉素和B(博来霉素)+ PFD显示在中间。年代cale bar: 1000 μm. On the right, from top to bottom, representative images of metabolites reduced in fibrosis: phosphoenol pyruvate (米/z166.9750),bisphosphoglycerate(米/z(264.9525),磷脂酸(米/z647.4675)和磷脂酰乙醇胺(米/z746.5140)。在左侧,从顶部到底部,在纤维化增强的代谢物的代表性图像:抗坏血酸(米/z175.0250,葡萄糖6-磷酸(米/z259.0230)N乙酰氨基葡萄糖磷酸(米/z300.0495)和UDP-N乙酰基d培养(米/z606.0755)。E)在用PBS,PBS + PFD,博来霉素和B + PFD处理的小鼠中(d描绘代谢物)的相对定量。单因素方差分析进行统计分析,与邦费罗尼事后测试。*:p≤0.05;* *:p≤0.01;***: PBS组与治疗组间p≤0.001。
为了阐明吡非尼酮的pharmacometabolic效果,第二比较对用或不用吡非尼酮7天的口服剂量(治疗纤维化动物进行图3b)。从这个分析,115辨别米/z物种被确定。通过数据库检索和通路分析,发现抗坏血酸和醛酸代谢在博来霉素诱导的纤维化中增强,但在吡非尼酮治疗后出现下调(图3b,表1和补充表S1)。这表明吡非尼酮在改变疾病的系统代谢谱中起着至关重要的作用。抗坏血酸有助于弹力蛋白、胶原蛋白和其他胶原结构域的ECM蛋白中羟脯氨酸的有效羟基化,从而支持吡非尼酮在调节中的重要作用从头ECM生产的代谢水平博莱霉素引起的纤维化。
为了进一步澄清吡非尼酮的纤维化过程中的作用,我们与吡非尼酮(PBS +吡非尼酮)治疗的健康小鼠进行代谢途径分析。这些数据表明单独用PBS处理的PBS +吡非尼酮基和小鼠之间的高代谢相似性(图2,3D和4)。这与我们之前在健康小鼠组织中对吡非尼酮进行的药代动力学研究一致,在该研究中,我们没有观察到吡非尼酮或其代谢物对已知代谢途径的显著影响[18]。然后,我们比较了来自博莱霉素+吡非尼酮和吡非尼酮与(PBS +吡非尼酮)治疗的健康小鼠治疗纤维化动物肺部。总共1076个分子是这些基团之间显著不同,与富集427个分子和649个分子与吡非尼酮治疗的纤维化的动物减少。途径富集分析识别的多个辨别通路,包括糖酵解/糖异生,氨基糖和核苷酸糖代谢,戊糖磷酸途径,戊糖和葡糖醛酸的相互转化,和果糖和甘露糖代谢(图3c)。值得注意的是,与对照(PBS +吡非尼酮)相比,抗坏血酸盐和aldarate代谢保持与吡非尼酮治疗的纤维化的动物不变。这些结果进一步支持吡非尼酮治疗对抗坏血酸和aldarate代谢的影响。
接下来,我们进行原位检测主要代谢途径的关键代谢物早些时候报道。我们选择了8个有代表性的显著调节的代谢物(4个上,4个下),它们在纤维化中有明显的差异调节(图3D和e)。其中纤维化下调的代谢物,我们包括磷酸烯醇丙酮酸,bisphosphoglycerate,磷脂酸和磷脂酰乙醇胺。有趣的是,磷脂酸和磷脂酰乙醇胺受到显着耗尽纤维化,并且这些部分被吡非尼酮治疗恢复。相反地,抗坏血酸,葡萄糖-6-磷酸,N-乙酰氨基葡萄糖磷酸和UDP-N乙酰基d-galactosamine纤维化期间上调。值得注意的是,抗坏血酸显著用吡非尼酮治疗减少,支持我们的路径分析。
在健康和纤维化肺组织中央通路相关的内源性代谢物的定量
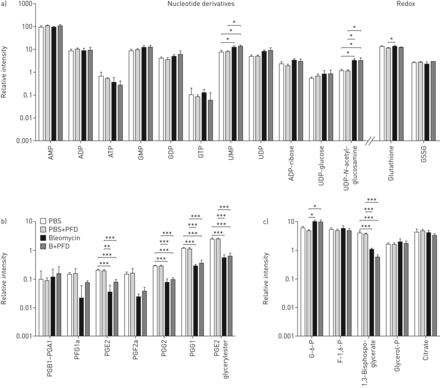
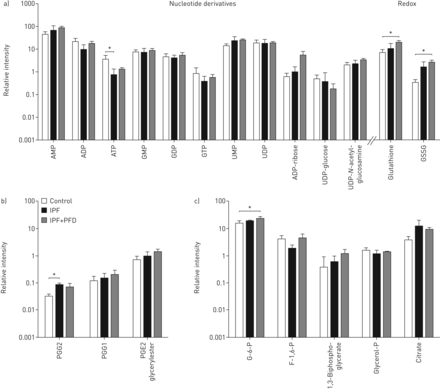
为了进一步研究在疾病状况的代谢物动力学,我们比较了在控制装置25种内源性代谢物(核苷酸衍生物,中央途径代谢物,前列腺素和氧化还原相关的代谢物)(PBS和PBS +吡非尼酮治疗)的相对丰度,博来霉素处理和博来霉素+吡非尼酮治疗的小鼠。米etabolite identification was performed using LC-MS on tissue MS/MS or accurate mass matching with databases (4 ppm mass accuracy;补充图S2和S3)。九出的25种代谢产物水平纤维化和控制组织之间显著不同。核苷酸衍生物中,UMP和UDP-N当与对照(比较乙酰氨基葡萄糖被显著在两个纤维化和吡非尼酮治疗的纤维化增加图4a)。我们还发现,前列腺素通路被高度管制。尽管前列腺素B1-A1不变,前列腺素E2,G2,G1和E2 glycerylester在博莱霉素均显著降低,与对照组相比博莱霉素+吡非尼酮治疗的小鼠(图4b)。最后,我们分析了来自糖酵解和TCA循环代谢物,并发现,1,3- bisphosphoglycerate被显著在肺中降低从博莱霉素和与对照组相比博莱霉素+吡非尼酮治疗的小鼠,而葡萄糖-6-磷酸在纤维化和吡非尼酮增加- 处理的纤维化组织(图4c)。
用PBS,PBS +吡非尼酮(PFD)处理在小鼠中内源性组织代谢物的相对丰度,或博莱霉素+ PFD(B + PFD)。代谢物分为a)核苷酸衍生物和氧化还原相关代谢物,b)前列腺素,c)糖酵解和三羧酸循环。数据以均数±表示sd(n=3),表示各组的相对浓度。单因素方差分析进行统计分析,与邦费罗尼事后测试。GSSG:谷胱甘肽二硫化物;PG:前列腺素;G-6-P:葡萄糖-6-磷酸;F-1,6-P:果糖-1,6-二磷酸;甘油-P:甘油磷酸。*:p≤0.05;* *:p≤0.01;***: PBS组与治疗组间p≤0.001。
吡非尼酮对IPF的药物代谢作用
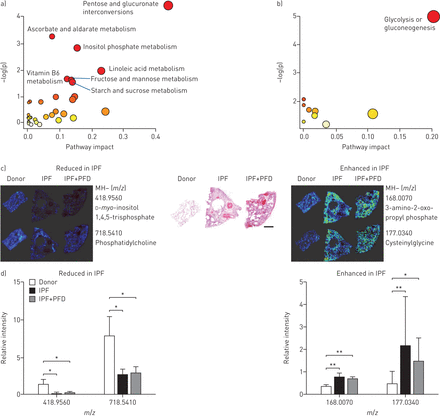
为了确定这种分析是否是识别纤维化的代谢足印在人体肺部,以及吡非尼酮在IPF的pharmacometabolic效果非常有用,我们从拒绝捐助者,治疗过的IPF患者移出肺进行在人体肺部歧视性代谢产物的途径分析和IPF患者吡非尼酮治疗在移植的时候。在作为与未经处理的IPF组织如前所述,我们最初比较供体类似的方法,以识别代谢途径纤维化期间推定调制(图5,表1和补充表S2)。总共825个分子供体和纤维化组织之间显著不同,具有480个分子富集和345个分子IPF降低。然后,我们从未经处理和吡非尼酮治疗IPF比较移植组织检查了终末期IPF吡非尼酮的代谢作用。从这个分析,173辨别米/z物种鉴定(图5和补充表S2)。
在特发性肺纤维化(IPF)患者和无吡非尼酮(PFD)治疗辨别代谢改变的路径分析。代谢途径是根据从富集(纵轴)和使用MetaboAnalyst拓扑分析(途径的影响,水平轴)他们的分数表示为圆。一)在IPF判别途径与捐助相比。b)中的判别途径在IPF PFD治疗后。c)中苏木精和从供体,未处理的IPF或PFD处理的外植IPF肺的曙红区段(IPF + PFD)患者被示出在中间。年代cale bar: 2000 μm. On the right, from top to bottom, representative images of metabolites reduced in IPF:d-myo肌醇1,4,5-三磷酸(米/z418.9560)和磷脂酰胆碱(米/z718.5410)。在左侧,从顶部到底部,在IPF增强代谢物的代表性图像:3-氨基-2-氧代丙基酯(米/z和半胱氨酸甘氨酸(米/z177.0340)。d)供体、IPF和经PFD处理的IPF (IPF+PFD)中(c)所示代谢物的相对定量。单因素方差分析进行统计分析,与邦费罗尼事后测试。*:p≤0.05;**:供体与治疗组间p≤0.01。
然后负责代谢分化代谢物进行途径的富集分析;调控代谢途径驾驶意义中列出补充表S2。我们确定了戊糖和葡萄糖醛酸互变,与在IPF影响最大途径。另外,抗坏血酸和aldarate通路,以及果糖和甘露糖代谢,是在IPF上调,和维生素B6代谢在IPF增加了与供体组织相比(图5a,表1和补充表S2)。相反,亚油酸和肌醇磷酸代谢以及淀粉和蔗糖途径在IPF中被下调。未经吡非尼酮处理和吡非尼酮处理的IPF移植组织的比较(图5b,表1和补充表S2)吡非尼酮可增强糖酵解/糖异生的信号。然后,我们执行原位上述途径的关键代谢物的定位(图5c和d),并证实本地化和显着减少d-myo肌醇在IPF 1,4,5-三磷酸和磷脂酰胆碱和吡非尼酮治疗IPF。与此相反,我们观察到定位和在3-氨基-2-氧代丙基磷酸和半胱IPF和吡非尼酮治疗IPF一个显著增加。
最后,我们测量的21种代谢物的相对丰度从控制,IPF和吡非尼酮治疗IPF肺几个代谢途径(核苷酸衍生物,中央途径代谢物,前列腺素和氧化还原相关的代谢物);五周明的21人显著调节。核苷酸衍生物中,ATP被显著在IPF降低和吡非尼酮治疗IPF与对照组织相比(图6a)。从氧化还原途径来看,吡非尼酮处理的IPF中谷胱甘肽和谷胱甘肽二硫均较对照组织显著升高(图6a)。前列腺素通路是较低范围在人中表达的内,尽管前列腺素G2在IPF与对照组相比显著增加。从糖酵解和TCA循环,葡萄糖与对照组织相比-6-磷酸显著在吡非尼酮治疗IPF增加。此外,果糖-1,6-二磷酸,它是参与糖酵解/糖异生,在IPF中显著下调,在这种疾病中暗示糖酵解/糖异生的失调(图6C)。糖酵解/糖异生途径增强在吡非尼酮管理(图5b)表明在IPF恢复糖酵解吡非尼酮可能发挥的作用。
供体、特发性肺纤维化(IPF)和吡非尼酮(PFD)治疗的IPF患者的内源性组织代谢物的相对丰度。代谢物分为a)核苷酸衍生物和氧化还原相关代谢物,b)前列腺素,c)糖酵解和三羧酸循环。数据以均数±表示sd(n=3),表示各组的相对浓度。单因素方差分析进行统计分析,与邦费罗尼事后测试。GSSG:谷胱甘肽二硫化物;PG:前列腺素;G-6-P:葡萄糖-6-磷酸;F-1,6-P:果糖-1,6-二磷酸;甘油-P:甘油磷酸。*:P≤0.05,控制和疾病组之间。
讨论
这个概念验证研究第一次证明,原位纤维化和吡非尼酮对小鼠和人类的纤维组织的pharmacometabolic影响期间代谢改变。纤维化组织具体而言,我们发现增加吡非尼酮的水平和相关代谢物利用高分辨率原位多发性硬化症。我们发现肝纤维化领域的质谱,以评估感兴趣的特定区域的代谢物组成。使用这种技术,我们就能够对多个样品中同时剖析代谢途径和确定的空间分布,以及检测的强度进行量化。最后,我们确定了重叠和独特的代谢指纹是推定与pharmacometabolic响应表征纤维化反应在人类和小鼠,共同吡非尼酮的纤维化。
由于每个治疗组的小鼠数量相对较少(n=3),这应该被视为一个概念验证研究,探索MALDI-FTICR-MSI在肺纤维化小鼠模型中检测代谢物的效用。为了证明我们的实验的统计意义和重现性,我们进行了分层聚类和偏最小二乘判别分析(补充图S1)。这些数据清楚地显示了PBS-、博莱霉素-和博莱霉素+吡非尼酮治疗组之间的分离,并强调了这种方法的威力。
代谢组学是由特定的细胞过程中产生内源性的全球代谢特征的研究。所提出的代谢分析,有可能加强纤维化过程的认识,促进诊断的生物标记物的发现,确定新的目标和改善目前的治疗潜力。重要的是,我们的数据表明,MALDI-FTICR-MSI能提供必要的了解,IPF组织复杂的微环境的时空分子特征的微观和分子分析能力。
研究吡非尼酮及其相关药物代谢物在肺内的分布,发现5-羟甲基吡非尼酮(米/z202.0863)和5-羧基吡非尼酮(米/z216.0655)在纤维化肺中更为丰富。然而,在纤维化肺中,它们大量定位于较不受影响的区域,COL1表达较低。这表明吡非尼酮在纤维化中的分布和代谢可能增强,其抗纤维化作用可能需要在受影响的区域积累。在肺成纤维细胞,5-hydroxymethyl pirfenidone和5-carboxy pirfenidone抑制转化生长因子(TGF) -β-induced胶原蛋白合成,证明这些代谢物antifibrotic活动(31]。
利用超灵敏的MSI,我们发现,同时可视化,数以千计的鼠标内源性代谢物和人的肺切片,从患病和控制组织的。这些包括核苷酸衍生物,以及中央代谢途径的代谢产物,氧化还原相关的代谢物和前列腺素,等等。我们观察到,在中间体糖酵解,核苷酸的代谢和磷酸戊糖途径的改变,纤维化地区拥有健康的肺相比。这是以前表明糖酵解在IPF [改变16]。K奥特曼等。(32]进一步建议,失调糖酵解结果在升高的乳酸水平,这可有利于疾病进展。纤维化对氧化磷酸戊糖途径的这种代谢开关可能表明在纤维化升高的能源需求和能源消耗现在高出。与此相一致,我们发现在IPF患者的ATP水平较低。类似地,细胞外ATP在支气管肺泡灌洗液从IPF样品[下降33]等人已经显示出IPF组织降低细胞内ATP [17],其可以由促进纤维化功能失调线粒体的积累34]。总的来说,这些研究结果表明与在IPF改变糖酵解的替代能源的梯级。
在我们的数据集中发现的其他代谢物与氧化还原机制有关。有趣的是,我们发现在博来霉素诱导的肺纤维化中,谷胱甘肽和谷胱甘肽二硫的水平没有变化,而在吡非尼酮治疗的IPF患者中,这些水平升高。在老鼠的二硫化谷胱甘肽,谷胱甘肽水平,抑制过度的TGF-β[35]。我们推测在IPF谷胱甘肽和二硫化谷胱甘肽水平的复苏可能表明在调节氧化还原失衡的吡非尼酮的作用,有助于持续纤维化36]。
值得注意的是,我们在小鼠和人类与纤维化观察到增加的抗坏血酸和aldarate新陈代谢。这与胶原代谢的提高和生产器官纤维化观察是一致的。在小鼠中,抗坏血酸和吡非尼酮治疗后aldarate代谢下降。抗坏血酸是用于酶催化所必需的胶原的三螺旋和胶原纤维的细胞外交联剂[热稳定性和脯氨酰残基赖氨酰的翻译后羟基化的关键共底物37,38,对胶原蛋白的合成和加工至关重要。因此,抗坏血酸和醛酸代谢在纤维化过程中的增强,以及吡非尼酮给药后相应的降低,表明其抗纤维化活性。这些数据也与吡非尼酮对胶原加工的作用一致,并支持其在抑制IPF成纤维细胞胶原纤维形成中的作用[39]。
纤维化地区脂质显著改变是最近的研究表明脂质,磷脂特别的,一致的纤维化增加,可以作为脂质信号通路介[作用40- - - - - -43]。此外,前列腺素,这些建议有伤肺抗纤维化的活动[44],也减少纤维化区域,这意味着这些可作为指标,以及潜在的相关指标,对肺纤维化的治疗。
通路富集分析进一步揭示假定的重叠,以及,在小鼠和人类纤维化鲜明的特点(图3,表1,补充表格S1和S2),以及几个因素可能占这些差异。首先,我们注意到博莱霉素致肺纤维化是一种自我分辨,容易被操纵模式,这不完全综述人类IPF,但它确实表明在不同层面强烈的共性,支持连续使用临床前试验[45]。第二,吡非尼酮对小鼠的治疗发生在疾病开始到纤维化高峰,而我们的IPF队列处于疾病的终末期,需要移植。因此,我们的数据也可能反映出不同疾病阶段治疗反应的重要差异。
IPF是多方面的,复杂的疾病,和博莱霉素致纤维化保持的肺纤维化的研究最多的模型。动力学分析来研究吡非尼酮治疗和吡非尼酮施用后早期发生的代谢途径的修改的代谢效应,因此仅限于这种模式。For example, pirfenidone and its metabolites are maximally detectable in lungs 45 min post-administration [18]。因此,我们成功地检测到增加吡非尼酮的水平,并在小鼠及其相关代谢产物,但不是人类,纤维化肺。这可能是由于及时,受控药物给药在小鼠中,这是难以在紧接外科手术前预移植患者临床概括。尽管上述因素,在引入支气管cryobiopsies为弥漫性实质性肺病的早期诊断[46,差异可以被最小化,并且MALDI成像对代谢物分析或药物代谢反应的适用性应该被考虑。
总的来说,我们的研究结果表明代谢剖面,在受肺纤维化地区改变。虽然结果是初步的基础上,我们提出,药代,并在这项研究中使用的代谢组学的组合可能最终导致改善了IPF的疾病机制和吡非尼酮的作用机制的了解这方面的证据的概念研究。此外,阐明吡非尼酮相关的代谢和其作用的细胞机制可促进抗纤维化药物的个体反应的预测。无标记的MALDI-MSI技术允许同时检测,可视化和两个外源的(药物及相关的代谢产物)和内源性代谢物的定量,比传统的分析技术提供竞争优势。因此,我们预计MALDI-MSI技术确定的药物和内源性代谢时空行为将广泛适用于药物疗效研究和阐明参与纤维化等病理状态下的生物活性小分子的代谢。
补充材料
补充材料
请注意:补充材料不是由编辑部编辑,因为它已经由作者提供的上传。
图S1。聚类分析和PLS-DA分析。erj - 02314 - 2017 - _figure_s1
图S2。用于代谢物鉴定LC-MS数据。erj - 02314 - 2017 - _figure_s2
图S3。对组织MS / MS数据进行代谢物的鉴定。erj - 02314 - 2017 - _figure_s3
病人的特点。erj - 02314 - 2017 - _patient
表S1和S2。erj - 02314 - 2017 - _tables
致谢
作者要感谢克劳迪娅 - Marieke弗鲁格,乌尔里克·巴克霍尔兹,加布里埃莱Mettenleiter和安德烈亚斯·沃斯从研究单位分析病理(亥姆霍兹慕尼黑中心,Neuherberg,德国),以及康斯坦斯海泽和Daniela Dietel从综合肺病中心(亥姆霍兹慕尼黑中心,慕尼黑,德国),提供技术援助。
脚注
这篇文章有提供补充材料www.qdcxjkg.com
作者贡献:A. Walch, O. Eickelberg, N. Sun和I.E. Fernandez设计了该研究。N. Sun,即Fernandez, M. Wei和M. Witting进行了实验。Verleden提供了来自健康捐赠者的肺组织、IPF和吡非尼酮治疗的IPF肺组织。N.孙和费尔南德斯起草了手稿。即Fernandez, N. Sun, A. Walch, O. Eickelberg和M. Aichler对结果进行了分析和解释。即Fernandez, N. Sun, A. Walch, O. Eickelberg, S.E. Verleden, M. Aichler, M. Wei, M. Witting和P. Schmitt-Kopplin起草和编辑了重要知识内容的手稿。G. Burgstaller和A. Feuchtinger支持免疫荧光实验。
利益冲突:无申报。
支持声明:本研究由Helmholtz Zentrum Munchen (TKP-Project)、德国肺研究中心(DZL)、德国联邦共和国教育和研究部(BMBF)资助;01ZX1310B和01KT1615),以及德意志联邦银行(HO 1254/3-1, SFB 824 C4, CRC/Transregio 205/1“肾上腺:健康和疾病的中央中继”)给A. Walch。本文的资助信息已存放在Crossref资助者注册表。
- 收到了2017年11月9日。
- 接受2018年7月15日。
- 版权©2018人队