摘要
我们调查了增加的呼气一氧化氮分数(F伊诺)水平和血液嗜酸性粒细胞计数在一般人群的慢性气道疾病中具有附加价值。
我们从哥本哈根一般人口研究中纳入了4677名年龄在20-100岁之间的人。根据支气管扩张剂使用前和使用后的肺量测定、自我报告的哮喘和吸烟史,参与者被细分为健康的从不吸烟(n=1649)、健康的一直吸烟(n=1581)、哮喘(n=449)、慢性阻塞性肺病(COPD) (n=404)、哮喘- COPD重叠(ACO) (n=138)和非特异性气流限制(n=456)。
相比之下F伊诺<25 ppb和血液嗜酸性粒细胞<0.3×109细胞·L−1患者的年龄和性别调整比值比(95% CI)为1.54 (1.29-1.84)F伊诺≥25 ppb或血液嗜酸性粒细胞≥0.3×109细胞·L−1和2.14(1.47-3.10)的个人F伊诺≥25 ppb,血液嗜酸性粒细胞≥0.3×109细胞·L−1.痰生成的比值比分别为1.13(0.91-1.41)和1.83(1.20-2.79),哮喘的比值比分别为1.54(1.22-1.94)和3.26 (2.16-4.94),COPD的比值比分别为1.03(0.80-1.32)和0.67 (0.36-1.27),ACO的比值比分别为1.32(0.88-1.96)和2.14(1.05-4.36)。在报告呼吸道症状的个体中,预测慢性气道疾病的类型在两种生物标志物之间没有差异,并且结合使用也没有改善。
的组合F伊诺血液嗜酸性粒细胞可能对一般人群的慢性气道疾病有附加价值,但在临床应用方面仍需进一步研究。
摘要
呼出的一氧化氮和血液嗜酸性粒细胞的联合可能对慢性气道疾病有附加价值http://ow.ly/jUmj30kod8B
简介
嗜酸性气道炎症越来越被认为是对皮质类固醇治疗高度敏感的患者的一个重要特征[1,2].呼出的一氧化氮(F伊诺)水平和血液嗜酸性粒细胞计数已被认为是确定和量化嗜酸性气道炎症程度的生物标志物[3.].虽然F伊诺血液嗜酸性粒细胞可能是同一炎症成分的衡量标准,这两种生物标志物似乎受到不同炎症途径的调控,它们之间的弱相关性以及针对2型t辅助细胞细胞因子驱动的炎症的大型临床试验的结果支持了这一点[4- - - - - -9].因此,有人建议将其用作临床重要炎症模式的补充生物标志物[5,10,11]。然而,关于结合这两种生物标志物的临床重要性的研究仍然有限。
在本研究中,我们调查了组合是否增加F伊诺在一般人群中,嗜酸性粒细胞水平和血嗜酸性粒细胞计数在慢性气道疾病中具有附加价值。
方法
研究设计和参与者
我们纳入了来自哥本哈根总人群研究(CGPS)第二次检查的5578名20-100岁的个体,该研究是一项基于人群的前瞻性队列研究,于2014年4月启动,并持续招募。在第二次试中,邀请的人士来自与第一次试相同的地区(2003-2014年),即有些是新邀请的人士,而有些则是在第一次试中接受考试的人士[12,13].居住在丹麦首都大区的个人是从丹麦国家民事登记系统中随机选择的,通过使用出生时或移民时提供给每个人的唯一身份号码来反映丹麦成年人口。在20-39岁的个体中,随机选择并邀请了25%的符合条件的个体,而所有≥40岁的符合条件的个体都是随机选择并邀请的。所有参与者都完成了一份全面的问卷调查,进行了体检,并提供了血液用于生化分析。在参加调查的当天,由一名医疗保健专业人员与参与者一起详细审查了问卷。该研究得到了Herlev和Gentofte医院(Herlev,丹麦)和丹麦伦理委员会的批准,并根据《赫尔辛基宣言》进行。所有参与者提供书面知情同意书。
呼出一氧化氮和血液嗜酸性粒细胞
F伊诺根据欧洲呼吸学会(ERS)和美国胸科学会(ATS)的建议,使用便携式手持设备NIOX VERO (Aerocrine, Solna,瑞典)的在线测量技术获得呼气量水平[188bet官网地址12,14].该仪器的最低检测限为5 ppb,测量范围为5 - 300 ppb。测量时,受试者处于坐姿,不使用鼻夹,因为这可能导致一氧化氮在鼻腔区域积聚并促进泄漏通过后鼻咽[14].在吸气阶段,人们需要通过带有保护过滤器的吹口吸入全部肺活量,以避免环境堵塞。在呼气阶段,每个人都有指导通过设备上的一个动画界面,以保持正确的恒定呼气流速。该仪器没有分析呼气量为aF伊诺如果个体未能维持正确的恒定呼气流速,并自动要求重复测量。因为肺活量测定和可逆性试验可能会有影响F伊诺气道内的水平[14],测量F伊诺通常在进行肺活量测定和可逆性试验前进行。卫生保健专业人员接受了在测量中正确使用标准操作程序的培训F伊诺并由更有经验的医疗保健专业人员进行了三次认证。按照制造商的建议,定期对仪器进行维护。一个F伊诺根据ATS的建议,<25 ppb为正常,≥25 ppb为升高[15].
使用ADVIA 120血液学系统(西门子医疗,慕尼黑,德国)测量新鲜样本的白细胞计数。分析须每日使用内部质量控制材料进行精密度测试,每月使用外部质量控制程序进行准确度测试[12].血液嗜酸性粒细胞计数报告在×109细胞·L−1与其他白细胞亚群一起,计算总白细胞计数的百分比。血液嗜酸性粒细胞计数<0.3×109细胞·L−1被认为正常且≥0.3×109细胞·L−1增加,因为截止时间与显著的疾病严重程度和慢性气道疾病恶化风险增加有关[5,10,12,16].
慢性气道疾病的定义
慢性气道疾病的临床分组是根据从调查问卷和肺功能测定中获得的信息,根据全球慢性阻塞性肺病倡议(GOLD)和全球哮喘倡议(GINA)商定的建议,采用最高似然原则确定的[17,18].
通过自我报告获得哮喘和吸烟的信息。哮喘被定义为对“你有哮喘吗?”这个问题的肯定回答。吸烟状况被定义为从不吸烟、曾经吸烟和现在吸烟。根据开始吸烟的年龄、吸烟时间和烟草消费量等信息,我们计算了前吸烟者和当前吸烟者的吸烟史(累积烟草消费量)(以包年为单位);1包年相当于20支香烟或等值香烟(如。雪茄烟,雪茄,烟斗),每天抽1年。
使用EasyOne肺活量计(ndd Medical Technologies,苏黎世,瑞士)在站立位置进行肺活量测量,不使用鼻夹。支气管扩张剂前1 s用力呼气量(FEV1)和用力肺活量(FVC)用至少三组值进行测量,肺活量测定的有效性基于至少两次差异<5%的测量值和正确的肺活量曲线目视检查。肺活量仪在CGPS中的应用经历了严格的验证过程[19].存在气流受限的个体,定义为支气管扩张剂前FEV1/FVC比值<0.70的患者还被要求进行可逆性测试:支气管扩张剂后FEV1在吸入400µg沙丁胺醇(a β) 15 min后,采用相同的程序测量FVC和FVC2-激动剂,来自干粉吸入器(Ventoline Diskus;GlaxoSmithKline, Brentford,英国)。以年龄和身高为协变量的健康无症状从不吸烟的子样本为基础,使用内部推导的参考值,分别计算男性和女性的预测值百分比[19].正常的下限(LLN),定义为FEV预测值的下五百分位1和FEV1/FVC,计算为均值- 1.645sd.
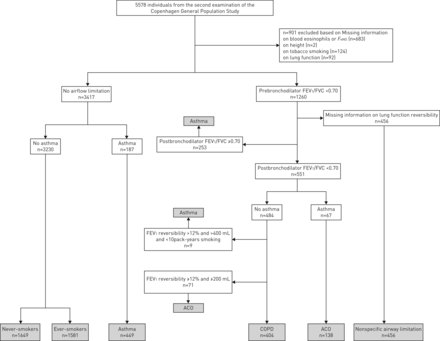
总共有4677人有足够的相关测量信息,其中1260人有支气管扩张剂前FEV气流限制1/ FVC < 0.70。在这些个体中,456人拒绝进行可逆性试验,因此缺乏支气管扩张剂后价值的信息。我们将参与者细分为以下六组(图1).1)健康不吸烟:不吸烟且有支气管扩张剂前FEV1/FVC≥0.70,无自述哮喘;2)健康的长期吸烟者:以前和现在有支气管扩张剂前FEV的吸烟者1/FVC≥0.70,无自述哮喘;3)哮喘:支气管扩张剂前FEV患者1/FVC≥0.70并自我报告哮喘,或支气管扩张剂前FEV1/FVC <0.70和支气管扩张剂后FEV1/FVC≥0.70,或支气管扩张剂前后FEV1/FVC <0.70的人,尽管没有自述哮喘,但有FEV1>可逆性12%,>可逆性400 mL,吸烟史<10包年;4) COPD:支气管扩张剂前和后FEV患者1/FVC <0.70,无自述哮喘或FEV1可逆性(FEV1可逆性<12%,<200 mL);5) ACO:支气管扩张剂前和后FEV患者1/FVC <0.70和自我报告哮喘或支气管扩张剂前和后FEV1/FVC <0.70的人,尽管没有自述哮喘,但有FEV1可逆性≥12%,≥200 mL;6)非特异性气流限制:支气管扩张剂前FEV患者1/FVC <0.70,无可逆性测试。
研究人群的流程图。F伊诺:呼出一氧化氮分数;FEV1:用力呼气量1 s;FVC:强迫肺活量;ACO:哮喘-慢性阻塞性肺疾病(COPD)重叠。
其他信息
身体质量指数(BMI)的计算方法为测量体重除以测量身高的平方(kg·m)−2).家族易感性被定义为至少有一个一级亲属(父亲、母亲和/或兄弟姐妹)患有相关疾病。如果参与者报告对不同的过敏原过敏,则被定义为过敏(即。霉菌、来自树木、草或杂草的花粉、尘螨、宠物或其他过敏原)或哮喘、花粉热或湿疹,这是对食物、药物、草、花、动物毛发或其他过敏原的反应。此外,儿童哮喘或过敏的信息是自我报告的。气道药物的使用定义为每天或几乎每天服用任何类型的哮喘/支气管炎药物(包括喷雾剂/干粉)。喘息是指呼吸时吹口哨或喘息。痰的产生是指每年连续三个月在早晨和/或白天从肺部排出痰。慢性咳嗽为持续>8周。呼吸困难是指在不同程度的活动中,夜间和/或坐着/休息时的呼吸急促。这些人被问及他们是在白天还是晚上有呼吸道症状。
统计分析
使用STATA/SE 13.1 for Windows (StataCorp, College Station, TX, USA)进行统计分析。采用Logistic回归模型。确定受试者工作特征和分类统计的曲线下面积(AUC);通过绘制敏感性和特异性来估计阳性结果阈值与概率截止。首先,临床属性与增加的F伊诺检测血嗜酸性粒细胞水平及计数。二是联想性增加F伊诺研究慢性气道疾病的症状和类型与血嗜酸性粒细胞水平和计数的关系。第三,在报告至少一种呼吸道症状的临床人群中研究了这两种生物标志物的预测能力(即。喘息,痰产,慢性咳嗽,呼吸困难和白天或晚上的呼吸道症状)。所有预测分析均根据年龄和性别进行了调整。两种生物标志物的所有分析分别进行和联合进行。
结果
在4677人中,1649人是健康的从不吸烟者,1581人是健康的一直吸烟者,449人患有哮喘,404人患有慢性阻塞性肺病,138人患有ACO, 456人患有非特异性气流限制(图1).与其他组相比,COPD、ACO和非特异性气流限制患者年龄更大(表1).哮喘、COPD患者,尤其是ACO患者肺功能较低,且报告有更多症状,气道药物使用较多。一般来说,无论吸烟与否,患有特异反应的健康个体与没有特异反应的人相比,似乎有更高的发病率F伊诺水平和血液嗜酸性粒细胞计数,而健康的当前吸烟者与健康的从未吸烟者和前吸烟者相比,无论是否存在特异反应,似乎都较低F伊诺血液嗜酸性粒细胞水平升高(图2而且网上补充数字S1-S4).
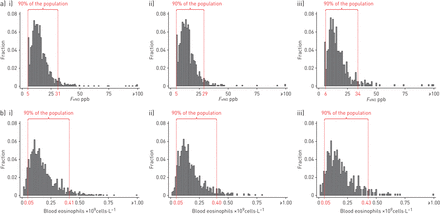
a)呼出一氧化氮分数(F伊诺)水平和b)血液嗜酸性粒细胞计数在i)健康从不吸烟ii)没有和iii)有特异反应。
临床特征
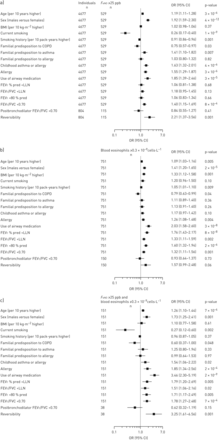
年龄较大,男性,支气管扩张剂前FEV1/FVC <0.70、可逆性试验阳性、自我报告的特异反应和使用气道药物均与患急性呼吸道疾病的风险增加相关F伊诺≥25 ppb,血嗜酸性粒细胞计数≥0.3×109细胞·L−1,分别分析和合并(图3).相比之下,只有较高的BMI,支气管扩张剂前FEV1/FVC
呼吸道症状
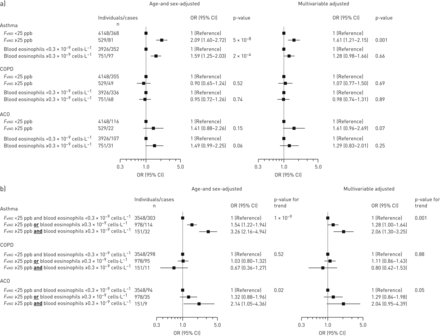
增加F伊诺在白天和夜间,该水平与喘息和呼吸系统症状的风险增加相关,而血液嗜酸性粒细胞计数的增加与所有类型呼吸系统症状的风险增加相关(图4).在对潜在混杂因素进行额外调整后,这些相关性减弱。相比之下F伊诺水平<25 ppb,血嗜酸性粒细胞计数<0.3×109细胞·L−1患者的年龄和性别调整比值比(95% CI)为1.54 (1.29-1.84)F伊诺≥25 ppb或血嗜酸性粒细胞计数≥0.3×109细胞·L−1和2.14(1.47-3.10)的个人F伊诺≥25 ppb,血嗜酸性粒细胞计数≥0.3×109细胞·L−1(图5).相应的优势比(95% CI)为痰液产生1.13(0.91-1.41)和1.83(1.20-2.79),慢性咳嗽1.22(0.96-1.55)和1.51(0.92-2.48),呼吸困难1.21(1.04-1.40)和1.03(0.73-1.46),白天呼吸症状1.34(1.12-1.61)和1.30(0.86-1.98),夜间呼吸症状1.33(1.06-1.68)和1.56(0.95-2.56)。在对潜在混杂因素进行额外调整后,结果减弱但相似。
与a)呼出一氧化氮分数增加相关的临床特征(F伊诺;≥25磅);B)血液嗜酸性粒细胞计数增加(≥0.3×109细胞·L−1);c)综合价值。可逆性定义为1 s的用力呼气量(FEV)1)可逆性≥12%,≥200 mL。采用Logistic回归模型。估计数字未经调整。p值来自Wald的测试。BMI:身体质量指数;慢性阻塞性肺病:慢性阻塞性肺病;LLN:正态下限;FVC:强迫肺活量。
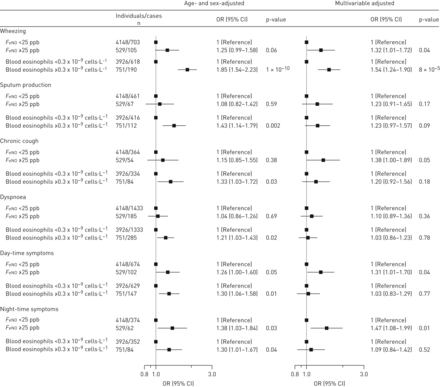
呼气一氧化氮水平和血液嗜酸性粒细胞计数增加与呼吸道症状的单独关联。采用Logistic回归模型。多变量调整包括年龄、性别、体重指数、吸烟状况、吸烟史、慢性阻塞性肺疾病和哮喘的家族易感、特异反应和气道药物的使用。p值来自Wald的测试。F伊诺:呼出一氧化氮分数。
慢性气道疾病
当分别分析这两种生物标志物时,一种增加F伊诺水平和血液嗜酸性粒细胞计数与哮喘风险增加相关,但与COPD或ACO无关(图6).相比之下F伊诺水平<25 ppb,血嗜酸性粒细胞计数<0.3×109细胞·L−1哮喘患者的年龄和性别调整比值比(95% CI)为1.54 (1.22-1.94)F伊诺≥25 ppb或血嗜酸性粒细胞计数≥0.3×109细胞·L−1个人3.26 (2.16-4.94)F伊诺≥25 ppb,血嗜酸性粒细胞计数≥0.3×109细胞·L−1.COPD的比值比(95% CI)分别为1.03(0.80-1.32)和0.67 (0.36-1.27),ACO的比值比(1.32 - 1.96)和2.14(1.05-4.36)。对其他潜在混杂因素进行校正后,结果减弱但相似。根据FEV确定阻塞性肺疾病的临床分组时,结果相似1/ fvc < lln (在线补充图S5).
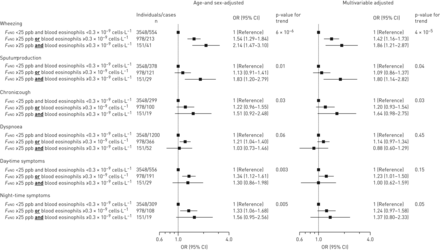
呼气一氧化氮水平和血液嗜酸性粒细胞计数增加与呼吸道症状的联合关联采用Logistic回归模型。多变量调整包括年龄、性别、体重指数、吸烟状况、吸烟史、慢性阻塞性肺疾病和哮喘的家族易感、特异反应和气道药物的使用。p值来自Wald的测试。F伊诺:呼出的一氧化氮含量。
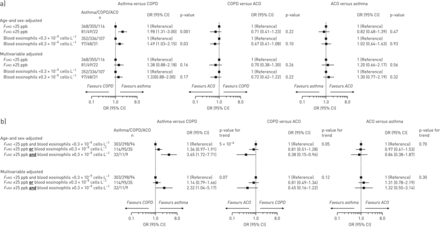
在另外的分析中,我们限制了慢性气道疾病患者的不同亚组。在哮喘和COPD个体亚组中,发病率增加F伊诺与COPD相比,血液嗜酸性粒细胞水平和血液嗜酸性粒细胞计数与哮喘风险增加相关,特别是当这两种生物标志物联合使用时(图7).同样,当COPD患者和ACO患者分别进行分析时F伊诺与COPD相比,ACO水平和血液嗜酸性粒细胞计数与ACO风险增加相关。在ACO和哮喘亚组中未观察到明显的相关性。
呼气一氧化氮水平升高和血液嗜酸性粒细胞计数与哮喘、慢性阻塞性肺疾病(COPD)和哮喘- COPD重叠(ACO)的关系a)单独的关联分析;B)组合关联分析。采用Logistic回归模型。多变量调整包括年龄、性别、体重指数、吸烟状况、吸烟史、COPD和哮喘的家族易感、特异反应和气道药物的使用。p值来自Wald的测试。F伊诺:呼出一氧化氮分数。
呼气一氧化氮水平和血液嗜酸性粒细胞计数增加有利于哮喘、慢性阻塞性肺疾病(COPD)或哮喘- COPD重叠(ACO)。a)单独的关联分析;B)组合关联分析。采用Logistic回归模型。多变量调整包括年龄、性别、体重指数、吸烟状况、吸烟史、COPD和哮喘的家族易感、特异反应和气道药物的使用。p值来自Wald的测试。F伊诺:呼出一氧化氮分数。
预测能力
在报告有呼吸道症状的人群中,F伊诺血液嗜酸性粒细胞在预测哮喘、COPD或ACO方面的敏感性和特异性较差(表2).阴性预测值较高(≥90%),阳性预测值较低(≤18%)。两种生物标志物之间没有观察到差异,它们的组合似乎并没有提高预测能力。预测哮喘的AUC (95% CI)值为0.62 (0.58-0.65)F伊诺≥25 ppb,血液嗜酸性粒细胞≥0.3×10为0.60 (0.57-0.64)9细胞·L−10.61 (0.58-0.64)F伊诺≥25 ppb和/或血液嗜酸性粒细胞≥0.3×109细胞·L−1.COPD对应的AUC (95% CI)值为0.68(0.65-0.72)、0.68(0.64 - 0.71)和0.69 (0.65-0.72),ACO对应的AUC值为0.63(0.57-0.68)、0.64(0.59-0.69)和0.64(0.59-0.69)。
在将分析限制到慢性气道疾病亚组后,在区分哮喘、COPD或ACO的预测能力方面,两种生物标志物及其组合之间没有观察到差异。尽管总体预测能力较差,但这两种生物标志物在区分哮喘和COPD方面似乎具有可接受的性能。
讨论
在这个来自一般人群的大随机样本中,我们发现与正常个体相比F伊诺与仅有一项生物标志物升高的个体相比,两项生物标志物均升高的个体发生呼吸道症状和哮喘的风险均增加,ACO的风险估计值也更高。在报告呼吸道症状的个体中,预测慢性气道疾病的类型在两种生物标志物之间没有差异,并且没有通过联合使用它们来改善;然而,使用这两种生物标志物似乎排除了慢性气道疾病,其阴性预测值≥90%。因此,我们的研究结果表明,尽管这两种生物标志物的组合在表征慢性气道疾病方面可能具有附加价值,但其潜在的临床应用仍需要进一步研究。
呼出的一氧化氮被认为是由与白细胞介素(IL)-4和IL-13激活相关的气道局部炎症引起的,而血液嗜酸性粒细胞被认为是由白细胞介素IL-5激活引起的全身性炎症[2].在大型临床试验中,mepolizumab(单克隆抗il -5)治疗显著降低了血液嗜酸性粒细胞计数,而对白细胞介素(il -5)没有任何显著影响F伊诺水平(7- - - - - -9],而lebrikizumab(抗il -13)和dupilumab(抗il -4和-13)的治疗减少F伊诺血液嗜酸性粒细胞计数明显增加,但无增加或增加幅度很小[4,6].这表明,这两种生物标志物不应互换使用,而应联合使用,以确定嗜酸性气道炎症的不同方面。在本研究中,我们不仅观察到结合这两种生物标志物的附加价值,而且在单独分析时,这些生物标志物与一些临床属性有不同的关联。气流受到更大限制,这是严重阻塞性肺病的众所周知的临床特征[20.,21],与血液嗜酸性粒细胞计数≥0.3×10的风险增加有关9细胞·L−1但不是用F伊诺级别≥25ppb。此外,特异反应性和吸烟的测量与F伊诺而不是血液中的嗜酸性粒细胞。
另一个有趣的发现是F伊诺血清嗜酸性粒细胞水平和血嗜酸性粒细胞计数与哮喘和ACO相关,但与COPD无关。我们并不一定相信F伊诺和血液嗜酸性粒细胞能够区分哮喘和ACO与COPD,但更能识别哮喘和ACO中更常见的病理生理特征,而不是COPD [22].然而,使用F伊诺血液嗜酸性粒细胞在有症状的个体中诊断慢性气道疾病类型的敏感性和特异性较低,这表明这两种生物标志物有其局限性,在常规实践中应用之前应在临床研究中进行更彻底的研究。然而,这两个生物标志物的阴性预测值≥90%,因此似乎有助于在一般人群中排除有症状的个体中存在的慢性气道疾病。由于阳性和阴性预测值也取决于疾病的患病率,而不考虑敏感性和特异性,因此本研究中观察到高阴性预测值与低敏感性和特异性相结合的一个潜在解释可能是一般人群中当前样本中慢性气道疾病的低患病率。
之前的研究表明F伊诺在哮喘和慢性阻塞性肺病患者中,嗜酸性粒细胞水平和血液嗜酸性粒细胞计数与疾病严重程度增加和急性发作独立相关[12,16,23- - - - - -26].然而,结合这两种生物标志物的附加价值还没有被广泛研究。在国家健康和营养调查中,结合F伊诺血液嗜酸性粒细胞在确定当前哮喘、喘息、哮喘发作和哮喘相关急诊就诊风险方面具有附加价值[5,11].此外,同样的研究人员还可以通过在哮喘患者中结合这两种生物标志物来观察附加价值,以确定气流限制的严重程度、支气管反应程度以及哮喘不受控制和哮喘频繁发作[10].最后,由于本研究中大多数哮喘患者病情较轻,中位数为F伊诺与那些患有更严重疾病的患者相比,血液嗜酸性粒细胞更低,这通常在二级护理中看到[27].
本研究的一个重要局限性包括慢性气道疾病临床分组的定义。尽管有可逆性和不可逆性气流限制的区别,但哮喘和COPD在临床表现和自然病史方面都是非常复杂的疾病,可能难以区分,特别是ACO的定义仍存在争议。尽管我们通过考虑GOLD和GINA的建议,采用了最高可能性原则来定义临床分组[18],我们的研究结果可以在临床环境中复制,在临床环境中可以更详细地描述慢性气道疾病的类型。另一个限制是我们无法确定所使用的气道药物的类型。最后,尽管在CGPS中使用肺量仪之前已经经历了严格的验证过程,但一些程序与ERS和ATS的建议不一致[28].
总之,结合F伊诺血液嗜酸性粒细胞可能对一般人群的慢性气道疾病有附加价值,但在临床应用方面仍需进一步研究。
补充材料
脚注
这篇文章有补充资料可从www.qdcxjkg.com
作者贡献:Y. Çolak和S. Afzal完全访问了研究中的所有数据,并对数据的完整性和数据分析的准确性负责。研究概念与设计:Y. Çolak, S. Afzal, B.G. Nordestgaard, J.L. Marott和P. Lange。数据的获取、分析或解释:Y. Çolak, S. Afzal, B.G. Nordestgaard, J.L. Marott和P. Lange。稿件起草:Y. Çolak。重要知识内容的手稿批判性修订:Y. Çolak, S. Afzal, B.G. Nordestgaard, J.L. Marott和P. Lange。统计分析:Y. Çolak和S. Afzal。已获资助:B.G. Nordestgaard和P. Lange。行政、技术或物质支持:B.G. Nordestgaard。研究指导:P. Lange。
利益冲突:Y. Çolak报告了勃林格殷格翰和阿斯利康在提交工作之外的个人费用。
利益冲突:P. Lange报告了阿斯利康和葛兰素史克的拨款,以及勃林格殷格翰、阿斯利康、诺华和葛兰素史克在提交工作之外的个人费用。
支持声明:伦德贝克基金会、Herlev和Gentofte医院内科和临床生物化学系以及丹麦肺肺协会。资助者在研究的设计和实施中没有任何作用;数据的收集、管理、分析或解释;文稿的准备、审查或者批准;或决定投稿发表。本文的资助信息已存入Crossref资助者登记处。
- 收到了2017年6月20日。
- 接受2018年6月4日。
- 版权所有©ERS 2018