摘要
肺动脉高压(PAH)是一种无法治愈的致命疾病。血管紧张素转换酶2 (ACE2)交替转换血管紧张素II (AngII)到血管紧张素-(1-7)(Ang-(1-7))导致Mas受体(Mas1)激活改善啮齿动物PAH模型。重组人ACE2在人多环芳烃中的作用尚不清楚。我们的目的是确定rhACE2在多环芳烃中的作用。
我们使用猪肺动脉定义了Mas1激活的分子效应,测量了人类PAH中的AngII/Ang-(1-7)水平,并进行了单次输注rhACE2 (GSK2586881, 0.2或0.4 mg·kg)的IIa期开放标签试点研究−1静脉注射)。
超氧化物歧化酶2 (SOD2)和炎症基因表达被确定为Mas1激活的标记物。在确认血浆ACE2活性在人PAH中降低后,5名患者被纳入试验。GSK2586881耐受性良好,心排血量和肺血管阻力显著改善。输注GSK2586881与2 - 4小时内炎症血浆标记物减少和2周时SOD2血浆蛋白升高相关。
多环芳烃的特征是ACE2活性降低。在一项初步研究中,ACE2的增加具有良好的耐受性,与改善肺血流动力学和减少氧化剂和炎症介质标志物相关。靶向这一途径可能对人类多环芳烃有益。
摘要
ACE2-Ang -(1-7) - mas1轴可能参与了人类肺动脉高压的病理生理过程http://ow.ly/pgS530jOxnd
简介
肺动脉高压(PAH)是一种高度病态的疾病,主要影响进行性肺血管闭塞的年轻女性,导致右心衰和死亡。虽然在改善多环芳烃预后方面取得了很大进展,但治疗方法尚不完善,目前尚无治愈方法。需要更新、更有效的治疗方法来解决多环芳烃的关键中断途径。
尽管已知肾素-血管紧张素-醛固酮系统在多环芳烃中被激活[1- - - - - -4],血管紧张素转换酶(ACE)抑制剂治疗这种疾病的试验尚未显示出益处[5- - - - - -8,虽然血管紧张素II (AngII) 1型(AT1)受体拮抗剂对大鼠肺动脉高压模型有益处,但这类药物尚未在多环芳烃患者身上试验[1].观察结果导致了AngII交替水解为血管紧张素-(1-7)(Ang-(1-7))的假设。通过ACE2可能是一种更有效的治疗干预手段。Ang-(1-7)激活存在于内皮细胞上的Mas受体(Mas1),具有血管扩张、抗炎和抗纤维化作用[9,10],在功能上拮抗AT的作用1受体刺激[11- - - - - -13].最后,ACE2-Ang -(1-7)轴的激活可减少糖尿病的氧化应激[14],表明对多环芳烃相关途径的影响[15- - - - - -17].因此,ACE2-Ang -(1-7) - mas1轴可能是一种有前途的PAH治疗途径。
我们和其他人已经证明,灌注ACE2和直接激活Mas1都可以改善多环芳烃的啮齿动物模型[18- - - - - -23],可能是通过改善细胞骨架功能,这与之前对ACE2的研究一致[24].此外,ACE2 - ang -(1-7)轴已在一个右心室衰竭模型中进行了研究,在该模型中,ACE2肽的服用可减少右心室肥厚和纤维化,并改善功能[19],表明对肺血管系统和右心室负荷应激反应都有潜在的有益影响。在人类患者中,没有美国食品和药物管理局批准的刺激Mas1的机制,也没有批准用于人类的直接Mas1激动剂。在健康志愿者和急性呼吸窘迫综合征(GSK2586881; GSK2586881;ClinicalTrials.gov标识符NCT01597635) [25].
我们在PAH患者GSK2586881的概念验证试点研究中验证了以下假设:与健康对照组相比,人类PAH中的ACE2活性降低,短期给药ACE2可能是安全的。我们进一步寻求识别Mas1激活的短期标记物,提示分子药物作用,这可能有助于未来对多环芳烃中Mas1激活的研究。
方法
动物实验
所有动物研究均获得美国田纳西州纳什维尔范德堡大学医学中心(VUMC)机构动物护理和使用委员会的批准。
ACE2在PAH患者中的观察性研究
人体研究由VUMC机构审查委员会(编号9401和151388)批准,并在ClinicalTrials.gov(标识符NCT01884051).所有患者在纳入研究前均给予书面知情同意。特发性和遗传性PAH患者,年龄≥18岁,根据临床专家的标准定义,包括[29].看到补充材料查看肾素-血管紧张素系统(RAS)肽测量和基于适体的超氧化物歧化酶2 (SOD2)蛋白测量的详细信息。
GSK2586881的试运行
该研究是一项I期剂量递增、开放标签概念验证研究,对象为特发性或遗传性PAH患者,功能等级为I - iii。主要终点是安全性,次要终点是疾病生物标志物(脑利钠肽、AngII/Ang-(1-7)比值、SOD2活性和硝基酪氨酸活性)的变化,以及PAH的全身和肺血流动力学和超声心动图指标,包括右室功能。我们计划3例患者0.2 mg·kg−1根据之前的安全数据,增加到0.4毫克·千克−1如果没有发生剂量限制毒性。看到补充材料详细的纳入和排除标准。
患者于2016年3月至2016年12月从VUMC肺动脉高压诊所招募。研究程序概述于补充表S3.简言之,患者接受了右心导管插入术。分别记录给药前1 h(−1 h)、给药前即刻(0 h)以及给药后1、2和4 h的血流动力学。用药后24 h,观察患者进行6分钟步行试验(6MWT)和超声心动图。患者在给药2周后返回进行安全性评估、6MWT和临床评估。评估的安全终点包括功能等级的改变、右心衰体征或症状的发展、6MWT距离、血浆电解质和肾功能标志物、全血计数和超声心动图衍生的右心室功能。
看到补充材料RAS肽测定、SOD2 ELISA、硝基酪氨酸点印迹法、细胞因子Luminex测定、异前列腺素和异呋喃测定
统计分析
人口统计数据的连续变量报告为均值与标准偏差。采用Wilcoxon秩和检验和Mann-Whitney u检验比较组间差异。组间分类变量比较采用卡方检验或Fisher精确检验。p值<0.05为有统计学意义。初步研究的数据使用配对双尾t检验进行比较。使用Prism 5.0版(GraphPad, La Jolla, CA, USA)和R 3.0.1版(www.r-project.org).
结果
ACE2在人体多环芳烃中的活性
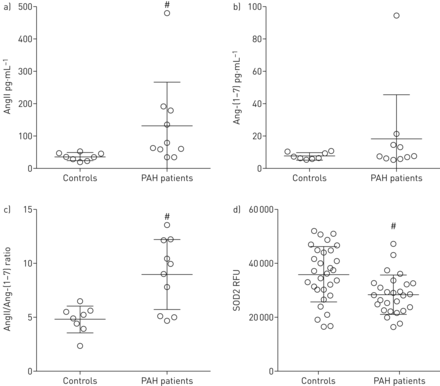
我们首先验证了与对照组相比,人类PAH患者ACE2活性被抑制的假设。我们招募了11名连续的遗传性或特发性PAH患者和8名健康对照(2名男性和6名女性)(补充表S1).我们测量了血浆中的AngII和Ang-(1-7),发现与对照组相比,PAH中AngII/Ang-(1-7)比值反映出ACE2活性显著降低(p=0.01) (图1一个- c)。这种差异是由血浆AngII的增加引起的,PAH中的AngII比对照组高出近4倍(p<0.003),而Ang-(1-7)在PAH中的差异不太显著与控制。
血管紧张素转换酶2 (ACE2)活性不足的证据在人肺动脉高压(PAH)。a - c)测定10例PAH患者和8例健康对照的血浆AngII和Ang-(1-7)水平,作为ACE2活性的标志物。对a) AngII、b) Ang-(1-7)和c) AngII/Ang-(1-7)比值的对数变换值采用Shapiro-Wilk w检验正态分布,允许参数检验。a) PAH中AngII升高(#: p<0.003)和c) AngII/Ang-(1-7)比值在PAH中升高(#: p=0.01),提示ACE2降低了PAH患者血浆中AngII向Ang-(1-7)的转化。d)在30名PAH患者和27名年龄、性别和体重指数匹配的对照组中,采用基于适体蛋白组学的方法测定血浆中SOD2蛋白水平。SOD2蛋白在多环芳烃中被还原。#: p = 0.002。AngII:血管紧张素II;Ang -(1 - 7):血管紧张素- (1 - 7);SOD2:超氧化物歧化酶2;RFU:相对荧光单位。
Mas1激活的生化效应
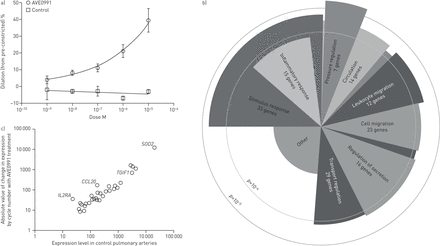
接下来,我们试图定义Mas1激活的分子后果.由于ACE2需要AngII作为底物,而Ang-(1-7)的半衰期较短,因此ACE2在离体动脉研究中的应用具有挑战性。随后,我们使用Mas1直接激动剂AVE0991来确定Mas1激活是否导致肺动脉血管扩张(图2一个).AVE0991在内皮素-1预缩的猪肺动脉中的应用[30.],我们发现作为AVE0991的函数,膨胀百分比呈剂量依赖性增加,这表明Mas1激活在该模型中具有与啮齿动物模型相似的生理效应[18,20.,21].
猪肺动脉高压模型中Mas受体(Mas1)激活的急性分子效应。a) AVE0991,直接Mas1激动剂,被施用于用内皮素-1预收缩的猪动脉。AVE0991给药后,扩张百分比呈剂量依赖性增加。暴露在与生物学无关的对照化合物中未见扩张。b)从接触AVE0991和未接触AVE0991的猪动脉中分离RNA,并进行RNA测序。基因本体分析显示包括炎症反应在内的几种途径的基因表达存在显著差异(p=10)−4)、细胞和白细胞迁移(p<10−4)和压力调节(p<10−5).c)当基因表达随药物暴露的绝对变化被绘制成依赖于对照动脉中的表达水平时,SOD2在Mas1激活的响应下,表达强烈上调。n = 8船只。
为了确定在这个分离的动脉模型中Mas1激活导致的基因表达的急性变化,我们从暴露于AVE0991和对照的动脉中分离出RNA,并进行RNA测序。显着改变的基因表现在补充表S2.使用基因本体论分析方法(图2 b),我们发现了一些通路的显著变化,包括与压力调节相关的基因(p<10)−5)、炎症反应(p=10−4)、白细胞和细胞迁移(p<10−4),再次表明Mas1激活对炎症和细胞骨架功能的潜在影响。为了确定肺动脉中Mas1激活的潜在标志物,我们比较了AVE0991前后肺动脉基因表达水平(图2 c).由于暴露于AVE0991,几个基因被上调,包括TGIF1(转化生长因子-β诱导因子同源箱1),CCL2(C-C基序趋化因子配体2)和SOD2.众所周知,CCL2在多环芳烃中很重要,这表明该研究与该领域的潜在相关性[31].SOD2是一种线粒体蛋白,可催化超氧化物产生过氧化氢和氧气,是一种有吸引力的标记物,基于先前的出版物[32- - - - - -34],以及已知的Mas1激活在糖尿病啮齿动物模型中减少氧化应激的作用[14],表明潜在的生物学合理性,以及暴露于AVE0991后其显著上调。在肺动脉中使用定量PCR进行验证可以在补充图S1.此外,SOD2在对照肺动脉中表达较高,并在Mas1激活后表现出显著的基因表达增加,这表明它可能是ACE2活性增加的生物学重要和敏感标记。
人体多环芳烃中的SOD2
接下来,我们试图确定人类多环芳烃患者和对照组患者中SOD2水平是否不同。我们使用基于适体的蛋白质组学分析方法测量了30例PAH患者(年龄49.5±13.2岁,体重指数(BMI) 29.8±8.2 kg·m)空腹外周血中血浆SOD2蛋白的相对含量−2年龄46.7±11.8岁,BMI 29.1±6.7 kg·m−2,五名男性)(图1 d).我们发现多环芳烃血浆中SOD2蛋白水平比对照组低25%(28 489±7112)与35 930±10 202相对荧光单位;p = 0.002)。
GSK2586881在PAH的中试
接下来,我们试图确定单一药物的安全性和潜在的急性血流动力学和生化影响注射。输注GSK2586881给药于人类PAH患者(见补充表S3有关协议的详情)。我们招募了5名PAH患者,并使用了两种不同的GSK2586881剂量(患者1-3,0.2 mg·kg)−1;患者4、5,0.4 mg·kg−1) (表1).所有患者接受至少两种多环芳烃定向治疗,包括前列腺素通路治疗。所有患者均完成了研究方案,研究药物给药未出现严重不良反应。1例患者在给药1小时内出现头晕,生命体征无变化(患者1),1例患者在夜间观察期间出现腿刺痛(患者5),不需要干预。
其他安全参数,包括6MWT距离(补充表S4).所有患者在基线时为功能II级,在2周随访时为功能II级,1例患者为功能i级与0.99±0.4 mg·dL−1;P =0.03),实验室值无显著变化(数据未显示)。24 h左右心室功能超声心动图指标无差异(补充表S5).任何患者在2周内均未检测到抗药物抗体(数据未显示)。药代动力学特征列于补充表S6.
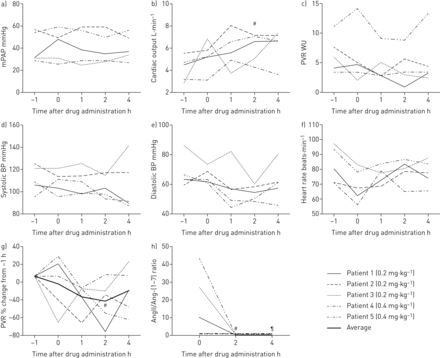
单剂量GSK2586881对平均肺动脉压无影响(补充表S7而且图3一);然而,我们观察到心排血量有统计学意义的增加(5.3±1.4)与6.1±1.3 L·分钟−1;P =0.008)研究用药后4小时,平均增加40% (图3 b).当心输出量增加而平均肺动脉压不变时,肺血管阻力(PVR)预计会降低。我们观察到在低入组人数的情况下PVR的显著变性,但当比较用药前和输注后正常PVR的合并时间点时,我们发现PVR有统计学意义上的显著下降,在用药后2 h达到最低点(p<0.05) (图3 g).对系统血流动力学无显著影响(图3 d- f)。
静脉注射GSK2586881对肺和全身血流动力学的影响。放置肺动脉导管并测量血流动力学(−1小时)。在GSK2586881暴露之前,再次记录肺血流动力学(0小时),然后在给药后1、2和4小时。n = 5。a) mPAP无显著变化。b)给药后2 h心排血量明显增加。#: p = 0.008。c) PVR, d)收缩压,e)舒张压和f)心率的个人原始数据。g)给药前(−1、0 h)与给药后(1、2、4 h)比较,PVR变化百分比明显降低。#: p < 0.05。h)分别在给药前(0 h)、给药后2、4 h测定AngII和Ang-(1-7)水平。在3例基线时AngII/Ang-(1-7)比值升高的患者中,该比值显著下降,提示使用GSK2586881可有效增强血管紧张素转换酶2。#: p=0.009和¶: p = 0.008与在2和4小时分别为0。mPAP:平均肺动脉压;PVR:肺血管阻力;WU:木材单位;BP:血压;AngII:血管紧张素II;Ang -(1 - 7):血管紧张素-(1 - 7)。
测定血浆AngII和Ang-(1-7)水平作为临床药理学指标。AngII/Ang-(1-7)比值的降低表明ACE2活性增加,因此研究药物有效增强。基线时AngII/Ang-(1-7)比值存在显著差异(图3 h).3例患者在基线时这一比率显著升高,在这些患者中,在给药2小时后这一比率降低到几乎无法检测到(26.5±16.5)与0.2±0.2;P =0.009),持续4 h(0.3±0.2;p = 0.008)。RAS肽变化的全部细节见补充图S3.
GSK2586881对人多环芳烃中SOD2的影响
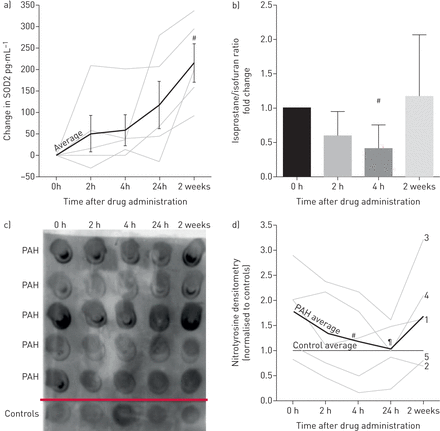
作为我们的体外动物模型显示,Mas1激活诱导了SOD2的表达,我们验证了GSK2586881可诱导PAH患者血浆中SOD2蛋白含量的假设(图4一).通过ELISA检测,我们发现血浆SOD2蛋白水平在2周内有显著的诱导(p=0.009)与基线值)提示GSK2586881诱导酶活性,证实了我们在动物模型中的发现,并表明这可能是人类多环芳烃中Mas1激活的标志。
GSK2586881对氧化应激标记物的影响。a)用ELISA法测定给药前(0 h)、给药后2、4、24 h和2周血浆SOD2蛋白水平。n = 5。2周时血浆SOD2水平显著升高。#: p = 0.009。b)我们测量血浆异前列烷和异呋喃作为氧化应激标记。异呋喃是类似于异前列腺烷的脂质过氧化产物,但是在氧气充足时形成的。异前列腺素/异呋喃比值降低,提示氧合改善。#: p < 0.05。c) 5名健康对照者和5名研究参与者血浆中的硝基酪氨酸点印迹法(PAH),以及d)密度测定定量。在1-5名PAH患者中,血浆硝基酪氨酸水平较对照组下降4小时(#: p=0.004),持续24 h (¶: p = 0.02)。看到补充图S1完整的原始印迹。SOD2:超氧化物歧化酶2;PAH:肺动脉高压。
GSK2586881对炎症血浆标志物的影响
我们的动物微阵列数据进一步表明,Mas1激活可能通过改变促炎基因表达模式来发挥作用。接下来,我们验证了急性GSK2586881给药后人类PAH患者会出现这种改善的假设。作为促炎信号减少的标记,我们测量了血浆细胞因子阵列和氧化应激标记。我们利用Luminex平台评估了GSK2586881对血浆细胞因子的影响(表2).与以往报道一致[35],与对照组相比,在时间点0 h, 9种测量细胞因子中的6种水平升高(白细胞介素(IL)-10, IL-1β,肿瘤坏死因子(TNF)-α, IL-13, IL-8和IL-4的p<0.05)。在GSK2586881给药后,测量到的细胞因子包括IL-10、IL-1β、IL-2和TNF-α被抑制,这些细胞因子早在给药后2小时就可以检测到,并且与持续的抗炎作用有关,2周后IL-1β、IL-6、IL-8和TNF-α水平降低(p<0.05)。这些数据共同表明,在PAH中使用rhACE2可广泛抑制炎性细胞因子。
ACE2对氧化应激的影响
已知多环芳烃会增加血浆中氧化脂质的水平,这是氧化应激的标志[16,17].异呋喃是类似于异前列腺烷的脂质过氧化产物,但异呋喃在氧气利用率增加的情况下更易形成[36].异前列烷与异呋喃的比值是衡量氧气有效性的有用指标。我们测量了试验参与者血浆中的异前列腺素和异呋喃,发现GSK2586881给药4小时后异前列腺素/异呋喃比值显著降低(p<0.05) (图4 b).
为了进一步评估GSK2586881对氧化应激标志物的影响,我们通过点印迹法定量了5个健康对照组和我们的研究参与者(图4 cd)。我们发现,与对照组相比,PAH患者基线时硝基酪氨酸含量增加(p=0.02)。GSK2586881给药后,PAH患者血浆硝基酪氨酸水平在4小时和24小时均下降(p=0.004和p=0.02)。在24小时时间点,GSK2586881给药后,多环芳烃硝基酪氨酸水平与对照组无差异,表明全身氧化应激显著降低。
讨论
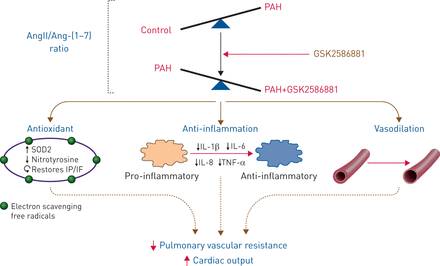
我们的研究旨在1)证明ACE2在人类PAH中的活性降低,2)在动物模型中定义Mas1兴奋的可靠读数,并确定这些读数是否与人类PAH潜在相关,3)在PAH患者中进行GSK2586881的试点试验,以确定这种生物制剂在人类PAH中是否潜在安全,并可能表现出血液动力学或生化功效。我们的目标是在猪肺动脉模型中获得与PAH相关的Mas1激动标记物,并测试GSK2586881在人类PAH患者中的血流动力学和药理学效应。这些实验表明,rhACE2在人多环芳烃中可能通过激活Mas1具有潜在的生化和血流动力学功效。研究结果和解释的视觉摘要显示在图5.
研究结果示意图。PAH:肺动脉高压;AngII:血管紧张素II;Ang -(1 - 7):血管紧张素- (1 - 7);SOD2:超氧化物歧化酶2;知识产权:isoprostane;如果:isofuran;IL:白介素;TNF:肿瘤坏死因子。
鉴于多环芳烃啮齿动物模型中令人信服的临床前数据[18- - - - - -21]和病理标本显示PAH中RAS表达上调[3.,4],对RAS通路的干预似乎有好处。在证明了这一途径与人类多环芳烃的相关性,并将炎症标志物和SOD2定义为与肺血管疾病相关的药物作用的潜在标志物之后,我们进行了一项初步研究,以评估GSK2586881在多环芳烃中的安全性,限制进入特发性和遗传性多环芳烃,因为我们的啮齿类动物模型实验与这些多环芳烃亚组最相关[18].我们招募了5名晚期疾病患者,包括那些针对前列环素途径的多环芳烃定向治疗。我们没有发现任何安全问题,尽管我们入组的患者数量相对较低。即使在这项小型研究中,也存在潜在的血流动力学疗效标记,包括改善心排血量和PVR。此外,还有额外的生化数据支持心排血量的改善:肌酐的下降可能与肾灌注的改善一致,异前列腺素/异呋喃比值的降低可能表明体循环氧输送的改善。
多环芳烃药物开发的一个主要障碍是缺乏有效的药物疗效生物学标记。我们试图克服这一限制,首先在相关组织中开发药物作用的标记物,即。猪的肺动脉。我们确定了SOD2和炎症途径基因对AVE0991暴露有强烈的反应变化。SOD2在多环芳烃的动物模型中发挥作用,尽管人类多环芳烃的数据有限[32- - - - - -34].利用蛋白质组学数据,我们发现与对照组相比,多环芳烃血浆中的SOD2蛋白减少了,这表明与人类可检测到的蛋白质水平潜在相关。人类和啮齿动物的数据显示炎症在多环芳烃中的作用[35,37,38],因此,我们测试了我们自己的多环芳烃人群中的细胞因子水平,并发现与对照组相比,血浆中的几种细胞因子水平升高。在证明了SOD2和炎症在PAH中的潜在相关性后,我们接下来测试了Mas1激活对人类PAH中这些标记物的潜在影响。我们发现,rhACE2增强在PAH患者血浆中的作用与Mas1在猪动脉中的直接激活类似。这些发现与血浆细胞因子最大程度抑制和血浆硝基酪氨酸水平最大程度降低(SOD2活性的下游标记物)时心排血量改善相关。血浆中SOD2水平在较晚的时间点上升,但这是意料之中的,因为SOD2位于线粒体中,在检测到血浆水平的变化之前,细胞周转是必需的。尽管AngII/Ang-(1-7)比值也反映了血浆ACE2活性的有效增加,但SOD2、硝基酪氨酸和细胞因子的这些变化可能更能反映Mas1的激活和下游信号的变化。事实上,之前的研究已经证明Ang-(1-7)抑制白细胞迁移和细胞因子表达[39,40].虽然炎症和SOD2是药物作用的潜在标志,但它们的水平可能会因其他暴露和病理而改变,因此与药物暴露的相对变化特别有趣。这一途径的未来药物试验可能会使用这些Mas1激动的标记物作为适应性试验设计中生化疗效的早期读数,或确定最有可能从这些干预措施中受益的患者。
氧化应激一直与多环芳烃有关[33,41- - - - - -46].氧化应激的全身标记物包括f2 -异前列腺烷,通过必需脂肪酸的自由基过氧化形成,以及硝基酪氨酸,酪氨酸被活性氮硝化的产物。硝基酪氨酸和异前列腺烷都与多环芳烃有关[17,44,47].相反,异糠醛是通过花生四烯酸的自由基过氧化作用形成的非酶化合物,表明在线粒体水平上氧化剂的产生增加,因此需要氧气来产生。我们假设,增加Mas1信号可以减少PAH患者氧化应激的总负担。我们通过斑点法发现血浆硝基酪氨酸减少,与这一假设一致。4小时时,血浆异前列腺素/异呋喃比值显著降低,这与心排血量改善最大的时间点相关,表明向组织输送氧气增加,该比值的降低反映了更大的氧依赖呼吸,尽管这一假设需要进一步证实。总的来说,数据令人放心,用硝基酪氨酸水平测量的总身体氧化应激没有增加,而是下降了,在给药后4和24小时,硝基酪氨酸水平下降到正常水平。
我们的研究受到试验参与者数量少的限制;然而,我们的目的是进行概念验证研究,并确定可用于更大规模试验的潜在药物疗效标记。我们在猪血管中AVE0991效应的RNA表达标记物被已知的猪转录组降低了,这与人类相比是有限的,因此可能有更显著的转录本变化无法被我们的方法识别;尽管如此,我们还是能够检测到可靠的读数。RAS肽家族的其他成员可以提供有关ACE2活性的信息,包括血管紧张素-(1-9)和alamandine [48];然而,这些化合物迅速降解,因此不能在我们的样品中测量。此外,我们没有给健康对照组服用rhACE2,以测量炎症化合物对氧化应激的影响;然而,文献支持在干预前后比较个体自身的细胞因子面板,而不是在这些测量的可变性下比较组[49,50].
总之,我们的数据显示,人类多环芳烃中ACE2活性的降低伴随着SOD2活性的降低,细胞因子表达的增加和氧化应激的增加。单剂量输注rhACE2 (GSK2586881)耐受性良好,可能具有潜在的血流动力学益处。GSK2586881给药与SOD2水平升高、炎症标志物减少和血浆氧化应激降低相关。GSK2586881作为PAH治疗药物的进一步研究是有必要的。
补充材料
确认
作者要感谢Aili L. Lazaar (GlaxoSmithKline, King of普鲁士,PA, USA)和Kelly Hardes (GlaxoSmithKline, Stevenage, UK)在规划临床研究、数据分析和提供手稿审查方面的协助。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
这项研究注册在clinicaltrials.gov标识符编号NCT01884051.
利益冲突:A.R. Hemnes报告了来自美国国立卫生研究院(NIH)和心血管医学研究与教育基金的资助,Actelion、拜耳和联合治疗公司的个人费用,以及葛兰素史克公司在研究进行期间的个人费用和非经济支持(进行实验的药物供应)。此外,她还拥有一项Annamometer专利(肺血管疾病的无创诊断)。e。a。奥斯汀获得了国家卫生研究院的资助。他曾担任Acceleron的顾问。E.L.布里顿获得了国家卫生研究院的资助。他曾担任Hovine Pharmaceuticals的顾问。e。j。开利得到了国家卫生研究院的资助。她与坎伯兰制药公司有未决的知识产权,并已从该实体获得授权。J.P. Fessel获得了NIH、Gilead、Actelion、LAM基金会和Parker B. Francis基金会的资助。C.D. Fike是代表美国和国外范德比尔特大学(Vanderbilt University)提交的专利申请的共同发明人,并授权Asklepion Pharmaceuticals使用静脉注射瓜氨酸治疗肺部疾病,目前没有经济补偿。 J.H. Newman has received grants from the NIH. M.E. Pugh has received grant funding from the NIH and has served as a consultant to Gilead. T.W. Rice has received grant funding from the NIH. He has served as a consultant to Avisa Pharma, ACI Clinical and Nestle. He is the Director of Medical Affairs at Cumberland Pharmaceuticals. I.M. Robbins has received funding from the NIH. J.E. Loyd has received grants from the NIH. J. West has received grants from the NIH and Cumberland Pharmaceuticals, and holds intellectual property without financial gain at Cumberland Pharmaceuticals.
支持声明:这项工作由国家心肺和血液研究所资助P01-HL-108800。该项目得到了国家先进转化科学中心CTSA奖UL1TR000445的支持。它的内容完全是作者的责任,并不一定代表国家促进转化科学中心或国家卫生研究院的官方观点。葛兰素史克以RAS肽检测的形式提供了研究化合物和实物支持。本文的资助信息已存入交叉参考基金注册.
- 收到了2017年12月18日。
- 接受2018年4月25日。
- 版权所有©ERS 2018