摘要
男性高雌二醇(E2)和低脱氢表雄甾酮硫酸盐(DHEA-S)水平是肺动脉高压(PAH)的危险因素,但性激素是否与女性的PAH有关尚不清楚。
年龄≥55岁的绝经后多环芳烃患者按年龄和体重指数与无心血管疾病的女性匹配。用免疫分析法测定血浆性激素水平。
低水平的DHEA-S (p<0.001)和高水平的E2 (p=0.02)与PAH相关。在PAH病例中(n=112),较低的DHEA-S水平与较差的血流动力学(p均<0.01)和更多的右心室扩张和功能障碍(p均=0.001)相关。较低的DHEA-S水平与较短的6分钟步行距离(6MWD) (p=0.01)和较差的功能等级(p=0.004)相关。Ln(1)µg·dL−1DHEA-S的降低与死亡风险翻倍相关(危险比2.0,95%可信区间1.5-2.7;p < 0.001)。E2水平越高,6MWD越短(p=0.03),功能等级越差(p=0.01)。
高E2和低DHEA-S水平与绝经后妇女多环芳烃的风险和严重程度有关。应研究激素调节作为多环芳烃的治疗策略。
摘要
较低水平的DHEA-S可预测绝经后多环芳烃患者的患病风险、临床严重程度和死亡http://ow.ly/jo6e30jOFni
简介
肺动脉高压(PAH)通常影响年轻女性,但最近的登记显示,女性甚至在老年人中也占主导地位[1].女性多环芳烃患者的生存率高于男性,这可能与右心室(RV)适应的差异有关[2].性激素水平随年龄增长的时间变化可能进一步改变多环芳烃的流行病学[3.].在没有临床心血管疾病的绝经后妇女中,我们已经证明性激素水平和性激素代谢和信号的基因型变异与RV功能相关,但这些关系在PAH中尚未得到广泛研究[4,5].
我们最近证实,与健康对照组相比,多环芳烃男性的循环雌二醇(E2)水平较高,脱氢表雄甾酮-硫酸根(DHEA-S)水平较低,且这种情况(高E2/低DHEA-S)与较差的临床状况有适度的相关性[6].雌激素在某些动物模型中可诱发肺动脉高压[7],但被推测有保护心脏的作用[8].在一项中试试验中,我们通过阿那曲唑阻断芳香化酶来降低E2水平,增加了6分钟步行距离[9].相比之下,脱氢表雄酮似乎对实验性肺动脉高压有持续的益处通过虽然这些研究主要包括雄性动物[10].最近的一项无偏代谢物谱研究表明,与健康对照组相比,多环芳烃患者中DHEA-S及其代谢物减少,且较低的DHEA-S循环水平与多环芳烃患者的死亡率相关[11].考虑到实验和临床研究中不同的观察结果,类固醇激素信号的复杂性以及激素作用、性别、年龄和其他临床因素之间的潜在相互作用,有必要在离散的多环芳烃患者人群中进行更全面的激素分析。
我们试图确定性激素水平(E2, DHEA-S,睾酮,孕酮,性激素结合球蛋白(SHBG))是否与绝经后妇女的PAH相关。我们比较了绝经后多环芳烃妇女的循环血浆中这些激素的水平,与没有临床心血管疾病的年龄和体重指数(BMI)相匹配的对照组相比。我们假设,较高的E2和较低的DHEA-S水平与PAH的高风险相关(如男性),但这一特征与肺血管和RV功能的标记物有不同的关系。
方法
研究样本
我们进行了一项病例对照研究,将患有PAH的绝经后妇女与没有临床心血管疾病的年龄和bmi相匹配的绝经后妇女进行比较。病例来自布朗大学(普罗维登斯,RI, USA)罗德岛医院肺动脉高压中心、宾夕法尼亚大学(Philadelphia, PA, USA)肺血管疾病项目和塔夫茨医学中心(Boston, MA, USA)肺动脉高压中心。对照组从动脉粥样硬化多民族研究(MESA)-RV研究中选择,该研究是先前描述的一项基于人群的流行病学队列研究[12].MESA-RV的排除标准包括体重为>300磅、怀孕、阻碍长期参与或接受心脏磁共振成像(MRI)和临床心血管疾病,定义为参与者在筛选问卷中回答为“是”,有医生诊断的心脏病发作、中风、短暂性缺血发作、心力衰竭、心绞痛、当前心房纤颤的病史,或既往接受过任何心血管手术。
使用相同方法确认病例和对照组的绝经后状态。在MESA和三个肺动脉高压中心中的两个,如果参与者回答“是”经历过更年期,并且“是”距离最后一次月经周期至少有12个月的时间间隔,则被视为绝经后。为了确保所有受试者的绝经后状态,研究样本中只包括年龄≥55岁的女性[13].目前激素治疗(雌激素、孕酮、睾酮化合物或脱氢表雄酮补充剂)的使用者被排除在外。
案例和控制定义
我们纳入了由治疗医师指定的患有特发性结缔组织病(CTD)或先天性心脏病(CHD)相关PAH的绝经后妇女。此外,PAH的传统血流动力学标准(静息时平均肺动脉压(mPAP)≥25 mmHg,平均肺毛细血管楔形压≤15 mmHg,肺血管阻力(PVR) >3 Wood单位)也是必须的。该研究包括流行(多环芳烃治疗)和偶发(treatment-naïve)患者。对照组来自MESA-RV, 1)心脏MRI测量正常心室和左室测量(射血分数、舒张末期质量和容积);2)无自述慢性阻塞性肺疾病、肺气肿或慢性支气管炎病史;3)肺量计无阻塞性或限制性通气缺陷[12].对照组按年龄(5岁以内)和体重指数(4 kg·m以内)随机2:1匹配−2).
临床变量
回顾了多环芳烃患者的医疗记录或当地研究注册表的临床数据。在(或尽可能接近于)采集性激素分析的同时,收集功能分级、6MWD、血流动力学、超声心动图、脑利钠肽(BNP)水平和PAH治疗。生存状况和死亡日期(如适用)由中心跟踪和报告。从采血到最后一次就诊的中位数时间为34.5个月(95% CI 27.5-43.0个月)。
类固醇激素水平
血液样本的抽取和储存采用了标准化的程序。在佛蒙特大学(Burlington, VT, USA)的临床生物化学研究实验室,使用Roche e411系统(F. Hoffman-La Roche, Basel, Switzerland)测量PAH病例和对照组的血浆性激素。E2组间变异系数为2.2 ~ 10.5%,DHEA-S 4.6 ~ 6.5%,睾酮2.3 ~ 5.6%,孕酮9.5 ~ 11.5%,SHBG 3.0 ~ 4.7%。
获得所有PAH和MESA参与者的知情同意。每个中心都获得了机构审查委员会(IRB)对这项研究的批准(罗德岛医院:IRB注册#021911;宾夕法尼亚大学:IRB注册#706091;塔夫茨:IRB注册#7437)。MESA方案得到了所有MESA站点的irb和国家心肺和血液研究所的批准。
统计分析
所有分析均采用SAS软件9.4 (SAS, Cary, NC, USA)进行。连续数据以中位数(四分位范围)表示,分类数据以n(%)表示。性激素水平是自然对数转换的。使用GLIMMIX程序完成建模。病例对照状态采用激素水平的广义估计方程(GEE)和经典三明治估计,假设二元分布,其中观察结果嵌套在匹配组内。同样,激素水平的模型由病例对照状态使用GEE和假设对数正态分布。使用SAS软件设计的宏完成年龄和BMI的病例对照随机匹配。在PAH病例中,性激素水平与临床指标之间的关系采用适当的多变量线性或二项回归分析。Cox风险回归用于模拟激素水平与生存率之间的关系,使用PHREG程序和似然比检验。利用最大检验检验比例风险假设,并利用SAS宏计算Cox比例风险模型的Harrell的c统计量[14].Kaplan-Meier估计用于用LIFETEST程序通过增加DHEA-S水平来估计死亡前的时间。最后一次追踪被用于权利审查。最后的模型进一步调整为准确的年龄和BMI值。所有假设均采用双尾检验进行检验,并计算95%置信区间估计值。α建立在0.05水平。
结果
该研究共纳入112例绝经后多环芳烃(PAH)妇女(表1).大多数患者有ctd相关的多环芳烃(58%),其中大多数(n=48, 74%)有系统性硬化,其次是特发性多环芳烃(35%)。受试者倾向于有中度血流动力学损伤,50%为功能III或IV级。在匹配年龄和BMI后,78例患者与149例对照进行对比分析。由于MESA-RV队列的多民族性质和排除了非规范心肺测量的个体,存在种族/民族的不平衡,特别是在白人(86%的多环芳烃病例,53%的对照组)和亚裔(1%的多环芳烃病例,28%的对照组)受试者中。总PAH队列(n=112)的临床特征与比较分析的病例(n=78)几乎相同。
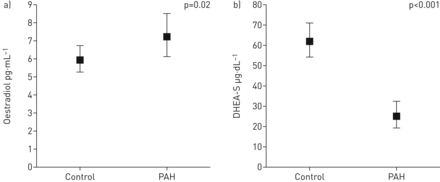
激素水平与多环芳烃状态的关系在表2,在线补充表S1,图1及在线补充图S1.除孕激素外,多环芳烃患者与对照组的所有激素水平均有显著差异。与对照相比,多环芳烃患者中DHEA-S水平降低60% (p<0.001) (图1而且在线补充表S1).相反,与匹配对照组相比,PAH中E2水平较高(p=0.02) (图1而且在线补充表S1).DHEA-S、总睾酮、生物有效睾酮和SHBG水平较低与多环芳烃几率增加相关。DHEA-S、总睾酮、生物有效睾酮和SHBG每降低一个单位,PAH的几率增加3 - 4倍(表2).当年龄和BMI作为连续参数加入模型时,这些结果没有变化。
匹配年龄和体重指数后,根据病例状态调整激素水平的参数估计。1)雌二醇;b)脱氢表雄甾酮硫酸盐(DHEA-S)。数据以中位数(95% CI)表示。PAH:肺动脉高压。
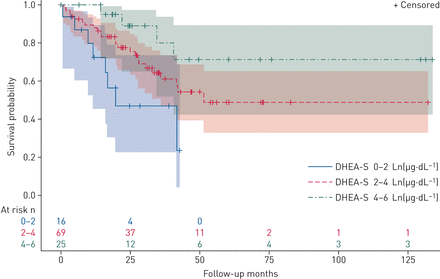
研究了所有病例(n=112)的循环激素水平和疾病严重程度指标之间的关系,并根据年龄和BMI进行了调整。通过功能等级、6MWD、血流动力学(包括较高的右心房压(RAP)、mPAP和PVR)和超声心动图(超声心动图)评估,较低的DHEA-S水平与更严重的疾病相关。表3,图2而且3.).例如,每个Ln(1)µg·dL−1) DHEA-S的下降与较短的6MWD(−30 m, 95% CI−54 ~−6.5 m;p = 0.01)。这些关系在肺血管和右心功能指标上是一致的。较低的DHEA-S水平可能与较低的心排血量(p=0.07)和较高的BNP水平(p=0.06)有关。最后,DHEA-S水平的较低增量与死亡率的增加相关(图4).Ln(1)µg·dL−1DHEA-S的降低与死亡风险翻倍相关(危险比2.00,95% CI 1.46-2.72;p<0.001),校正年龄和BMI (表4).Cox模型进一步调整了PAH类型、6MWD、RAP和功能等级,DHEA-S的估计没有变化,尽管由于样品量较小,精度较低。1名受试者失访。中位随访时间为24.8个月(95% CI 19.6-30.0个月),由于此窗口期死亡病例极少,因此无法计算中位生存时间。前25%的患者在25个月时死亡(95% CI 16.0-35.6个月),在此时间点有36例死亡和74例仍活着(被删减)。
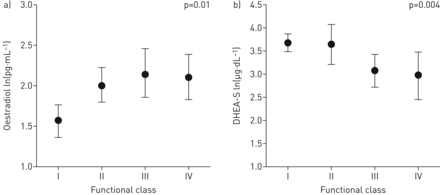
肺动脉高压(PAH)病例中按功能类别调整激素水平的参数估计。1)雌二醇;b)脱氢表雄甾酮硫酸盐(DHEA-S)。数据以中位数(95% CI)表示。p值:跨类别趋势检验。
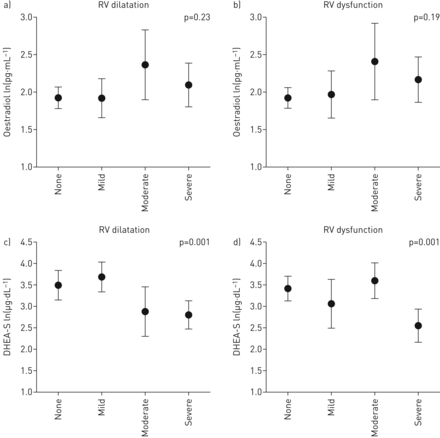
根据肺动脉高压(PAH)病例超声心动图上右心室(RV)扩张程度(a, c)和功能障碍程度(b, d)对激素水平的调整参数估计。a, b)雌二醇;c, d)脱氢表雄甾酮硫酸盐(DHEA-S)。数据以中位数(95% CI)表示。p值:跨类别趋势检验。
肺动脉高压病例的Kaplan-Meier生存估计和95%置信限。随访期间有危险的受试者数量。硫酸脱氢表雄酮(dhea - s: dehydroepiandrosterone-sulfate。
较高水平的E2与较短的6MWD和较高的RAP相关(表3).每Ln(1 pg·mL−1) E2增加与6MWD缩短32 m相关(95% CI−62 ~−4 m;P =0.03),也反映在较差的功能类(图2).虽然其他循环激素和疾病标志物之间存在一些显著的关系(如。较低的睾酮水平和较高的mPAP和BNP水平),这些发现是不一致的或不那么有力的(在线补充图S2和S3).脱氢表雄酮- s是唯一与存活有关的激素。
由于脱氢表雄酮是E2和睾酮的前激素(睾酮可以芳香化成E2),我们研究了激素之间是否存在相关性。首先,E2和DHEA-S水平(r=0.17)或睾酮(r=0.22)之间没有显著相关性。DHEA-S水平与睾酮水平之间存在一定的相关性(r=0.55)。其次,当模型中加入E2或睾酮时,DHEA-S水平与多环芳烃风险和所有临床严重程度指标之间的显著关联不受影响(数据未显示),表明DHEA-S结果的独立性。第三,在DHEA-S模型中加入E2和睾酮,在总睾酮模型中加入E2时,没有明显的调节作用(数据未显示)。
最后,在敏感性分析中,病例对照比较仅局限于白人和黑人受试者,结果是相同的,没有证据表明在激素水平和临床结果之间的模型中种族的影响修改(或相互作用)(数据未显示)。当我们将我们的分析局限于特发性多环芳烃病例亚组时,DHEA-S的结果没有变化,包括较低的DHEA-S水平和死亡率之间的关系(p=0.02)。然而,由于样本量较小(n=26)(数据未显示),病例和对照组之间的E2水平差异不再明显。E2水平越高,6MWD越低(−31 m, 95% CI−55 ~−8 m;p=0.01)。未治疗的PAH患者数量很少(n=11,匹配病例的14%;N =22,不匹配的情况为20%)。当我们从分析中排除这些受试者,只包括流行(那些多环芳烃特异性治疗)病例(数据未显示)时,结果没有变化。
讨论
我们发现,与没有临床心肺疾病的年龄和bmi匹配的对照组相比,特发性、CTD和冠心病相关的绝经后妇女的特征是DHEA-S、睾酮和SHBG水平较低,而E2水平较高。较低的DHEA-S水平与显示PAH临床严重程度较高的多种指标密切相关,包括运动耐受性(6MWD,功能级别)、右心室后负荷(mPAP, PVR)和右心室功能(RAP,右心室扩张和功能障碍,可能是心输出量和BNP)。DHEA-S的低水平与死亡风险的增加有关。较高水平的E2与较短的6MWD、较高的RAP和较差的功能等级相关,但与生存率无关。绝经后妇女的低DHEA-S/高E2情况与我们对多环芳烃男性的研究相似[6],尽管绝经后妇女的相关性更强,部分原因可能是样本量的差异。令人惊讶的是,绝经后女性多环芳烃患者的睾丸激素水平在男性多环芳烃患者中未被检测到。DHEA-S、E2和睾酮的研究结果并不相关,这意味着它们都可能对肺循环和DHEA-S的RV有直接影响。
临床前和观察性研究表明,DHEA-S可能在多环芳烃患者的心肺功能中发挥重要作用。DHEA受体与内皮型一氧化氮合酶偶联,DHEA调节内皮素-1的合成并抑制内皮素-1启动子活性[15,16],是PAH的两个主要病理和治疗靶点。人肺动脉内皮细胞(PAECs)积极代谢DHEA,治疗伴有DHEA的PAH患者的PAECs会降低信号转换器和转录激活因子3 (STAT3) [17,是肺血管重构的重要中介。较低的DHEA- s水平与全身内皮功能障碍和血管重构有关,补充DHEA可恢复男性和绝经后女性的正常血管功能[18,19].恢复脱氢表雄酮a水平可以有效减轻肺后负荷,因为多环芳烃的特征是两性中低循环水平的脱氢表雄酮- s,这些低水平与较差的血流动力学(包括较高的PVR)相关。
此外,较低水平的DHEA-S与较差的RV功能相关,这可能解释了与6MWD和功能级别的关系。DHEA-S水平低与左心衰的临床严重程度和死亡风险增加有关[20.].脱氢表雄酮逆转心肌细胞肥大,提高组织胶原蛋白和纤维连接蛋白水平[21减少心肌纤维化,多环芳烃患者右心室重塑和失代偿的关键表型变化[22].在Sugen/缺氧肺高压模型中,DHEA治疗可改善心脏指数,抑制RV毛细血管稀疏、纤维化和氧化应激[10],提示DHEA可能对右心室和肺血管系统有直接的有益作用。
在男性和绝经后女性中,较低的DHEA-S水平与多环芳烃风险和疾病严重程度有关,但性激素水平如何与性、治疗反应和多环芳烃的结果相互作用尚不清楚。DHEA与一氧化氮、内皮素-1和RV重构的关键联系可以解释患病率和生存率的性别差异,以及使用磷酸二酯酶5型抑制剂和内皮素受体拮抗剂治疗的患者的不同治疗反应[23,24].本研究中联合治疗的高比率(>80%)禁止分析治疗特异性相互作用。最近一项使用无偏代谢物谱分析的研究表明,与未匹配的对照组相比,多环芳烃患者中DHEA-S及其代谢物减少,且较低的DHEA-S循环水平与死亡风险增加有关[11],但DHEA-S水平与临床测量之间的关系尚未报道。在8例慢性阻塞性肺疾病相关肺动脉高压患者中,使用3个月DHEA的开放标签治疗与6MWD显著增加和血流动力学改善相关[25].总之,这些观察结果表明,脱氢表雄酮应该作为一种潜在的多环芳烃治疗方法进行研究。
鉴于女性的优势和雌激素与骨形态发生受体II型通路之间的重要交叉点,雌激素在肺血管疾病中的作用一直备受关注[26].在男性和本研究中,与对照组相比,在多环芳烃中观察到较高的E2水平,且较高的E2水平与一些临床严重指标相关,但E2水平与死亡率之间没有关系,当我们将分析局限于特发性多环芳烃时,E2信号减弱。这可能是因为循环中的E2水平不能反映肺循环中的生产、代谢或影响,而所有这些都在肺血管疾病中显示出重要作用。另外,E2可能在肺血管- rv回路中有不同的影响,导致与疾病指标的关系被稀释。在一项小型安慰剂对照、双盲、随机临床试验中,我们发现芳香化酶抑制剂阿那曲唑可降低E2水平并增加6MWD,但对RV功能无影响[9].阿那曲唑可降低循环中的E2水平,但其程度低于乳腺癌中所报道的[27].外周水平可能不能反映局部的心肺活动,因此可以解释这里看到的不那么强烈的联系。对于雌激素水平下降的绝经后妇女,更敏感的E2及其代谢物检测可能更有价值。
由于类固醇信号是复杂的,而且单个激素在生物学上高度相关,我们试图确定我们的一些发现是否共线。孕激素,E2和睾酮的母体激素,在病例和对照组之间没有变化,也没有观察到与任何临床测量的关联。同样,在我们的病例中,没有证据表明生物学相关激素(E2和睾酮;脱氢表雄酮- s和E2;DHEA-S和睾酮)。在我们的试验中,阿那曲唑降低了E2的水平,但对DHEA-S、睾酮、生物可利用性睾酮或SHBG的水平没有影响[9].这表明,正如在实验模型中所看到的[19,28], DHEA-S, E2和可能的睾酮对多环芳烃有独特和直接的影响,应该加以描述。同样的事实是,考虑到暴露(性类固醇合成、代谢和信号)和疾病的复杂性,离散的激素分析可能会错过重要的信号,而这些信号本可以用整个“激素体”的系统生物学方法揭示[29].
本研究的局限性在于,在主要治疗的PAH患者中只测量了一次激素水平,并且病例和MESA对照来自两个不同的抽样人群。在多环芳烃病例中,临床数据是在抽血时或在抽血时尽可能接近性激素水平时收集的,范围是全面的。在多环芳烃病例中,激素测量和临床评估的时间差异可能偏向于零值。虽然性激素的纵向评估可能会更有启发性,但在运动耐受性、血流动力学和超声心动图的范围内,尤其是DHEA-S和E2(在较小程度上)的显著关联,以及在两性中观察到的高E2/低DHEA-S信号的一致性,强烈表明这些关系不仅是副现象,而且对疾病病理学很重要。多年来,健康的绝经后妇女的激素测量结果已被证明是稳定的[30.,31],但尚不清楚多环芳烃中性激素水平的变化是否更快。对照样本中亚洲受试者多于PAH病例;没有亚洲受试者的敏感性分析也得出了相同的结果。尽管性激素(及其作用)会因种族而异[5,30.],与疾病指标的关联和缺乏种族效应修正表明,在病例和对照组中看到的激素水平差异不是由于种族,而是与多环芳烃有关。考虑到队列的绝经后性质,大多数病例有ctd相关的多环芳烃。与多环芳烃一样,ctd主要影响女性。两项针对系统性硬化症女性的小型研究表明,E2水平较高,脱氢表雄甾酮- s水平较低[32,33];对多环芳烃亚型和敏感性分析(仅包括特发性多环芳烃受试者)的调整没有改变我们的结果。RV功能的附加和更多信息度量(即。MRI、n端促激素BNP)在临床上不可用。
结论
较低水平的DHEA-S可预测绝经后多环芳烃患者的患病风险、临床严重程度和死亡。此外,在病例中观察到较低水平的睾酮和较高水平的E2,并使用一些临床指标进行跟踪,但这些关系不那么稳健,不能预测结果。每种激素之间的关系不同,似乎没有相互关联。总之,这些观察结果支持了性类固醇在多环芳烃和右心室衰竭发展中的重要性,并提示激素调节可能是肺血管疾病的一种可行的治疗策略。
补充材料
补充材料
请注意:补充材料不由编辑部编辑,上传时由作者提供。
补充材料erj - 00467 - 2018 - _suppl_material
补充FigureS1erj - 00467 - 2018 - _figs1
补充FigureS2erj - 00467 - 2018 - _figs2
补充FigureS3erj - 00467 - 2018 - _figs3
确认
该手稿已经过所有研究者的科学内容和数据解释的一致性与以前的MESA出版物的审查。重要的评论在提交出版之前已经被纳入。作者感谢MESA研究的其他研究者、工作人员、多环芳烃患者和参与者的宝贵贡献。参与MESA调查人员和机构的完整名单可在此找到www.mesa-nhlbi.org
脚注
本文的补充资料可从www.qdcxjkg.com
利益冲突:S.M. Kawut报告了Actelion、联合治疗公司、吉利德、肺生物技术公司、拜耳和心血管医学研究与教育基金的资助(用于研究和CME),以及来自美国胸科学会的个人费用(用于旅行),在提交的工作之外。
利益冲突:J.R. Klinger报告了来自Actelion, United Therapeutics, Gilead, Eiger和Bayer的资助,在提交的作品之外。
利益冲突:H.I. Palevsky报告了在提交的工作之外,从Actelion、Janssen、Bayer、GSK和United Therapeutics收取的个人费用。
利益冲突:I.R. Preston报告了来自Actelion的拨款和个人费用,来自拜耳和吉利德的拨款,以及来自Arena、联合治疗和辉瑞的个人费用,这些都是在提交的工作之外。
利益冲突:A. Smith报告了Actelion、Gilead和United Therapeutics在提交作品之外的资助。
利益冲突:M. Whittenhall报告了在提交的工作之外,从Actelion、拜耳、吉利德和联合治疗公司收取的个人费用。
利益冲突:C.E. Ventetuolo报告了拜耳、Acceleron和United Therapeutics的个人费用,以及CHEST基金会(Actelion赞助)和Eiger支付给她所在机构的经费,这些都在提交的工作之外。
利益冲突:C. Archer-Chicko报告了Actelion在提交作品之外的个人费用。
支持声明:这项工作是在国家卫生研究院的国家普通医学科学研究所(P20 GM103652)的机构发展奖(IDeA)的支持下完成的,来自美国心脏协会的11FTF7400032,以及来自国家心肺和血液研究所的K24-HL103844。国家心脏、肺和血液研究所的合同R01-HL086719、R01-HL077612、HHSN268201500003I、N01-HC-95159、N01-HC-95160、N01-HC-95161、N01-HC-95163、N01-HC-95164、N01-HC-95165、N01-HC-95166、N01-HC-95166、N01-HC-95166、N01-HC-95166、N01-HC-95166、N01-HC-95166、N01-HC-95167、N01-HC-95168和N01-HC-95169提供了对MESA的支持,国家推进转化科学中心的拨款ul1 - tr000040、ul1 - tr001079和ul1 - tr001420。本文的资助信息已存入Crossref基金管理人登记处.
- 收到了2018年3月6日。
- 接受2018年4月26日。
- 版权所有©ERS 2018