摘要
确定了药物治疗反应测试雌性生殖道Ser1159Pro对囊性纤维化调节剂治疗具有响应性http://ow.ly/dvsq30jcBMw
编辑器:
囊性纤维化(CF)是一种致命的多系统遗传疾病,由囊性纤维化跨膜电导调节因子(CFTR)突变引起,CFTR是一种氯转运体,对呼吸气道和其他导管上皮表面的管腔液体稳态至关重要。ivacaftor和lumacaftor/ivacaftor的批准改变了一些CF患者的治疗选择,这两种药物分别适用于罕见III类突变子集杂合子的患者[1或普通II类突变Phe508del的纯合子[2].尽管,超过40%的CF患者不符合雌性生殖道突变特异入选标准和排除这些疗法,虽然它是不切实际的CFTR为每个新pharmacotherapy-responsive进行临床试验检测突变鉴定,药物审批过程的进化现在允许扩张基于药品标签在体外生理反应测试。事实上,基于病人细胞的新方法的发展,如培养肠道类器官[3.,4或鼻上皮球体[5)许可证在体外靶向CFTR分子疗法的测试。在这里,我们报道了一种新的临床前试验,在这样的患者中证明了患者特异性的CFTR功能矫正体外随后开始治疗和功能矫正在活的有机体内.此外,虽然lumacaftor/ivacaftor治疗有不良呼吸影响的报道[6],对治疗适应期的全面描述以前没有报道过,这里我们提供这一现象的详细描述。
一名38岁男性患者经汗液试验诊断为CF,具有典型的临床病程和不确定的CFTR基因分型,尽管CF自我治疗的依从性很强,但由于肺功能下降,人们越来越担心他的健康。受CFTR突变特异性药物疗法的出现和改进的基因检测的可用性的启发,这位极其积极的患者寻求CFTR基因测序分析,发现了一个罕见的、特征差的突变ser119pro (C . 3475t >C) [7和常见的II类突变Phe508del (c.1521_1523delCTT)。他在CF患者群体中进行了个人调查,然后开始在自己的护理团队中进一步考虑评估和治疗方案。他接受了CFTR临床前治疗反应试验[5分离鼻部上皮细胞,培养成球形和气液界面(ALI)单层细胞,并测量其对ivacaftor和/或lumacaftor的反应。
该方案是由辛辛那提儿童医院医疗中心机构审查委员会批准的。鼻细胞培养和分析如既往报道[5,8].
通过刮除法从两个下鼻甲中获得鼻上皮细胞,用Accutase (Innovative Cell Technologies Inc., San Diego, CA, USA)混合、分散,悬浮在含抗生素和ro激酶抑制剂的dmemf12培养基中,并接种到涂有VitroCol的培养皿中(Advanced BioMatrix, San Diego, CA, USA)。用受辐照的小鼠胚胎成纤维细胞饲喂细胞预先播种。每天更换培养基,5天后去除抗生素,保持培养直到鼻细胞融合。用0.1%胰蛋白酶分离细胞,然后保持球形或ALI细胞单层培养。
鼻上皮细胞球形培养和camp诱导肿胀的测量:培养的鼻上皮细胞悬浮在生长因子降低的基质中,浓度为500 000细胞·mL−1100 μ l等价物播种于16 mm四孔板中。孵育后(37°C, 5% CO2在培养过程中每天更换dmemf12基培养基,直到球体成熟(7-10天)。在培养基中加入含forskolin(10µM)和IBMX(100µM)的磷酸盐缓冲盐水以增加细胞内cAMP水平之前(基线)和1小时后,在孵育的显微镜室中通过捕捉明亮视野图像测量鼻上皮细胞球形肿胀。在增产时,一些井使用lumacaftor (3 μM)预处理48 h,或一些井使用ivacaftor (1 μM)预处理。鼻上皮细胞球形肿胀是通过手动勾画球形管腔,然后自动测量管腔面积,通过配对显微照片确定刺激前后球形管腔面积的变化。
ALI细胞单层培养和camp诱导的短路电流测量:将培养的鼻细胞悬浮在dmemf12为基础的培养基中,并将其接种到Transwell板(Corning, Inc., NY, USA)覆盖iv型胶原蛋白的透明透性插入物(孔径0.4 μm)上,约260 000个细胞·cm−2.细胞保存至成熟(4-6周),直到经上皮阻力达到约500-1000µΩ·cm−2.选择的插入物在研究前用lumacaftor (3 μM)预处理48小时。插入物安装在Ussing室中,并在不对称的氯溶液中研究,以产生基底外侧至顶端的氯-分泌梯度。用100µM阿米洛利阻断ENaC和钠转运。在两个室中分别加入Forskolin(10µM)和IBMX(100µM)增加cAMP,刺激CFTR。对于选择插入,添加ivacaftor(1µM)以增强CFTR。最后,将CFTR抑制剂-172(10µM)加入根尖室阻断CFTR电流。在电压钳位条件下测量短路电流和电阻。
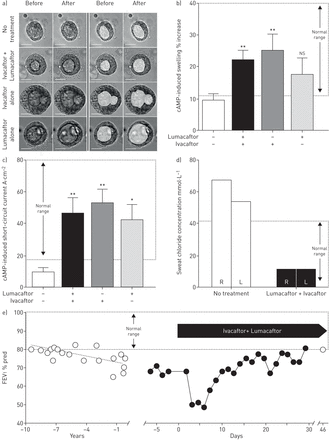
药物治疗反应试验显示,经lumacaftor/ivacaftor治疗的鼻上皮球体在camp刺激下肿胀,腔区面积平均增加22.27%,而未治疗的为9.37% (p=0.002)。单独使用ivacaftor也可以得到纠正(p=0.005),单独使用lumacaftor也有纠正的趋势(p=0.065)。这些结果表明Ser1159Pro/Phe508del鼻上皮球体对lumacaftor/ivacaftor的药理学校正体外(图1一个b),这在开始昂贵的终身治疗之前很重要。
囊性纤维化跨膜电导调节(CFTR)特异性药物治疗的临床前试验和临床反应。从患者获得鼻腔上皮细胞,保持球形或气液界面(ALI)单层细胞培养,用于测量camp诱导、cftr介导的生理反应体外(a - c)。然后开始口服lumacaftor/ivacaftor治疗,并测量治疗相关的生物标志物和临床结果反应(d-e)。a)在没有或存在ivacaftor + lumacaftor治疗的情况下,添加forskolin和IBMX刺激camp诱导的cftr依赖性肿胀的活化前后鼻细胞球形的代表性显微镜照片。白色掩蔽表示椭球腔。比例尺:100µM。b)从显微照片确定camp诱导的球形管腔面积的变化,如图10-11所示。对每种条件下成对的管腔面积变化进行评估。c)在有或没有lumacaftor和/或ivacaftor预处理的培养下,camp诱导的ALI细胞单层短路电流变化。每种条件下评估3至4个ALI细胞单层。d) lumacaftor/ivacaftor治疗前2周和治疗后7周获得标准的临床氯汗试验结果,显示右(R)和左(L)手臂氯汗的治疗相关正常化。e)测量患者1秒内用力呼气量(FEV)1)或使用个人手持式肺活量计(Spiro PD 1.0, PMD保健;Allentown, PA, USA)(封闭圈)。lumacaftor/ivacaftor治疗第46天,FEV1为肺功能实验室预测值的79%。t形条表示标准误差。* *: p < 0.01;*: p < 0.05;ns: p>0.05与不含lumacaftor或ivacaftor的ALI细胞单层比较,采用方差分析计算。b和c所示值的正常范围代表健康受试者的95%置信区间,如先前报告[4].
lumacaftor和ivacaftor单独或联合治疗ALI单分子膜,证实了这种药理学反应。所有处理条件都导致短路电流增加,证实了CFTR的功能修正。(图1 c),以及个别ALI与球体反应之间的相关性此前已有报道[5].
首次证明药效学校正者在体外, lumacaftor/ivacaftor治疗的效果得到证实在活的有机体内在开始治疗5周后进行汗液测试。患者的汗液氯化物试验正常为11 mEq·L−168 mEq·L异常−1和54毫克当量·L−1治疗开始前2周的记录(图1 d).
ivacaftor/lumacaftor治疗开始后1天,患者在休息时出现呼吸困难,轻度喘息,胸部不适,1秒内用力呼气量(FEV)下降1)至预测的50%。在接下来的3天里,他报告呼吸困难恶化,持续的喘息和胸痛,以及全身“流感样”症状的出现,包括不适、全身肌肉疼痛、头痛、嗜睡和食欲不振。FEV持续下降149 - 50%的预测。经过5天的治疗,他注意到肺部和全身症状的改善,尽管持续的胸闷和开始的湿盗汗。治疗1周后,患者全身症状缓解,胸闷、呼吸困难、喘息持续改善,但咳嗽和痰量增加(每天2-3汤匙)。FEV1增加到预测值66%至77%之间。在治疗的第3和第4周,患者报告有轻微呼吸困难,喘息减轻,轻微胸闷,产生稀薄、透明到略黄的痰液。他恢复剧烈运动,导致短暂的胸闷、明显的喘息、痰量增加和运动后咯血,所有这些在停止运动后数小时内消失。
开始lumacaftor/ivacaftor治疗大约1个月后,患者报告“感觉他的肺是干净的”。他之前的基线自发性咳嗽没有出现,仅在气道清除治疗期间出现咳嗽,产生一汤匙无粘性黄白色痰液,顺便说一下,患者还注意到水源性皱纹消失,这是ivacaftor治疗的报道效果[9].经过46天的治疗,FEV1增加到预测的79%;较预估的68%改善了11% (图1 e).
本报告通过对患者来源的鼻上皮球体进行一项新的CFTR治疗反应试验,确定ser1199pro是一种可耐受ivacaftor治疗的CFTR等位基因。研究结果支持扩大适用于CFTR特异性药物治疗的CFTR突变列表,包括ser119pro,并支持基于此发展审批范式的可行性在体外基于单元的CFTR功能测试。鼻上皮细胞和肠上皮细胞似乎都适合用于这一目的,但鼻上皮细胞与下呼吸道上皮细胞相比,与肠上皮细胞更相似;根据我们的经验,病人发现鼻上皮细胞的方法简单而且可以忍受。最后,该患者非凡的毅力导致了对启动lumacaftor/ivacaftor治疗的初始适应期的全面描述,以及随后的恢复和积极的临床反应,这可能对CF患者和医师社区有用。
脚注
利益冲突:无声明。
- 收到了2017年10月5日。
- 接受2018年3月12日。
- 版权©2018人队