摘要
吸入高渗盐水(HS)是粘液阻塞性肺病的有效疗法。然而,与HS管理有关的作用机制和原则仍然尚不清楚。
一个在体外系统气溶病的曝气量与速率相当的速率在活的有机体内条件。共聚焦显微镜测量正常和高浓度黏液状态下气道表面液体(ASL)体积和细胞高度反应。
HS雾化使ASL高度迅速增加,细胞高度降低。虽然细胞高度没有在相同的时间内恢复,但在雾化结束后,增加的ASL体积很快被重新吸收。对重复HS给药的ASL体积反应迟钝,但可通过在HS给药之间插入低渗盐水恢复。hs诱导的ASL水化时间延长,气道表面黏液浓度高,细胞体积略有减少。
HS雾化产生渗透诱导的ASL高度增加,这受到活性钠吸收和细胞体积诱导的细胞水分渗透性降低的限制。气道表面黏液延长HS的作用通过粘液依赖性渗透力,表明高浓度粘液患者HS的作用时间延长。
摘要
本研究提供了高渗盐水对粘液阻塞性疾病气道表面水合作用的影响程度的见解http:///wly/favd30ir9bj.
介绍
粘液纤毛清除的有效性在很大程度上取决于粘液的水合作用。正常情况下,气道上皮细胞具有吸收和分泌离子的能力通过活性离子输送,水的运动受经上皮渗透梯度控制。这种分泌和吸收之间的平衡的净效果是维持粘液层水合作用在足够的水平,以促进有效的粘液清除[1].黏液浓度高,清除不清,是许多黏液阻塞疾病的特征,包括囊性纤维化(CF) [2、原发性纤毛运动障碍[3.]和非CF支气管扩张症[4].
雾化高渗盐水(HS)是一种有效的治疗成人CF [5,6]和非CF支气管扩张症[7,8],改善粘液纤毛清除率,1例患者用力呼气量 尽管HS具有临床应用价值,但其作用机制仍然是推测性的。加速粘液纤毛清除通过与粘蛋白的静电相互作用[9]、膨胀气道表面液体(ASL)水化[10]或抑制上皮钠通道(ENAC)[9]大多数机制研究将大量HS沉积在人支气管上皮(HBE)表面,并没有模拟在活的有机体内气溶胶交付。此外,使用培养的HBE细胞的大多数研究在HBE表面上没有内源正常的正常(2%固体)或过浓度(〜8%固体)粘液[5,10].
根据临床使用规定,HS雾化至下气道表面,体积小(nL·cm)−2·敏−1)量(约15分钟)。在这项研究中,安在体外雾化系统被开发模仿在活的有机体内气道上皮的气溶胶输送率显示了一系列的粘液浓度,从“正常”到粘液阻塞的情况。主要目的是表征HS对气道表面水合作用的动力学。辅助目标是确定提高HS治疗肺部疾病疗效的策略。由于在临床实践中使用的雾化剂和HS的强度差异很大,而且HS的渗透有效性取决于氯化钠(NaCl)输送到气道表面的速率,我们的研究是在µg NaCl沉积cm中进行的−2·敏−1,而不是在给定沉积速率下的HS百分比。其中一些数据以前以摘要的形式报告过[11- - - - - -15].
方法
方法的详细信息请参见在线补充材料.
HBE文化和顶端粘液含量
从移植肺中分离出的原代HBE细胞维持在气液界面,直到完全分化。每天清洗培养表面,产生少量残留粘液模拟正常上皮的HBE培养物,而保留黏液层2周生成HBE制剂,产生更高的黏液成分。
ASL的共焦测量
用2.0µM calcein-AM (Invitrogen, Carlsbad, CA, USA)标记原代HBE细胞基底外侧。加入5µL的德州红葡聚糖(70 000 MW, 5 mg·mL),观察ASL−1;英杰公司)腔的。HS(7%)溶液使用振动网格雾化器雾化(Aeroneb Lab;Aerogen,戈尔韦,爱尔兰共和国),修改以提供小容量(nL·min-1)。根据囊性纤维化基金会指南,每天清洁喷雾器,并定期测试其功能。该系统安装在一个环境室中,该环境室控制气流,调节温度为37°C,湿度>50%,二氧化碳为5%,并与扫描共聚焦显微镜连接通过高速XZ共焦扫描测量细胞和ASL高度。在基线成像后,以规定的速率将7%的HS雾化到HBE细胞的顶端表面,并每隔30秒测量影响。
ELISA法测定白细胞介素-8的分泌
在雾化3,8或18μgNaCl·cm后24小时测量HBE中白细胞介素(IL)-8的生产−2·敏−1或PBS假朦胧(对照)。为了比较,平行培养用大量添加高渗盐水(100µL 7%溶液)处理。根据制造商的方案,使用人IL-8 ELISA试剂盒(R&D Systems, Minneapolis, MN, USA)测定培养基中IL-8的浓度。简单地说,孵育后,将培养基取出。样品和标准品加入到预包有抗人IL-8单克隆抗体的微孔板中,孵育2小时。每孔洗涤并与人IL-8特异性的酶联多克隆抗体孵育2小时。冲洗孔,去除未结合的抗体-酶试剂,在室温下每孔加入底物溶液20 min,停止酶反应,将光密度结果与标准曲线比较,确定IL-8浓度。
数学建模
W的气道流体运输模型黑影等.[16,用于构建人类气道离子和流体运输的综合模型[17,18].该模型求解了膜电位(V一个,Vb),胞内钠、氯、钾离子浓度([Na+]我, (Cl−]我,[K.+]我细胞外离子浓度([Na+]e, (Cl−]e,[K.+]e)和细胞外和细胞内液量(We,W我) [18].对于HS模拟,具有高浓度NaCl的水被“将”加入到顶端表面上的用于指定的体积。
统计分析
所有数据分析和图形都在Sigmaplot(Systat Software,San Jose,Ca,USA)进行。比较平均值通过单向ANOVA,具有HOLM-SIDAK方法,用于在统计上显着的发现中的成对多重比较。对于非正常数据,使用kruskal-wallis单向Anova,其中有多个组比较通过邓恩的方法。配对t检验或Mann-Whitney秩和检验在适当的情况下使用。
结果
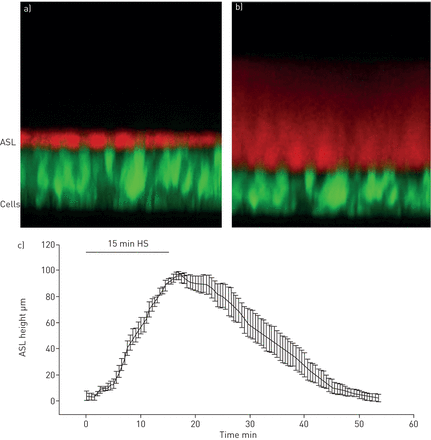
第一组研究集中于HS对根尖表面“正常”黏液浓度(1.9±1.7%固体)的HBE培养物的影响。HS以8µg NaCl·cm的速率送往HBE培养15分钟−2·敏−1(7% HS在110 nL·cm下分娩−2·敏−1)模仿人类受试者的标准喷射雾化器递送率(在线补充材料).观察到ASL高度迅速显著增加,反映了渗透驱动的经上皮液流动对HS沉积的响应[19) (图1)在雾化终止后,渗透膨胀ASL的净再吸收立即开始,ASL高度在60秒内恢复到基线高度 气溶胶开始后分钟。
a) 用钙黄绿素(一种荧光绿色染料)和德克萨斯红葡聚糖(一种细胞不透性红色染料)染色的气道表面液体(ASL)染色的气道上皮细胞横截面的XZ共焦图像;b) 在给予渗透刺激(高渗盐水(HS))后,ASL高度增加,同时细胞高度下降;c) 将HS雾化于人支气管上皮培养物表面(8 微克氯化钠·厘米−2·敏−115分钟)导致ASL高度的显着瞬态增加,持续<1小时。每个实验n = 8。
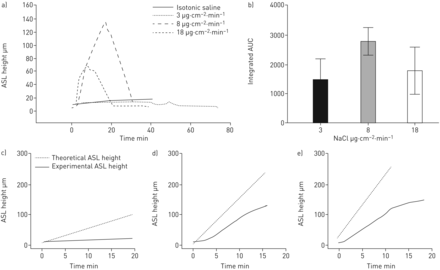
在临床实践中,喷射雾化器通常在〜15分钟内以4ml剂量递送HS,而振动网雾化器在〜5分钟内提供相同的体积。为了解决HS输送率是否会影响ASL体积反应,在不同的雾化速率下,将恒定的盐总质量雾化到HBE表面上,因此雾化的持续时间。选择用于研究的速率被设计为MIMIC交付7%HS通过喷射星云(8µg NaCl·cm)−2·敏−1),振动网状星云(18µg NaCl·cm)−2·敏−1)和任意定义的“慢”雾化器(3μg·cm−2·敏−1) (图2一个).8 μ g NaCl·cm和18 μ g NaCl·cm−2·敏−1速率使ASL高度迅速而显著地增加。培养物对3µg NaCl·cm的响应−2·敏−1相对于ASL体积膨胀,速率要小得多,但由于星云持续时间延长,速率要长得多。所有培养物,不论雾化速率如何,一旦停止雾化,就会迅速从ASL吸收增加的体积。
高渗盐水(HS)输送速率的变化对气道表面液体(ASL)体积反应的影响。a)三种雾化HS(低3µg NaCl·cm)的ASL高度的比较−2·敏−1;8µg NaCl·cm−2·敏−1;高18µg NaCl·cm−2·敏−1),持续时间不同,以保持盐的总输送质量不变。等渗盐水作为对照。与等渗盐水对照组相比,所有组均P <0.05。b)绝对身高变化和总水合作用(随时间的综合面积)均有利于中剂量方案,但没有达到统计学意义(p=0.373)。c, d, e)理论高度表明,如果所有的盐沉积导致进入ASL的水的等摩尔通量,ASL高度的预期上升。实验ASL高度线表示实验中观察到的实际ASL高度变化。这两条线不能覆盖表明水从上皮细胞运输到肌萎缩性侧索硬化症的抑制。c)低剂量雾化(3µg NaCl·cm)−2·敏−1):理论斜坡4.72μm·min−1与实验斜率为0.45µm·min−1(p < 0.001);d)中剂量雾化(8µg NaCl·cm)−2·敏−1):理论斜率14.92µm·min−1与实验斜率为8.66µm·min−1(p < 0.001);e)大剂量雾化(18µg NaCl·cm)−2·敏−1):理论斜坡51.49μm·min−1与实验斜率为20.78µm·min−1(p < 0.001)。每个实验条件N =4。
ASL高度数据的曲线下面积(AUCs)被计算为星云溶液的“水化活性”指数。有趣的是,盐沉积速度较快(18µg·cm)−2·敏−1)与标准喷射星云速率(8µg·cm)相比,产生了更低的总ASL水化,尽管在统计学上没有差异−2·敏−1).气溶胶沉积较慢(3µg·cm)−2·敏−1)产生了较低的峰值和AUC值的趋势,而速度较快(图2 b).
假设没有活性钠+-介导的体积吸收或在雾化过程中顶端膜水渗透性的变化,不断积累的盐沉积到气道上皮表面,预计会产生ASL体积的线性增加。在所有的研究中,测量到的ASL高度与预测高度一致(图2汉英).实测的ASL高度与预测值的偏差可以反映活性钠+渗透驱动的水流向HBE表面的速率,或者两者兼有。
关于纳的作用+在ASL卷响应到HS管理的运输,我们推测了NA+在开始服用HS后,运输会立即改变HS诱导的ASL体积扩张的幅度。为了实验研究这种可能性,ASL体积对低剂量HS的反应(3 微克氯化钠·厘米−2·敏−1)在有和没有选择性ENaC阻滞剂(VX-371;Vertex制药公司,波士顿,马萨诸塞州,美国)。与单纯HS相比,VX-371共给药50µg·mL−1)在雾化过程中产生更快速和持久的ASL反应(图3A).气道上皮离子和水传输的数学模型,定量分析了HS介导变化与ASL高度和活性NA的关系+ENaC阻断存在和不存在时的吸收(图3B.).模型与实验数据的拟合是通过维持Na来实现的,实验数据描述了在没有ENaC抑制的情况下,ASL对HS的反应+在HS雾化和增加钠的过程中,以基本速率输运+在再吸收阶段,运输大约是原来的五倍。该数学模型复制了具有ENaC抑制作用的ASL动力学效应,具有更快速的ASL高度积累和超调速率,与活性Na的抑制一致+HS管理期间的吸收。
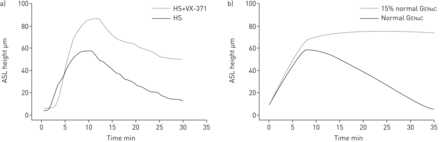
钠重吸收对高渗生理盐水(HS)介导的气道表面液(ASL)高度的影响a)高渗盐水(8µg NaCl·cm)的实验数据−2·敏−1在钠通道阻滞剂(VX-371在50µg·mL-1);b)正常上皮钠通道电导(G)下HS效应的数学模型预测博)(与实验数据一致)和15%的正常G博.
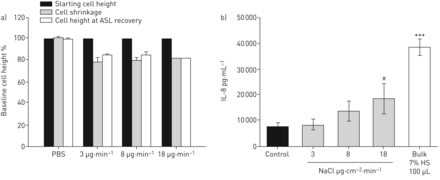
以前的研究已经证明HS可以减少细胞体积[20.,21],从而抑制细胞的水渗透性[21- - - - - -23].此外,研究表明,给药高渗盐水也会导致气道上皮内的炎症变化,特别是IL-8,一种已知的中性粒细胞趋化剂[24- - - - - -26].因此,我们测量了HBE细胞体积对HS气雾剂的反应和IL-8的产生,以测试细胞水渗透性的降低是否减弱了ASL对雾化HS和/或诱导的促炎细胞因子的反应。图4一细胞高度(细胞体积的替代品)在HS雾化期间和之后比初始细胞高度减少了约20% (p<0.01)。相反,等渗盐水雾化处理对细胞体积没有影响。这些数据表明腔内HS的沉积渗透地将水从细胞吸引到表面通过顶端膜水通道。图4 b在气管表面雾化HS或PBS对照后24小时,HBE可累积产生IL-8。与PBS对照相比,随着HS剂量的增加,IL-8的产生逐步增加(在18 μ g剂量和散装剂量上与对照组有统计学差异)。
a)细胞体积随高渗盐水(HS)在不同HS沉积速率下的渗透刺激而变化。在所有的高渗刺激速率下,观察到细胞高度降低20%,这与基线和等渗(PBS)生理盐水给药显著不同(Holm-Sidak方法p<0.01)。细胞高度在实验期间(60分钟)没有恢复。无论HS给药率如何,细胞体积减少都是一致的发现。每个条件的N =4。b)随着雾化或散装HS剂量的增加,产生白介素(IL)-8。与对照组(PBS)相比,18µg剂量和大剂量(100µL 7% HS)有统计学差异。#:P <0.002通过HOLM-SIDAK方法;***:P <0.001。
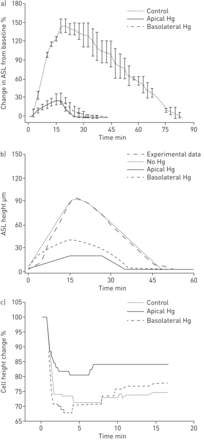
进一步使用药理学方法研究细胞水渗透率对ASL体积反应的贡献。因为在HBE上皮的顶端和基底外膜中鉴定了汞敏感的水通道(水吡啶蛋白)[27,28,实验评估了这些通道在hs介导的ASL体积反应变化中的作用。由于长期接触汞会产生脱靶毒性,因此该方案涉及对汞和HS的急性接触[29].如图所示图5一个顶部和基底外侧的氯化汞(HgCl2)显著降低了ASL对HS雾化反应的体积反应。与基底外侧水通道蛋白抑制相比,顶端水通道蛋白抑制导致细胞高度的降低较小。这些数据表明,在雾化HS环境下,细胞体积稳态主要由顶端膜水渗透性(图5 b).建模研究模仿实验数据(图5 c).
在顶部或基底外侧与氯化汞(Hg)孵育导致气道表面液体(ASL)对雾化高渗盐水(HS)(8µg NaCl·cm)的反应减弱−2·敏−1)与本土文化相比。实验数据。p < 0.001通过霍尔姆-西达克方法的比较控制。b)实验数据的数学模型。每个条件的N =8。c)在没有(对照)或有选择性阻断根尖或基底外侧细胞膜的情况下(所有比较中p<0.001),细胞高度变为雾化HS。
我们假设,HS政府将后观察到的细胞体积持续减少限制了HBEs对HS重复给药的反应能力。通过对HBE培养物进行连续HS处理(8µg NaCl·cm),验证了这一假设−2·敏−1),第二次施用后15分钟后,在第一个HS剂量后返回基线后15分钟。与初始HS施用相比,第二局的ASL高度和AUC显着减少(图6).
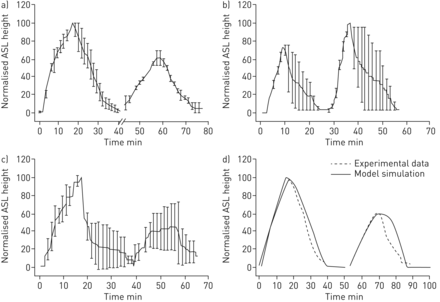
连续气道表面液体(ASL)体积对雾化7%高渗盐水(HS)15分钟(8µg NaCl·cm)的反应−2·敏−1).a)雾化HS对ASL体积的顺序反应。当两种相同的HS剂量分开15分钟时,观察到第二次雾化HS对ASL的反应较小。x轴上的间断表示两次剂量之间的时间间隔。HS以8µg NaCl·cm雾化−2·敏−1连续给药15分钟。第二个高峰的ASL高度是第一个高峰的~ 60%。Mann-Whitney秩和检验p<0.001。b)在给HS之间进行低渗盐水冲洗。低渗溶液给药产生的细胞肿胀与随后给HS改善的ASL体积反应相关(第一次给药的140%)。疗效差异有统计学意义(p=0.002)通过Mann–Whitney秩和检验)有利于后低张峰。c)在第一次和第二次HS给药之间插入等张冲洗液。当用等张盐水丸分离HS剂量时(Mann–Whitney秩和检验p=0.78),未观察到相同的第二剂量效应。第二峰ASL高度保持在∼第一个峰值的50%。d)在模型模拟中,第二次给药期间,人支气管上皮顶膜的通透性降低至基础通透性的10%。每种情况下n=4。
接下来,我们直接测试了第二HS给药的有效性降低的假设,反映了细胞体积减少的HBE细胞水渗透性,而不是持续加速Na+运输。为了测试该观点,在第一雾化HS给药后,瞬时添加(3分钟)到HBE的顶面的少量的低级盐水(0.63%NaCl,10μl)。施用低渗盐水刮板导致细胞溶胀(高度32±9μm增加),其将细胞高度恢复到基线水平。低渗推注的插入与ASL和AUC的统计学上较大的反应相关联(图6 b).相反,使用等渗生理盐水(0.9% NaCl, 10µL)后,细胞既没有肿胀,也没有对随后的HS刺激反应的恢复(图6 c).建模这种现象预测,在基线水平的〜10%的〜10%降低,将产生与实验观察到的第二HS给药的AUC衰落(图6 d).
接下来,我们研究了高浓粘液的存在是否与粘膜阻塞性疾病相关[30.]改变了hs诱导的水化动力学,利用HBE培养物表现出高浓缩黏液(12±4.3%固体)。CF是一种以高浓粘液为特征的疾病。然而,其他粘膜阻塞疾病,例如原发性纤毛运动障碍[3.]和非CF支气管扩张症[4]表现出高浓度粘液,我们之前已经证明,在高浓度粘液存在的情况下,CF细胞和正常HBE对雾化高渗盐水的反应类似[13].因此,我们将黏液的研究重点放在正常HBE的高浓度黏液上,以使这些数据与其他可能的黏液阻塞性肺疾病相关。hs前,高浓度黏液培养物的ASL高度约为正常黏液培养物的3倍。值得注意的是,与正常黏液培养相比,高浓度黏液培养中ASL高度随HS的变化显著增加(图1和7一个).虽然正常和高浓度粘液培养物在停止雾化后立即吸收增加的ASL体积,但高浓度粘液培养物的再吸收速度较慢与正常黏液培养(5.5与2.8µm·敏−1, p = 0.052;图7 b).在杂交粘液培养物中,HS诱导的ASL体积膨胀的总持续时间约为正常的粘液培养物的两倍。此外,在重复的HS给药方案中,第二次施用HS产生与第一施用类似的ASL响应(图7 c).与此相关的是,在被高浓黏液覆盖的HBEs中,细胞高度对HS的反应较低(15±4.7%)与23±5.7%),但差异无统计学意义。
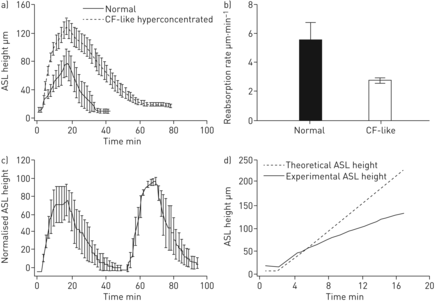
研究了高浓度黏液在人支气管上皮(HBE)表面对雾化高渗盐水(HS)(8µg NaCl·cm)的影响−2·敏−1)在诱导气道表面液体(ASL)体积反应中。a)在正常(2%粘液)状态下,雾化期间ASL体积增加三倍。HBE培养具有过育粘液(12%)(囊性纤维化(CF) - 麦克风)在基线ASL上方的ASL中表现出七倍增加。此外,在高分浓度的粘液HBE文化中增加了ASL高于基础水平的持续时间。b)重吸收的速率(基线AS1的时间,μm·min−1)的差异有统计学意义(p < 0.05)。经Mann-Whitney秩和检验,p=0.052。c)对高浓缩培养物连续给药两次HS。ASL高度差有利于第二次剂量(p<0.001)。d)如果所有的盐沉积留在表面,并导致进入ASL的水的等摩尔通量和实验中观测到的实际ASL高度的变化,则理论上ASL高度的预期上升。与图2 c–e;在存在完整粘液层(12%固体)的情况下,在HS交付间隔早期,实际和预期ASL高度更接近彼此。
在高浓度溶液中,ASL响应峰较大,NaCl和水的吸收较慢与正常黏液培养表明,在高浓度黏液系统中,有一种额外的力量控制着水的流动。以产生一个指数的大小,这一效应,预测与比较HS给药期间测量的ASL高度(图7 d).与正常黏液培养相比,高浓度黏液的早期给药值明显接近预测值(图2汉英),暗示浓缩粘液的存在产生了延迟液体吸收的额外粘液相关的渗透力[30.].
讨论
我们的在体外对雾化HS输送到含2%黏液固体的HBE培养物的临床相关率的研究显示,HS诱导的肌萎缩侧索硬化症体积迅速扩大。这种对HS气溶胶的ASL扩张与报道的类似在活的有机体内用同步加速器断层摄影术测量小鼠,用光学相干断层摄影术测量HBE培养[31,32].此外,据报道HS的急性雾化可降低慢性阻塞性肺病患者的气道黏液浓度[33].因此,ASL膨胀的结果与我们的研究结果相对照,即在HS星云化过程中ASL的渗透量可能不超过370 mOsm·L−1(见稍后),认为HS对粘液间隙的主要影响是通过ASL体积扩张和黏液稀释。
响应于HBE表面上的渗透活性NaCi的沉积,通过水通量介导HS诱导的ASL体积响应。两种观察结果表明,水素介导的Transepithelial水通量将ASL的响应占据了雾化HS。首先,响应于HS响应HS的水与细胞高度/体积的减少,表明细胞内水进入ASL。这个概念与以前的研究一致[21[报道,HBE的水素主导的顶端膜水渗透率比基于基石膜高〜10倍。请注意,此配置允许使用单元卷中的更改作为“秒计”以检测ASL渗透性。对HS气溶胶的细胞体积反应表明ASL达到了〜370 MOSM·L的渗透性−17% HS, 7.7µg NaCl·cm−2·敏−1),远低于直接添加HS。第二个观察结果是,HgCl阻断了ASL对HS雾化的反应2,水通道蛋白3-5的抑制剂,已知在HBEs中表达。这些数据,连同提出的细胞模型数据,强烈表明水通道蛋白介导的细胞水渗透性参与了ASL对雾化HS的体积响应(图4).
HS雾化对细胞体积减少和经上皮Na的影响+迁移可能解释了预测ASL对HBE表面HS沉积的响应与实测响应之间的差异。首先,细胞体积的减少与细胞水渗透性的降低有关,限制了水向高渗腔的流动。其次,在ENaC阻断剂活性钠存在的情况下,HS给药的最大反应更大+在气溶胶给药期间,运输除去沉积的NaCl的组分。一种有趣的观察,从活性NA的建模中出现+对HS的运输回应是NA增加+为了模拟气溶胶停止后的ASL体积吸收速率,需要传输速率。这种效应可能反映了局部ENaC胞外抑制剂的稀释,例如ATP,加速HS施用期间的吸收率[34].
HS治疗反应的一个关键问题与气道表面黏液的浓度有关。HBE表面存在高浓度黏液与ASL高度增加、单次HS给药后ASL水化持续时间更长以及对重复HS剂量的更大反应有关。我们假设黏液作为“海绵”,提供浓度依赖的聚合物凝胶介导的渗透驱动力,加上hs诱导的渗透梯度,调节HBE表面最大黏液/ASL高度。在高浓粘液培养中,ASL对HS雾化反应的持久性增加,与CF中HS作用时间的延长相对应在活的有机体内粘液纤毛清除研究[5,35].
此外,我们的研究旨在确定增加雾化HS的有效性以扩大ASL水化的策略,包括HS递送率和重复给药的研究。我们发现非常慢的HS交付率是相对无效的。我们推测这一发现反映了NaCl的沉积速率与内源性活性的经上皮Na的速率相似+吸收(36].在近似喷射雾化器的速率下递送HS在增加ASL水合时有效,但没有观察到疗效的进一步增加,以振动振动网状氧化剂较快的速率。在快速HS给药结束时观察到AUC的绝对减少和ASL体积膨胀的速度(18μgNaCl·cm−2·敏−1)与经上皮水渗透性的大幅降低一致。基于我们对IL-8的测量和这种细胞因子的促炎特性,更快的雾化速度可能是有害的。
与HS给药频率相关的一个重要观察是,HS给药4小时后HBE细胞高度没有恢复到基线水平。我们推测,细胞体积调节机制的缺失反映了水的渗透性降低。很可能是HS后顶端水渗透性恢复的延迟解释了在有正常粘液的HBE培养物上第二次HS给药的迟钝反应(图5).重要的是,低渗盐水诱导的上皮细胞肿胀可恢复第二次HS反应。这些数据表明,在轻度肺病患者中,可能需要新的策略来优化重复HS剂量的有效性。相反,在患有严重(12%黏液固体)疾病的受试者中,重复HS剂量可能是一种有效的策略。
综上所述,在粘液浓度正常的情况下,HBE培养物的ASL体积随着雾化HS的交付而增加,其速率与临床交付相似,但在雾化终止后立即开始重吸收。雾化速度快或慢都不能改善肌萎缩性侧索硬化症的水合作用。然而,HS雾化作用在高浓度黏液的HBE培养中更为显著和持久,可能反映了高浓度黏液产生的渗透力增加。这些数据预测了HS在黏液阻塞性疾病患者中的作用持续时间延长。
补充材料
致谢
作者愿承认北卡罗来纳大学(UNC)组织培养核心(NIH P30 DK065988和CFF RDP Bouche15R0),以及他的编辑埃里克罗伊(UNC CF研究中心,Chapel Hill,NC,USA)帮助。该项目由囊性纤维化基础(CFF)Leroy Matthews医生科学家奖(CFF Gorals12LO)提供资金,以及Button07xx0,NIH R01HL125280-01A1和NIH P30DK065988-11。
脚注
这篇文章的补充材料可从www.qdcxjkg.com.
作者贡献:概念和设计:J.L. Goralski和B. Button。数据采集:J.L. Goralski, B. Button和W.R. Thelin。数据建模:D. Wu。数据解释,起草和工作的关键修订:J.L. Goralski, R.C. Boucher和B. Button。
利益冲突:R.C.Boucher在提交的工作之外报告Proion Sciences的个人费用。
利益冲突:W.R. Thelin是Parion Sciences的员工,报告了提交的工作之外的非经济支持;此外,他还拥有一项专利- VX-371是Vertex制药公司的专利分子。
支持声明:本研究由囊性纤维化基金会(GORALS12LO和BUTTON07XX0)和美国国立卫生研究院(1R01HL125280-01A1和P30DK065988-11)支持。本文的资金信息已存入CrossRef Resder注册表.
- 收到了2017年12月19日。
- 接受2018年2月28日。
- 版权©2018人队