文摘
血管生成是一个关键因素的恶化恶性胸膜间皮瘤(MPM)和反血管增生对MPM策略可能有效。氨肽酶N (APN) / CD13促进肿瘤血管新生和与不良预后相关;然而,其在MPM的临床意义尚不清楚。
连续37名患者手术切除MPM,我们评估免疫组织化学之间的关系的APN / CD13表达式在切除肿瘤和生存。MT95-4此外,抗肿瘤和抗血管新生的影响,完全人性化anti-APN / CD13单克隆抗体,在老鼠身上进行评估orthotopically植入EHMES-10(大量表达的APN / CD13)和msto - 211 h(几乎不表达的APN / CD13) MPM细胞。
高肿瘤的APN / CD13表达式与MPM患者的不良预后有关(p = 0.04),和MT95-4治疗小鼠的肿瘤生长和血管生成减少窝藏EHMES-10但不是msto - 211 h细胞。此外,在小鼠窝藏EHMES-10细胞,MT95-4结合顺铂比顺铂单独有效地抑制肿瘤的发展。
总的来说,这些结果表明,APN / CD13涉及MPM的攻击性。这里,MT95-4治疗肿瘤进展可能通过抑制血管生成减少,暗示APN CD13 /作为一个潜在的分子MPM的治疗目标。此外,MT95-4与顺铂联合治疗可能是一种很有前途的方法来治疗MPM表现出高的APN / CD13表达式。
文摘
氨肽酶N (APN) / CD13是一个潜在的治疗目标在间皮瘤表现出高的APN / CD13表达式http://ow.ly/dzmu30iGKzd
介绍
恶性胸膜间皮瘤(MPM)是一种罕见但咄咄逼人的预后差的恶性肿瘤,随着全球MPM-related死亡人数继续增加(1,2]。只有少数患者MPM有资格获得多峰性治疗,包括手术和放射治疗,患者有效的治疗策略(MPM是有限的;因此,小说系统性治疗是必要的。
血管生成是一个关键因素在固体肿瘤的恶化和MPM的微脉管密度是一个独立的预后因子3- - - - - -6),这表明MPM治疗抗血管新生的策略可能是有益的。这是由以前的报告显示,贝伐单抗与培美曲塞+顺铂治疗改善患者生存MPM (7]。
氨肽酶N (APN) / CD13锌2 +端依赖,膜结合ectopeptidase乳沟催化作用的n端氨基酸小肽。APN / CD13由967个氨基酸的氨基端胞质域,一个跨膜域和一个大细胞外域,它包含活性部位。APN / CD13广泛表达于哺乳动物细胞,如肾近端小管上皮细胞和髓系祖细胞,在小肠上皮细胞以及中枢神经系统突触膜。此外,APN / CD13多功能酶还参与病毒受体功能、细胞分化和抗原表达8- - - - - -12]。此外,APN / CD13与肿瘤进展通过促进血管生成和肿瘤细胞入侵(13- - - - - -18]。APN的表达CD13 /在各种类型的肿瘤,包括肺癌、胰腺癌和结肠癌,以及急性淋巴细胞白血病,据报道(19- - - - - -22];然而,MPM的表达的临床意义还有待阐明。这些研究结果的基础上,我们提出的APN / CD13与MPM进展和是一个有吸引力的目标治疗MPM的分子。确定APN / CD13 MPM的意义,我们研究了APN / CD13表达之间的相关性进行免疫组织化学染色和患者生存的患者手术切除MPM切除肿瘤。此外,确定APN的疗效/ CD13 MPM的分子目标治疗,我们检查了MT95-4的抗肿瘤和抗血管新生的影响,完全人性化anti-APN / CD13单克隆抗体(mAb),在一个原位植入MPM的小鼠模型。使用此动物模型,我们还研究了MT95-4是否影响的抗肿瘤效应细胞毒性剂顺铂。
材料和方法
患者的临床和病理特征
我们检查了连续37 MPM患者进行术前化疗(顺铂加培美曲塞)和激进手术部门胸外科的广岛大学(广岛,日本)2008年2月到2015年8月。根治手术的主要资格标准是MPM的组织学证实诊断,包括临床亚型T0-3 / N0-2 M0疾病,之前没有治疗这种疾病,年龄20 - 75年,东部合作肿瘤组性能状态0或1,预测术后用力呼气量在1 s > 1000毫升。通过免疫组织化学染色,我们调查了APN / CD13表达式从MPM患者在切除肿瘤。6个病人死于MPM-unrelated原因被排除在外。这个研究是广岛大学医院的伦理委员会批准,按照建立的道德标准进行1975年的赫尔辛基宣言。所有患者允许知情同意在写作和使用他们的样品。
前置/ CD13免疫组织化学
Formalin-fixed,石蜡包埋组织标本用鼠标马伯孵化与人类的APN / CD13(美国加利福尼亚州圣何塞徕卡生物系统,)在4°C一夜之间,洗在PBS和孵化与生物素化的兔子anti-mouse IgG抗体(美国向量实验室,伯林盖姆,CA)。免疫反应是放大使用VECTASTAIN ABC工具包(向量实验室)和抗体绑定与3形象化,3-diaminobenzidine解决方案作为发色体。部分被苏木精复染色和脱水。一些部分被孵化与正常小鼠免疫球蛋白作为消极的控制。
基于免疫组织化学染色标本分类
综述了应用部分由两位病理学家都忽视病人的临床状态。肿瘤细胞的比例显示高或低染色确定五个随机微观领域通过计算单个肿瘤细胞高倍镜下。APN / CD13表达水平是评估在至少200肿瘤细胞放大×400。的平均比例导引和/ CD13+肿瘤细胞在肿瘤的17%;因此,我们将17%作为截止值设置为归类肿瘤与高或低的APN / CD13表达式。
细胞和文化
两个人类MPM细胞系,EHMES-10 msto - 211 h,被用于这项研究。EHMES-10细胞建立的胸腔积液患者特别大学MPM(松山、日本)23,24)和msto - 211 h细胞从美国购买类型文化集合(美国弗吉尼亚州马纳萨斯)。BALB / c小鼠原发性肺动脉内皮细胞从细胞购买生物制剂(美国芝加哥,IL)。MPM细胞系是RPMI 1640培养基培养(美国纽约Gibco,大岛)补充10%胎牛血清和1%青霉素和链霉素。鼠标在鼠标内皮细胞培养基培养内皮细胞/ w(细胞生物制剂)。所有细胞培养在37°C公司5%2湿润的气氛。msto - 211 h和鼠标动脉内皮细胞解冻后6个月内使用,和EHMES-10细胞被短串联重复序列分析验证(Promega、东京、日本)。
试剂和动物
mt - 95 - 4是在我们实验室开发的如前所报道(25)与顺铂从日本购买Kayaku(日本东京)。男性重度联合免疫缺陷(SCID)小鼠(6周)从克丽购买日本(日本大阪)。动物是维护根据伦理指南使用广岛大学的动物研究。
流仪结果
流仪分析MPM细胞系进行如前所述[25]。
定量实时聚合酶链反应
提取RNA,反转录的互补和实时定量PCR进行如前所述[25]。所使用的引物是Hs00174265_m1 APN / CD13、Hs00900055_m1对血管内皮生长因子(VEGF)和4352935 eβ-actin(所有从应用生物系统公司、弗雷明汉马,美国)。
原位移植模型
EHMES-10 (3×106)或msto - 211 h (1×106)细胞被注入SCID小鼠如前所述的胸腔23)和小鼠被随机分配到控制或药物治疗组。MT95-4·kg(0.3或1毫克−1)和控制人类免疫球蛋白(Sigma-Aldrich,圣路易斯,密苏里州,美国)每周腹腔内注射两次,与顺铂(3毫克公斤−1)注射i.p。每周1次。所有老鼠死亡28天(EHMES-10)或21天(msto - 211 h)肿瘤细胞接种后,胸肿瘤移除很仔细,重,和胸膜腔积液收获用1毫升注射器,紧随其后的是体积测量。
评价胸肿瘤的微血管密度
微脉管密度是CD31免疫组织化学染色后评估在胸肿瘤如前所述26]。
扩散分析
EHMES-10或msto - 211 h (1×104每100毫升)细胞被播种在96 -孔板在不同浓度和孵化MT95-4 36 h。细胞增殖是评估通过测量介质的吸光度在每个使用细胞计数Kit-8 (Dojindo、熊本、日本)。
在活的有机体内分析细胞凋亡
被用于冷冻组织部分原位细胞凋亡的检测终端原位dUTP尼克end-labelling (TUNEL)使用原位细胞凋亡检测设备(豆类生物医学、志贺、日本)。使用显微镜的放大图像捕获×200 (bz - 9000;日本基恩士、大阪、日本)和阳性细胞计数测定每张幻灯片1000个细胞。
血管生成抗体阵列分析
血管生成抗体阵列分析中描述补充材料。
量化的VEGF
EHMES-10 (1×105)细胞被播种在24-well盘子和培养的MT95-4(40μg·毫升−1)或人工控制免疫球蛋白12或48 h。文化上层清液VEGF浓度是衡量使用酶联免疫试剂盒(研发系统,明尼阿波利斯,美国)根据制造商的指示。
基质降解试验
执行一个矩阵退化试验使用细胞入侵检测工具(美国细胞生物学实验室,圣地亚哥,CA)根据制造商的指示。总之,细胞被播种在插入膜板的上表面与矩阵的蛋白质。矩阵的降解蛋白质是必要的种子细胞通过膜的孔隙。最后,入侵细胞被染色和量化。鼠标主肺动脉内皮细胞,暂停2×105细胞在不同浓度的重组人类的APN / CD13被播种的上表面插入膜与基底膜板矩阵的解决方案。EHMES-10和msto - 211 h细胞,暂停2×105细胞包含MT95-4(20μg·毫升−1)或人工控制免疫球蛋白被播种在插入膜板的上表面与矩阵的蛋白质。入侵细胞数在三个随机的微观领域每后48 h。
统计分析
确切概率法和Mann-Whitney u测验进行确定的APN / CD13表达与临床病理参数之间的显著差异。总体生存记录的日期由于MPM手术死亡的日期。kaplan meier方法被用来估计的概率被生存率较评估生存和意义。单变量和多变量分析预后的预测因素进行使用Cox比例风险回归模型来评估APN / CD13表达式作为一个独立的预后MPM的标志。独立预测因素从参数中被确定在一个单变量分析的假定值< 0.1。为在体外实验中,数据被表示为均值±扫描电镜和团体之间的差异进行分析t以及与Dunnett或单向方差分析事后测试。为对比组在活的有机体内与Dunnett、单因子变异数分析事后测试或Bonferroni的多重比较测试执行。统计分析使用棱镜version 6(美国GraphPad拉霍亚,CA)和人民币13.0版(SAS研究所卡里、数控、美国)。假定值都记录为双尾和p < 0.05被认为是具有统计学意义。
结果
前置/表达CD13 MPM患者的总生存期较短有关
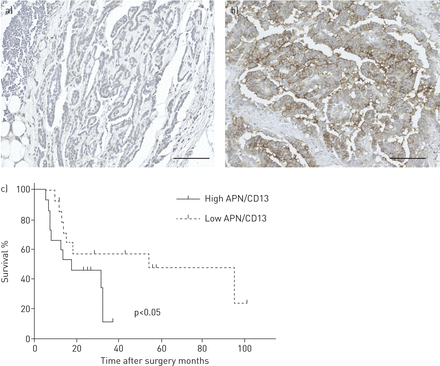
调查的APN / CD13 MPM的临床意义,我们在切除肿瘤免疫组织化学评估APN / CD13表达并分析其与MPM患者的生存。代表图像的正面和负面的免疫组织化学染色的APN / CD13在切除肿瘤所示图1一个分别和b。我们观察到的APN / CD13染色在肿瘤细胞的细胞膜和细胞质,15和16个肿瘤被归类为表现出高和低的APN / CD13表达式,分别。APN / CD13表达和临床病理的变量之间的关系所示表1。(范围)手术年龄中值为64(48 - 72)年和19个病人在随访期间死亡。无显著关系的APN / CD13表达与年龄、吸烟史、新辅助化疗效果或组织学观察;然而,我们无法调查APN / CD13表达式之间的关系和性,因为女性患者不包括在内。高水平的患者平均存活时间的APN / CD13表达显著短于低水平的患者的比例导引(17.3 / CD13表达式与54.4个月;p = 0.04) (图1 c)。此外,调查APN CD13 /作为一个独立的预后指标,进行了单变量和多变量分析使用Cox比例风险回归模型。多变量分析表明,高的APN / CD13表达与组织学(nonepithelioid)之间的独立与不良预后相关因素与单变量分析(p < 0.1表2)。
免疫组织化学染色法对氨肽酶N (APN) / CD13在肿瘤组织中实时获得患者恶性胸膜间皮瘤(MPM)。)代表的负面形象的APN / CD13染色。b)代表的积极形象的APN / CD13染色。酒吧规模:100μm。c)患者的总体生存MPM与比例导引的状态/ CD13表达肿瘤。审查病人由垂直标记表示。p- - - - - -价值取决于生存率较。
MT95-4抑制肿瘤发展的APN / CD13 expression-dependent方式
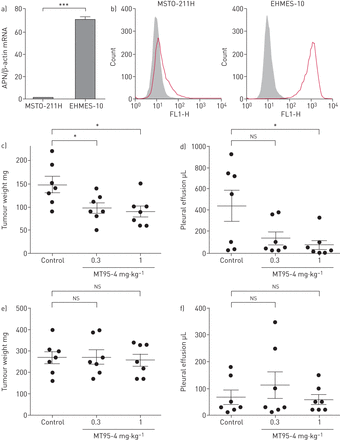
确定比例导引的疗效/ CD13 MPM的分子的目标,我们检查了MT95-4的抗肿瘤效应,完全人性化anti-APN / CD13马伯,MPM的原位移植小鼠模型,利用MPM细胞系EHMES-10 msto - 211 h。定量实时PCR和流仪分析表明,EHMES-10细胞大量表达的APN / CD13、而msto - 211 h细胞几乎不表达的APN / CD13 (图2一个和b)。在活的有机体内管理MT95-4·剂量的0.3和1.0毫克公斤−1显著降低肿瘤重量(方差分析;分别为p = 0.03, p = 0.01)。此外,政府的MT95-4 1.0毫克公斤−1的数量明显减少胸腔积液(方差分析;p = 0.02)在小鼠体内窝藏EHMES-10细胞(图2 c和d);然而,在老鼠窝藏msto - 211 h细胞,MT95-4政府减少肿瘤重量和胸腔积液的量(图2 e和f)。
在活的有机体内MT95-4对胸肿瘤重量和胸腔积液的影响在一个恶性胸膜间皮瘤的原位移植模型(MPM)。a)表达水平的氨肽酶N (APN) / CD13 mRNA在人类的MPM细胞定量实时PCR分析。数据意味着±扫描电镜一式三份的样品。* * *:p < 0.001。b)的APN /人类MPM细胞表面表达CD13通过流式细胞术分析。氟)评价肿瘤重量和胸腔积液MPM细胞产生的严重联合免疫缺陷(SCID)小鼠使用c, d) EHMES-10或e, f) msto - 211 h细胞。EHMES-10 (3×106)或msto - 211 h (1×106)细胞接种到SCID小鼠的胸腔,紧随其后的是治疗MT95-4·kg(0.3或1毫克−1)或一个isotype-matched控制单克隆抗体i.p。每周注射两次。胸肿瘤重量和胸腔积液进行评估在4周(EHMES-10)或3周后(msto - 211 h)肿瘤细胞接种。水平线表示均值±扫描电镜与七个老鼠每组。通过与Dunnett单向方差分析的数据进行分析事后测试。*:p < 0.05与对照组;ns:不重要。
MT95-4抑制肿瘤血管生成在一个前置/ CD13 expression-dependent方式
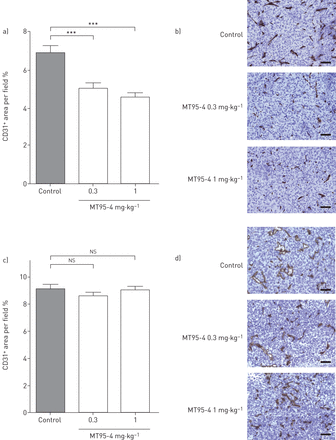
调查MT95-4在胸膜腔内肿瘤的抗血管新生的影响,我们评价胸膜腔内肿瘤的微血管密度在老鼠窝藏EHMES-10或msto - 211 h细胞CD31免疫组织化学染色。MT95-4管理显著降低微脉管密度(方差分析;所有p < 0.001)在老鼠窝藏EHMES-10胸膜腔内肿瘤细胞(图3一和b),但不是在老鼠窝藏msto - 211 h细胞(图3 c和d)。
MT95-4治疗在胸肿瘤血管生成的影响。模拟)小鼠移植与a、b) EHMES-10或c, d) msto - 211 h细胞治疗MT95-4·kg(0.3或1毫克−1)或一个isotype-matched控制单克隆抗体i.p。每周注射两次。CD31的面积+船只在小鼠移植)EHMES-10或c) msto - 211 h细胞计算中描述的材料和方法。n = 7 /组。通过与Dunnett单向方差分析的数据进行分析事后测试。* * *:p < 0.001与对照组;ns:不重要。b, d)免疫组织化学染色中CD31胸肿瘤来源于b) EHMES-10或d) msto - 211 h细胞。酒吧规模:100μm。
MT95-4增强顺铂抗肿瘤效应的MPM的小鼠模型
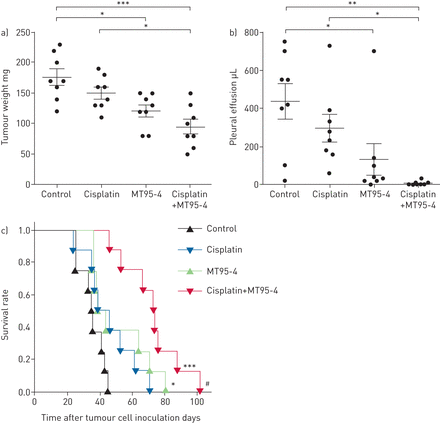
MT95-4证实在小鼠的抗肿瘤效应窝藏MPM细胞表现出高水平的APN / CD13表达式,我们调查是否MT95-4政府影响的抗肿瘤效应细胞毒性剂顺铂。老鼠窝藏EHMES-10细胞处理车辆,MT95-4,顺铂或MT95-4与顺铂联合治疗。所示图4一和b, MT95-4与顺铂联合治疗显著降低肿瘤重量(方差分析;p = 0.009)和胸腔积液(方差分析;与顺铂相比,p = 0.04)。此外,MT95-4与顺铂联合治疗显著延长小鼠的生存时间窝藏EHMES-10细胞(图4 c)。
在活的有机体内MT95-4治疗效果与顺铂的原位移植模型使用EHMES-10细胞恶性胸膜间皮瘤。a、b) MT95-4治疗效果与顺铂)肿瘤重量和b)胸腔积液严重联合免疫缺陷(SCID)小鼠窝藏EHMES-10细胞。EHMES-10 (3×106)细胞接种到SCID小鼠的胸腔,紧随其后的是治疗MT95-4·kg(0.3毫克−1i.p。每周两次)、顺铂(3毫克公斤−1i.p。每周1次)或MT95-4·kg(0.3毫克−1)联合顺铂(3毫克公斤−1)。胸肿瘤重量和胸腔积液进行评估肿瘤细胞接种后4周。水平线表示均值±扫描电镜每组八老鼠。数据分析单向方差分析和Bonferroni多重比较检验。*:p < 0 0.05;* *:p < 0.01;* * *:p < 0.001。c) MT95-4治疗结合顺铂对小鼠窝藏EHMES-10细胞的生存。生存率较假定值测定。*:p < 0.05与对照组;* * *:p < 0.001与对照组;#:p < 0.01与顺铂单药治疗组。
MT95-4对增殖和细胞凋亡的程度的影响
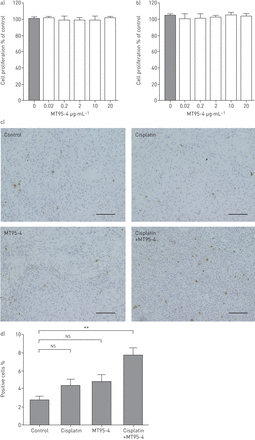
通过抑制血管生成MT95-4有抗肿瘤效果在活的有机体内;我们进一步研究了其他机制抗肿瘤的效果。大量试验表明,MT95-4没有抑制增殖率EHMES-10和msto - 211 h的细胞在体外(图5一个和b)。接下来,我们评估细胞凋亡原位通过TUNEL使用冰冻组织切片,发现MT95-4本身并没有显著增加凋亡细胞的数量。然而,与顺铂结合MT95-4并显著增加凋亡细胞的数量(图5 c和d)。
MT95-4对增殖和细胞凋亡的程度的影响。a、b)扩散中量化)EHMES-10和b) msto - 211 h细胞后36 h在不同浓度的MT95-4面前。数据均值±扫描电镜一式三份的样品。c, d)在活的有机体内分析胸EHMES-10产生的肿瘤细胞的凋亡。老鼠窝藏EHMES-10细胞治疗MT95-4·kg(0.3毫克−1i.p。每周两次)、顺铂(3毫克公斤−1i.p。每周1次)或MT95-4·kg(0.3毫克−1)联合顺铂(3毫克公斤−1)。肿瘤细胞接种后4周,老鼠牺牲。c)胸肿瘤进行评估终端原位细胞凋亡的dUTP尼克end-labelling。描述的计算阳性细胞在材料和方法。n = 3 /组。酒吧规模:100μm。d)定量免疫组织化学分析。数据均值±扫描电镜并分析了单向方差分析与Dunnett事后测试。* *:p < 0.01与对照组;ns:不重要。
抗血管新生的影响MT95-4取决于抑制细胞外基质降解,但不是血管生成的抑制因素
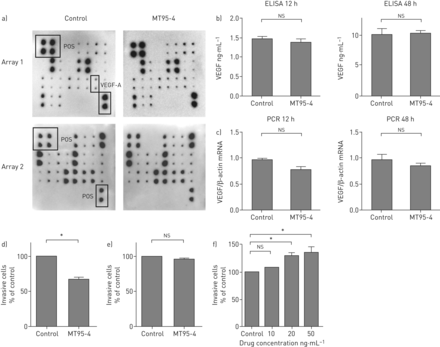
的抗血管新生活动MT95-4演示在活的有机体内,我们探讨了机制MT95-4抗血管新生的影响。我们第一次调查MT95-4是否直接影响肿瘤细胞产生的血管生成因子的表达在体外。使用一个血管生成抗体阵列,43血管生成因子的表达水平比较EHMES-10细胞之间有或没有MT95-4治疗。所示图6、治疗与MT95-4 EHMES-10细胞并不影响血管生成因子的表达。为了验证这些发现,我们评估了蛋白质和mRNA水平最重要的血管生成因子,即。VEGF在接受MT95-4 EHMES-10细胞。我们的研究结果显示,治疗EHMES-10与MT95-4并不影响VEGF蛋白或细胞信使rna水平(图6 b和c)。鉴于血管生成因子没有起到关键作用的抗血管新生作用MT95-4,我们提出MT95-4的抗血管新生作用在活的有机体内是通过抑制细胞外基质降解,从而抑制血管内皮细胞的入侵到血管周围间质。评估这一假设,我们执行一个矩阵退化试验。首先,评估是否MT95-4抑制细胞外基质降解通过封锁的APN / CD13间皮的细胞,一个矩阵退化试验进行了使用EHMES-10(大量表达的APN / CD13)或msto - 211 h(几乎不表达的APN / CD13)细胞悬液含有MT95-4(20μg·毫升−1)或人工控制免疫球蛋白。入侵EHMES-10 MT95-4镇压,但不是msto - 211 h (图6 d和e)。第二,我们调查是否APN / CD13直接促进小鼠血管内皮细胞的入侵矩阵的降解蛋白质。矩阵退化试验使用鼠标主肺动脉内皮细胞悬浮液含不同浓度的重组人类的APN / CD13表明重组人类的APN / CD13剂量依赖性的方式促进了内皮细胞的入侵(图6 f)。
抗血管新生的影响MT95-4取决于基质降解的抑制,但不是血管生成的抑制因素。)血管生成抗体阵列分析EHMES-10细胞治疗MT95-4或人工控制免疫球蛋白。POS:积极控制;VEGF:血管内皮生长因子。b, c) EHMES-10细胞(1×105)被播种24-well板块和培养MT95-4(40μg·毫升−1为24小时)或人工控制免疫球蛋白。呈现单个点的密度是使用化学发光检测系统。b) VEGF浓度培养基,ELISA测定c) VEGF mRNA水平被定量实时PCR分析。d, e) MT95-4对入侵的影响d) EHMES-10和e) msto - 211 h矩阵退化细胞试验。重组体人氨基肽酶N / f)效应CD13鼠标主肺动脉内皮细胞的入侵。入侵细胞的数量计入三个随机每口井的微观领域。数据意味着±扫描电镜一式三份样品和分析的t检验或与Dunnett的单向方差分析事后测试。*:p < 0.05与对照组;ns:不重要。
讨论
在这项研究中,我们发现高APN / CD13表达可能与MPM患者的不良预后相关,表明MT95-4,完全人性化anti-APN / CD13马伯,对小鼠的抗肿瘤和抗血管新生的影响窝藏EHMES-10细胞(大量表达的APN / CD13),而不是那些窝藏msto - 211 h细胞(几乎不表达的APN / CD13)。老鼠窝藏EHMES-10细胞,MT95-4管理局结合顺铂抑制肿瘤发展更有效和长期生存与顺铂治疗。此外,在体外实验表明,抗血管新生的影响MT95-4可能介导的抑制细胞外基质降解,从而抑制血管内皮细胞的入侵,但不是通过抑制血管生成因素产生的肿瘤细胞。
我们的研究结果清楚地表明,高APN / CD13表达在肿瘤细胞与MPM患者的不良预后有关。尽管APN / CD13表达与预后不良相关各种肿瘤类型(19- - - - - -22),可能通过促进肿瘤细胞入侵和血管生成的能力(13- - - - - -18),其临床意义MPM仍然未知。我们所知,这是第一个研究报告之间的关联的APN / CD13表达在肿瘤细胞和MPM病人预后。这些结果表明,APN / CD13参与肿瘤侵犯MPM的病人。
检查的有效性的APN / CD13 MPM的治疗目标,我们测试了MT95-4的抗肿瘤效果,完全人性化anti-APN / CD13马伯建立在我们的实验室25),在MPM的原位移植小鼠模型,利用MPM细胞表现出高或低的APN / CD13表达式。我们发现MT95-4政府抑制肿瘤进展和血管生成在肿瘤表现出高的APN / CD13表达式。这些结果表明,治疗策略针对比例导引/ CD13可能构成一种有前途的治疗方法选择MPM表现出高的APN / CD13表达式。仅作为MT95-4治疗并不影响细胞增殖(图5一个和b),细胞凋亡(图5 c和d)或衰老(数据未显示),我们建议MT95-4抑制肿瘤进展主要通过抑制血管生成在MPM肿瘤表现出高的APN / CD13表达式。
一项研究报道,贝伐单抗与培美曲塞+顺铂治疗不可切除的患者的整体存活率显著提高MPM (7),因此重申MPM的抗血管新生疗法的重要性。在这项研究中,我们展示了一个反血管增生的影响中和APN / CD13表达在肿瘤细胞的MPM小鼠模型窝藏MPM细胞表现出高的APN / CD13表达式。这一结果与先前的研究报告,同意APN / CD13中和或击倒在小鼠的肿瘤细胞减少intratumoural微血管密度(25,27]。贝伐单抗政府抑制VEGF的活动由肿瘤细胞分泌;然而,我们的研究结果表明,MT95-4治疗没有MPM细胞抑制VEGF的表达。此外,血管生成抗体数组的使用使我们观察到MT95-4治疗并不影响43血管生成因子的表达水平,包括VEGF,由MPM细胞产生。这些结果表明,抗血管新生的影响与MT95-4治疗并不是抑制介导的血管生成因子。矩阵退化试验表明,血管内皮细胞的侵袭性增强的APN / CD13和MT95-4抑制细胞外基质降解由肿瘤细胞抑制的APN CD13 /活动。因此,我们建议的抗血管新生作用MT95-4治疗通过前置/ CD13活动的抑制,这是参与细胞外基质降解的元素,如entactin和IV型胶原蛋白(基底膜组件)[13,28),从而抑制血管内皮细胞的释放和迁移到血管周围间质(29日,30.]。
APN / CD13表达在肿瘤细胞和良性的基质细胞促进肿瘤进展和血管生成27]。作为MT95-4不承认鼠APN / CD13 [25),抗肿瘤,抗血管新生的影响MT95-4描述在这个研究可能是通过抑制APN的活动/ CD13只在肿瘤细胞表达。当用于患者MPM, MT95-4可能通过抑制的APN / CD13起到更强的抗肿瘤作用在肿瘤细胞和基质细胞的活动。虽然APN / CD13表达并不局限于肿瘤微环境,治疗方法包括MT95-4针对比例导引/ CD13应该在临床使用是可行的。值得注意的是,APN / CD13缺乏小鼠不会导致生理或组织学异常31日]和ubenimex、CD13 / APN抑制剂已被使用在临床实践中,没有严重不良反应(32]。此外,我们发现MT95-4治疗结合顺铂,一个基本的细胞毒性剂用于治疗MPM,发挥更强的抗肿瘤作用与MT95-4治疗仅MPM的小鼠模型。这是以前报道,CD13-overexpressing异种移植表现出对顺铂的敏感性降低在活的有机体内(33]。此外,ubenimex增强抗癌药物的影响,包括顺铂诱导癌细胞凋亡[34]。在我们的研究中,MT95-4结合顺铂,但不是MT95-4,凋亡细胞的数量明显增加,表明联合治疗可能的tumour-suppressing效应解释为诱导凋亡由MT95-4在肿瘤细胞通过抑制APN CD13 /活动。这些结果表明,MT95-4结合顺铂治疗可能是一种很有前途的治疗策略治疗MPM-specific肿瘤表现出高的APN / CD13表达式。
这项研究有一些局限性。首先,病人预后分析中包括的数量小,比例导引的意义/表达CD13 MPM需要验证在较大和前瞻性临床研究。第二,所有MPM患者在这个研究经历了术前化疗和对化疗是否会影响APN / CD13表达在肿瘤细胞的水平。第三,我们不能透露的精确机制MT95-4治疗相关的抗肿瘤和抗血管新生的影响。因此,进一步的调查澄清这一点是必要的。
总之,我们表明,APN / CD13表达可能与MPM患者的不良预后有关。此外,我们的研究结果显示,MT95-4,完全人性化anti-APN / CD13马伯,抑制肿瘤进展可能通过抑制血管生成MPM的原位移植小鼠模型表现出高水平的APN / CD13表达式。此外,我们表明,MT95-4与顺铂治疗增强抗肿瘤效果,一个基本的细胞毒性剂用于MPM治疗。这些发现表明,APN / CD13代表一个潜在的治疗目标在MPM MT95-4结合顺铂治疗可能是一种有前途的治疗战略MPM-specific肿瘤表现出高水平的APN / CD13表达式。
补充材料
脚注
可以从本文的补充材料www.qdcxjkg.com
作者贡献:t大月:概念和设计,数据收集,数据分析和解释,手稿写作。中岛美嘉:概念和设计,数据分析和解释和修订手稿。y高山,美国秋田犬:概念和设计,数据分析和解释。h .岩漠t .此外,宫本茂,y Horimasu, h . Iwamoto k .购买香烟,m .宅一生和n . Kohno:数据分析和解释。y基金经理人和m .冈田克也:数据收集和提供学习材料。n .服部年宏:概念和设计、金融支持、数据分析和解释,稿件写作,和手稿的最终批准。
利益冲突:没有宣布。
支持声明:本研究部分由Ryokufukai的资助。
- 收到了2017年8月7日。
- 接受2018年2月24日。
- 版权©2018人队