摘要
鼻腔高流量(NHF)在睡眠期间减少微小通风和通风载荷,但机制尚不清楚。我们假设NHF以与生理而不是解剖的死区成比例的通风。
11受试者(五种对照和六种慢性阻塞性肺病(COPD)患者)用经皮二氧化碳接受多瘤创造(CO2)在代谢罩下监测。在稳定的非快速眼动2期睡眠期间,受试者接受NHF (20 L·min)−1),间歇5-10分钟。我们测量有限公司2生产和计算死亡空间通风。
对照和COPD患者与NHF类似地反应。NHF减少的微小通风(从5.6±0.4至4.8±0.4 L·min−1;P <0.05)和潮气量(从0.34±0.03至0.3±0.03升; P <0.05)没有能源支出的变化,经皮CO2或肺泡通气。死腔通气显著降低(从2.5±0.4 L·min降至1.6±0.4 L·min)−1;P <0.05),但不是呼吸速率。死空间通风的减少与基线生理死区分数相关(R.2= 0.36;P <0.05),但不适用于呼吸速率或解剖死空间体积。
在睡眠期间,NHF由于基线生理死区分数的程度而平衡死亡空间通风的总体降低,NHF降低了微小的通风。
摘要
鼻腔高流量降低了在睡眠期间对照和COPD患者的死亡空间通风http:///wly/ujhd30jazwa.
介绍
鼻高流量(NHF)是一种呼吸支持的方法越来越多地使用在一些临床设置。在NHF期间,以高流速(2-60 L·min)将温暖和湿润的空气送到患者的鼻子−1)[1].NHF可辅助通气和预防呼吸衰竭的成人和儿童插管[2-5.].已经提出了几种机制来解释使用这种治疗观察到的反应。NHF可能导致呼吸系统的改进[6.],使呼吸道更湿化[7.],减少解剖死区[8.那9.],末期呼气量增加[10.-12.]及因呼吸工作减少而减少对呼吸设备的需求[4.那9.那13.-15.].通风需求的降低归因于解剖鼻死空间的冲洗[8.];但是,死空间体积和二氧化碳的动态测量(CO2)在潮汐呼吸期间的生产未进行,留下NHF产生的效果的实际动作机制。
睡眠是学习NHF的生理机制的独特机会,因为我们可以避免潜在的有意识的混乱。我们以前表明,在清醒和睡眠中对NHF的通气反应是不同的[16.].这些差异可以解释当在临床环境中检查NHF机制时报告的异质反应。事实上,当控制睡眠时,我们观察到对NHF的更均匀反应。两分钟通风和呼吸的工作减少,同时有效2水平保持不变[9.].通气减少可能是由于鼻死腔冲洗导致死腔通气减少[8.那17.].然而,通过减少呼吸功,NHF也可以减少CO2生产,因此,减少维持恒定水平所需的微小通风量2.
为了确定微小通气的减少是由于呼吸功的减少还是死腔通气的减少,我们测量了NHF对CO的影响2在对照组和慢性阻塞性肺病(COPD)患者睡眠期间的生产。具体而言,使用代谢罩和标准多面体创造与CO2监测,我们测量了CO2在稳定睡眠期间生产和计算肺泡通风,而不使用NHF。我们假设NHF会降低死区空间通风,减少量取决于死亡空间的程度。我们还假设,与对照组相比,COPD患者将显示有限公司的减少2生产,从而降低肺泡通气。
方法
参与者是从美国约翰霍普金斯肺诊所和美国周围社区招募的。包括18岁的主题,并包括参加的同意。排除标准在研究前8周内加剧了COPD或严重疾病,严重的心脏和肝病,家庭使用氧气(O.2)和/或慢性用途阿片类药物,苯二氮卓类药物或其他镇静剂。
在之前的研究中[9.],我们检测到30-40%的微小通风,呼吸和潮气量的减少,使用NHF。正如我们计划调查代谢率的变化是否有助于微小通风减少,我们估计需要10个受试者才能繁殖先前观察到的通风影响,并研究了代谢率变化的贡献。
该研究得到了约翰霍普金斯医疗机构人类调查审查委员会的批准。
设备设置
在代谢引擎盖下进行读取的受试者进行过夜睡眠研究以测量CO2使用NHF的生产。在研究期间,我们收集了标准的多面组信号,包括经皮CO2(TCM3;辐射计医疗,Brønshøj,丹麦)。用呼吸诱导体积描记法监测通风(respitrace; Ami,Ardsley,NY,USA)。在协议的开始时,受试者穿着侧面掩模附着在肺炎骨膜镜中[18.]和最终的CO2显示器(保鲜,文图拉,美国,美国)。受试者通过掩模呼吸〜30秒,以校准呼吸诱导物理学谱系与集成的肺骨膜仪信号。此外,参与者进行了缓慢的呼气机动,以引发准确的潮汐合作2读。我们缩放了经皮运作2测量得到的潮汐端CO2值。经过校准程序后,口罩被摘除,受试者仅佩戴鼻套管用于间歇性输送NHF。
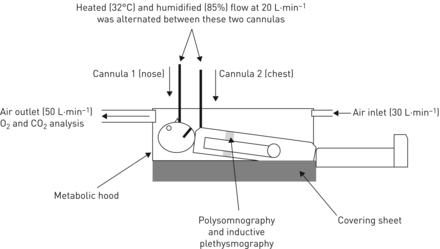
一旦参与者被完全监测并舒适地躺在床上,我们放置一个代谢罩(夸克RMR;遮住头部和胸部以收集被试者呼出的空气(图1).该系统允许测量O2消费和有限公司2在没有戴面具的人中生产。连接在引擎盖上的长片围绕受试者的身体的上部,避免空气泄漏。泵将空气从引擎盖上连续吸出空气,向分析设备引导呼出空气向罩出口,远离其他潜在的泄漏点。收集呼出的空气并分析计算CO2生产,O.2消耗和能量消耗。
实验装置的示意图表示。受试者接受多导睡眠描记术研究,监测心电图、眼电图、脑电图、肌电图、脉搏血氧仪和经皮二氧化碳(CO .)2).用呼吸感应体积描记法监测通风,在实验开始时用流量传感器校准。一旦监测受试者,我们将一种覆盖受试者的上半身的代谢罩。该系统由刚性塑料透明盖组成,附接到塑料片,该塑料板围绕受试者的上半身坐落。纸张在主题周围创造了一个高电阻区域,避免了空气泄漏。另外,泵从罩内部吸入空气,将流量引导到分析设备,远离其他潜在的泄漏点。空气可以通过空气入口或通过系统进入罩,或通过用于鼻高流量(NHF)递送。我们从罩中保持高吸气流动,以尽量减少泄漏。氧气(O.2)消费和合作2在出口流动下测量生产。参与者穿着鼻腔插管(插管1),用于间歇性递送高流量疗法(20 L·min−1, 85%湿度,32°C)。在受试者的胸部放置一个额外的导管(导管2),以便在NHF关闭时输送高流量。因此,我们保持了发动机罩内部的恒定流量。
在我们的环境中,我们试图确定有限公司2NHF疗法期间的生产和能源支出,这将改变输送到引擎盖内部的流动。因此,在泵中收集来自罩的空气的高流速(50升·min−1保持)以避免泄漏并确保恒定的实验条件。到罩的进入流动是NHF流量的总和(20 L·min−1)房间空气入口流(30 L·Min−1).每当关闭对象的鼻子时,我们就会向受试者的胸部发起交付平等的流量通过辅助套管,将整体流到引擎盖恒定的内部保持(图1).由于重要的是保持恒定的流动到代谢罩,我们进行了一系列试点实验使用恒定的来源的一氧化碳2确保交替的NHF不会干扰代谢测量。
研究协议
在大约19:00升至睡眠中心允许受试者习惯于实验程序,并在睡眠研究之前标准化其活动水平。一旦参与者完全监控,我们就开始交付20 L·min的流程−1,85%的湿度和32°C通过鼻腔插管,用于适应的伴侣。我们使用了改进的S8连续正气道压力机(ResMed,Bella Vista,Australia),能够产生高达30 L·min的恒定流量−1.该设备还设计了一个特殊的软管主动加热,以保持温暖和潮湿的输送空气。在22:00 - 23:00之间,受试者以20 L·min的NHF启动睡眠−1.当受试者处于稳定的非快速眼球运动(NREM)第2阶段睡眠时,我们在5到10分钟间隔开/关(图2.).在关闭NHF期间,以与NHF相同的速率、湿度和温度打开第二套管(进入受试者胸部)。对于每个受试者,当睡眠中断的间隔时间不存在,并且脉搏波振幅>比基线没有显著降低50%(作为皮质或皮肤神经活动的标志)时,选择对NHF开/关试验。平均而言,每个受试者获得了三对NHF开启/关闭试验。对测量结果进行总结,得出每个受试者“关闭”和“开启”的平均值,用于统计比较。
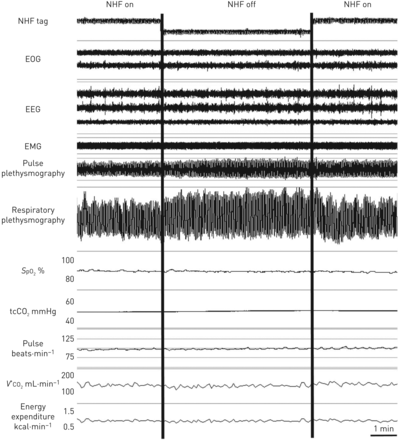
实验方案。NHF:鼻腔高流量;EOG:电动眼图;EMG:电灰度;S.宝2:通过脉冲血液测量测量的动脉氧饱和度;有限公司2:二氧化碳;tcCO2:经皮CO.2;V.'有限公司2:CO.2生产。参与者在NHF下睡觉(20 L·Min−1湿度85%,32°C)。一旦实现非快速眼动第二阶段睡眠,我们交替向鼻腔输送NHF(打开NHF)和无流输送(关闭NHF)。在NHF关闭期间,我们向受试者的胸部输送相同的流量,以保持发动机罩内部的恒定流量。我们选择的月经期没有唤起或交感神经活动的变化。在NHF开启期间,我们可以观察到通气减少,但一氧化碳没有变化2生产或能量消耗
参数计算和统计分析
使用Remlogic PolySomNography记录站(Natus,Pleasanton,CA,USA)记录数据并转移到Igorpro数据分析软件(WaveMetrics,奥斯威宝或美国)。我们从校准的呼吸诱导体积描记术信号中衍生微小的通风,呼吸率和潮气量。使用肺泡通风等式计算生理死空间通风:P.华2= 0.863×V.'有限公司2/(V.'E.-V.'D.), 在哪里P.华2是动脉公司2张力(为此校准的经皮CO2使用测量),V.'有限公司2是co.2产量(用代谢罩测量),V.'E.是分分钟通风V.'D.是每分钟的生理死空间通风[19.].
通过通过呼吸速率除去死空间通风来计算潮汐死空间量。被计算为死空间级数作为潮气量除以潮气量。如前面所述的参与者的高度估计解剖学死空间体积[20.-22.].
有和没有NHF的测量值通过配对t检验进行比较。对照组与COPD患者的缓解程度采用非配对t检验进行比较。用Pearson相关系数分析死空间变化与基线死空间的相关性。我们认为p值<0.05具有统计学意义。
结果
12名参与者被招募(六个对照和六名COPD患者),但一个主题(带COPD)无法在代谢罩下睡觉,并被排除在外。表格1显示已注册人口的人口统计数据。
我们在98个NHF开/关审判中检测到12中的12个觉醒,其中一些显然是由NHF的状态转变(ON OFF或OFF)的过渡引起的反之亦然).一旦检测到唤醒,我们等待较长的时间,直到受试者达到稳定睡眠或者如果睡眠未恢复,则排除在该段的分析。
代谢罩下NHF对睡眠时呼吸模式的影响
在图2.,我们展示了在一个个体(COPD1)睡眠期间,NHF开关条件对通风的影响。可以看出,我们的实验设置NHF打开和关闭在睡眠中(见“NHF标签”跟踪)不干扰睡眠连续性(看到electro-oculogram,脑电图和肌电图的痕迹)或导致自主神经活动的激活,在图中以稳定的心率(脉冲)和脉冲波振幅在这个病人。通过比较潮气量信号(见呼吸容积描记图)和O值来说明NHF对通气的影响2饱和,经皮有限公司2、有限公司2生产和能源支出。虽然在NHF偏离条件下潮汐量增加,但实木同期没有变化2阿,2饱和,CO.2生产或能源支出,表明肺泡通风没有改变。
NHF对通风的影响
显示了合并的数据图3..在基线上,与对照组相比,COPD患者略微但没有统计学上显着的更高的微小通风(对照4.9±0.5 L·min−1与COPD患者6.4±0.6 L·min−1;呼吸频率(对照组15.8±1.0次·min)−1与COPD患者18.4±1.3次·min−1;没有显着的)和死亡空间通风(控制1.8±0.3 L·min−1与COPD患者3.2±0.6 L·min−1;不显著)。
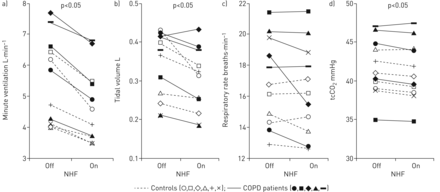
对照组对照组和慢性阻塞性肺病(COPD)患者的鼻高流量(NHF)的通气反应:a)分钟通风,b)潮气量,c)呼吸速率和d)经皮二氧化碳(TCCO2).该绘图显示两个条件下每个参数的平均单个值(NHF OFF / NHF(20L·min)−1)))。各个控制和COPD患者通过不同的符号鉴定(始终使用相同的受试者编码系统图3-5.).我们观察到所有受试者的微小通风显着减少(NHF 5.6±0.4升·分钟−1与NHF浓度4.8±0.4 L·min−1)与使用NHF。除一名受试者外,所有受试者使用NHF也显著减少潮气量(NHF减少340±30 mL)与NHF在300±30毫升)。总体而言,呼吸率没有显着变化,但值得注意的是观察一个人的呼吸率降低,没有减少潮气量。我们注意到了略微但统计学意义,减少了TCCO2使用NHF (NHF off 42.6±1.2 mmHg)与NHF在42.1±1.2 mmHg上)。
响应NHF,我们注意到所有受试者的微小通风都显着降低,如图所示图3A(NHF OFF 5.6±0.4 L·min−1与NHF浓度4.8±0.4 L·min−1;p < 0.05)。通风的降低与潮气量的减少有关(图3B.)从NHF关闭(340±30 mL)到NHF开启(300±30 mL;p < 0.05)。呼吸频率无显著变化(图3C.)和经皮CO的减少最小2(图3d),其从NHF(41.7±1.1mmHg)落到NHF(41.3±1.2 mmHg; P <0.05)。这些参数的变化对于NHF响应于NHF而言是类似的对照和COPD患者。值得注意的是,有一个参与者有一个适度的COPD(女性,55岁,占1,38%的预测的38%的强迫呼气量),他从NHF OFF减少了微小的通风(7.7 L·min−1)至NHF (6.7 L·min−1)由于呼吸率降低了17%至15.5呼吸·分钟−1她的潮气量没有明显变化(从413毫升到433毫升)。
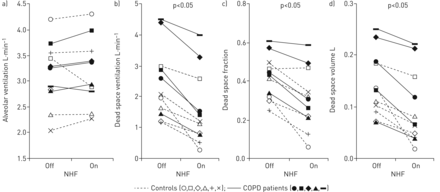
在图4A,我们显示孔隙通风的汇集数据,其在控制和COPD受试者中保持不变。然而,死空间通气的大量(〜40%)降低(NHF OFF 2.5±0.4 L·min−1与NHF在1.6±0.4 L·min−1;p < 0.05;图4B.)、死区分数(NHF off 0.42±0.03与NHF 0.31±0.05;p < 0.05;图4C.)和死空间(NHF OFF 144±19毫升与NHF浓度98±22 mL;p < 0.05;图4D)与使用NHF。在对照组和COPD患者中,死腔通气的减少情况相似。值得注意的是,中度COPD患者将呼吸频率从18.6次·分钟降低到15.5次·分钟−1如前所述,在两组肺泡通气中均无显著变化(NHF关闭3.3 L·min)−1与NHF浓度为3.4 L·min−1)或经皮CO2(NHF OFF 40.3 mmhg与NHF在39.5 mmhg上)。但是,她的死亡空间通风了大幅减少(1.1 L·min−1)这是由于呼吸速率的降低和潮汐死空间体积的减少(NHF OFF 236毫升与NHF在214毫升)。
肺泡通风和死亡空间与鼻高流量(NHF)控制和慢性阻塞性肺病(COPD)患者:a)肺泡通气,b)死空间通风,c)死空间分数(死空间体积/潮气体积)和d)死空间。该绘图显示两个条件下每个参数的平均单个值(NHF OFF / NHF(20L·min)−1)))。各个控制和COPD患者通过不同的符号鉴定(始终使用相同的受试者编码系统图3-5.).使用NHF后,肺泡通气无显著变化。然而,在所有受试者中,NHF显著减少死腔通气(NHF关闭2.5±0.4 L·min)−11.7±0.3 L·min−1),死空间馏分(NHF OFF 0.43±0.03至NHF 0.33±0.04)和死空间(NHF OFF 150±20ml至NHF 100±20mL)。
死腔通风减少的决定因素
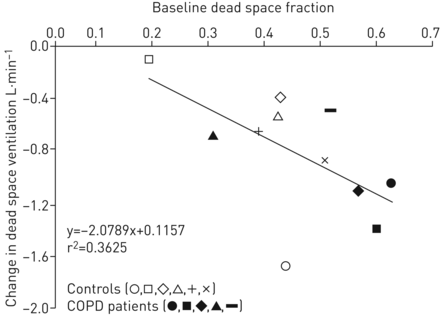
基线呼吸频率、微小通气和解剖死腔体积与死腔通气减少或潮死腔体积减少均无相关性。相反,基线时的生理死腔程度与使用NHF减少死腔通气相关:个体在基线时死腔比例越大,使用NHF减少死腔通气的程度就越大。可以看出图5.,死区分数每增加10%,有208ml·min−1使用NHF (r2= 0.36;p < 0.05)。
讨论
在目前的工作中,我们评估了在睡眠中使用NHF对通风的影响,并直接测量了CO2生产使用代谢罩和多重创新术。首先,我们观察到睡眠期间对NHF通风的反应在COPD患者和对照中类似。其次,由于肺泡通风,CO的显着变化,使用NHF的使用导致微小通风的显着降低。2生产,能源支出或经皮合作效应2.三,减少死空间通风依赖于生理死区分数,而不是基线NHF的基线呼吸衰减空间体积,呼吸速率或微小通风。虽然我们没有观察到肺泡通风或合作的减少2在我们短期的NHF试验中生产,仍有可能较长时间的NHF试验也会影响这些参数。
之前的一些研究已经证明,在上呼吸道模型中使用成像技术,NHF可以冲洗解剖死腔[8.或者在志愿者中的人类上气道[17.].然而,由于技术限制,这些研究不能阐明NHF对死腔间隙的影响,也没有评估CO2生产及新陈代谢[17.].我们能够证明基线生理死腔体积与给定流速下死腔冲刷量有关。已知生理死区与潮气量直接相关[23.].我们现在表明,潮汐停止空间分数越低,NHF的死空间通风的减少越低。因此,由于与具有较低死区分数的人员相比,它似乎具有较高的潮汐量的潮汐量受益于NHF的使用。
在不同的临床环境中,NHF已被广泛用于治疗呼吸衰竭。空气的加温和增湿允许输送更高的流量,创造一个低水平的呼气末正压和增加呼气末肺容量[10.-12.].此外,NHF在睡眠和清醒期间减少了微小通风,而无需增加2水平(9.那16.那24.那25.].当个体清醒或睡眠时,对NHF的呼吸模式反应明显不同[16.],从而解释个人之间呼吸率响应的潜在差异[16.].为了排除这一混杂因素,我们确定了睡眠时的呼吸反应,并表明NHF在对照组和轻至中度COPD患者中同样减少了分钟通气和死腔通气。此外,死腔通气的减少与肺泡通气无变化相关2生产或经皮CO2。这与之前的研究形成了对比,在之前的研究中,我们和其他人已经表明,随着分钟换气次数的减少,呼吸功显著减少[4.那9.那13.-15.].
这些差异有几个解释。首先,我们的NHF的ON / OFF试验可能太短暂,无法转化为CO的变化2生产和能源支出。其次,在睡眠期间,能源支出较低,适用于通风量低的个体,我们预计与呼吸肌肉活动有关的低能源支出。因此,呼吸作品的变化可能太小而无法通过测量能耗来检测。第三,对NHF的通气反应在对照组和COPD患者中类似,这表明这些组之间的呼吸力学没有明显不同。此外,注册的患者数量太小,不能在COPD患者和对照中的反应之间排除微小差异。我们也无法比较性别之间的差别响应。实验设计的复杂性阻止了更大样本的入学。此外,我们的患者没有严重的阻塞。患有更严重的COPD疾病的患者可能已经显示对NHF的差异反应。
我们的研究也有几个优点。首先,本研究在非常可控的环境下进行开/关实验,不影响代谢罩的变量。第二,多导睡眠描记术用于控制与睡眠阶段变化、运动和意识影响有关的生物变量。因此,我们获得了稳定的NREM阶段2-3睡眠的数据,在这个阶段,呼吸模式和代谢非常有规律,可以检测到一氧化碳的微小变化2生产。第三,我们使用校准的呼吸诱导容积描记术对通气进行量化,该方法没有任何可能因使用鼻或口罩而引起的人工通气变化。综上所述,我们的数据表明,对NHF的即时呼吸反应是由于死腔通风的减少。这些变化是否转化为能量消耗的减少可能取决于长时间使用NHF或对高呼吸需求的患者。
我们的研究具有立即临床意义。首先,我们证明在使用NHF期间的肺泡通气仍然是恒定的,并且驾驶员减少分钟通风是死亡空间通气的降低。因此,NHF在患者患者中特别有用,最大化其卸载呼吸系统的可能性。其次,我们现在提供对先前研究中观察到的NHF的异质反应的解释。虽然有些人降低了他们的动脉公司2对NHF的反应,其他人确实降低了呼吸频率[24.].我们假设具有较高生理死区空间通风的个体显示动脉公司的减少2.最后,虽然有限公司2在我们对NHF短暂的开/关试验中,产量保持不变,长时间使用NHF可能会导致呼吸功和CO的减少2并可预防夜间高碳酸血症。然而,需要更长时间暴露于NHF的研究来进一步评估这些假设。
总之,我们表明,在睡眠期间短期使用NHF期间的微小通风机制与CO的减少无关2生产。相反,它是由死腔通风的减少造成的。微小通气减少的程度与基线生理死亡空间的数量相关,以死亡空间分数测量。因此,NHF可以用来卸载呼吸系统,特别是在死亡空间分数很高的患者。
脚注
兴趣冲突:P. Biselli报告了国家卫生研究院(NIH)(HL105546)的补助金,并在研究期间,巴西资助机构Fapesp和CNPQ的补助金。K. Fricke在研究期间报告了NIH(HL105546)的赠款。L. Grote报道Resmed Foundation和Philips Foundation,Resmed(演讲人局和学习支持),飞利浦(演讲人局)的个人费用,伊玛(演讲嘉宾主席团和学习支持)的个人费用,和Weinmann(顾问)的个人费用,在提交的工作之外。在。Braun在研究期间报告了NIH(HL105546)的补助金。J. Kirkness已收到来自NIH(HL105546)的赠款,并且是Fisher&Paykel Healthcare的临床事务总监,在进行和出版研究期间。P. Smith在研究期间报道了来自NIH(HL105546)的补助金。A. Schwartz在进行研究期间报告NIH(HL105546)的赠款。H. Schneider报道了NIH(HL105546)的赠款,咨询和非金融支持的个人费用来自FICHER&Paykel Healthcare的CF患者的设备,来自Resmed的赠款(对于赞助的对NHF在COPD中的NHF的影响)以及个人费用 from TNI Medical (for consultancy; high flow in COPD), during the conduct of the study; personal fees for consultancy from Fisher & Paykel Healthcare and TNI Medical, outside the submitted work; in addition, H. Schneider has a US patent: 7,080,645 issued to TNI Medical (anti-snoring device, method for reducing snoring, and a nasal air cannula).
支持声明:这项研究由Ministerio da Ciencia Tecnologia e Inovacao,慰问Nacional de Desenvolvimento Cientifico e学府(格兰特200817/2012-4),Fundacao德帕罗尽管做Estado de圣保罗(格兰特2012/05190-0)和美国健康和人类服务部门,国家卫生研究院国家心脏,肺,和血液研究所(拨款105546)。本文的资金信息已存入CrossRef Resder注册表.
- 已收到2017年10月31日。
- 公认2018年4月10日。
- 版权所有©ers 2018