摘要
本研究的目的是评估皮肤黑色素瘤患者阻塞性睡眠呼吸暂停(OSA)的严重程度与癌变和肿瘤生长相关的生物标志物水平之间的关系。
这项多中心观察性研究包括新诊断为黑色素瘤的患者。将患者分为非osa(呼吸暂停-低通气指数(AHI) 0 ~ 5事件·h-1),轻度OSA (AHI 5-15事件·h-1)和中度严重的OSA(AHI> 15次事件·H.-1).采用elisa法检测患者血清缺氧及肿瘤黏附相关生物标志物(血管内皮生长因子(VEGF)、白细胞介素(IL)-8、细胞内粘附分子(ICAM)和血管细胞粘附分子(VCAM)-1)和肿瘤侵袭性标志物(S100钙结合蛋白B (S100B)和黑色素瘤抑制活性(MIA))。将年龄、性别和体重指数调整后的logistic模型拟合到每个生物标志物上,并以AHI为因变量。
360例患者(52.2%为男性,中位(四分位范围)年龄55.5(43.8-68.0)岁,AHI事件为8.55(2.8-19.5)·h-1).VEGF,IL-8,ICAM-1,S100B和MIA的水平与OSA的严重程度无关。OSA患者的VCAM-1水平高于没有OSA的患者(轻度OSA:差距(或)2.07,P = 0.021;中度严重OSA:或2.35,P = 0.013)。
在皮肤黑色素瘤患者中,OSA与VCAM-1的升高水平相关,这可能表明OSA在肿瘤发生中的贡献通过integrin-based附着力。
摘要
在皮肤黑色素瘤患者中,OSA与肿瘤发生的生物标志物表达增加有关http://ow.ly/mLo430i9Z8j
介绍
阻塞性睡眠呼吸暂停(OSA)是一种流行疾病,影响≥10%的成年人[1-3.].阻塞性睡眠呼吸暂停的特点是上呼吸道的重复阻塞,导致间歇性缺氧和睡眠中断。阻塞性睡眠呼吸暂停会增加心血管和神经认知后果的风险[4.].
皮肤黑色素瘤是一种黑色素细胞起源的肿瘤。黑色素瘤的发病率在世界范围内呈上升趋势,据估计欧洲和美国每10万居民中有10-30例新的黑色素瘤病例。与皮肤肿瘤相关的死亡中,黑色素瘤占90% [5.].恶性肿瘤一旦扩散就没有有效的治疗方法[6.-8.].黑素细胞向黑色素瘤的致癌转化是多种生理病理途径复杂变化的结果,这些生理病理途径控制细胞周期进展和凋亡[9.].鉴定加速黑素瘤进展的可治疗疾病以及参与这一进展的途径对于降低黑素瘤的死亡率至关重要。
最近,研究表明阻塞性睡眠呼吸暂停与更高的癌症患病率、发病率和死亡率有关[10-12].具体来说,最近的两项研究表明,OSA与皮肤黑色素瘤侵袭性之间存在关系[6.那13].由于OSA的缺氧雷诺循环导致的全身炎症可激活增强肿瘤进展的不同的物理病理学途径[14那15].两种疾病都与循环中黏附分子水平升高有关,如细胞间黏附分子(ICAM)-1 [16-18]和血管细胞粘附分子(VCAM)-1 [17那19那20.];炎症细胞因子,如血管内皮生长因子[21那22]和白细胞介素-8 [7.那16那23];以及黑色素瘤预后和严重程度的生物标志物,如S100钙结合蛋白B (S100B) [7.那24]及黑色素瘤抑制活性(MIA) [7.].
阻塞性睡眠呼吸暂停患者患肿瘤的风险可能增加,但迄今为止,阻塞性睡眠呼吸暂停所起的具体作用尚未明确[25].本研究的目的是评估致癌生殖和肿瘤生长和OSA之间的关系。因此,我们测量了六个,该生物标志物代表不同的物理病理学途径,可以链接OSA和黑色素瘤。
方法
学习规划
这项辅助、观察、前瞻性、横断面和多中心临床研究在西班牙29家教学医院进行,包括皮肤黑色素瘤患者。简单地说,睡眠呼吸障碍的存在和严重程度与黑色素瘤的侵袭性之间的关系被分析。本研究得到了各参与医院伦理委员会的批准。所有参与者均签署知情同意书参与本研究。
病人的选择
患者在每个参与中心的皮肤病或肿瘤学单位进行患者。如果患者诊断出侵入皮肤黑素瘤的诊断,患者最初有资格参加该研究,年龄> 18年,并签署了知情同意参加该研究。初始排除标准包括原发性未知黑色素瘤,静脉内黑色素瘤原位,黑色素瘤,怀孕,白天呼吸或心力衰竭以及目前的连续阳性气道压力治疗(CPAP)。因为患者的转移状态可能会强烈影响癌症的循环生物标志物的水平,所以排除了那些转移状态的患者(图1).
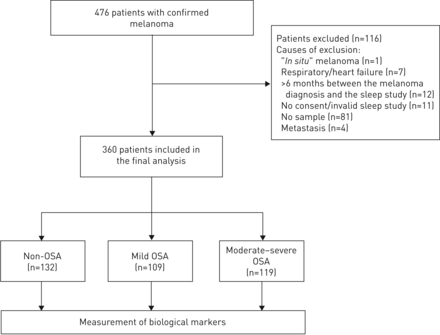
研究流程图。阻塞性睡眠呼吸暂停。
睡眠研究
研究中纳入的患者在每个中心的睡眠单元被诊断为皮肤黑色素瘤后,接受了最多6个月的多普勒成像检查。呼吸多普勒记录仪包括连续记录口鼻流量和压力、心率、胸腹呼吸运动和动脉血氧饱和度(S.敖2).培训的人员手动打印媒告数据。呼吸暂停被定义为Oronasal气流的中断> 10 s。低丙酮痤疮定义为> 10 s的Oronasal气流减少30-90%,其与氧气去饱和≥3%相关。呼吸暂停症 - 低尿症指数(AHI)定义为录音期间每小时呼吸暂停事件加上低吞咽事件的数量;此外,录制时间的百分比与S.敖2< 90%是录音机。此外,测量基线饱和度、平均饱和度、最低饱和度和氧饱和度指数(ODI)分别为3%和4%。
将患者分为以下三组:非osa组(AHI 0-5事件·h-1轻度睡眠呼吸暂停组(AHI 5-15事件·h)-1中、重度睡眠呼吸暂停组(AHI >15事件·h)-1).
评估皮肤黑素瘤的生长速率
根据Breslow指数(以毫米)计算皮肤黑色素瘤生长速率除以肿瘤切除日期与患者在稳定的,预先存在的病变或时间暗示恶性转化的日期之间的差异。他们注意到了一个新的和改变病变的外观[6.].皮肤黑色素瘤的生长速率分为:慢-中(<0.49 mm·月)-1)和快速(≥0.5 mm·月-1) [26].
循环分子的测量
08:00 ~ 09:00 h采集空腹静脉血。血液标本离心分离血清,所有标本立即ali引物、冷冻并保存在−80°C。
两种不同的方法,IE。采用多重分析和传统elisa方法对循环分子进行定量分析。简单地说,Q-Plex ELISA (Quansys Biosciences, Logan, UT, USA)技术允许在微尺度水平上同时测量和检测多种蛋白质。该技术涉及一系列定量夹心elisa,使用标准曲线进行数据插值。使用夹心elisa,捕获抗体被标记到96孔微滴度板上,并与样品中的靶蛋白结合,次级抗体或检测抗体与靶蛋白上的不同表位结合。链霉亲和素-辣根过氧化物酶预先与二抗结合并用于产生信号。所测信号与样品中目标蛋白的量成正比。
用Q-View Imager分析两种多重蛋白(VEGF和IL-8)。按照制造商的建议,采用单个elisa检测VCAM-1、ICAM-1、MIA和S100B。对于每一项检测,生成标准曲线以确定蛋白质的浓度。每种蛋白的敏感性和ELISA标记见表online补充表E1.
切除后黑色素瘤肿瘤组织的分子测量
测量VEGF的表达水平和缺氧诱导因子(HIF)-1α的水平,并在这种患者队列中报道[27来确定是否评估这些生物标志物在切除后的黑色素瘤肿瘤组织中的丰度,可以更准确地确定肿瘤的侵袭性。在本研究中,我们评估了这些生物标志物的表达水平与OSA严重程度的关系。在福尔马林固定、石蜡包埋的黑色素瘤标本4 μm厚切片上,采用免疫组化方法评估VEGF和HIF-1α的水平。使用Leica Bond Polymer Refine Kit (Leica Biosystems, Newcastle, UK)在Leica Bond- iii染色剂(Leica Biosystems, Newcastle, UK)上进行免疫染色。黑色素瘤样本用1:2稀释的抗vegf预稀释抗体(ab27620;Abcam, Cambridge, UK)和1:100稀释的抗hif -1α抗体(ab51608;Abcam)。染色结果由两位对患者的分期和临床特征不了解的病理学家独立分析。考虑到阳性的百分比(<25%,25-50%,51-75%和>75%)和表达强度(负低或高),对vegf特异性染色进行评分。hif -1α特异性核染色评分考虑是否存在阳性细胞。
统计分析
定量变量表示为中位数(四分位区间(IQR)),因为这些变量是非正态分布的。用绝对频率和相对频率来描述定性变量。我们进行了双变量分析,根据AHI组分析研究变量。定量变量比较采用Kruskal-Wallis检验,定性变量比较采用Pearson卡方检验或Fisher精确检验。logistic回归模型(根据年龄、性别和体重指数(BMI)调整)对每个elisa进行拟合作为解释变量,AHI按严重程度(非OSA、轻度OSA和中度重度OSA)分类为因变量。采用Hosmer-Lemeshow拟合优度检验对校准进行评估。所有检验均为双尾检验,差异有统计学意义(0.05)。使用R版本3.3.1进行统计分析。
结果
病人的特点
在最初招募的476名患者中,360名经睡眠研究并提供至少一份血清样本的皮肤黑色素瘤患者被纳入最终分析(图1).患者的临床特征和人口统计变量显示在表1.研究人群包括体重超重且有轻度睡眠呼吸暂停的中年男性和女性(AHI 8.55 events·h)-1,范围2.80-19.5事件·h-1).
血清标志物分析
提出了VEGF,IL-8,ICAM-1,VCAM-1,S100B和MIA的循环水平的测量结果图2.非OSA,轻度OSA和中度严重的OSA患者的血清IL-8,ICAM-1,S100B和MIA水平相似(P = 0.436,P = 0.259,P = 0.560和P = 0.328).这些生物标志物与皮肤黑素瘤的炎症,进展和预后有关,与OSA的严重程度没有显着相关。相比之下,VEGF的血清水平在轻度OSA(OR)1.26,95%CI 0.20.28和中度严重的睡眠呼吸暂停(或1.61,95%CI)中表现出增加的趋势(P = 0.165)0.85-3.06)组(图2和表2).类似地,我们观察到,睡眠呼吸暂停患者VCAM-1的血清水平显着高于非OSA患者,适用于温和的OSA(或2.07,95%CI 1.12-3.89; P = 0.021)和中等在调整BMI,年龄和性别后,--Severe OSA(或2.35,95%CI 1.20-4.66; P = 0.013)(表2和图2).根据ODI三环(数据未显示)比较组也得到了类似的结果。
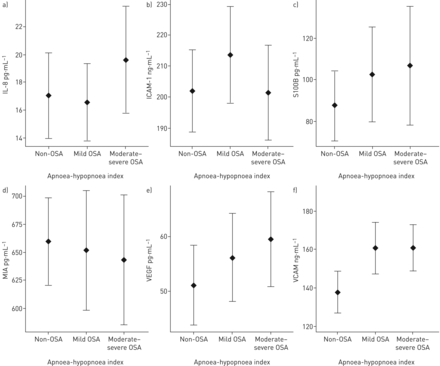
生物标志物的循环水平。一)白介素8 (IL);b)细胞内粘附分子(ICAM)-1;c) S100钙结合蛋白B (S100B);d)黑色素瘤抑制活性(MIA);e)血管内皮生长因子(VEGF);f)血管细胞粘附分子(VCAM)。数据以中位数(四分位数范围)表示。阻塞性睡眠呼吸暂停。
肿瘤组织样本分析
评估VEGF和HIF-1α在肿瘤切除后的组织样本中的表达水平表3.虽然在中重度OSA患者中HIF-1α阳性染色肿瘤比例中观察到这一趋势,但调整后的分析报告称,非OSA患者和轻度OSA患者中HIF-1α阳性染色肿瘤比例相似(OR 1.52, 95% CI 0.64-3.75;p=0.35)和中度严重OSA (OR 1.82, 95% CI 0.73-4.77;p = 0.21) (表3).对于VEGF,肿瘤组织样品中染色细胞的比例为75%,适用于三组。获得切除肿瘤组织样品中的VEGF表达的差距,并且在组之间没有出现显着差异(表3).
皮肤黑素瘤生长率与VCAM-1之间的关系
VCAM-1水平按平均值分为以下两类:VCAM-1水平高(高于平均值)和VCAM-1水平低(低于平均值)。研究发现,高血清VCAM-1水平与皮肤黑色素瘤快速生长呈正相关(图3) (1.59, 95% CI 0.91-2.76),但两者之间的相关性没有达到统计学意义(p=0.112)。
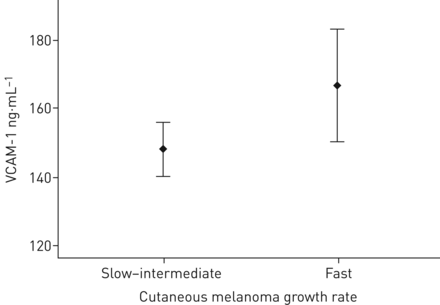
血管细胞粘附分子(VCAM)-1的循环水平与皮肤黑色素瘤生长速度的关系数据以中位数(四分位数范围)表示。
讨论
在本研究中,我们描述了如何在皮肤黑色素瘤的患者队列中,OSA严重程度与VCAM-1肿瘤粘附相关生物标志物的血清水平有关,但不是与肿瘤侵袭性相关的血清标记水平相关作为VEGF,IL-8,ICAM-1,S100B和MIA,或VEGF和HIF-1α的水平和肿瘤组织样品中的表达。
ICAM-1循环水平的增加以及ICAM-1与AHI之间的相关性此前已有报道[16那19那28].血管内皮生长因子在OSA患者的循环水平经常升高,并在组织供氧中发挥调节作用[22那28].据报道,OSA患者的IL-8水平高于健康对照的患者[16那29],而S100B水平在OSA患者中升高,但与疾病的严重程度无关[24那30.].我们只观察到VCAM-1水平升高和VEGF水平中度升高,这可能是由于人群之间的差异,因为我们的队列包括皮肤黑色素瘤和OSA患者;皮肤黑色素瘤效应,与VEGF的增加独立相关[31那32],与IL-8一起[28那32],ICAM-1 [18那33], S100B [7.那34那35]和mia [7.那35那36,可以掩盖OSA对这些蛋白的影响,这可能解释了为什么我们没有观察到之前报道的这些生物标志物在OSA患者中的差异。尽管皮肤黑色素瘤的存在可能会对OSA对感兴趣的生物标志物的贡献产生潜在的上限影响,但该研究并不是为了解决这个问题,因此目前必须停留在推测阶段。在本研究中,我们无法评估OSA和皮肤黑色素瘤的具体独立影响。这进一步支持了将OSA和皮肤黑色素瘤与本研究中探索的生物标志物的相关关系分离的必要性。然而,这项研究并不是为了解决这种特定的可能性。事实上,我们需要包括两个额外的匹配组(没有皮肤黑色素瘤和没有OSA;然后进一步评估治疗OSA对相关生物标志物的影响,以分离皮肤黑色素瘤和OSA对这些生物标志物的独立和重叠贡献。
一些病理生理机制,包括关键的中间分子,将OSA与癌症的侵袭性联系起来。OSA患者血清VCAM-1水平高于健康对照组[17那19那28,这主要是由于缺氧压力。OSA可增强皮肤黑色素瘤的侵袭性,增加VCAM-1水平。
VCAM-1的分泌形式是由于其从细胞表面释放时的蛋白水解分裂通过中性粒细胞衍生的丝氨酸蛋白酶的活性。VCAM-1主要涉及白细胞转型迁移和白细胞保留到组织中[37].VCAM-1在炎症细胞募集中起核心作用,其表达可由促炎细胞因子(如VEGF)迅速诱导[38].VCAM-1由于其多种函数引导肿瘤传播,形成转移性核桃和支持血管生成过程而起到重要作用20.].可见,缺氧应激引起的OSA可提高血清VEGF水平,刺激VCAM-1表达,促进肿瘤发生。VCAM-1循环水平与黑色素瘤生长速度之间的关系支持了这一假设。尽管结果在统计学上没有显著性,但可能存在一种积极关联的趋势,并应进一步探索。
首次有报道称,在已经患有皮肤黑色素瘤的OSA患者中,肿瘤发生的生物标志物水平升高。这些发现可以突出VCAM-1在OSA患者肿瘤发生中的重要性,它可能是OSA与皮肤黑色素瘤相关的一个途径。在本研究中,我们观察到随着OSA严重程度的增加,摘除后黑色素瘤肿瘤组织中HIF-1α有升高的趋势,尽管调整后的分析显示轻度OSA和中度/重度OSA之间的表达水平相似。肿瘤样本中VEGF水平与OSA严重程度之间未观察到显著相关。考虑到它们的可获得性,与皮肤黑素瘤患者OSA显著相关的生物标志物由循环血液样本测量的水平组成,这一事实可能与它们的临床效用有关。VEGF和VCAM-1的循环水平可能有助于识别具有较高致癌和肿瘤生长风险的黑色素瘤和OSA患者。此外,测量VEGF和VCAM-1循环水平不仅对皮肤黑色素瘤患者很重要,而且对OSA患者也很重要,因为这些生物标志物在肿瘤发生的初始阶段起着重要作用,血清VCAM-1和VEGF水平升高的OSA患者更容易发生肿瘤发生。这些发现支持了以下假设,即通过增加循环VEGF和VCAM-1水平来治疗皮肤黑色素瘤和OSA患者可以减少肿瘤的发生并改善肿瘤预后。
间歇性缺氧和唤醒,OSA的Hallmark特征被认为是OSA的主要病理生理后果,这促进了促进OSA与其有害后果相关的中间机制的激活,并且可能有助于增加癌症风险增加[25].与实验室和动物实验的证据一致[39,之前的观察试验已经报道,随着OSA水平的增加,癌症发病率也会增加[40那41].这些观察性研究表明,阻塞性睡眠呼吸暂停患者夜间低氧血症与癌症死亡率之间存在关联。值得注意的是,在未接受治疗的患者中,低氧指数与癌症发病率之间的相关性略强。治疗的应用允许取消呼吸暂停可能有助于减少这些与癌症相关的血管生成生物标志物。虽然有数据明确表明睡眠呼吸暂停和癌症风险之间的关联,但绝对缺乏证据表明CPAP治疗对降低OSA患者的肿瘤侵袭性可能有积极作用。虽然CPAP治疗对OSA和癌症患者的影响尚未探索,但基础研究已经确定了CPAP治疗在肿瘤发生相关机制中的作用。事实上,克哈布斯等等。[42]研究了18例OSA患者CPAP治疗1个月前后外周血白细胞全基因组表达。基因集富集分析比较了每个患者在cpap治疗前后的白细胞,表明OSA治疗导致肿瘤过程中部分基因集下调。此外,Hernandez -jimenez等.[43]表明,OSA诱导循环单核细胞和自然杀伤细胞的功能改变,这可能有利于肿瘤免疫逃逸。在cpap治疗的患者中未观察到这一发现。最后,一个lmendros.等.[44]在鼠模型中评价是否表征OSA表征慢性间歇性缺氧导致在循环中释放肿瘤促进外来体。这些研究人员观察到,在间歇性缺氧期间释放的外泌体模仿OSA增加了TC1肺肿瘤细胞的恶性性质体外.此外,在本研究中,作者在CPAP治疗前后的6周和之后评估了来自10名成人人类患者的EXOSOMES,并报道了与OSA患者的患者从6周的粘附性CPAP后的患者增加增殖和迁移。治疗。
CPAP治疗是治疗OSA的金标准,应该被认为是OSA的一线治疗方案。下颌骨前移装置也被考虑用于阻塞性睡眠呼吸暂停的治疗,特别是在轻度-中度阻塞性睡眠呼吸暂停[45].对皮肤黑色素瘤和OSA患者进行有效的OSA治疗可能有助于降低与癌症相关的标志物水平。由于缺乏证据表明CPAP治疗在癌症进展中的可能积极作用,目前这种可能性应被认为是推测性的。需要进一步研究评价CPAP治疗对致瘤生物标志物的作用以及OSA和癌症患者的预后。
这项研究的主要优势在于它的前瞻性和相对较大的队列规模,这使得我们能够适当测量OSA严重程度对与癌变和肿瘤生长相关的生物标志物的潜在影响。然而,目前的研究有几个局限性,值得评论。首先,睡眠习惯和倒班工作这些与癌症有关的变量没有被报告[12].其次,这项研究的结果与皮肤黑色素瘤特别相关。正因为如此,VCAM-1和VEGF的关系在其他类型的癌症中不存在。第三,本研究评估皮肤黑色素瘤患者OSA严重程度与肿瘤相关生物标志物水平之间的关系;然而,目前还没有关于CPAP治疗对这些生物标志物的影响的信息。
总之,我们的研究表明,在皮肤黑色素瘤患者中,OSA与高水平的循环VCAM-1肿瘤黏附相关生物标志物独立相关,但与肿瘤侵袭性相关的循环标志物水平无关。肿瘤粘附相关通路的激活可能与所观察到的OSA严重程度与黑色素瘤的关系有关。还需要进一步的研究来确定OSA严重程度与癌症之间的中间通路。
补充材料
脚注
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:该项目得到了西班牙卫生部FIS 2016/01772、Sociedad Española de Neumología y Cirugía Torácica (SEPAR)和Sociedad Valenciana de Neumología的支持。F. Santamaria-Martos获得了“莱莱达agur大学”的博士前奖学金。本文的资金信息已存入Crossref资助者注册表.
利益冲突:没有宣布。
- 收到了2017年9月15日。
- 公认2018年1月29日。
- 版权©2018人队















