摘要
在一些患有阻塞性睡眠呼吸暂停(OSA)的患者中,呼气时上颚下垂到腭咽,限制了通过鼻子的气流或将其从口腔排出。我们假设这种现象导致呼气流量限制(EFL),并与吸气“孤立的”腭塌陷有关。我们还想提供一种强有力的非侵入性方法来识别这种梗阻机制。
使用自然睡眠内窥镜,22名OSA患者的1211次呼吸被评分为是否有腭脱垂。患者水平的塌陷部位(舌相关、孤立腭、咽侧壁和会厌)也被描述。用最大会厌压力下的呼气阻力量化EFL。开发了一种非侵入性EFL指数(EFLI)来检测是否存在腭脱垂和仅使用流量信号的EFL。此外,还评估了使用鼻压的有效性。
EFLI >0.8的临界值检测腭脱垂和EFL的存在,>的准确性分别为95%和82%。伴有腭脱垂的呼吸比例预测孤立吸入性腭塌陷的准确率为90%。
这项研究表明,呼气腭下垂可以无创量化,与EFL相关,并预测吸气孤立性腭下垂的存在。
摘要
呼气性腭下垂可以无创量化,并预测吸气孤立性腭下垂http://ow.ly/vm6c30hB839
简介
阻塞性睡眠呼吸暂停(OSA)是一种常见的疾病,其特征是在睡眠时反复发生上呼吸道萎陷[1,导致睡眠碎片化[2和交感神经激活[3.].未经治疗的阻塞性睡眠呼吸暂停也与不良的神经认知(白天嗜睡、注意力下降)有关[4- - - - - -6和心脏代谢并发症(高血压、糖尿病、中风)[4,7,8].
在阻塞性睡眠呼吸暂停患者中,上呼吸道阻塞是由睡眠中一个或多个咽部部位(腭、舌基部、侧壁和会厌)塌陷引起的[9,10].在我们小组现有的内窥镜下识别这些结构的调查过程中,我们观察到,在一些人的软腭和小舌在呼气时下垂(膨胀)到腭咽(图1).这些情况很容易识别,因为它们产生严重的咽部狭窄/颤动,偶尔呼气流出口腔的方向改变(单向气流,即。用鼻子吸气,用嘴呼气)。所涉及的软盘组织(软腭和小舌)的运动通常非常剧烈,并引起觉醒。
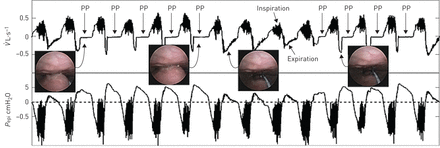
上颚在呼气时向腭咽突出或“膨胀”(上颚脱垂,用“PP”表示)。左边的两张内窥镜图像显示了两种不同呼吸呼气时腭咽部气道视图的腭脱垂。左起第三张内窥镜图像显示正常呼气时打开的气道。右边的内窥镜图像也显示了腭脱垂发生前的开放气道。上图为测气仪测得的气流( )和底部的痕迹显示同时测量的会厌压力(Pepi).这张图清楚地显示了一个明显的和可重复的呼气流模式,每当腭脱垂(气球)进入腭咽。在反复腭脱垂(箭头标识为腭脱垂)期间,尽管会厌压力增加,但呼气流量没有增加,可见呼气流量限制。在腭脱垂期间,呼气气道正压在会厌处形成,与呼气鼻流量的相应增加无关。
)和底部的痕迹显示同时测量的会厌压力(Pepi).这张图清楚地显示了一个明显的和可重复的呼气流模式,每当腭脱垂(气球)进入腭咽。在反复腭脱垂(箭头标识为腭脱垂)期间,尽管会厌压力增加,但呼气流量没有增加,可见呼气流量限制。在腭脱垂期间,呼气气道正压在会厌处形成,与呼气鼻流量的相应增加无关。
此外,研究表明,在50%的呼吸中,呼气流量限制(EFL)与吸气流量限制相结合[11,是一种常见的临床发现[11- - - - - -14,并有可能用于预测阻塞性肺疾病[15]和麻醉诱导过程中面罩通气的效率[16睡眠呼吸障碍的患者。然而,其作用机制尚不清楚。
我们假设EFL是典型的由腭脱垂引起的。因此,我们分析了自然睡眠时与血流和会厌压同时记录的内窥镜视频来验证这一假设。此外,我们假设,腭脱垂在睡眠时产生明确的、可重复的呼气内气流特征,可以从呼气流量(由肺描记仪和鼻插管测量)自动识别,因此可以从临床多导睡眠图诊断腭脱垂。因此,我们开发并验证了一种EFL指数(EFLI,一个介于0到1(最严重的流量限制)之间的正数),以检测金标准内窥镜所定义的呼气脱垂的存在。此外,还研究了腭脱垂和导致吸气气道塌陷的结构之间的关系。此外,作为一项额外的临床验证,在一个单独的亚组患者中同时测量了肺描记仪流量和鼻压。测定了测气仪流量与鼻压EFLI的相关性。
方法
参与者
目前的结果是通过对导致上气道塌陷的结构与气流模式之间关系的调查中获得的数据进行进一步分析而得出的[17,18].简单地说,伴有呼吸暂停-低呼吸指数(AHI) >的OSA患者10次·h−1应邀参加。排除标准包括使用呼吸刺激剂或抑制剂(包括阿片类药物和苯二氮卓类药物)、心力衰竭或肺部疾病、中枢性睡眠呼吸暂停和怀孕。参与者提供书面知情同意,并由我们医院的机构审查委员会批准。
内窥镜的研究
设置
参与者接受了包括脑电图(EEG)、下巴肌电图(EMG)、眼电图(EOG)、心电图(ECG)、胸腹运动、体位和脉搏血氧测量在内的生理多导睡眠图检查。根据标准的临床标准对睡眠、觉醒和呼吸事件进行评分(睡眠不足:流量减少30%,伴有≥3%的去饱和或觉醒)[19].评估通气流量通过附在密封鼻罩上的气测仪(Hans Rudolph, Shawnee, KS, USA)。用参考大气的压力传感器(Validyne, Northridge, CA, USA)监测掩膜压力。咽腔压力测量采用5-French Millar导管(6个压力传感器相距0.75 cm)通过鼻孔插入,尖端置于下咽。为了观察气道,通过第二个鼻孔插入直径2.8毫米的儿科支气管镜。除EEG、EMG、EOG和ECG以125 Hz采样外,其余信号均以500 Hz采样频率采集,图像以30帧·s采样−1.
协议
参与者被要求以仰卧位或侧卧位睡觉。显微镜的尖端最初放置在软腭上方,以观察腭咽。然后将镜尖推进口咽,以可视化口咽和下咽结构。这一过程重复进行,在整个晚上观察尽可能多的咽部呼吸。
内窥镜分类金标准和EFL金标准
由于研究的侵入性和在阻塞性睡眠呼吸暂停患者自然睡眠时进行内镜检查的固有挑战,整晚观察所有呼吸的咽部结构是不可行的。如果呼吸发生在:1)觉醒,2)快速眼动(REM)睡眠,2)镜头在口咽部,3)粘液或唾液模糊内窥镜视野或4)光线不充足时,呼吸被排除在外。根据内镜视频的视觉检查,非快速眼动睡眠期间的剩余呼吸被标记为与腭脱垂相关或不相关。如果上颚脱垂,呼吸被标记为上颚脱垂(上颚游离边缘翻转到尾部方向,见图2 b)或呼气时膨胀(由于腭后部运动导致腭咽50%狭窄)进入鼻咽。
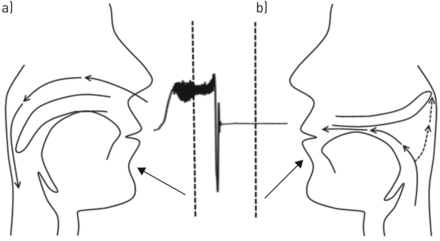
在一些患者中,在呼气时,软腭和小舌脱垂(球囊)进入腭咽,产生严重的咽狭窄和呼气流出口腔的重定向(通过鼻子呼吸a)和通过口腔呼吸b)。图中所示的气流仅显示由附在鼻罩上的测气仪所测得的鼻流量。
气道塌陷的部位或机制分为舌相关梗阻、孤立腭塌陷、咽侧壁塌陷和会厌塌陷。按照以前的出版物中所述进行分类[17].简单地说,如果舌头在呼气结束时处于“后位”(接触会厌和/或将会厌向后推并遮住声带),则认为是导致塌陷的主要结构。由于舌和腭之间的解剖关系,舌相关梗阻几乎总是与腭阻塞有关。如果侧壁在吸气和呼气时都使气道在侧向方向变窄,则认为侧壁是塌陷的主要部位。会厌塌陷定义为会厌前后侧(折叠)塌陷[17,18].孤立性腭塌陷被定义为不涉及其他气道结构的腭水平塌陷。当有多个结构发生梗阻时,咽部负压最小时结构塌陷占主导地位。这一分类是由两名研究人员在患者水平的基础上进行的,差异由第三名研究人员解决。为了描述腭脱垂和吸气塌陷部位之间的关系,计算每个患者的腭脱垂呼吸比例(PP%,内镜下呼吸%)。
EFL的确定是基于同时观察流量和会厌压力,并通过测量呼气时会厌压力峰值的呼气阻力)。R亚历山大-伍尔兹被定义为R亚历山大-伍尔兹=Pepi马克斯/ 经验值.呼吸与R亚历山大-伍尔兹> 20而言不啻2O·s·L−1被标记为EFL。要确定R亚历山大-伍尔兹截止20cmh2O·s·L−1每次呼吸时,测定呼气流量峰值时的阻力(补充图S1).我们假设在呼气流量达到峰值时,大多数呼吸的阻力是正常的;该值为8.0 (5.7-11.7)cmH2O·s·L−1(括号中的值是四分位范围(IQR))。的R亚历山大-伍尔兹EFL检测的截止点设置为中位数+两个IQRs,即20 cmH2O·s·L−1.值得注意的是,我们使用R亚历山大-伍尔兹绝不意味着压力和流量之间存在线性(欧姆)关系R亚历山大-伍尔兹是不受压力影响的湿陷性的特征度量。此外,考虑到非efl呼吸的呼气阻力范围很广(即。1≤R亚历山大-伍尔兹≤20而言不啻2O·s·L−1)的情况下,“较少呼气流量限制”一词可能更合适。然而,为了简单,所有的呼吸都伴随着R亚历山大-伍尔兹≤20而言不啻2O·s·L−1被称为非efl呼吸。
经验值.呼吸与R亚历山大-伍尔兹> 20而言不啻2O·s·L−1被标记为EFL。要确定R亚历山大-伍尔兹截止20cmh2O·s·L−1每次呼吸时,测定呼气流量峰值时的阻力(补充图S1).我们假设在呼气流量达到峰值时,大多数呼吸的阻力是正常的;该值为8.0 (5.7-11.7)cmH2O·s·L−1(括号中的值是四分位范围(IQR))。的R亚历山大-伍尔兹EFL检测的截止点设置为中位数+两个IQRs,即20 cmH2O·s·L−1.值得注意的是,我们使用R亚历山大-伍尔兹绝不意味着压力和流量之间存在线性(欧姆)关系R亚历山大-伍尔兹是不受压力影响的湿陷性的特征度量。此外,考虑到非efl呼吸的呼气阻力范围很广(即。1≤R亚历山大-伍尔兹≤20而言不啻2O·s·L−1)的情况下,“较少呼气流量限制”一词可能更合适。然而,为了简单,所有的呼吸都伴随着R亚历山大-伍尔兹≤20而言不啻2O·s·L−1被称为非efl呼吸。
无创性EFLI
我们假设腭脱垂导致EFL,并在呼气时产生独特的流动形状(图1)是可以客观识别的。因此,我们试图以自动化的方式量化这种独特的呼气流形状。
为了自动识别腭脱垂和EFL,呼气流量( 经验值)首先被自动识别[20.].明显的呼气流形状(如图所示)图1而且2通过将呼气流量分为偶数(对称)和奇数(不对称)分量,并测量奇数分量的均方根来量化。看到补充材料参阅EFLI的详细计算,以及为何采用这种信号处理技术的进一步原理。
经验值)首先被自动识别[20.].明显的呼气流形状(如图所示)图1而且2通过将呼气流量分为偶数(对称)和奇数(不对称)分量,并测量奇数分量的均方根来量化。看到补充材料参阅EFLI的详细计算,以及为何采用这种信号处理技术的进一步原理。
腭脱垂与金标准EFL的关系
通过内窥镜将所有呼吸分为腭脱垂或非腭脱垂,通过流量和会厌压力(通过计算会厌压力峰值时的阻力)将呼吸分为“EFL”或“非EFL”。腭脱垂和EFL之间的关系是通过Fisher精确测试确定的。
确定呼气流量受限呼吸的EFLI阈值
下一步是从流量信号中获取相同的信息。因此,为了确定EFLI阈值,数据被分为两组:训练集(n=606次呼吸)和验证集(n=605次呼吸)。从训练集中,使用接收者工作特征(ROC)曲线识别阈值,并最大化分类器的性能,即。EFLI。然后使用验证集测试该阈值的敏感性和特异性。
同时测量气速描记器流量和鼻压的临床验证
共有10例患者完成了前瞻性验证多导睡眠描记术[18,21]以评估在我们的方法中使用鼻压作为通气流量的临床替代的有效性。为了同时测量鼻压(鼻套管)和通气流量(带口鼻面罩的肺描描仪),改进的套管(Hudson RCI“过耳”,切成适合口罩下方;Teleflex, Morrisville, NC, USA)提供了一种鼻压信号,该信号与口罩压力相关,以反映临床可用的压力信号。1768次呼吸(平均±sd每名受试者177±75次呼吸)从多导睡眠图中随机抽取。对于每次呼吸,使用鼻压估算EFLI(使用平方根变换线性化[22,23]),然后分别用气速记录仪流量进行量化比较。
统计分析
除非另有说明,数据用平均值±标准差或平均值±标准误差表示。组间比较采用未配对双尾t检验或Wilcoxon符号秩检验。Fisher精确检验用于分类变量之间的关联。采用Kruskal-Wallis检验和Dunn's多重比较检验,以检验PP%是否在不同地点的崩溃灵感。由于在同一患者中,会厌塌陷总是发生在另外一个塌陷部位之外,因此我们将会厌塌陷从Kruskal-Wallis分析中排除。采用简单线性回归法建立肺活量EFLI与鼻压测量EFLI之间的关系模型。差异有统计学意义(p<0.05)。使用MATLAB软件(MathWorks, Natick, MA, USA)进行分析。
结果
内窥镜的研究
病人的特点
内窥镜检查研究涉及22例OSA患者(平均±0.01)sd年龄51.6±8.2岁,女性7例),平均±1例sdAHI为48.5±28.9个事件·h−1体重指数(BMI)为33.1±6.2 kg·m−2.表1介绍参与者的特征和多导睡眠参数。
用内窥镜检查呼吸
1211次呼吸(平均±sd分析非快速眼动睡眠时55±26次呼吸。226例(18.7%)为腭脱垂,985例(81.3%)为非腭脱垂。Fisher精确测试用于确定位置是否对腭脱垂的发生有任何影响。28%的仰卧呼吸与腭脱垂相关,而只有5%的侧卧呼吸被归为腭脱垂。差异有统计学意义(p<0.0001)。
腭脱垂与气道塌陷部位的关系
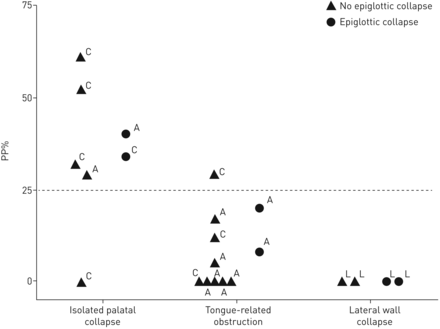
Kruskal-Wallis检验显示,中位PP%在不同的塌陷吸入部位有显著差异(Kruskal-Wallis统计值10.94;p = 0.0013)。Dunn's试验显示,孤立腭塌陷患者的PP%明显高于舌相关梗阻患者(平均等级差7.5;P =0.036)和侧壁塌陷(平均等级差11.9;p = 0.0063)。PP%在舌相关梗阻和侧壁塌陷患者之间相似(平均等级差4.4;p = 0.67)。图3显示所有个体的PP%的散点图。对于PP% >25%的临界值,识别腭塌陷患者的敏感性/特异性为85.7%/93.3%。对于EFLI >0.8的临界值,敏感性/特异性完全相同。
所有个体伴有腭脱垂的呼吸比例的散点图(PP%,内镜下呼吸%)。单纯腭塌陷患者的PP%明显高于舌源性梗阻和咽侧壁塌陷患者。会厌塌陷的发生预计不会改变PP%。每个个体的上颚处气道崩溃的方向也显示出来:同心(C)、正侧(A)或侧侧(L)。注意,如果使用呼气流量限制指数>0.8 (EFL%)的呼吸比例而不是PP%,则可以获得类似的25%的阈值。
腭脱垂与EFL的关系
93%的腭脱垂呼吸表现为EFL,而非腭脱垂呼吸仅为11%。这种差异具有统计学意义(双尾p<0.0001)。这表明约89%的EFL呼吸与腭脱垂有关。
EFLI在判断腭脱垂和EFL中的准确性
EFLI测定腭下垂的ROC曲线分析结果为均值±se曲线下面积(AUC)为0.997±0.0013 (p<0.0001)。选择阈值EFLI为0.8来区分腭脱垂呼吸(EFLI >0.8)和非腭脱垂呼吸。这导致了平均值±se在训练集中使用时,敏感性为94±2.6%,特异性为99±0.5%。当EFLI阈值为0.8应用于测试集时,平均±se灵敏度为92±3.1%,特异性为99±0.8%。如图4,有无腭脱垂呼吸的EFLI分布有明显差异。第二次ROC曲线分析用于区分EFL呼吸(R亚历山大-伍尔兹> 20而言不啻2O·s·L−1)从非efl呼吸使用EFLI。这导致了平均值±seAUC为0.82±0.02 (p<0.0001)。同样的EFLI阈值为0.8,检测EFL呼吸的准确性为82%。有趣的是,如果呼吸与R亚历山大-伍尔兹> 25而言不啻2O·s·L−1被认为是EFL呼吸,平均值±seAUC增加到0.86±0.02 (p<0.0001), EFLI阈值为0.8导致检测EFL呼吸的准确性提高到85%。这表明腭脱垂可能与更严重的EFL相关(用更高的R亚历山大-伍尔兹),用“呼气流形状”计算的呼气流量指数可以更准确地检测。
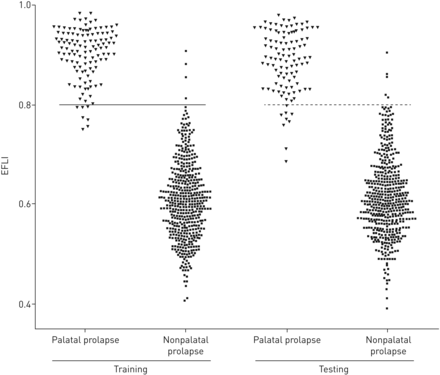
与呼气流量限制(EFL)相关的呼吸明显具有不同的EFL指数(EFLI)分布,因此对EFL的检测具有较高的敏感性和特异性。
同时测量气速描记器流量和鼻压的临床研究
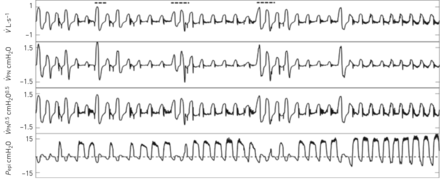
鼻压研究涉及10名不同的患者(平均±0.01)sd年龄57.2±8.2岁;2名女性),平均值±sdAHI为42.0±25.5个事件·h−1BMI为29.6±6.5 kg·m−2(表1).图5展示了一个在非快速眼动睡眠期间用全面罩加肺描记仪和鼻导管测量的EFL追踪的例子。由空气记录仪测量的气流( )与从鼻压(
)与从鼻压( PN) (r = 0.90;P <0.0001)和线性化的鼻压(
PN) (r = 0.90;P <0.0001)和线性化的鼻压( PN0.5) (r = 0.91;p<0.0001),表明从鼻压信号中可以可靠地检测到EFL (补充图S4).
PN0.5) (r = 0.91;p<0.0001),表明从鼻压信号中可以可靠地检测到EFL (补充图S4).
非快速眼动睡眠中呼气流限制(EFL)的追踪实例。用气速计( )及鼻插管(
)及鼻插管( PN).鼻压也使用平方根变换(
PN).鼻压也使用平方根变换( PN0.5).在EFL期间,呼气气道正压在会厌水平形成(Pepi)呼气流量没有增加。粗虚线上面的顶部痕迹显示评分唤醒。
PN0.5).在EFL期间,呼气气道正压在会厌水平形成(Pepi)呼气流量没有增加。粗虚线上面的顶部痕迹显示评分唤醒。
EFL对英语语言交流的影响
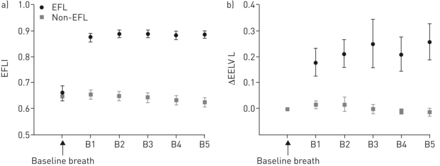
由于EFL可以引起呼气末正压,从而可能增加EELV,因此也研究了连续5次EFL呼吸中EELV的变化。EELV的变化(与基线呼吸相比)在所有五次EFL呼吸中显著增加了~ 200 mL (p<0.0001) (图6).这种EELV的增加是相当大的,可能会潜在地影响吸气力学。
呼气流量限制指数(EFLI)与呼气末肺容积(EELV)增加相关(校正胸腹感容积描记术),与呼气阻力增加和呼气流量减少一致。B1-B5:呼吸次数1-5。a)所有EFL呼吸EFLI >0.8,所有非EFL呼吸EFLI <0.7。b) ΔEELV EFL呼吸组明显大于非EFL呼吸组。EFLI由气速计流量计算。
讨论
本研究的主要结论是:1)EFL与呼气时软腭脱垂/膨胀进入鼻咽有关,2)呼气时腭脱垂的OSA患者更容易在吸气时出现(孤立的)腭下垂,3)呼气时腭脱垂产生的特征流型可由鼻压信号自动检测,具有较高的敏感性和特异性。这些结论是基于下列结果得出的。1)金标准EFL(咽压增加但呼气流量不增加)患者与腭脱垂相关的发生率为89%。2) 7例孤立性腭塌陷患者中6例的PP%(来自内镜)或EFLI >0.8 (EFL%,来自流型)为>25%。其他部位塌陷的15例患者中有14例PP%和EFL% <25%。3)内镜下腭脱垂病例采用EFLI鉴别,准确率为>95%。4)气垫测量EFLI与鼻压测量EFLI的相关性为>0.9 (p<0.0001)。
上颚在呼气和EFL时脱垂
尽管先前的研究报告了与呼气相关的梗阻[11- - - - - -14,25- - - - - -30.],这些研究主要是指由于呼气时咽压下降而导致的呼气狭窄[26,28- - - - - -30.].因此,据我们所知,这项研究首次证明了在一些病人呼气时,上颚/小舌脱垂或气球进入气道(图1而且2)导致呼气气流突然减少。这些情况与咽驱动压力的增加有关(如图所示图1在会厌水平形成呼气正压),因此呼气阻力高(>20 cmH)2O·s·L−1)的鼻部呼吸通路,在接受检查的呼吸中占89%。虽然年代tanescuet al。[11]报告了在非呼吸暂停严重打鼾者和OSA患者中存在耦合的吸气和EFL(持续或减少的流量与声门上压力的增加相关),但他们无法确定EFL背后的机制。在本研究中,我们证实腭脱垂是导致EFL的主要机制。年代阿法尔[31和S阿法尔和R德国艾迪[32)提出软腭的“阀状”行为可能是导致呼气阻塞的潜在机制。他们报告了肥胖麻醉患者在口鼻通气过程中出现的呼气阻塞,并假设这是由这种阀样行为引起的。最近,Satoet al。[16]还描述了软腭瓣膜样阻塞是睡眠呼吸障碍的麻醉患者在面罩通气时呼气阻塞的潜在机制。我们的结果证明,通过通过对软腭和小舌的直接观察,可以发现上颚在呼气时确实可以表现出瓣膜一样的行为。此外,我们已经证明,这种行为可以很容易地识别在常见的测量鼻压信号。
在一项实验研究中,Woodson[14]使用视频成像来检查在呼气期间,由于鼻持续气道正压(CPAP)突然下降,咽部结构是如何运动的。与我们的研究相反,他们没有观察到腭脱垂。然而,这可能是由于他们的实验范式与我们对睡眠中自然呼吸的研究存在差异。减少CPAP可能不会产生脱垂腭所需的力量。
腭脱垂检测的自动化
本研究还测试了一种从血流信号中识别腭脱垂的算法。提出了一个稳健指数(EFLI),并通过自然睡眠内窥镜(图4)和临床测量的鼻压(补充图S4).我们使用气测仪测量流量来建立指数。然而,由于该方法旨在作为一种临床工具,我们使用标准的鼻压信号来验证它。值得注意的是,EFLI不依赖于流量的绝对(校准)值,这有利于使用未校准的流量信号实现。此外,该指数为每次呼吸提供一个连续的规范化值。最终,我们设想通过报告EFLI >0.8睡眠时的呼吸比例(每个状态或每个体位)或与腭脱垂相关的被评分的阻塞性呼吸事件(睡眠不足)的比例来总结单个患者的呼吸水平数据。
EFLI的临床意义
我们的研究表明,部分OSA患者出现腭脱垂,并引起EFL。我们推测,这种现象可能是由于上颚拉长、小舌肿胀和/或多余的腭组织在气道中移动更自由。临床上,与脱垂相关的过度颤动和组织运动可独立促成觉醒。此外,通过口腔的气流分流可能导致转向嘴呼吸,这本身可能增加上呼吸道的折叠性[33](并降低对CPAP治疗的依从性[34])。最后,在某些情况下,腭在鼻咽中的位置可能为后续吸气时气道受损提供了先决条件[11].
有趣的是,当腭脱垂存在时,发现随后的吸气次数和潮气量往往减少。这是因为吸气时气道压力必须降到某一水平以下(如。−5而言不啻2O;补充图S3)以移开脱垂的上颚,重新打开气道。从我们的生理测量和内窥镜数据可以明显看出这一点(补充图S3).这一过程减少了吸气潮气量,并产生了“细呼吸”,在临床睡眠研究中,可被评为睡眠不足。此外,由于腭部脱垂导致的EELV增加本身可能会减少吸气流量,因为现在需要更多的负吸气压力来产生吸气流量。
腭脱垂引起的EELV变化也可能具有重要的临床意义。研究发现,在EFL期间,EELV平均增加200-250毫升。图6)可改善气道的通畅和塌陷,从而达到稳定的效果[35- - - - - -37].肺容量的增加也被证明能大大减少睡眠障碍性呼吸[38]和消除流量限制所需的CPAP水平[39]。此外,阿拥挤的城市et al。[24]之前在一位患有严重阻塞性睡眠呼吸暂停的37岁患者身上观察到自发性呼气阻力(在我们的研究中称为EFL)。他们报道了EELV与呼气正压(EPAP)之间的联系,并提示呼气阻力可以增加睡眠时的EELV通过EPAP的产生,可能在吸气时稳定上呼吸道[24].在这项研究中,我们发现腭下垂进入鼻咽导致这些时期的高呼气阻力和EPAP在会厌水平的积聚(图1而且5).因此,腭瓣失活导致非efl呼吸时会厌正压逆转(图1而且5).这种从EFL阶段到非EFL阶段的过渡可能是由于觉醒(图5)和/或提高EELV超过阈值(图1);然而,这需要进一步的研究。
这种先前被低估的咽塌模式,通过EFLI量化,可能预示着某种气道表型。需要进一步的研究来测试EFLI是否可以帮助识别对特定疗法(如悬雍垂腭咽成形术)有反应的患者[40,41],添加鼻呼气阻力疗法(Provent) [42], epap [12,13,下颌前进装置[43]、体位疗法[44,45]及上呼吸道刺激疗法[46,47].我们的结果显示,仰卧位比侧卧位腭脱垂更常见。我们推测EFLI较高的患者可能对下颌推进装置和上气道刺激反应较弱,原因如下。如果上颚在呼气时脱垂,它可能需要很大或拉长,并且必须与舌根分离(即。上颚和舌头之间的联系更少)。下颌骨的推进和上呼吸道的刺激,可能会使舌头向前移动,但在这类患者中,上颚向前移动的效果可能较差。
限制
这项研究有几个局限性。首先,由于研究的侵入性和在OSA患者自然睡眠时进行内窥镜检查的固有挑战,我们的样本量相对适中(n=22)。然而,检查的呼吸次数(1211次)足够大,不同的呼气流模式同样很好地代表。重要的是,阈值是从50%的数据(训练集)中获得的,并在未用于寻找阈值的剩余50%的数据(测试集)上进行验证。这确保了EFLI在检测呼气脱垂时的稳健性。第二个限制与选择呼吸以获得PP% (图3)作为吸气孤立性腭塌陷的指标。因此,需要进一步的研究来验证临床常规多导睡眠描记术中25%的临界值。第三个限制与内窥镜检查过程中大视频文件的存储有关。每录制1分钟,系统产生约1.1 GB的数据,这限制了我们整夜连续存储视频文件的能力。”尽管如此,我们在夜间平均记录每位受试者150±49分钟的内窥镜图像,以建立一个有代表性的不同部位塌陷/流动模式的库。此外,视频文件每隔5-10分钟存储在小文件中,以防止丢失帧和信号与视频之间的不同步。
补充材料
脚注
本文的补充资料可从www.qdcxjkg.com
利益冲突:s.a Sands报告了研究期间美国心脏协会(AHA)和国家卫生研究院(NIH)的资助,以及提交工作之外剑桥声音管理公司的个人咨询费。
利益冲突:L. Taranto-Montemurro报告了在进行研究期间NIH的拨款,AHA的拨款和Novion制药和Cambridge Sound Management的个人费用,在提交的工作之外。D.P.怀特报告了在提交的工作之外,从飞利浦呼吸设备公司(担任首席科学官)、Apnicure公司(担任首席医疗官)和NightBalance公司(担任顾问)支付的个人费用。
利益冲突:A. Wellman报告了NIH和Philips respiratory onics在进行研究期间的拨款,Varnum Sleep and Breathing Solutions和Cambridge Sound Management的拨款,以及提交工作之外的拜耳公司的个人费用;此外,a . Wellman还获得了气道和气流因子的专利。
支持声明:本研究在Brigham and Women’s Hospital进行,并得到了来自中国开封OMPA公司总裁范红兵的慈善资助,以及来自飞利浦呼吸系统公司和美国国立卫生研究院(R01HL102321, R01HL128658, P01HL095491, UL1RR025758)的研究资助。S.A. Sands得到了美国心脏协会(15SDG25890059)和美国胸科学会基金会的支持。L. Taranto-Montemurro得到了美国心脏协会(17POST33410436)的资助。M. Marques和P.R. Genta得到了Fundação de Amparo à Pesquisa do Estado de São Paulo (FAPESP)的支持。本文的资助信息已存入Crossref基金管理人登记处.
- 收到了2017年7月13日。
- 接受2017年11月29日。
- 版权所有©ERS 2018