摘要
我们评估了环丙沙星吸入性干粉(DPI)对非囊性纤维化支气管扩张、前一年有两次或两次以上加重和痰中有预先确定的细菌的患者的疗效和安全性。
在该第三阶段,双盲,安慰剂对照试验,患者随机2:1至两次的每日环丙沙星DPI 32.5mg或安慰剂,其两种治疗方案组成14或28天的ON / OFF治疗循环48周。主要终点是第一次加剧和加重频率的时间。
共有416例患者被随机分为14天开/关方案(环丙沙星DPI (n=137)和安慰剂(n=68)或28天开/关方案(环丙沙星DPI (n=141)和安慰剂(n=70)。环丙沙星DPI开/关14天明显延长至第一次加重时间与合并安慰剂(中位时间>336与186天;危险比0.53,97.5%CI 0.36-0.80;P = 0.0005),与匹配的安慰剂相比,减少了加剧的频率39%(均匀的加重0.6与1.0;发病率比0.61,97.5% CI 0.40-0.91;p = 0.0061)。环丙沙星DPI治疗28天的疗效与安慰剂无统计学差异。环丙沙星DPI的安全性较好。
环丙沙星DPI耐受性良好,有潜力成为一种有效的治疗非囊性纤维化支气管扩张症的选择。
摘要
在呼吸1中,14天循环使用环丙沙星吸入性干粉可减少支气管扩张加重http://ow.ly/po4s30gNfl0
介绍
支气管扩张症是一种慢性呼吸系统疾病,其特征是生活质量下降,并由气道感染和炎症引起反复发作[1,2].病情加重与症状负担增加有关;发病率和死亡率风险也随病情加重频率而增加[2].急性加重在慢性细菌感染患者中更为常见。铜绿假单胞菌尤其是死亡和住院的危险因素[2].非囊性纤维化支气管扩张症(NCFB)的主要治疗目标是减少病情加重和预防疾病进展[3.- - - - - -5,但目前还没有被批准用于这些目的的疗法。
环丙沙星吸入干粉(DPI)正在开发中,以减少具有重大疾病负担的NCFB患者的病情加重。这是一种抗生素药物装置组合,包括环丙沙星吸入粉末,使用PulmoSphere技术配制(诺华,San Carlos, CA, USA) [6],以及一个袖珍呼吸吸入器(补充图S1).CiProfloxacin DPI在NCFB患者的通风肺区达到高且可重复的药物沉积水平[7].传统上,28天周期方案用于囊性纤维化(CF),目的是最大化治疗效果,同时最小化耐药性,但这种治疗策略对NCFB的适用性尚不清楚。一项II期研究显示,在NCFB患者中应用环丙沙星DPI 32.5 mg,每日2次,持续28天,痰中总细菌负荷减少>3倍;最常见的病原体是铜绿假单胞菌,流感嗜血杆菌和金黄色葡萄球菌.值得注意的是,细菌负荷的最大减少发生在治疗早期(8±1天),并持续在治疗期间;在治疗停止后不久,细菌负荷增加,在治疗结束后2个月内几乎恢复到基线水平[8].这些发现提示较短的治疗周期,如14天的开/停,可能适合环丙沙星DPI治疗NCFB患者。
三氯氧氟沙星DPI的两阶段III呼吸试验的目的是评估延长时间14-和28天的效果和安全性14-和28天的CiProfloxacin DPI,并在第48周内降低NCFB患者的恶化频率[9].在这里,我们报告了第一项研究的结果,RESPIRE 1 (ClinicalTrials.gov标识符NCT01764841).
方法
研究设计和治疗
研究设计的详细资料已公布[9].简言之,RESPIRE 1是一项平行组、随机、双盲、国际、安慰剂对照试验。在该试验中,患者通过一项计算机随机计划,以2:1(环丙沙星DPI:安慰剂)的比例随机接受每日两次环丙沙星DPI 32.5 mg或安慰剂的间歇性方案。治疗周期为14天(12个周期)或28天(6个周期),共48周。末次给药后随访8周(图1).在活性治疗组和匹配的安慰剂之间进行比较(即。患者随机分为14天或28天服用/停用安慰剂与可比较的环丙沙星DPI方案)或合并安慰剂(所有患者都用安慰剂治疗与指定的环丙沙星DPI方案)取决于具体的结局(见终点部分)。合规评估通过每次就诊时收集研究药物包,并以治疗后的天数为基础。不循环或治疗中断,如。由于病情恶化,未纳入依从性计算。
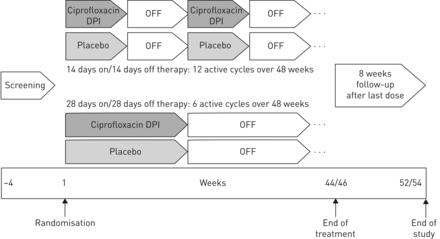
呼吸研究设计。DPI:吸入用干粉。
获得了所有适当的伦理批准和患者的书面知情同意。
研究人群
纳入初步诊断为NCFB(研究人员确定的特发性或感染后病原学)、经计算机断层扫描确诊、病情稳定(过去30天内无加重症状)的患者[9].关键的纳入标准是:在过去12个月里,在医疗记录中记录并经复查医疗记录确认的至少两次病情加重,以及在筛查至少一种预先指定的病原体时痰标本的培养呈阳性:铜绿假单胞菌,流感嗜血杆菌,莫拉克斯氏菌属复活,金黄色葡萄球菌,链球菌引起的肺炎,Stenotrophomonas maltophilia要么伯克不过.如果在筛查前至少使用6个月,则允许进行稳定的慢性大环内酯治疗。如果患者在给药前4周内接受了全身或吸入抗生素治疗,则排除在外。也排除了活动性变应性支气管肺曲霉病、活动性或积极治疗的非结核分枝杆菌肺部感染或筛查结核、临床医生初步诊断为慢性阻塞性肺病或有记录的慢性哮喘的患者。
终点
分级分析方法得到了监管当局的同意。美国食品和药物管理局(FDA)和欧洲药品管理局(EMA)/其他机构(补充图S2).主要终点为:1)开始环丙沙星DPI治疗后48周内第一次加重的时间与2)环丙沙星DPI在48周研究期间的加重频率与匹配的安慰剂(EMA /其他)。对于主要终点,加重需要满足三个标准:1)超过正常日常变化的至少三种症状或症状(呼吸困难、喘息、咳嗽、24小时痰量或痰脓)连续至少2天恶化,2)发烧(体温>38.0°C)或不适/疲劳,3)全身抗生素治疗(“主要终点定义”)。作为次要终点,评估了不太严格的加重定义(至少一种上述症状或症状恶化的呼吸事件和全身抗生素使用)。其他次要终点包括微生物学结果、生活质量评估和肺功能。的补充材料包括主要和次要端点的这些和预定义子组的详细信息(补充部分S1),以及安全终点,包括不良事件(补充部分S2).
分析
有关随机化过程及计算样本数目的详情,已于先前公布[9].Aksamitet al。[9[基于盲目数据中的较低数量的恶化事件,反映样本大小的调整。
主要疗效分析在全分析集进行,定义为所有随机化的患者(与打算治疗的人群相同)。对于从随机化到第一次急性加重的主要终点时间(定义为从随机化到第一次合格急性加重的时间),使用Cox比例风险模型检验环丙沙星DPI和混合安慰剂之间的差异。自变量为治疗组、地理区域、治疗前阳性文化铜绿假单胞菌以及慢性大环内酯类药物的使用。对于加重频率的主要终点,采用泊松回归模型调整过/过分散、上述自变量和研究时间作为补偿变量,分析48周内与匹配安慰剂相比的加重次数。
统计分析按预先定义的层次顺序进行(补充图S2)使用SAS版本9.2 (SAS Institute, Cary, NC, USA)。如果环丙沙星DPI的优越性假设不能被证实,那么所有后续的终点都是描述性的,而不管结果的p值。为了考虑两个积极治疗组(环丙沙星DPI 14和28天开/关)的多重检测,使用了Bonferroni调整,每个试验的α水平为0.025(双侧)。
结果
病人
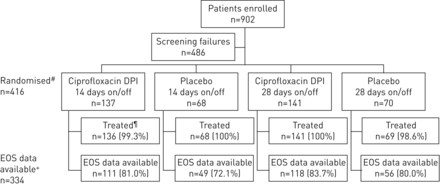
第一次患者访问于2013年5月,最后一次访问于2016年3月。416名患者随机分配,80.3%在学习结束(EOS)访问中提供数据(图2).随机化患者最多的国家是以色列(12.7%)、澳大利亚(12.5%)和新西兰(12.3%)(补充表S1).
耐心的性格。DPI:吸入用干粉;EOS:学习结束。#:随机按地理区域分层,治疗前阳性文化铜绿假单胞菌大环内酯类药物的长期使用;¶:患者随机接受至少一种治疗剂量;+:EOS数据的患者包括完成治疗和随后的后续的患者,或过早停止治疗,但遵循计划的EOS(52/54周),或过早停止治疗,但完成了计划的8周后的计划.
对患者的人口统计特征和基线特征进行了平衡(表1).大部分患者为女性(68.5%),平均年龄为~ 65岁铜绿假单胞菌基线(61%)(见补充表S2对于其他基线病原体)。基线药物使用率高,>80%的患者接受至少一种伴随呼吸药物(补充表S3).
超过70%的患者(416名患者中的297名)完成了治疗;早期停药的主要原因是不良事件或退出研究。治疗依从性很高(积极治疗组94%)(表2).
主要终端
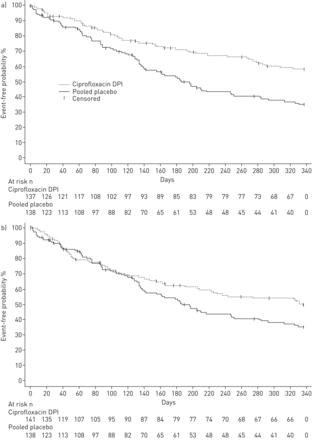
与联合安慰剂组相比,环丙沙星DPI 14天的开启/关闭时间在48周内显著延迟首次加重时间(风险比(HR) 0.53, 97.5% CI 0.36-0.80;p = 0.0005) (表3和图3一).对于CiProfloxacin DPI 14天的Ciprofloxacin DPI,第一种加剧的中值时间为> 336天(97.5%CI 290至> 336),ON / OFF和186天(97.5%CI 136-282)用于合并安慰剂。对于Ciphofloxacin DPI 28天ON / OFF,还可以看到延迟至首次加剧,但差异没有达到统计学意义与合并安慰剂(HR 0.73, 97.5% CI 0.50-1.07;p = 0.0650;第一次发作的中位时间为336天,97.5%置信区间206至>336与186天,97.5% CI 136-282) (表3和图3 b).
接受环丙沙星吸入性干粉(DPI)的患者第一次加重的时间a) 14天开/停或安慰剂b) 28天开/停或安慰剂。对于主要的终点,需要达到三个标准:1)在至少三个症状或症状(呼吸困难,喘息,咳嗽,24-h痰体积或痰脓)超出正常日常变异的标准中至少2天,2)发烧(体温> 38.0°C)或萎靡不振,3)全身抗生素治疗。
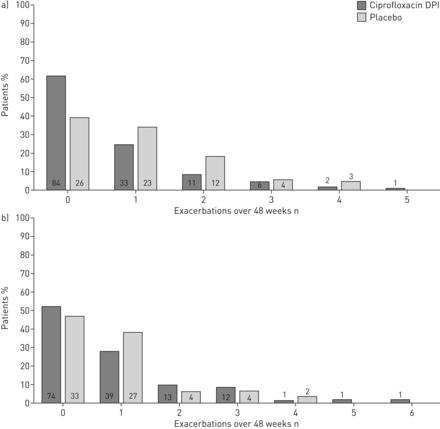
环丙沙星DPI 14天开/关显著降低了急性加重的频率与48周内匹配安慰剂39%(发病率比(IRR) 0.61, 97.5% CI 0.40-0.91;p = 0.0061) (表3和图4一).均值±sd环丙沙星DPI 48周内的加剧次数为14天开/关臂为0.6±1.0,与匹配安慰剂臂中的1.0±1.1相比。Ciphoxacin DPI 28天的治疗效果ON / OFF较低,与匹配安慰剂(表3和图4 b).均值±sd环丙沙星DPI组28天的急性加重次数为0.8±1.1,安慰剂组为0.8±1.0。
对于吸入的环丙沙星干粉(DPI)A)14天接通或匹配安慰剂和B)28天,接通或匹配安慰剂或匹配安慰剂或匹配安慰剂或匹配安慰剂或匹配安慰剂,或匹配安慰剂或匹配安慰剂的患者,为48周的频率。在酒吧内或上方的数字表示患者的数量。对于主要的终点,需要达到三个标准:1)在至少三个症状或症状(呼吸困难,喘息,咳嗽,24-h痰体积或痰脓)超出正常日常变异的标准中至少2天,2)发烧(体温> 38.0°C)或萎靡不振,3)全身抗生素治疗。
在48周中,61.3%的患者使用环丙沙星DPI治疗14天,而52.5%的患者使用环丙沙星DPI治疗28天,42.8%的安慰剂组患者在主要终点没有经历方案定义的加重。
亚组分析
对于两个主要终点,探索性分析显示,环丙沙星DPI在所有亚组中开启/关闭14天的治疗效果一致与安慰剂(补充图S3A).环丙沙星DPI 28天的开启/关闭也显示出类似但不那么明显的模式(补充图S3B.).在两个方案中,每个子组内的97.5%置信区间广泛重叠,表明关键预先指定的子组没有影响修改。
次要终点
在fda指定的分析中,根据主要终点定义,环丙沙星DPI 14天开/关差一点错过了第一个次要终点的加重频率(图5).相应的均值±sdCiprofloxacin DPI的加重次数为0.9±1.2,14天ON / OFF臂,1.2±1.3用于汇集安慰剂组。敏感性分析(对于由于未完成48周的研究的患者而言,在研究中为主要终点定义的加剧事件的数量,而不是完成48周的患者的偏移量,而不是事件数量的外推)表示正义名义CiProfloxacin DPI 14天开/关臂的显着效果(FRIS 0.6898,97.5%CI 0.4833-0.9845; P = 0.0193)。正如预期的那样,平均值±sd根据较不严格的定义,加重次数较高(环丙沙星DPI 14天开/关1.2±1.5与汇集安慰剂1.6±1.5)。
美国食品和药物管理局(FDA)和欧洲药品管理局(EMA)/其他机构对环丙沙星吸入干粉(DPI)的分级分析结果:a) 14天开/关,b) 28天开/关与混合安慰剂(PPL)或匹配安慰剂(MPL)。人力资源:风险比;IRR:发病率比;EOT:治疗结束;SGRQ:圣乔治呼吸问卷;生活质量- b相对过饱和度:支气管扩张症呼吸系统症状域评分;FEV1: 1秒内用力呼气量。#:急性加重的首要(严格)定义是符合三个独立标准的呼吸事件:1)超过正常日常变化的至少3个症状或症状恶化至少连续2天(呼吸困难、喘息、咳嗽、24小时痰量或痰脓),2)发烧(体温>38.0°C)或不适/疲劳,3)全身抗生素治疗;¶:较不严格的急性加重定义是至少有上述一种症状或体征恶化并全身使用抗生素的呼吸系统事件;+:铜绿假单胞菌,流感嗜血杆菌,莫拉克斯氏菌属复活,金黄色葡萄球菌,链球菌引起的肺炎,Stenotrophomonas maltophilia要么伯克不过(消除病原体被定义为ET的EOT在对象中的EOT中的负培养物导致,其具有至少一个预先指定病原体的正基线培养物中的所有预先指定的病原体;至少将新病原体的发生定义为阳性培养物在基线上没有针对该病原体的阳性培养的受试者中EOT的一个预先规定的病原体。实线与安慰剂在层次测试中有显着差异;虚线表示未达到统计学意义。所有终点的α水平为0.025,置信区间为97.5%。
由于分析的层次性质,这是确定的先验,未对FDA分析计划中的任何其他二级端点进行正式的确认意义测试。
对于EMA/others分析,环丙沙星DPI 14天开/关到达第一个次要终点(第一次加重的时间)(图5一个).第二个次要终点(根据不太严格的定义的加重频率)与主要终点一致,平均±显著降低sd按环丙沙星较不严格定义的加重次数DPI 14天开关(0.9±1.3)与匹配的安慰剂(1.4±1.3)。环丙沙星DPI 14天开/关也有统计学差异与对接下来的两个次要终点(EOT时消除预先规定的基线病原体)使用安慰剂与在圣乔治呼吸问卷(SGRQ)症状成分评分中,合并安慰剂和从基线到EOT的变化与合并的安慰剂)。
在FDA或EMA/其他指定的分析中,环丙沙星DPI 28天的开启/关闭没有达到主要终点的统计学意义,次要终点分析仅是描述性的;资料载于图5 b.
安全
环丙沙星DPI耐受性良好,不良事件和治疗紧急不良事件(包括药物相关和严重治疗紧急不良事件)的发生率在组间相似(表4和补充表S4).总的不良事件发生率为83%,治疗组之间总体不良事件发生率没有不平衡。治疗紧急呼吸系统不良事件,包括支气管痉挛,在治疗组之间具有可比性。两组因紧急治疗不良事件而停止治疗的情况相似(表4).
看到了一种肌腱炎(安慰剂组);没有报告的肌腱破裂病例。肌肉骨骼不良事件在环丙沙星DPI组中以数值较高的速率发生(约20%)与12%);这种差异主要是由于关节痛、背痛和骨关节炎的发病率较高。
报告的严重急诊不良事件大多与呼吸相关(补充表S4).在治疗紧急严重不良事件的类型和数量上,积极组和安慰剂组之间没有明显的差异。共报告了6例紧急治疗死亡病例(1例环丙沙星DPI 14天开/关组,2例环丙沙星DPI 28天开/关组,3例合并安慰剂组)(补充表S4).这些死亡都没有被认为与研究药物有关。
环丙沙星最小抑菌浓度的变化
在基线时,416名患者中有102名(24.5%)的病原体对环丙沙星的最低抑菌浓度(MIC)升高(根据系统性环丙沙星断点定义为耐药,具体见补充部分S2)从他们的痰中分离出来。与安慰剂相比,在研究期间,从治疗前到任何时间点,环丙沙星DPI患者中出现mic(全身间断点耐药)升高的病原体的患者数量更多(137例中有28例(20.4%),使用环丙沙星DPI的141人中有37人(26.2%),使用环丙沙星DPI的138人中有17人(12.3%),使用环丙沙星DPI的14天,使用环丙沙星DPI的28天,使用联合安慰剂。EOS访问,测试结束发生8周后,病原体与高架麦克风隔绝26例(6.3%)和易感病原体在基线(10 137(7.3%)、13 141名(9.2%)和138(2.2%)三个环丙沙星DPI 14天开/关,环丙沙星DPI 28天开/关和汇集安慰剂,分别)。在任何时间点(包括基线和根据全身环丙沙星断点定义的EOS),至少有一株痰液中MIC升高的患者比例,环丙沙星DPI开启/关闭14天的患者为54.0%,环丙沙星DPI开启/关闭28天的患者为53.9%与安慰剂组为36.2%。
讨论
RESPIRE是NCFB中最大的安慰剂对照、双盲III期试验项目,也是首个显示长期间歇吸入抗生素对NCFB患者有显著益处的项目。RESPIRE 1也是第一个研究14天和28天治疗周期的疗效的。CF治疗的常规周期为28天[10.],并曾在国家病毒署进行过研究,但成功有限[11.,12.].在RESPIRE计划中选择14天开/关作为治疗方案是受II期试验数据的指导[8].
环丙沙星DPI 14天开/停臂治疗在48周内首次发作的时间和发作频率上均有统计学意义的改善。亚组分析表明,该方案对具有一系列不同基线特征的患者有效,包括基线阳性或阴性的患者铜绿假单胞菌培养及有无大环内酯类药物慢性伴随使用者。然而,应该注意的是,亚组分析在本质上是探索性的,亚组的规模小限制了确定的结论。事后对治疗所需数量的计算确定了4.5名患者需要使用环丙沙星DPI治疗14天,以防止336天内的一次恶化。一些次要终点(EMA/others分析)在14天开/停臂治疗中也具有统计学意义,包括SGRQ症状成分评分测量的呼吸症状显著改善,考虑到支气管扩张患者的高症状负担,这一点值得注意[13.].
环丙沙星DPI 28天开/关组的观察结果支持环丙沙星DPI 14天开/关组的疗效,但未达到预定义的显著性水平。
患者入选标准的设计是为了尽量减少因疾病病因(如。不包括那些具有免疫缺陷障碍的人,积极或积极地治疗不泛滥的分枝杆菌感染,或活性过敏性支气管肺胰岛素,并用最有可能经历细菌恶化的患者富集人群。然而,研究期间的平均恶化的均值低于上一年的恶化数量(如据报道的学习招生)。已知参与临床试验以影响参与者行为[14.,患者可能会更加坚持物理治疗和辅助治疗,从而减少基线症状的波动,并可能减少研究期间恶化的数量。然而,在研究过程中并没有收集到辅助治疗和依从性的数据,因此我们无法证实这一假设。
CiProfloxacin DPI具有良好的安全性,并且耐受良好;> 70%的患者完成治疗。总体而言,治疗紧急的不良事件率,包括呼吸事件,跨治疗组通常低且可比。没有观察到严重的全身氟喹诺酮相关事件的增加。在该48周的研究中,潜在的全身副作用(如恶心或头痛)罕见地报道(总计5.3%的恶心和7.0%的头痛),可能反映了与环丙沙星DPI治疗相关的低系统浓度[15.].
随着MICS的增加是任何抗生素治疗的潜在缺点,研究了七种预定病原体的麦克风的变化。使用长期吸入抗生素在慢性感染中预期通过选择具有抗性基因的细菌来增加抗微生物抗性。然而,使用吸入疗法的系统断点是有问题的,并且它们不太可能准确地适用于这种处理场景,因为在痰中达到的浓度大大超过计算的MICS [15.,16.].然而,根据全身性突变点,>组中20%的患者的MICs在基线时升高至环丙沙星,这可能反映了该患者群体中先前抗生素使用的沉重负担与频繁恶化相关[17.].亚组分析未显示基线病原体、MICs高于全身断点的患者疗效降低。虽然>50%的环丙沙星dpi治疗的患者在研究期间的任何时间点至少有一种MIC升高的分离物,但在EOS中,基线时具有易感病原体的患者的这一比例下降到<10% (与安慰剂组为2%),这与NCFB患者吸入性抗生素试验的meta分析报告的耐药率相似[18.].MIC的增加可能被细菌负荷的净减少和总体临床效益所抵消,包括恶化和抗生素的减少。还需要进行更多的研究,以监测长期使用环丙沙星DPI期间的环丙沙星耐药性,并确定吸入治疗的相关耐药断点。
我们承认这项研究有局限性。临床实践中恶化的不同定义,一个专家小组最近讨论的主题[19.,可能影响了患者参加这项试验的资格。目前对病情加重的定义存在相当大的异质性[19.]因此,较前一年中的恶化的可能性可能在中心之间变化。与此相关,用于确定审判资格的加剧的定义依赖于临床判断而不是特定标准,因此与用于主要终点的临床判断不那么严谨。占据了这些因素,所有这些因素都可能导致低于预期的初始审判率恶化。在这一经验的基础上,我们鼓励未来试验的调查人员利用严格的定义,以获得作为入境标准的加剧。然而,这种方法的潜在缺点是在已经有限的人口中进一步减少了审判入学。
另一个方法上的限制是计算机断层扫描不是集中验证的,中心之间的差异可能影响对疾病严重程度的评估或导致对放射学结果的过高估计与入选标准。在研究设计时,用于评估NCFB严重程度的有效预后指标尚未发表[2,20.],本试验收集的数据不包括计算严重程度评分所需的完整信息,包括放射严重程度。因此,治疗对疾病严重程度组的影响无法确定。未来的研究可能受益于针对具有更高恶化风险的患者群体。在临床试验中,严重性评估工具的作用还有待确定。衡量与健康相关的生活质量变化的最合适方法,特别是在使用试验性药物的临床试验中,也是不确定的。尽管RESPIRE 1包括了SGRQ和生活质量-支气管扩张指标,但这些指标是基于不同的回忆期,长期循环治疗数据收集的最佳时间点尚不清楚。
最后,积极组和安慰剂组的随机比例为2:1,虽然积极组和安慰剂组对患者有吸引力,因为积极治疗的可能性更高,但这意味着较小的安慰剂组更容易受到方差的影响,这可能会影响环丙沙星DPI和匹配的安慰剂组之间的分析结果。
总之,呼吸1试验表明,用环丙沙星DPI治疗减少了NCFB患者的恶化,施用频繁的加剧和痰液中存在的病原体。在/关闭治疗14天内看到统计学上显着的改进,而28天接通/脱离治疗则看到改善趋势。治疗良好耐受。与其他长期抗生素治疗的其他研究一致,看到麦克斯的增加。我们的研究结果表明,具有环丙沙星DPI的长期间歇性吸入抗生素治疗可以在选定的NCFB患者中提供治疗益处。
补充材料
披露的信息
补充材料
t . Aksamiterj - 02052 - 2017 - _aksamit
T-J。知识ERJ-02052-2017_BANDEL.
A. de Soyza.erj - 02052 - 2017 - _de_soyza
J.S.elERJ-02052-2017_LBORN.
大肠Operschallerj - 02052 - 2017 - _operschall
大肠Polverinoerj - 02052 - 2017 - _polverino
r·威尔逊erj - 02052 - 2017 - _wilson
K.L.温斯洛普erj - 02052 - 2017 - _winthrop
确认
我们感谢病人,研究人员(见S3补充部分)以及助长呼吸的研究中心。我们还感谢Ulrike Krahn(Bayer Ag,Wuppertal,Germany),协助统计分析,杰夫艾尔(拜耳美国LLC,Whippany,NJ,USA)用于微生物学数据评估和批评数据,Maxine Lau(Bayer AG,德国)为药物检修投入以及Fusion MD(蒙特利尔,加拿大)和Highfield:Communication(牛津,英国),为拜耳AG提供资金的医疗写作服务。A. de Soyza,R. Wilson和J.s.Elborn承认支持Embarc和医学研究委员会资助的Bronch-UK在支气管扩张的同行支持和建议中协作。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:本研究得到拜耳公司的支持。本文的资金信息已存入Crossref资助者注册表.
本研究注册于ClinicalTrials.gov与标识符NCT01764841.
利益冲突:可以在本文旁边找到披露www.qdcxjkg.com
- 收到了2017年10月6日。
- 接受2017年11月20日。
- 版权©2018人队