摘要
本II期随机、双盲、多中心研究(NCT00930982)研究了环丙沙星吸入干粉(DPI)治疗非囊性纤维化支气管扩张的安全性和有效性。
预先定义的潜在呼吸道病原体培养阳性的成年人(包括铜绿假单胞菌而且流感嗜血杆菌)被随机分配到环丙沙星DPI 32.5 mg组或安慰剂组,每天两次,持续28天(随访56天)。在整个研究过程中监测痰中细菌密度(主要终点)、肺功能检查、健康相关生活质量和安全性。
60名受试者接受环丙沙星DPI 32.5 mg, 64名接受安慰剂。接受环丙沙星DPI治疗的受试者在治疗结束时痰中总细菌载量显著降低(p<0.001) (-3.62 log10CFU·g−1(范围-9.78-5.02 log . log10CFU·g−1))与安慰剂相比(-0.27 log10CFU·g−1(范围-7.96-5.25 log . log10CFU·g−1));此后计数增加了。在环丙沙星DPI组中,40名受试者中有14人(35%)在治疗结束时报告病原体根除与49名安慰剂组中有4名(8%)(p=0.001)。无异常安全结果报告,支气管痉挛发生率低。
环丙沙星DPI 32.5 mg,每日两次,持续28天,耐受性良好,与安慰剂相比,非囊性纤维化支气管扩张患者的总细菌负荷显著降低。
非囊性纤维化(CF)支气管扩张是一种严重影响患者健康相关生活质量(HRQoL)的慢性和使人衰弱的呼吸系统疾病。该病的特征是异常和不可逆的支气管扩张,并与呼吸道阻塞、气体转移不良和慢性支气管感染导致的发病率和死亡率增加有关[1- - - - - -3.].高达64%的支气管扩张患者是慢性致病菌感染,最常见流感嗜血杆菌而且铜绿假单胞菌[3.].这些感染破坏宿主的防御系统和呼吸道上皮细胞,并可导致感染和炎症的恶性循环,伴随持续症状、频繁急性加重和疾病进展[4].主要的治疗挑战之一是慢性气道感染的临床管理,因为常见的抗生素耐药性(特别是口服抗菌药),系统施用抗菌药的常见副作用和对吸入抗菌药的不耐受(支气管痉挛)。这些问题使得非cf性支气管扩张成为一种难以治疗的疾病,目前还没有批准的抗菌疗法用于长期治疗[3.- - - - - -6].
非cf性支气管扩张的超适应症治疗包括全身和雾化抗菌剂、口服和吸入溶粘液剂、高渗剂、支气管扩张剂和痰清技术[7,8].然而,这些治疗方法不能充分控制患者可能经历的病情加重次数,在某些情况下,其益处尚未得到充分调查。目前的欧洲指南指出,缺乏足够的证据支持它们用于治疗支气管扩张的恶化[9].有必要开发新的治疗方法,有效地治疗潜在的慢性感染,从而减少支气管化脓和恶化的次数,并防止疾病进展。
环丙沙星是一种广谱抗菌药物,已被证明对非cf性支气管扩张相关病原体具有杀菌活性,包括铜绿假单胞菌[10].环丙沙星已使用PulmoSphere™技术(诺华制药公司,瑞士巴塞尔)配制成吸入用干粉(DPI),与小型便携式呼吸驱动T-326吸入器一起使用[11].利用PulmoSphere技术控制活性药物的颗粒大小和密度,可使药物最佳地输送到中央和下气道。在健康志愿者和CF和慢性阻塞性肺病患者中进行的临床试验结果表明,环丙沙星DPI耐受性良好,药代动力学反映了有效的肺靶向和低系统性暴露[12- - - - - -14].
除了呼吸功能的测量外,评估健康状况的技术越来越多地被评估,并已在非cf支气管扩张患者中得到验证。其中包括圣乔治呼吸问卷(SGRQ),这是一份自行完成的问卷,旨在测量慢性气流受限患者的HRQoL [15,16].此外,疲劳影响量表已被用于衡量疲劳与疾病严重程度标志物之间的相关性[17].
本研究的目的是评估环丙沙星DPI治疗28天的安全性和有效性,随访56天,通过检查细菌载量和其他重要临床结果的变化,以及耐受性,对非cf性支气管扩张患者进行治疗。
材料与方法
研究对象
年龄≥18岁的成年受试者符合纳入研究的条件:经高分辨率计算机断层扫描证实为特发性或感染后非cf支气管扩张(排除其他病因的调查记录);有急性加重史(在过去12个月内,两次或两次以上全身性抗菌药物治疗或一次或多次因肺加重而静脉注射抗菌治疗);肺部状态稳定,定义为症状稳定,在过去30天内不需要新的治疗干预;进入研究前病情稳定≥30天;如果他们能够产生一份≥5 mL的治疗前痰样本,该样本对预先定义的潜在呼吸道病原体培养呈阳性(铜绿假单胞菌(粘液或非粘液),金黄色葡萄球菌,链球菌引起的肺炎,流感嗜血杆菌,莫拉克斯氏菌属复活肠杆菌科,Stenotrophomonas maltophilia而且无色菌xylosoxidans).进一步的细节包含在在线补充材料中。
研究排除标准包括:活动性非结核分枝杆菌感染、近期明显咯血(前4周内需要临床干预的量)以及在随机分组前4周内使用雾化抗菌药物作为维持治疗,或使用全身抗菌药物治疗急性发作。长期服用抗菌药物的受试者可以停药1个月后再进入研究。为了符合临床实践,允许慢性大环内酯类药物作为支气管扩张的稳定抗炎维持治疗,但前提是在随机分组前至少30天开始治疗。
有恶化或其他指征需要使用抗生素的受试者停止研究。
本研究的进行符合所有当地法律法规要求,并符合《赫尔辛基宣言》的伦理原则和国际协调会议准则E6:良好临床实践。所有受试者均提供书面知情同意书。
研究设计
这是一项多中心、随机、安慰剂对照、双盲研究(注册于www.clinicaltrials.gov标识符编号NCT00930982).入组的受试者接受环丙沙星DPI 32.5 mg(相当于50 mg干粉)或匹配的安慰剂b.i.d。这是一种T-326吸入器(诺华)。受试者在第1天前21天接受了筛查,并接受了28天的治疗,在治疗结束时(EOT)以及第42、56和84天(图1).研究治疗在标准维持治疗后进行。
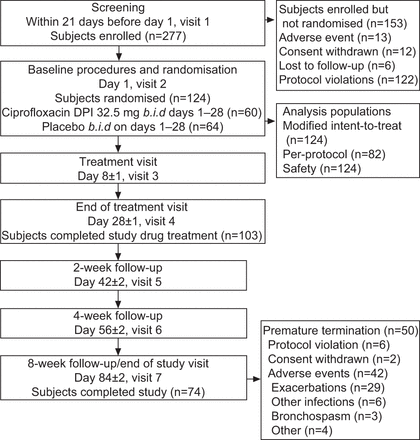
研究设计与受试者配置。筛查失败的方案违反包括未培养阳性菌(n=23)、痰量不足(n=50)、1 s外用力呼气量(n=6)、筛查过程中病情加重(n=2)、使用抗菌药物(n=6)、无进一步信息(n=25)和其他(n=10)。DPI:吸入用干粉。
在首次治疗前第1天、首次治疗后30±10分钟、第8天、29天、42天、56天和84天以及过早停止研究时进行肺功能测试。在每次研究访问中,在治疗开始前和过早停止研究时采集用于培养和药敏测试的自发痰样本。此外,受试者在第1天、第8天、第29天、第42天、第56天和第84天的前一天采集了24小时的痰样本。
受试者在第1天、第29天、第56天和第84天以及过早停止研究时完成了患者报告的HRQoL测量,即SGRQ。
从筛查开始到第84天或直到提前终止研究,每次来访均监测体检和实验室检查结果异常的发生率以及不良事件(AEs)的发生。明显的支气管痉挛(定义为绝对用力呼气量(FEV)下降≥15%1)),局部刺激和咳嗽是特别有趣的ae,因为吸入治疗。在第1天、第8天、第29天和第84天以及过早停止研究时测量生命体征参数(血压和脉搏率)。
临时的分析
在EOT评估的~ 70名受试者达到主要终点后,计划进行中期分析。独立的数据监测委员会建议继续进行这项研究。进一步的细节包含在在线补充材料中。
研究终端
主要疗效终点是确定环丙沙星DPI对痰中预先定义的潜在呼吸道病原体总细菌密度的影响,通过测量对数的减少1028天治疗期后每克痰cfu,并比较改良意向治疗(mITT)人群(定义在在线补充材料中)中环丙沙星DPI和安慰剂之间的差异。
次要终点包括病情恶化的时间、新的潜在呼吸道病原体的出现、基线病原体耐药性的出现、炎症生物标志物的变化以及24小时痰量和颜色的变化。肺功能(FEV)基线变化1在第29、56和84天,除AEs和体检、生命体征和实验室分析结果外,还评估了用力肺活量(FVC))和健康状况(SGRQ)。研究定义的“根除”是基线培养阳性受试者(所有受试者)的有效基线后痰样本中细菌无法生长。在筛选、随机化、第8天(治疗期间)、EOT以及EOT后14、28和56天采集样本。在研究提前终止时也采集了样本。
统计分析
两组人群被考虑进行疗效分析:mITT和per-protocol(在在线补充材料人群中定义)。主要分析对mITT人群和方案人群进行,采用双向ANCOVA方法,以基线细菌负荷为协变量,包括治疗组和研究中心,比较环丙沙星DPI和安慰剂在EOT时总细菌负荷的变化。
用颜色表分析痰液颜色和量的变化,用频率表分析24 h痰液量。首席研究员向调查人员提供了粘液、黄色、绿色和棕色痰的照片。FEV的变化1采用双向ANCOVA分析,基线值为协变量,因素包括治疗组和研究中心。肺功能参数(FEV1和植被覆盖度(FVC)作为绝对原始值和预测的%进行描述性统计分析。
安全分析集(在在线补充材料中定义)用于所有安全评估。研究治疗开始后和EOT后7天内发生的不良事件被归类为治疗紧急事件或现有不良事件的恶化。实验室变量、生命体征和其他安全数据通过汇总统计进行描述(在在线补充材料中定义)。
样本量估计在在线补充资料中有描述。
结果
研究人群
从2009年6月29日到2010年9月17日,在6个国家(澳大利亚、德国、西班牙、瑞典、英国和美国)的35个中心,总共对277名受试者进行了筛查,124名受试者被随机分配到治疗组(103名完成治疗,74名完成研究)。在随机受试者中,60人接受环丙沙星DPI 32.5 mgb.i.d。64人接受安慰剂b.i.d。(图1).大多数在随机分组前停用痰液的受试者提供的痰液样本不足(即.一个无法培养出预先定义的病原体的样本)。所有随机分组的受试者被纳入安全组和mITT组,82名受试者(环丙沙星DPI组和安慰剂组分别为37名和45名)被纳入方案组。尽管有大量的受试者被排除在方案人群之外(主要是因为受试者不产生痰而无法进行EOT培养),但mITT和方案人群的疗效分析结果是相似的。这里给出了所有端点的mITT数据,以及主要端点的每个协议结果。每个方案的其余结果在在线补充材料中给出。
两个治疗组的人口学特征和基线特征相似(表1).环丙沙星DPI与安慰剂在任何基线特征上均无显著差异。年龄、性别和种族特征与接受筛查但非随机分组的患者相似。
功效
治疗依从性和持续时间
治疗依从性(通过计算使用/未使用胶囊和使用/未使用设备的数量来衡量)在两个治疗组中都很高;环丙沙星DPI组97%的受试者依从性≥80%,安慰剂组94%的受试者依从性≥80%。两组平均治疗时间为26天。
主要终点
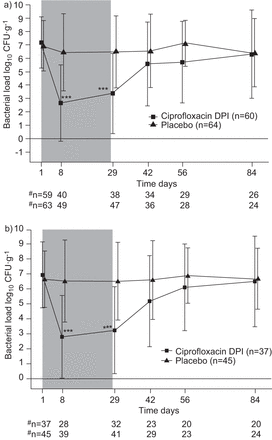
环丙沙星DPI组治疗期间和EOT时CFU计数的平均减少显著增加(-3.62 log10CFU·g−1,范围-9.78-5.02 log10CFU·g−1)与安慰剂组(-0.27 log10CFU·g−1,范围为-7.96-5.25 log10CFU·g−1;p < 0.001) (图2一个).环丙沙星DPI组与安慰剂组相比,在第42天和56天观察到CFU计数无显著降低,然后在第84天再次加入。在方案分析中,与安慰剂组相比,环丙沙星DPI组在治疗期间和EOT时CFU计数的平均降低模式相似(p<0.001) (图2 b).所选病原体在基线和EOT时的平均菌落计数显示在图3.
a)改良意向治疗人群和b)每个方案人群的平均细菌负荷。只考虑有效培养的结果。如果有>25鳞状上皮细胞而无铜绿假单胞菌或者有≤25个白细胞铜绿假单胞菌-阴性培养治疗前。DPI:吸入用干粉。阴影区域表示治疗时间(天)。#:痰培养有效的患者数。* * *: p < 0.001。

所选病原体在基线和治疗结束时的平均菌落计数。只考虑有效培养的结果。如果有>25鳞状上皮细胞而无铜绿假单胞菌或者有≤25个白细胞铜绿假单胞菌-阴性培养治疗前。DPI:吸入用干粉;EOT:治疗结束。
二次端点
在整个研究过程中,环丙沙星DPI组(60名受试者中有22名(36.7%))报告至少一次病情加重的受试者比安慰剂组(64名受试者中有25名(39.1%);危险比估计0.802,95%可信区间0.443-1.454;p = 0.605)。每个时间段需要干预的新发急性加重的受试者数量列于图4.其中,环丙沙星DPI组有14名受试者需要抗菌治疗干预,包括2名需要住院,而安慰剂组有18名受试者需要抗菌治疗,包括5名需要住院(风险比估计为0.674,95% CI 0.324-1.402;P =0.338(分层对数秩检验,按中心分层,小中心合并)。根据研究方案,所有需要抗菌治疗的患者均应停止治疗;然而,其中三名受试者(环丙沙星DPI组两名,安慰剂组一名)完成了研究。关于这三个主题的进一步信息载于在线补充材料。前42天内需要抗菌治疗的病情加重次数(治疗28天,随访14天;这段时间可能受抗菌治疗影响最大)环丙沙星DPI组为7例,安慰剂组为12例。需要干预的受试者的恶化率铜绿假单胞菌两组在基线时相似(环丙沙星DPI组为23.5%,安慰剂组为27.8%与环丙沙星DPI组为23.1%,安慰剂组为25.0%)。在线补充材料中提供了恶化的概述。
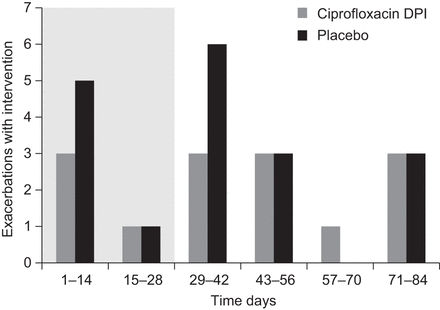
在整个研究过程中,需要抗菌药物干预的病情恶化的发生情况(修改意向治疗人群)。环丙沙星DPI组的22名受试者和安慰剂组的25名受试者经历了加重。其中,环丙沙星DPI组的14名受试者和安慰剂组的18名受试者需要抗菌治疗。DPI:吸入用干粉。阴影区域表示治疗时间(天)。
根除(细菌培养阴性;仅考虑有效培养的结果)在环丙沙星DPI组42名受试者中观察到20名(48%),而在第8天,安慰剂组51名受试者中观察到6名(12%)(p<0.001),在EOT时,环丙沙星DPI组40名受试者中观察到14名(35%),安慰剂组49名受试者中观察到4名(8%)(p=0.001) (表2).接受环丙沙星DPI治疗的受试者在治疗期间出现新的潜在呼吸道病原体的频率低于安慰剂组(分别为12和24名受试者)。基线后分离出的新病原体与基线时分离出的新病原体的频率相似(表1),除了美国maltophilia与基线后的17名受试者(10名环丙沙星DPI组,7名安慰剂组)相比,5名受试者在基线时(2名环丙沙星DPI组,3名安慰剂组)中分离出来。
两组患者EOT恢复的总痰量均低于基线时;环丙沙星DPI组和安慰剂组较基线的平均百分比变化分别为-17.7%和-9.6%。与安慰剂组相比,环丙沙星DPI组在EOT和4周随访时痰颜色清晰的受试者更多(表3).
对FEV无明显影响1或FVC在环丙沙星DPI组或安慰剂组。均值±sdFEV变化1从基线到EOT,环丙沙星DPI组改善0.06±8.36%,安慰剂组恶化-0.40±10.06%。
环丙沙星DPI组与EOT组之间的平均高敏c反应蛋白值降低,但安慰剂组升高(-1.09 mg·L)−1与4.02 mg·L−1分别;p = 0.173)。与安慰剂相比,环丙沙星DPI在EOT时显著降低,表明治疗对绝对中性粒细胞计数的影响(-0.36×10)6细胞·毫升−1与0.60×106细胞·毫升−1分别;p = 0.014)。
最低抑菌浓度(MIC)增加到>4 mg·L−1(被定义为与环丙沙星系统治疗临床相关的水平),被认为可能或可能与研究药物的管理有关,直到研究结束,环丙沙星DPI组的6名受试者报告了以下病原体,而安慰剂组的受试者没有报告:铜绿假单胞菌(n = 4),美国maltophilia(n = 1)流感嗜血杆菌(n = 1)。在这些受试者中,有一位提前终止了研究,有四位在研究结束时MIC下降到易感水平。一个有粘液的实验对象铜绿假单胞菌耐受性在第30天达到峰值(MIC 64 mg·L)−1),降低至4 mg·L−1(第44天和第63天)和8 mg·L−1第92天。安慰剂组的一名受试者经历了短暂的MIC增加美国maltophilia从1 mg·L−1至4 mg·L−1.
EOT时,环丙沙星DPI组和安慰剂组受试者SGRQ评分较基线的平均变化分别为-2.52分和+0.38分,表明环丙沙星DPI组有所改善。环丙沙星DPI组与安慰剂组校正后SGRQ评分的平均差异为-3.56 (95% CI -7.3-0.1;p = 0.059);对基线SGRQ和研究中心进行了调整。在应答者分析中发现了类似的趋势:40%的接受环丙沙星DPI的受试者和32%的接受安慰剂的受试者报告EOT评分提高了4分以上。
安全
治疗突发事件、药物相关事件和严重事件的摘要在表4.在这段时间内,没有死亡发生,也没有严重的不良事件被认为与研究治疗有关。该研究的中止总结在图1.
在整个研究过程中(直到第84天),环丙沙星DPI组的22名受试者(3名受试者过早停止治疗)和安慰剂组的26名受试者(6名过早停止治疗)报告了至少一次支气管扩张加重的AE。其中,环丙沙星DPI组17名受试者报告的18起事件和安慰剂组13名受试者报告的14起事件被归类为“晚期事件”,在EOT后7天发生>。在每个治疗组中,由于ae而过早终止研究的受试者数量相似:环丙沙星DPI组和安慰剂组分别为19名(31.7%)受试者和23名(35.9%)受试者。
环丙沙星DPI组和安慰剂组特别感兴趣的ae包括支气管痉挛(分别为60例中的3例和64例中的3例;每组2例发生在治疗期间,被认为与治疗有关)。研究者报告的支气管痉挛ae(共6例)均不符合该研究对支气管痉挛的特定定义。报告了治疗引发的咳嗽(0 / 60和5 / 64受试者,分别)和咯血(1 / 60和2 / 64受试者,分别)。
两组实验参数均无显著变化。环丙沙星引起的肝功能或血清肌酐变化均未检测到。
讨论
相对较少的随机临床试验专门针对非cf型支气管扩张患者进行。定期、长期雾化庆大霉素对非cf型支气管扩张患者有显著疗效;然而,需要持续治疗以确保持续疗效[18].在3个月的随访中,结果指标与基线相似[18].需要有强有力证据支持的新疗法。
本研究旨在纳入慢性感染相关病原体的受试者,其支气管扩张的严重程度足以考虑使用吸入抗生素进行治疗。我们纳入了感染后和特发性支气管扩张的非cf受试者,他们占所有非cf支气管扩张病例的70%至80% [19,20.].我们排除了对治疗反应可能受复杂因素影响的病因,例如,原发性睫状体运动障碍引起的粘液清除不良、过敏性炎症和免疫缺陷。招募需要相对大量的研究中心,但尽管可能引入了任何变异,但结果是结论性的,而且主要分析中治疗和中心之间的相互作用项不显著(p=0.214)。
目前的研究结果首次显示,在非cf型支气管扩张中,与安慰剂相比,环丙沙星DPI在治疗28天后产生了具有统计学意义的总细菌负荷降低。细菌数量减少3倍以上,相当于细菌负荷减少99.9%。此外,接受环丙沙星DPI的受试者在EOT时细菌培养阴性的比例高于接受安慰剂的受试者。非cf型支气管扩张中最常见的两种病原体菌落数量减少,铜绿假单胞菌而且流感嗜血杆菌以环丙沙星DPI治疗观察。虽然该研究没有证明报告病情恶化的受试者数量有显著差异,但观察到环丙沙星DPI倾向于环丙沙星,这表明它可能是治疗这类患者的有效药物。肺部细菌负荷的减少应减少气道炎症和病情加重的风险,这是由痰脓毒性减少的观察所支持的。既往数据支持痰液颜色与支气管炎症之间的相关性[21].因此,本研究的结果显示了一种对支气管扩张的病理生理学有临床意义的影响的新模式。
目前可用或正在开发的雾化抗菌药最常见的给药间隔是28天的治疗周期,随后28天的治疗周期。在EOT和研究结束之间,观察到细菌负荷迅速恢复到接近基线值。然而,在第56天,也就是在这一建议的循环方案中恢复治疗时,细菌负担仍然明显减少。细菌负荷迅速下降然后反弹与环丙沙星DPI对加重模式的明显影响一致,即。在研究的前42天内,相对于安慰剂的抑制作用和随后的发病率变得相似。
使用该方案(28天治疗/28天治疗)的一个重要理由是尽量减少抗生素耐药性的发展。病原体接触抗菌剂后会产生耐药性;28天的停止治疗期消除了抗菌药物的选择压力,使病原体的易感性恢复到治疗前的水平[22,23].本研究观察到MIC变化所表明的潜在耐药性发展:来自环丙沙星DPI组的6名受试者的分离物经EOT后MIC增加,其中4名受试者的分离物随后在56天时MIC下降。
除了临床疗效参数的改善外,EOT时SGRQ观察到接受环丙沙星DPI的受试者报告的健康状况的改善趋势,尽管治疗时间很短。这接近于临床相关的改善(SGRQ -4.0点;较低的分数代表较高的HRQoL) [24].在第56天也观察到了这种趋势,但在研究结束时没有观察到,这表明任何报告的健康状况的好处都是暂时的。
环丙沙星DPI 32.5 mgb.i.d。能很好地忍受;观察到的AE在呼吸系统疾病患者中很常见,最常报告的AE是病情加重[25,26].实验室参数未观察到显著变化,药物相关ae发生率较低,环丙沙星DPI组与安慰剂组之间无显著差异。在整个治疗期间,与非cf性支气管扩张相关的ae的发生率很低,包括支气管痉挛、咳嗽和咯血。
在感染后或特发性非cf性支气管扩张患者中,与安慰剂相比,环丙沙星DPI 32.5 mg显著降低了细菌负荷,其疾病情况和严重程度值得考虑吸入抗生素治疗。环丙沙星DPI耐受良好b.i.d。28天。环丙沙星DPI在次要临床和生活质量相关终点观察到的改善无统计学意义。因此,需要进一步的研究来评估长期间歇环丙沙星DPI治疗的临床效果。
致谢
所有分析均由研究发起人进行,数据审查委员会负责验证所有临床失败数据。作者还要感谢D. Bilton(英国伦敦皇家布朗普顿医院)和G. Tino(宾夕法尼亚大学医院,PA,美国)在盲法中期分析方面的工作,L. Zhou(第三方统计学家;Axio Research西雅图,华盛顿特区,美国)和F. Woodward(变色龙通信国际,伦敦,英国),他们在拜耳制药公司的资助下提供医学写作服务。作者要感谢各招聘中心的主要调查员:John Armstrong(亚历山德拉公主医院,布里斯班),Michael Chia(伯恩赛德战争纪念医院,图拉克花园,阿德莱德),Harvey Newnham(阿尔弗雷德医院,墨尔本),Fergal O'Donoghue(奥斯汀医院,海德堡,墨尔本),Matthew Peters(康科德归国总医院,悉尼康科德),David Serisier (Mater卫生服务,南布里斯班),Philip Thompson(查尔斯Gairdner爵士医院,内德兰,珀斯);德国:Helgo Magnussen (Pneumologisches Forschungsinstitut GmbH am Krankenhaus Großhansdorf, Großhansdorf), Stephanie Korn (Universitätsmedizin der Johann Gutenberg Universität Mainz, Mainz), Gerd Stähler (Klinik Löwenstein dGmbH, Löwenstein), Andreas Eich (Interdisziplinäres Facharztzentrum Sachsenhausen (IFS), Infektiologikum,法兰克福),Olaf Burkhardt (Zentralklinik Bad Berka, Bad Berka), Lutz Volgmann (Pneumologische Praxis Hannover Nordstadt, Hannover), Karlheinz Franz (Lungenpraxis Witten),Witten), Axel Kroker (Pneumologische Schwerpunktpraxis Kroker, Schaeben, Schmidt, Koblenz), Ekkehard Beck (IFG研究所für Gesundheitsförderung GmbH, Rüdersdorf), Andrés De Roux (Pneumologische Praxis am Schloß Charlottenburg,柏林),Petra Mikloweit (Pneumologisches Forschungsinstitut Hohegeest GbR, Geesthacht), Lutz von Versen (Praxis Walter Meier,柏林),Thomas Schultz (MECS GmbH,柏林);西班牙:Marcelino Salgueiro Rodriguez和Rosario Arias(圣地亚哥大学医院,圣地亚哥德孔波斯特拉),Pilar Cordero(巴达霍兹因塔克里斯蒂娜大学医院),Jaume Sauleda Roig(帕尔马德马略卡岛的儿子杜雷塔大学医院);瑞典:安妮卡·霍辛(乌普萨拉CF中心,乌普萨拉); UK: Joseph Elborn (Belfast City Hospital, Belfast), Charles Haworth (Papworth Hospital, Cambridge), Nabil Jarad (Bristol Royal Infirmary Hospital, Bristol), Paul Walker (University Hospital Aintree, Liverpool), Andrew Wilson (Norfolk and Norwich University Hospital, Norwich); and USA: Tala’at Al-Shuquairat (Central Utah Clinic, Provo, UT), Mark Metersky (University of Connecticut, Farmington, CT), Varsha Taskar (University of Texas Health, Tyler, TX), Angela Wang (Scripps Clinical Medical Group, La Jolla, CA), Jonathan Ilowite (Winthrop University Hospital, Mineola, NY), Jose Marquina (Pulmonary, Critical Care and Sleep Medicine, Naples, FL), Gwen Huitt (National Jewish Health, Denver, CO) and Ikeadi Ndukwu (La Porte County Institute for Clinical Research, Inc., Michigan City, IN).
脚注
这篇文章有补充资料可从www.www.qdcxjkg.com
支持声明
这项研究由德国拜耳制药公司赞助。R. Wilson和A. De Soyza感谢国家卫生研究所(NIHR)基础设施以NIHR生物医学研究单元资助(英国伦敦皇家布朗普顿医院)和综合地方研究网络资助(英国其他中心)的形式提供的支持。
临床试验
这项研究注册在www.clinicaltrials.gov标识符编号NCT00930982.
权益声明书
利益冲突信息可以在本文的在线版本中找到www.www.qdcxjkg.com
本文于2016年4月修改,以更正许可证信息中的错误。
- 收到了2012年5月4日。
- 接受2012年9月15日。
- ©2013人队
ERJ开放文章是开放获取的,并根据(188滚球软件创作共用署名非商业性许可协议3.0)