摘要
青少年的哮喘控制通常不理想,但很少有研究评估这一人群的哮喘治疗方法。
这事后分析评估了布地奈德/福莫特罗(BUD/FORM)维持和缓解治疗(MART)在6个随机双盲试验中治疗青少年(12-17岁)持续性哮喘的有效性和安全性。主要终点为首次严重加重的时间。次要终点包括严重加重次数、哮喘相关症状、夜间觉醒次数、早高峰呼气流量、1 s内用力呼气量、按需用药和哮喘控制问卷五项评分。
在青少年(n=1847)中,BUD/FORM MART在降低首次严重加重的风险(危险比(HR) BUD/FORM MART)方面与每项研究的比较项相似或更有效与比较器0.15 - -1.01;合并HR 0.49, 95% CI 0.34-0.70),与成人亚组结果相当(n= 12197)。在次要终点观察到BUD/FORM MART的治疗效果相似。BUD/FORM MART的按需用药低于比较组,青少年的BUD/FORM按需用药低于成人。治疗耐受性良好。
该分析支持在患有持续性哮喘的青少年中使用BUD/FORM MART,其疗效和安全性与成人报告一致。
摘要
BUD/FORM MART在患有持续性哮喘的青少年中的疗效/安全性与在成人中的报道一致http://ow.ly/UYLv30fGDPF
简介
青春期是身体、情感、认知和生活环境快速变化的时期。这些变化为这一年龄组的哮喘治疗带来了独特的挑战,因此,青少年哮喘患者是一个独特的患者群体[1].在青少年中,哮喘控制通常不理想,发病率很高[2- - - - - -5),以及坚持定期吸入治疗(这是所有年龄组的潜在问题[6,7)可能特别贫穷[5,8].尽管如此,很少有研究评估治疗在这一特定人群中的疗效。
全球哮喘倡议(GINA)指南提出了循序渐进的哮喘管理方法,建议成年人和青少年在步骤3-5时选择吸入皮质类固醇(ICS)/福莫特罗(FORM)组合的维持和缓解治疗(MART) [1].布地奈德/福莫特罗(BUD/FORM) MART提供低日常维持剂量的联合治疗,并根据需要额外吸入。与固定剂量维持治疗加单独的缓解药物治疗相比,使用BUD/FORM MART可确保缓解药物使用的任何增加与ICS的增加相匹配,确保当症状增加时针对炎症[9].在针对≥12岁哮喘患者的双盲随机对照试验中,与ICS/长效β相比,BUD/FORM MART显著降低了严重发作2-激动剂(LABA)维持(或高剂量ICS)加短效β2-激动剂(SABA)用于持续性哮喘患者,同时达到至少类似水平的哮喘控制[10- - - - - -15].
目前,已发表的数据有限,评估ICS/LABA方案特别适用于青少年。这事后进行了个体患者水平的分析,以评估BUD/FORM MART在青少年(12-17岁)中的有效性和安全性,这些青少年被纳入随机双盲对照试验,评估该方案治疗持续性哮喘。
方法
数据来源和研究选择
符合纳入条件的研究是在持续时间≥6个月、年龄在12-18岁的持续性哮喘患者中,将BUD/FORM MART与主动比较器进行比较的任何随机双盲试验。本个体患者水平的分析是针对制造商(阿斯利康)提交给欧洲药品管理局的Symbicort MART (SMART)的监管档案进行的,目的是将该方案在欧洲的许可适应症扩大到包括≥12岁的患者。因此,分析的数据来源是阿斯利康临床试验数据库,包括截至2015年11月完成的研究。
为了确定是否有符合纳入标准的非阿斯利康试验,对PubMed数据库和Cochrane数据库进行了单独搜索(在线补充资料).
阿斯利康临床试验数据库中确定了7项符合标准的研究:SD-039-0667 (STEAM) [10], sd-039-0668 (step) [11], sd-039-0673 (stay) [12, sd-039-0734(微笑)[13], sd-039-0735(罗盘)[14),NCT00242775(提前)15),NCT00839800(樱花)16].其中,六项被纳入分析:NCT00839800由于该研究仅随机选取了21名年龄≥16岁的青少年,因此被排除在外。从PubMed和Cochrane数据库的搜索中没有发现其他研究。
个别研究设计
每项研究的详细方法和结果已于以前发表[10- - - - - -15].所有研究均包括年龄≥12岁、诊断为持续性哮喘的患者(欧洲呼吸学会/美国胸科学会定义[188bet官网地址17]), 6个月,尽管在研究期间每天使用ICS,但仍有症状。五项研究要求患者在前一年有一次或多次哮喘发作[10,11,13- - - - - -15].个别研究的入学标准概述于在线补充表S1.其中一项研究包括儿童(年龄4至11岁)[12],但不包括在这里提出的分析。
每项研究都包括2周的磨合期,在此期间患者接受常规ICS剂量[11,12,14,15], BUD/FORM (Symbicort;阿斯利康,瑞典哥德堡)160/4.5 μg,每日2次[13]或BUD 200 μg·日-1[10]作为控制药物。被认为没有很好地控制磨合药物的患者(标准见在线补充表S1),然后随机接受BUD/FORM MART或常规固定剂量维持治疗加额外缓解治疗(表1).比较者:BUD (Pulmicort;阿斯利康),FORM (Oxis;阿斯利康(AstraZeneca)和特布他林(Bricanyl;阿斯利康)通过与用于BUD/FORM的涡轮桨相同的设备;氟替卡松加沙美特罗/ fluticasone (Seretide;葛兰素史克(GlaxoSmithKline, Brentford, UK)进行管理通过Evohaler [14]或Diskus [15].三项研究的治疗时间为6个月[10,14,15]和12个月的剩余试验[11- - - - - -13].
所有研究均按照赫尔辛基宣言和良好临床实践指南进行,并获得独立的伦理委员会批准。所有患者和青少年的父母或监护人都获得了书面同意。
数据提取和端点
个体患者水平的数据来自阿斯利康临床试验数据库。
该分析的主要疗效终点为首次严重加重的时间,定义为需要口服皮质类固醇(OCS)≥3天[13- - - - - -15]和/或因哮喘恶化而住院/急诊室治疗(在线补充资料).之所以选择第一次严重加重的时间,是因为这是六项研究中五项的主要终点[11- - - - - -15];一项研究[10]招募了一个疾病相对较轻的人群,因此将呼气峰值流量(PEF)作为主要终点。
次要疗效终点包括严重加重总次数、哮喘相关症状改变、夜间觉醒次数、早晨PEF、1 s用力呼气量(FEV)1)、按需用药的使用情况和哮喘控制问卷(ACQ-5)五项评分(仅在三项研究中测量[13- - - - - -15])。哮喘症状总评分基于患者的日记记录,每天完成两次,给出白天和晚上的评分,每个评分为0 - 3(0:无症状,3:妨碍正常活动或睡眠),每日总评分为0 - 6。这一终点最初不是分析的一部分,但在初步临床回顾后取代了白天哮喘症状评分,因为人们认为夜间哮喘症状负担只能通过夜间觉醒来部分体现。
通过不良事件的类型和发生率来评估安全性。
统计方法
所有统计分析均使用SAS软件(版本9.4;SAS研究所,卡里,北卡罗来纳州,美国)。
研究内亚组分析
在每项研究中对青少年(12-17岁)亚组进行统计分析。在每项研究中,对成人(≥18岁)亚组进行了额外的分析,以评估在青少年中观察到的效果是否与在成人中一致。由于青少年亚组中的患者/事件数量相对较少,预计在个别研究的青少年亚组分析中,将没有足够的证据显示治疗组之间的统计学显著差异。同样,考虑到预期的低功率,没有进行比较青少年和成人亚组之间治疗效果的统计交互试验。除非另有说明,所有的统计分析都是预先规定的,并且在可能的情况下与原始研究中的计划一致。由于在青少年亚组中患者/事件的数量通常较少,调整或分层对国家的影响并不总是合适的。成人子集以与青少年子集相同的方式进行分析,以确保可比性。所有假设检验均采用双侧替代假设进行;p值<5%被认为有统计学意义,多次试验无校正。
完整的分析集[18]用于所有疗效分析,即。所有随机分组的青少年和成年患者,随机分组后的数据。使用Cox回归分析主要终点,即到首次严重加重的时间。使用泊松回归分析严重加重的总次数,并以研究时间的自然对数作为偏移量,并包括离散度参数。用于支气管扩张剂前FEV1和ACQ-5,使用线性回归分析随机访视与所有剩余随访平均值之间的变化,并对随机访视值进行调整。采用线性回归分析哮喘症状总评分、夜间觉醒百分比、按需吸入次数和早晨PEF,并与磨合期平均值(即。随机化前10天以上的平均值)和治疗期间的平均值(不包括随机化当天)作为结果变量,并根据磨合期平均值进行调整。
个体患者数据亚组元分析
除了预先指定的研究内分析,个别患者的数据被汇集在各个研究和一个整体的“BUD/FORM”中与比较者”的估计值分别为成人和青少年。这些汇总或“元”个体患者数据分析使用了之前为每个终点概述的相同方法,除了在可能的情况下对研究和国家进行了调整。第一次严重加重的时间分析包括研究作为分层变量,国家作为协变量。对于严重恶化的总数,研究被作为协变量纳入,但由于收敛问题,不可能包括国家。其余的汇总分析包括研究和国家作为协变量。
考虑到研究之间的差异,应谨慎解释合并治疗估计。通过在每个合并亚组分析模型中添加一个研究-治疗相互作用项,并使用似然比检验比较相关模型,进行了各研究亚组内治疗效果异质性的正式统计检验[19].
资金来源的作用
阿斯利康(该研究的赞助公司)为此制定了分析计划事后分析,并资助和执行分析。该手稿由作者在阿斯利康(AstraZeneca)资助下,在一位医学作家的协助下完成。
结果
病人
来自6项研究的1847名青少年被随机分配到BUD/FORM MART (n=694);BUD加特布他林(225例);BUD/FORM加特布他林(n=441);BUD/FORM + FORM (n=115);或沙美特罗/氟替卡松加特布他林(n=372)。青少年人口的人口统计及基线特征载于表2(关于成年人口统计数据(n= 12197),见联机补充表S2).在每项研究中,与病史和严重程度相关的基线特征在各个治疗组中通常得到很好的平衡。在基线参数的研究中观察到的差异反映了招募的患者平均哮喘严重程度的差异。
功效
主要终点
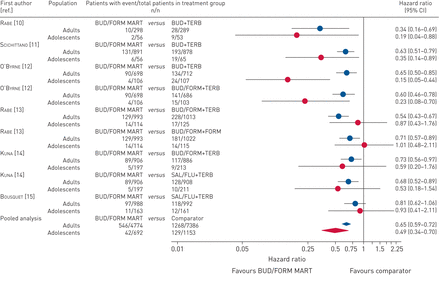
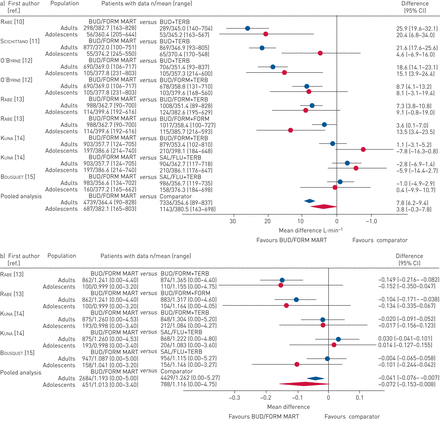
对于第一次严重加重的主要终点时间,BUD/FORM MART在青少年人群中与比较者相似或更有效(图1) [10- - - - - -15].6项研究中有5项在数值上有利于BUD/FORM MART的所有治疗比较的危险比(HRs)(范围从0.15到0.93)[10- - - - - -12,14,15],其余研究(HR 1.01)中BUD/FORM MART和比较器(BUD/FORM + FORM视需要)的结果相似[13].
森林图治疗时间与第一次严重加重比较。不同研究的剂量不同(表1).从以治疗为因素的Cox回归模型中获得的估计值。合并分析:通过研究分层的Cox模型,布地奈德/福莫特罗(BUD/FORM)与以非bud /FORM作为治疗变量,以国家作为协变量。异质性p值0.1995(成人)和0.0435(青少年)。MART:维持和缓解疗法;TERB:特布他林;萨尔/流感:氟替卡松加沙美特罗/ fluticasone。
在汇总分析中,发现在青少年人群中,BUD/FORM MART组严重加重的风险低于比较组(HR 0.49, 95% CI 0.34-0.70) (图1).然而,在合并估计中存在统计学上显著的异质性(似然比检验,p=0.04) (图1).
对于第一次严重加重的时间,在个体研究和汇总分析中观察到的青少年人群的结果与在成人人群中观察到的结果一致。
二次端点
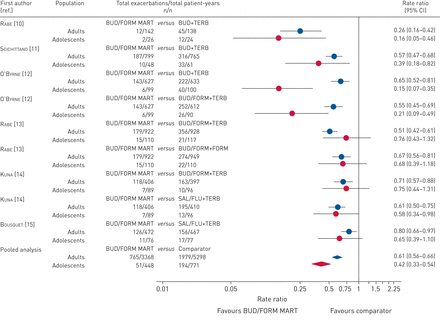
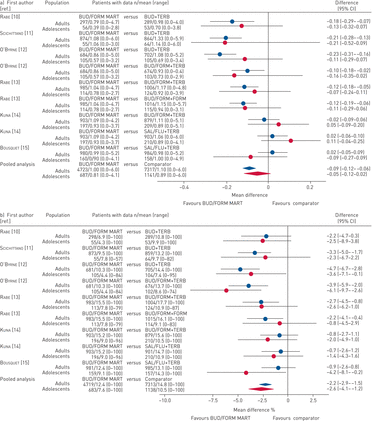
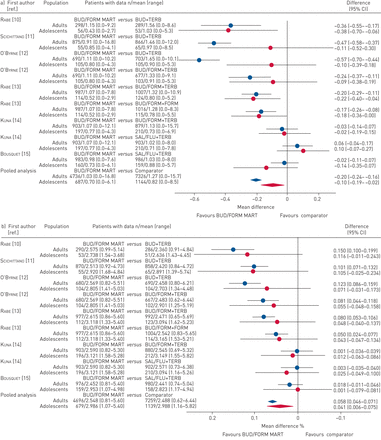
次要终点的森林图,包括严重加重总次数、哮喘症状评分、夜间觉醒次数、按需吸入次数、FEV1,早晨PEF和ACQ-5分数表示为图2,3.,4而且5.所示为所需吸入量的箱形图图6.在青少年亚组中,在六项研究中的五项中,对所有次要终点的评分都倾向于BUD/FORM MART与比较器(10- - - - - -13,15].此外,对于这些次要终点,汇总估计有利于BUD/FORM MART,尽管许多分析显示出统计学上显著的异质性(图2- - - - - -5).对于这些次要疗效终点,在个体研究和汇总分析中观察到的青少年人群的结果与在成人人群中观察到的结果一致。
严重加重的森林图(次要终点)。不同研究的剂量不同(表1).从泊松回归模型中获得的估计值,将处理作为一个因素,记录时间作为一个偏移变量,并对过度分散进行了调整。合并分析:布地奈德/福莫特罗泊松回归模型(BUD/FORM)与not-BUD/FORM作为治疗变量,以研究作为协变量,log time作为偏移量,并对过度分散进行调整。异质性p值0.012(成人)和0.0262(青少年)。
次要终点森林图a)哮喘症状评分;B)夜间醒来。不同研究的剂量不同(表1).使用ANCOVA,以磨合期平均值和治疗期平均值之间的变化为结果变量,治疗为一个因素,并对磨合期平均值进行调整。合并分析:布地奈德/福莫特罗的ANCOVA模型(BUD/FORM)与以not-BUD/FORM为处理变量,调整磨合期平均值,并以研究和国家为协变量。异质性p-值a) <0.0001(成人)和0.2172(青少年);B) 0.038(成人)和0.5193(青少年)。MART:维持和缓解疗法;TERB:特布他林;萨尔/流感:氟替卡松加沙美特罗/ fluticasone。
次要终点森林图a)按需吸入;B)用力呼气量1秒。不同研究的剂量不同(表1).使用ANCOVA,以磨合期平均值和治疗期平均值之间的变化为结果变量,治疗为一个因素,并对磨合期平均值进行调整。合并分析:布地奈德/福莫特罗的ANCOVA模型(BUD/FORM)与以not-BUD/FORM为处理变量,调整磨合期均值,并以研究和国家为协变量。异质性p-值a) <0.0001(成人)和0.1311(青少年);B) <0.0001(成人)和0.6051(青少年)。MART:维持和缓解疗法;TERB:特布他林;萨尔/流感:氟替卡松加沙美特罗/ fluticasone。
次要终点森林图a)呼气流量晨峰;B) 5项哮喘控制问卷评分。不同研究的剂量不同(表1).使用ANCOVA,以磨合期平均值和治疗期平均值之间的变化为结果变量,治疗为一个因素,并对磨合期平均值进行调整。合并分析:布地奈德/福莫特罗的ANCOVA模型(BUD/FORM)与not-BUD/FORM作为治疗变量,调整a)磨合期平均值和b)随机访问值,并以研究和国家为协变量。异质性p-值a) <0.0001(成人)和0.0026(青少年);B) 0.003(成人)和0.2383(青少年)。MART:维持和缓解疗法;TERB:特布他林;萨尔/流感:氟替卡松加沙美特罗/ fluticasone。
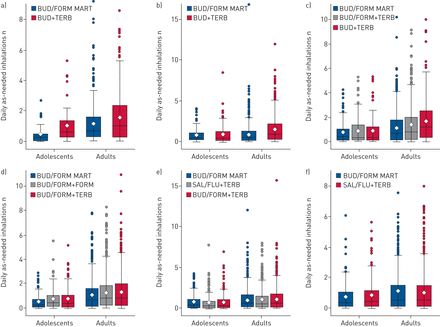
青少年和成人按需吸入的平均数量的箱形图。一)R安倍et al。[10];b)年代cichittanoet al。[11];c) O”Byrneet al。[12];d) R安倍et al。[13];e) Kunaet al。[14];B e)ousquetet al。[15].平均值用一个空心的菱形表示,中间值用每个盒子内的一条水平线表示。方框的底部和顶部分别代表第25和第75百分位。异常值用圆表示,定义为超出上四分位数加上1.5倍四分位数间范围的观测值。晶须延伸到最极端的非离值。芽/形式:布地奈德/ formoterol;MART:维持和缓解疗法;TERB:特布他林;萨尔/流感:氟替卡松加沙美特罗/ fluticasone。
与对照组相比,接受BUD/FORM MART治疗的青少年患者较少需要OCS治疗严重急性发作,尽管数量较少(联机补充表S3).在青少年中,BUD/FORM MART组的平均按需吸入使用量普遍低于比较组(图3 c和5),BUD/FORM MART的平均按需使用量在各项研究中始终低于成人(平均值范围为0.43 ~ 0.85)与0.91−1.15吸入/天;图5).在青少年中,在≥1天内使用12次BUD/FORM的患者较少(范围0.9-7.3%),只有1例患者使用>10天(14天)。
ICS使用
在四项研究中,BUD/FORM MART组的平均每日ICS剂量低于比较组(联机补充表S4和图S1) [10,11,14,15].BUD/FORM MART的ICS日剂量较高与SD-039-0673研究中需要的BUD/FORM加特布他林[12]和SD-039-0734研究中的两个比较器组[13]符合研究设计的预期。
安全
接受BUD/FORM MART治疗的青少年与接受比较治疗的青少年不良事件发生率和不良事件类型相似(联机补充表S5和S6).青少年经历严重不良事件或因不良事件而停止治疗的比例非常低,在治疗比较中相似(联机补充表S5和S6).
所有治疗都有良好的耐受性,在使用BUD/FORM MART或比较组的青少年中,没有报告有致命结局的不良事件。
讨论
尽管有有效的治疗方法,但无论年龄大小,哮喘患者仍会周期性恶化,并可能进一步恶化为严重恶化,需要进行医疗干预。哮喘是儿童和青少年中最常见的慢性疾病之一,但由于哮喘在患者生命的这些时期变化很大,因此特别难以控制,儿童和青少年哮喘发病率仍然高得令人无法接受[20.].本分析评估了来自双盲随机对照试验的全部证据,这些试验关于BUD/FORM MART在患有持续性哮喘的青少年中的临床疗效和安全性,这是一个很少被研究的年龄组。在包括1847名青少年的六项双盲研究中[10- - - - - -15],在临床观察和患者报告的结果中,我们发现BUD/FORM MART比固定大剂量ICS方案(BUD)更有效,与ICS/LABA比较维持方案(BUD/FORM和沙美特罗/氟替卡松)相当或更有效。在青少年中观察到的疗效和安全性与在成人中观察到的基本一致。这种一致性在临床研究中和整个临床研究中都很明显,并且与选择的比较治疗和使用的BUD/FORM维持剂量无关。
在本分析的青少年人群中,在所有6项双盲研究中,点估计倾向于BUD/FORM MART用于严重急性加重的次数,其中5项用于首次严重急性加重的主要终点时间。次要终点的结果支持主要终点的结果。尽管在所有临床试验设计允许进行比较的研究中,随机分组到BUD/FORM MART的青少年使用了较低的按需剂量,并且接受了较低的ICS平均日剂量,但这些结果还是取得了。由于之前已经提出了关于青少年是否可能过度使用BUD/FORM MART的担忧(考虑到SABA的过度使用在该年龄组中很高),该患者组的按需使用量低于成年人的发现是令人鼓舞的。
在目前的分析中,BUD/FORM MART在青少年亚组中观察到的安全性与该方案之前的文献报道一致[10- - - - - -15].BUD/FORM MART对青少年患者具有良好的耐受性,ics相关不良事件的频率非常低,即使在那些大量按需使用的患者中(在线补充表S6).在青少年人群中没有发现死亡报告,也没有发现系统性不良事件风险增加或新的安全问题。
根据需要使用BUD/FORM来应对恶化的症状,可以管理潜在的气道炎症,以防止或减少恶化(作为“抗炎缓解剂”),这是BUD/FORM MART概念的重要组成部分。ICS是哮喘管理的主要手段,已被证明可降低与哮喘相关的发病率[5].然而,不坚持常规ICS治疗可能与哮喘不受控制和加重风险增加有关[21,22].在青少年时期,患者对常规哮喘维持治疗的依从性往往会下降[5,23],因为患者开始对自己的哮喘护理承担更多责任,并获得更大的独立性。有人认为,该人群的依从性部分取决于药物的感知益处和感知不良事件的总体平衡[4,5,8].因此,治疗方案应根据青少年哮喘患者的需要、生活方式和心理社会状况进行调整[1].使用单一的BUD/FORM吸入器进行维持和缓解可能有助于克服对常规维持治疗的不良依从性,确保患者在需要额外剂量以缓解症状时接受ICS,并因FORM而经历快速发作的支气管扩张。
本分析的数据来源是阿斯利康临床研究数据库,允许访问个别患者的数据。为了检查是否有其他非阿斯利康赞助的研究可以考虑,我们对文献进行了回顾,寻找评估ICS和任何速效支气管扩张剂在单一吸入器中的组合用于维持和必要的缓解青少年持续性哮喘症状的随机对照试验。文献检索确定了本分析中包括的6项研究,并发现没有其他研究符合本分析的纳入标准;因此,我们认为目前的分析反映了撰写本文时的全部数据。
这种分析受到一些限制。尽管有大量的青少年进行评估,但每项研究中的青少年数量相对较低,因此分析不足以证明每项研究中的青少年治疗效果的证据。这在估计治疗效果的广泛置信区间中很明显。虽然六项研究的汇总数据产生了更窄的置信区间,但应谨慎对待汇总估计,因为所包括的研究具有不同的设计、比较器和剂量,而且许多正式的汇总估计异质性统计检验表明,跨研究对一个亚组的单个汇总估计是有问题的。对试验中基线疾病特征数据的评估表明,青少年人群的哮喘严重程度可能略低于成人人群,这可能部分促成了观察到青少年亚组中按需使用较低的BUD/FORM。另一个可能的限制是,平均每日ICS剂量的计算是基于规定的维持剂量,假设完全符合规定(以及在BUD/FORM MART的情况下,在电子日记中记录的所需吸入次数)。
本分析中纳入的比较方案反映了每项研究进行时的哮喘治疗指南(2001-2006年);然而,所有的治疗方案仍然是现行GINA指南中步骤3-5的治疗方案,因此仍然是适当的比较对象[1].
青少年持续哮喘的管理尤其具有挑战性;坚持定期维持治疗通常很差,哮喘控制一般不理想,发病率高得不可接受。先前纳入年龄≥12岁患者的随机对照试验表明,与ICS/LABA维持(或高剂量ICS)加SABA相比,在持续性哮喘患者中,BUD/FORM作为维持和缓解治疗均可显著降低严重恶化的风险,同时实现至少相似的哮喘控制水平和较低的长期类固醇负荷。这事后分析表明,BUD/FORM MART在这些试验的青少年亚组中的疗效(包括严重急性发作的减少)和安全性与成人和整个研究人群的报告一致。与比较组相比,青少年的平均按需用药水平较低,青少年的BUD/FORM按需用药水平较低。这些发现支持在患有持续性哮喘的青少年中使用BUD/FORM MART,并且考虑到治疗这一年龄组的挑战,具有特殊的临床意义。
补充材料
披露的信息
补充材料
h . Bisgaarderj - 01688 - 2017 - _bisgaard
c . Joruperj - 01688 - 2017 - _jorup
d . Lythgoeerj - 01688 - 2017 - _lythgoe
确认
该手稿由作者在阿斯利康(AstraZeneca)资助下,在一位医学作家的协助下完成。医学写作协助由Claire Mwape和Katharine Williams (in science Communications,施普林格Healthcare, Chester, UK)提供,遵循良好出版实践(GPP3)准则(www.ismpp.org/gpp3).
作者贡献:所有作者均参与了数据解读、构思、撰写和修改稿件。D. Lythgoe负责统计分析。所有作者都可以完全访问分析中的所有数据,H. Bisgaard(通讯作者)对提交发表的决定负有最终责任。所有作者都阅读并批准了最终的手稿。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
支持声明:阿斯利康(该研究的赞助公司)为此制定了分析计划事后分析,并资助并实施了分析。本文的资助信息已存入交叉参考基金注册.
利益冲突:可以在本文旁边的网站上找到信息披露www.qdcxjkg.com
- 收到了2017年8月18日。
- 接受2017年9月30日。
- 版权所有©ERS 2018