摘要
哮喘是一种与氧化应激相关的疾病,但在成人中与哮喘预后的相关性研究很少。我们旨在研究几种与氧化应激和各种哮喘结果相关的生物标志物之间的关系。
来自哮喘遗传和环境流行病学研究(EGEA2)的1388名成年人(平均年龄43岁,44%患有哮喘)进行了横断面分析。测量了三种血液抗氧化酶活性(氧化应激反应的生物标志物)和呼出冷凝物8-异前列腺素和血浆荧光氧化产物(FlOPs)水平(损伤的两种生物标志物)。生物标记物与哮喘患者(1)曾经哮喘和(2)哮喘发作、哮喘控制和肺功能之间的关系,使用经年龄、性别和吸烟调整的回归模型进行评估。
反应的生物标志物与哮喘结局无关。较高的8-异前列腺素水平与既往哮喘显著相关(一个四分位范围的优势比增加1.28 (95% CI 1.06-1.67)。在哮喘患者中,8-异前列腺素水平与成人发作哮喘呈负相关(0.63,0.41-0.97),FlOPs水平与哮喘发作(1.33,1.07-1.65)、哮喘控制不良(1.30,1.02-1.66)和肺功能不良(1.34,1.04-1.74)呈正相关。
我们的研究结果表明,8-异前列腺素与儿童期哮喘有关,而FlOPs与哮喘的表达有关。
摘要
氧化应激相关的损伤似乎与哮喘的表达和控制有关http://ow.ly/VSxG30fGNuz
介绍
哮喘是一种慢性气道炎症性疾病,全世界约有3.5亿人受到影响[1]。这种异质性疾病[2,3.]目前已在细胞和分子水平上进行研究,为其预防和控制提供了新的机会[4,5]。氧化应激反映了暴露于活性氧(ROS)和抗氧化防御之间的不平衡,参与了哮喘的病理生理机制[6]。在哮喘中,ROS是通过代谢反应内源性产生的[7,8]和外源性环境因素(如。空气污染物与吸烟)[8,9]。
为了中和ROS的过量产生,机体通过酶系统发展抗氧化防御,包括超氧化物歧化酶(SOD)与过氧化氢酶和谷胱甘肽过氧化物酶(GPX)偶联[10,11]。这些抗氧化酶是对抗ROS的第一道防线,是氧化应激反应中感兴趣的生物标志物[8]。此外,ROS与细胞膜上的脂质,特别是花生四烯酸相互作用,释放出脂质过氧化的最终产物8-异前列烷[12]。然而,关于反应的生物标志物(SOD、GPX和过氧化氢酶)之间的关系的研究很少[13- - - - - -16]或损伤的生物标志物(8-异前列腺素)[6,12和哮喘特征,特别是在成年人,他们的结果是不一致的。
荧光氧化产物(FlOPs)是氧化过程的全球生物标志物,包括蛋白质和DNA氧化以及脂质过氧化[17],他们对流行病学越来越感兴趣。这种损伤的生物标志物已被发现与慢性疾病有关[18]如冠心病[19]和慢性肾脏疾病[17]。然而,据我们所知,还没有研究评估FlOPs和哮喘之间的关系。
利用哮喘遗传和环境流行病学研究(EGEA)中>1000名成年人的广泛生物学和表型特征,我们旨在调查从不同生物区室测量的与氧化应激相关的反应和损伤的生物标志物与哮喘结果之间的关联。
方法
人群与研究设计
EGEA是一项法国队列研究,在20年里进行了三次调查。第一次EGEA调查(EGEA1)包括20世纪90年代初在法国五个城市招募的5个胸科诊所的哮喘患者、他们的一级亲属和基于人群的对照(n=2047)。2003-2007年完成了对参与者的随访(EGEA2),包括1601名完成完整检查的受试者,几乎全部为成年人。在每次调查中,所有受试者都回答了一份基于国际标准化工具的问卷,用于诊断哮喘,并确定呼吸道和过敏症状、治疗方法和环境暴露。协议和描述特征已经在前面描述过[20.,21]。EGEA系列已通过ISO 9001认证,并在Biobank网络中引用[22]。
本分析使用EGEA2收集的数据。仅纳入有任何生物标志物测量和吸烟状况可用数据的成年参与者(年龄≥16岁)(n=1388;联机补充图E1).在成年人中,未纳入分析的参与者(n=183)在年龄、性别、吸烟状况、身体质量指数(BMI)和哮喘特征(联机补充表E1).
哮喘的结果
哮喘患者是对经过验证和标准化的英国医学研究委员会、欧洲煤钢共同体、美国胸科学会(ATS)和欧洲共同体呼吸健康调查问卷中的四个问题有积极回答的参与者:“你是否曾在喘息时发作过呼吸困难?”、“你哮喘发作过吗?”、“这个诊断被医生确认了吗?”以及“在过去12个月里你有哮喘发作吗?”,或者对至少两个问题做出积极回答,并对医疗记录做出积极评价。病例一级亲属哮喘被定义为对前两个问题至少有一个有肯定答案[21,23]。在本分析纳入的614名哮喘患者中,536人(87.3%)被医生确诊为哮喘。在曾经患有哮喘的参与者中,当前哮喘的定义是报告有呼吸道症状(喘息、夜间胸闷和剧烈活动后、休息时或夜间出现呼吸困难)或哮喘发作,或在过去12个月内因呼吸问题而使用吸入和/或口服药物[24]。如前所述,在3个月内评估哮喘控制情况[25],尽可能符合2015年全球哮喘倡议的定义,该定义基于白天/夜间症状的频率、缓解药物的使用和活动限制。哮喘加重的定义是在过去12个月内因呼吸问题或因呼吸困难而使用口服类固醇而入院或紧急入院[26]。
关于哮喘预后的定义、肺功能、药物使用以及过敏和炎症特征的更多细节见在线补充资料。
与氧化应激相关的生物标志物
反应的生物标志物
红细胞抗氧化酶活性的测定如前所述[27,28]按照标准程序。酶活性以U·g为单位表达1血红蛋白(Hb)的SOD和GPX和在k·g1Hb代表过氧化氢酶(1k对应一阶反应的速率常数)。所有样本均在里尔大学(法国里尔)生物化学分子生物学实验室按照经过验证和标准化的程序进行分析。每种酶促试验的变异系数均<10%。
损伤的生物标志物
使用RTube收集呼气凝结物(EBC),方法标准化,如前所述[22]。简单地说,用去离子水冲洗RTube并彻底干燥。参与者以潮汐量口服呼吸到连接到冷冷凝器(- 20°C)的口管内。他们舒服地坐在有头枕的地方。所有的头枕和座椅靠背都略微倾斜,以避免在呼吸过程中唾液污染。呼吸平静而有规律。15分钟后,EBC立即按等分分离,并按照标准化程序在−80°C保存。
使用特异性酶免疫测定试剂盒(8-异前列腺素EIA试剂盒;开曼化学,安娜堡,MI,美国)根据制造商的协议。50 μL未提取的EBC重复测定,8-异前列腺素水平由8个校准点(0.8-2.0-5.1-12.8-32-80-200-500 pg·mL)的校准曲线计算−1,其中0.8 pg·mL−1是最低点)。8-异前列腺素的检出下限为4.0 pg·mL−1检测内变异系数<20%。
等离子体触发器水平的测量如前所述[18,29]。简单地说,等离子体被提取到乙醇/醚(3/ 1v /v)的混合物中,并使用荧光光谱仪(激发波长360 nm,发射波长430 nm)进行测量。荧光以相对荧光强度(RFU)·mL表示−1的等离子体。
板间变异、保存时间和日变化不影响任何生物标志物水平(数据未显示)。关于血液和EBC收集以及生物标志物测量的更多详细信息,请参见在线补充资料。
统计分析
SOD、GPX、FlOPs和8-异prostanes由于分布偏斜,进行对数变换,用几何平均值表示(Q1-Q3)。
在没有哮喘的参与者中,研究了每个生物标志物与年龄、性别、BMI和吸烟状况之间的关系,以便独立于疾病评估这些关系。
我们使用回归模型来调查所有参与者中每种生物标志物与既往哮喘之间的关系,以及既往哮喘参与者中每种生物标志物与哮喘特征、肺功能、过敏和炎症特征之间的关系。“部分控制”和“未控制”哮喘被重新归为一类,因为未控制组的哮喘患者数量较少。
使用广义估计方程进行回归分析,以考虑个体之间的家族依赖性。多元回归模型考虑了年龄(连续)、性别和吸烟状况(从不吸烟、以前吸烟或现在吸烟)作为潜在的混杂因素。对FlOP水平与哮喘结局之间的相关性进行敏感性分析,并对重度吸烟进行调整,以每年卷烟包数或每日烟草消费量(g·天)表示1)而不是吸烟状态。
为了便于解释结果,我们使用四分位范围(定义为第25百分位和第75百分位之间的距离)重新缩放了生物标志物水平,并将生物标志物典型“高”水平的参与者与典型“低”水平的参与者进行了比较。
使用SAS统计软件(9.3版;SAS研究所,卡里,北卡罗来纳州,美国)。p值<0.05为有统计学意义。
结果
参与者特征
表1显示了纳入分析的1388名参与者的特征。其中有哮喘病史的614人。他们的平均年龄为43岁,51%为女性,23%为吸烟者。患有哮喘的参与者比没有哮喘的参与者(p<0.0001)更多为男性(p=0.01)和更年轻。此外,他们有较高的过敏致敏率,1 s内用力呼气量(FEV)较低1)和支气管高反应性高于无哮喘的参与者(均p<0.0001)。
在曾经患有哮喘的参与者中,89%目前患有哮喘;32%的哮喘得到部分控制,11%的哮喘得不到控制;34%哮喘发病年龄≥16岁;在过去12个月中,66%的人报告使用过哮喘治疗(吸入或口服药物),40%的人报告使用过吸入皮质类固醇(ICS), 38%的人报告哮喘发作,14%的人报告哮喘加重,78%的人报告有呼吸道症状。
在所有参与者中,氧化应激生物标志物的几何平均值(Q1-Q3)为1218 (1036-1449)U·g1Hb对SOD和39.1 (34.2-45.3)U·g1Hb代表GPX;均值±sd过氧化氢酶为163±40.4k·g1Hb。8-异前列腺素的几何平均值为2.88 (1.31 ~ 6.66)pg·mL−193.3 (79.9 ~ 106) RFU·mL−1失败。
无哮喘参与者氧化应激生物标志物的描述
在反应的生物标志物中,过氧化氢酶活性在BMI较高的人群中较高(p趋势=0.02),当前吸烟者和戒烟者的发病率高于不吸烟者(p趋势= 0.004)。然而,过氧化氢酶与重度吸烟之间没有明显的联系。GPX活性与年龄呈正相关(p趋势=0.01),女性高于男性(p<0.0001)。SOD活性与年龄呈负相关(p趋势<0.0001)且与BMI呈正相关(p趋势= 0.003) (联机补充表E2).
在损伤的生物标志物中,8-异前列腺素水平与年龄呈负相关(p趋势=0.01),女性高于男性(p=0.04)。FlOPs水平与年龄呈正相关(p趋势<0.0001),当前吸烟者和戒烟者的发生率高于不吸烟者(p趋势< 0.0001) (联机补充表E3).此外,在当前吸烟者和戒烟者中,FlOPs水平与每年香烟包数呈正相关(p趋势= 0.03);在当前吸烟者中,FlOPs水平与每日烟草消费量呈正相关(p趋势= 0.001) (在线补充图E2).
生物标志物与哮喘状态之间的关联
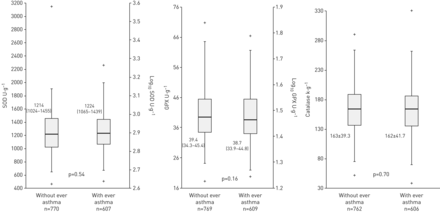
每一种生物标记物根据哮喘的分布显示在图1和2。不同哮喘组SOD、GPX、过氧化氢酶活性差异无统计学意义。相反,患有哮喘的参与者与没有哮喘的参与者相比,8-异前列腺素水平较高,FlOPs水平较低。在调整年龄、性别和吸烟状况后,只有8-异前列腺素水平与哮喘之间的相关性仍然显著(表2).
根据既往哮喘与氧化应激反应相关的生物标志物水平。箱线图显示每种哮喘状态的生物标志物水平的中位数(柱状)、第一和第三四分位数(方框)、第一和99百分位数(胡须)以及最小值和最大值(+)。左边的y轴表示原始生物标记物浓度,右边的y轴表示对数10浓度。过氧化氢酶没有对数转化。数据以几何平均值(Q1-Q3)或平均值±表示sd。SOD:超氧化物歧化酶;GPX:谷胱甘肽过氧化物酶。
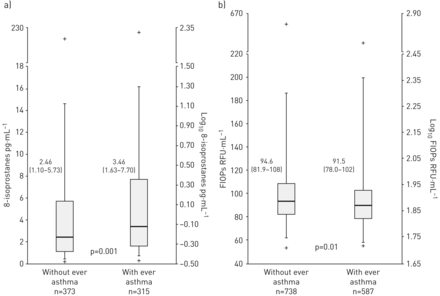
根据既往哮喘,与氧化应激相关的损伤生物标志物水平。箱线图显示每种哮喘状态的生物标志物水平的中位数(柱状)、第一和第三四分位数(方框)、第10和第90百分位数(a)、第1和第99百分位数(胡须)(b)以及最小值和最大值(+)。FlOPs:荧光氧化产物。数据以几何平均值(Q1-Q3)表示。
既往哮喘患者中生物标志物与哮喘预后的关系
在患有哮喘的参与者中,SOD、GPX和过氧化氢酶活性与哮喘预后或肺功能之间没有显著相关性(联机补充表E4).
相反,损伤的生物标志物与几种哮喘结局相关(表2).与儿童期哮喘相比,较低水平的8-异前列腺素与成年期哮喘显著相关。未发现其他显著相关性。
较高的FlOPs水平与成人发病哮喘、哮喘控制不良、哮喘发作、任何哮喘治疗和过去12个月吸入性皮质类固醇的使用显著相关。此外,FlOPs水平与肺功能不良之间存在显著的正相关。FlOPs水平始终与FEV呈负相关1(r =−0.16,p = 0.0001)。在对年龄、性别和吸烟状况进行调整后,除了FlOPs与成人哮喘之间的关联外,所有这些关联仍然显著。FlOPs水平与呼吸道症状之间无显著相关性(表2).当我们调整年龄、性别和重度吸烟(以包年数或每日烟草消费量表示)后,结果没有变化(数据未显示)。
在患有哮喘的参与者中,没有观察到任何生物标志物与支气管高反应性之间的显著关联。
讨论
本研究调查了与氧化应激相关的生物标志物与各种哮喘结果之间的关系。我们发现任何反应的生物标志物与哮喘结果之间没有显著的相关性。关于损伤的生物标志物,在8-异前列腺素水平与既往哮喘之间观察到正的和显著的相关性。在患有哮喘的参与者中,我们首次发现8-异前列腺素与儿童期哮喘之间存在显著的正相关,而FlOPs水平与哮喘控制不良、哮喘发作、任何哮喘治疗、肺功能不良和中性粒细胞性哮喘之间存在显著的正相关。
我们研究的主要优势是调查了几种参与氧化应激反应或氧化应激引起的损伤的生物标志物与各种哮喘特征之间的关系。的确,虽然反应的生物标志物是细胞内的,反映了抗氧化酶的活性[8],则会出现在“氧化应激链”的起点[30.,31]在环境和疾病之间的连续性中。相反,FlOPs是氧化应激的一个全球性标志,反映了来自DNA、蛋白质和脂质的氧化产物的混合物[18],而8-异前列腺素是脂质过氧化的特定产物[32]。这两种损伤的生物标志物存在于氧化应激链的末端,更有可能与哮喘有关。此外,我们研究了氧化应激在全身水平和接近肺部的呼气冷凝物。大多数患有哮喘的参与者是在胸科诊所作为哮喘患者招募的,通过标准化和验证的问卷,建立了一个仔细的程序,包括真正的哮喘患者。其他人则根据哮喘诊断问题的答案,被招募为哮喘患者的一级亲属。这导致了一组哮喘患者的严重程度和对乙酰胆碱的反应。详细的表型特征包括各种哮喘结局,这与氧化应激生物标志物的关系很少被研究。EGEA研究中没有显示与哮喘状态和哮喘相关表型相关的随访偏倚,本研究中纳入的成年哮喘患者代表了哮喘病例及其一级哮喘亲属的原始研究人群。氧化剂/抗氧化状态,因此生物标志物水平,取决于每个人对抗氧化反应的能力,涉及遗传因素,生活方式和环境因素。虽然在我们的分析中并不是所有这些参数都被考虑在内,而且不能排除未测量的混杂因素,但我们已经调整了相关的潜在混杂因素,如年龄、性别和吸烟状况,这些被认为与我们研究的生物标志物有关。
与之前规模较小的研究相比,我们没有发现红细胞SOD、GPX和过氧化氢酶活性与哮喘特征之间存在任何显著相关性(n ~ 30-150)。在这些研究中,较低的GPX水平始终与哮喘有关[13- - - - - -15,33];然而,对于SOD和过氧化氢酶,与增加[13,14,33]或减少[15,34根据哮喘状况报告。除了技术测量的差异外,结果之间的差异可能部分原因是哮喘结局(哮喘、严重哮喘或突发哮喘)或身体部位(红细胞、血浆或血清)的差异。抗氧化酶与哮喘之间的关系是复杂的,涉及多个内源性和外源性因素,可以影响生物标志物水平。此外,很难横断面确定生物标志物水平的变化是哮喘的原因还是后果。我们的无效结果,以及文献中的差异发现,表明反应的生物标志物可能与哮喘中的氧化应激研究不是最相关的。然而,纵向研究可能会对这种关系提供更多的见解。
我们发现EBC 8-异前列腺素与哮喘之间存在显著的正相关,这与之前的研究一致,包括aldakheel等。[12]。总的来说,结果表明8-异前列腺素水平可能是研究哮喘的相关生物标志物。此外,我们的研究结果证实,显示自由基局部产生的EBC [6,是一种有效的非侵入性方法,用于测量与氧化应激相关的生物标志物。
此外,我们调查了患有哮喘的参与者中8-异前列腺素与哮喘结局之间的关系。有趣的是,在哮喘患者中,我们观察到儿童发病哮喘患者的8-异前列腺素水平高于成人发病哮喘患者。然而,我们没有观察到8-异前列腺素与其他哮喘结局之间的任何显著相关性。此外,我们证实8-异前列腺素与肺功能或支气管高反应性之间缺乏关联,这与之前的研究一致[35,36]。我们假设,一个人患哮喘的时间越长(例如,从童年起),肺部的组织损伤就越大,而高8-异前列腺素水平反映的是长期损伤,或疾病的“背景”,而不是其表现。然而,我们没有观察到哮喘持续时间与8-异前列腺素水平之间的显著相关性(数据未显示)。另一种假设是成人哮喘和儿童哮喘,这是两种不同的哮喘表型[4,37],可能有部分不同的生物学机制。
我们发现FlOPs水平与既往哮喘呈负相关,尽管调整后这种相关性不再显著。在患有哮喘的参与者中,较高的FlOPs水平与哮喘控制能力差、肺功能差和中性粒细胞性哮喘显著相关。在过去12个月里,我们一致观察到FlOPs水平、哮喘发作、使用任何哮喘治疗方法和使用ICS之间存在显著的正相关。然而,未发现与当前哮喘、成人发作哮喘或呼吸道症状有显著相关性。据我们所知,以前没有关于FlOPs和哮喘之间关系的研究发表过。然而,FlOPs与其他慢性炎症疾病如慢性肾病(CKD)之间存在显著的正相关[17]或冠心病[19的报道。除去有CKD或心血管病史的参与者后,我们的结果没有改变(数据未显示)。
有趣的是,在FlOPs和中性粒细胞性哮喘之间观察到显著的正相关,这表明FlOPs可能与非过敏性表型有关。此外,在文献中,与我们的分析一样,FlOPs被证明与刺激性暴露有关,如烟草烟雾([18),在线补充资料)或职业性接触刺激性化学品(如。清洁产品)[29],这也与非过敏性哮喘表型有关[37- - - - - -40]。
基于这些发现,FlOPs似乎是衡量氧化应激的一个很好的生物标志物,氧化应激是与几种慢性疾病相关的病理生理机制。在我们的研究中,一些参与者在采血时没有禁食,一些潜在的混杂因素如胆固醇没有被考虑在内。虽然FlOPs测量的标准化还需要更多的研究,但我们的研究结果表明,这种氧化标记物与哮喘的表达有关。
在我们的研究中,8-异前列腺素和FlOPs与哮喘结局的关系似乎存在差异。事实上,在调整后,只有8-异前列腺素与既往哮喘相关,并且在既往哮喘参与者中,这两种生物标志物与哮喘预后的关系也有所不同。解释这些不同结果的确切机制超出了我们流行病学研究的范围。如前所述,这些生物标志物属于不同的生物过程,并在不同的区域进行测量。8-异前列腺素是脂质过氧化的主要生物标志物,在呼出的冷凝物中测量,可能反映了气道衬液的组成[6],因此可能更好地代表气道过程和反映肺部炎症。FlOPs水平是几种氧化过程的生物标志物,反映了来自DNA、蛋白质和脂质的氧化产物的混合物。这种生物标记物已在血液中测量,血液是体内大量抗氧化防御的容易获得的来源[13],因此可以更好地反映系统水平的氧化。
此外,氧化应激反应的生物标志物与损伤的生物标志物均无相关性,EBC中测量的8-异前列腺素与血液中测量的FlOPs之间未观察到相关性(数据未显示)。总的来说,所有这些结果都强调了研究属于不同生物过程的几个区室中的生物标志物的兴趣,并表明8-异前列腺素和FlOPs对哮喘的评估是互补的。
结论
总之,我们的研究结果表明EBC 8-异前列腺素似乎与儿童期哮喘有关,而FlOPs似乎与成人哮喘的表达和控制有关。不能从这项流行病学研究中推断出直接的临床意义。然而,如果重复,我们的研究结果将表明,FlOPs水平可能有助于识别哮喘负担较高的哮喘患者。需要进一步的研究,特别是通过纵向研究,以确定在临床实践中测量FlOPs水平的潜在兴趣。
补充材料
补充材料
请注意:补充材料不是编辑部编辑的,上传时是作者提供的。
补充方法和表格erj - 01193 - 2017 - _supplement
图E1。研究人群的流程图。erj - 01193 - 2017 - _figure_e1
图E2。非哮喘参与者血浆荧光氧化产物水平的箱线图,根据吸烟状况、当前吸烟者和已戒烟者每年香烟包数以及当前吸烟者的每日烟草消费量。FlOPS:荧光氧化产物。箱形图显示每个类别的中位数(柱状)、第一和第三四分位数(方框)、第一和99百分位数以及最小和最大值(围栏)。除了不吸烟者、戒烟者、吸烟者和第一类(少于10包/年)的当前吸烟者和戒烟者,栅栏代表第1和第99百分位,星星代表最低和最高。erj - 01193 - 2017 - _figure_e2
披露的信息
补充材料
诉Sirouxerj - 01193 - 2017 - _siroux
确认
EGEA合作组。协调:V. Siroux(2013年起担任流行病学首席研究员);F. Demenais(遗传学);一、Pin(临床方面);R. Nadif(生物学);F. Kauffmann (PI 1992-2012)。呼吸流行病学:Inserm ex-U 700,巴黎:M. Korobaeff (EGEA1)和F. Neukirch (EGEA1);巴黎:I. Annesi-Maesano (EGEA1-2);Inserm ex-U 1018, Villejuif: F. Kauffmann and M.P. Oryszczyn (EGEA1-2);Inserm U 1168, Villejuif: N. Le Moual, R. Nadif和R. Varraso; and Inserm U 1209 Grenoble: V. Siroux. Genetics: Inserm ex-U 393, Paris: J. Feingold; Inserm U 946, Paris: E. Bouzigon, F. Demenais and M.H. Dizier; CNG, Evry: I. Gut and M. Lathrop. Clinical centres: Grenoble: I. Pin and C. Pison; Lyon: D. Ecochard (EGEA1), F. Gormand and Y. Pacheco; Marseille: D. Charpin (EGEA1) and D Vervloet (EGEA1-2); Montpellier: J. Bousquet; Paris Cochin: A. Lockhart (EGEA1) and R. Matran; Paris Necker: E. Paty (EGEA1-2) and P. Scheinmann (EGEA1-2); and Paris-Trousseau: A. Grimfeld (EGEA1-2) and J. Just. Data and quality management: Inserm ex-U155 (EGEA1): J. Hochez; Inserm U 1168, Villejuif: N. Le Moual; Inserm ex-U780: C. Ravault (EGEA1-2); Inserm ex-U794: N. Chateigner (EGEA1-2); and Grenoble: J. Quentin (EGEA1-2).
作者感谢所有参与该研究的建立和所涉及检查的各个方面的人员:面试官、肺功能测试和皮肤刺痛测试的技术人员、血液取样、IgE测定、编码器、参与质量控制、数据和样本管理的人员以及所有中心监督该研究的人员。作者感谢三个临床研究中心(CIC)-内克尔inserm,格勒诺布尔和马赛,他们支持了这项研究,并对参与者进行了检查。他们还感谢在里尔(CIC-Inserm)和Annemasse (Etablissement Français du Sang)储存生物样本的生物银行。他们感谢所有参与的人,没有他们,这项研究就不可能进行。
脚注
这篇文章有补充资料可从www.qdcxjkg.com
收稿日期:2017年6月16日
支持声明:该研究部分由国家医院临床研究计划(PHRC-national 2012, EvAdA)、anr - ce -2009、北加莱海峡地区、默沙东公司(MSD)、GA2LEN项目、全球过敏和哮喘欧洲网络、AGIR pour les diseases Chroniques基金会、根据REA资助协议编号PCOFUND-GA-2013-609102,欧盟第七框架计划(FP7/2007-2013)的人民计划(Marie Curie行动),通过由法国校园协调的PRESTIGE计划,以及由凡尔赛大学圣昆丁-伊夫林EDSP博士资助。本文的资助信息已存入交叉参考基金注册。
利益冲突:可以在本文旁边的网站上找到信息披露www.qdcxjkg.com
- 版权所有©ERS 2017